3-6金属氧化物详解
金属-氧化物-半导体场效应管(MOS-FET)

R 'L R d // R L
gm rbe
②输入电阻
Ri
Vi
.
Rg
V 'o I 'o
R L Vs 0 ,
Ii
③输出电阻
Ro
Rd
4.1.2 共漏放大电路
共漏 共集
(1)静态分析 VG=VDDRg2/(Rg1+Rg2) VGS= VG-VS= VG-IDR ID= IDSS[1-(VGS /VP)]2 VDS= VDD-IDR
反映VGS对ID的控制作用 gm=ID/VGS VDS=const (单位mS) (毫西门子)
gm可以在转 移特性曲线上求取,即曲线的斜率
(3) 安全参数 ① UBRXX——反向击穿电压 XX:GS、DS ② PDM——最大漏极功耗 由PDM= VDS ID决定 做开关管使用时目前用Ron ID2 评估
双极型三极管
噪声 较大
温度特性 受温度影响较大 输入电阻 几十到几千欧姆 静电影响 不受静电影响
场效应三极管
较小
较小,可有零温度系数点 几兆欧姆以上 易受静电影响 适宜大规模和超大规模集成
集成工艺 不易大规模集成
4.1
FET放大电路应用
双极型三极管
场效应三极管
CCCS
两点不同:
VCCS
受控源类型
③输出电阻
Ro
I 'o
V 'o I 'o
R L 0 s 0 ,V
I 'o
V 'o V 'o 1 R gm
V 'o - g m Vgs R
V 'o = - Vgs
氧化物的分类

氧化物的分类
按与氧化合的另一种元素的类型分为金属氧化物与非金属氧化物;按成键类型或组成粒子类型分为离子型氧化物与共价型氧化物。
按照氧的氧化态分为普通氧化物(氧的氧化态为-2)、过氧化物(氧的氧化态为-1)、超氧化物(氧的氧化态为-1/2)和臭氧化物(氧的氧化态为-1/3)。
按照酸碱性及是否与水生成盐,以及生成的盐分为酸性氧化物、碱性氧化物和两性氧化物、中性氧化物、复杂氧化物。
氧化物属于化合物(当然也一定是纯净物)。
其组成中只含两种元素,其中一种一定为氧元素,另一种若为金属元素,则称为金属氧化物;若另一种不为金属元素,则称之为非金属氧化物。
广义上的氧化物是指氧元素与另外一种化学元素组成的二元化合物,如二氧化碳(CO₂)、氧化钙(CaO)、一氧化碳(CO)等。
但氧与电负性更大的氟结合形成的化合物则一般称为氟化物而不是氧化物。
2020年高考化学之《考前抓大题》10 物质结构与性质(二)(解析版)

大题10 物质结构与性质(二)1.锌在工业中有重要作用,也是人体必需的微量元素。
回答下列问题:(1)Zn原子核外电子排布式为________。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。
第一电离能I1(Zn)________I1(Cu)(填“大于”或“小于”)。
原因是______________________。
(3)ZnF2具有较高的熔点(872 ℃),其化学键类型是________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂__。
(4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。
ZnCO3中,阴离子空间构型为________,C原子的杂化形式为______。
(5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为________。
六棱柱底边边长为acm,高为ccm,阿伏加德罗常数的值为N A,Zn的密度为________g·cm-3(列出计算式)。
【答案】(1)[Ar]3d104s2(或1s22s22p63s23p63d104s2)(2)大于Zn核外电子排布为全满稳定结构,较难失电子(3)离子键ZnF2为离子化合物,ZnCl2、ZnBr2、ZnI2的化学键以共价键为主,极性较小(4)平面三角形sp2(5)六方最密堆积(A3型)【解析】(1)Zn原子核外有30个电子,分别分布在1s、2s、2p、3s、3p、3d、4s能级上,其核外电子排布式为1s22s22p63s23p63d104s2或[Ar]3d104s2,故答案为:1s22s22p63s23p63d104s2或[Ar]3d104s2;(2)轨道中电子处于全满、全空、半满时较稳定,失去电子需要的能量较大,Zn原子轨道中电子处于全满状态,Cu失去一个电子内层电子达到全充满稳定状态,所以Cu较Zn易失电子,则第一电离能Cu<Zn,故答案为:大于;Zn核外电子排布为全满稳定结构,较难失电子;(3)离子晶体熔沸点较高,熔沸点较高ZnF 2,为离子晶体,离子晶体中含有离子键;根据相似相溶原理知,极性分子的溶质易溶于极性分子的溶剂,ZnF 2属于离子化合物而ZnCl 2、ZnBr 2、ZnI 2为共价化合物,ZnCl 2、ZnBr 2、ZnI 2分子极性较小,乙醇、乙醚等有机溶剂属于分子晶体极性较小,所以互溶,故答案为:离子键;ZnF 2为离子化合物,ZnCl 2、ZnBr 2、ZnI 2的化学键以共价键为主,极性较小; (4)ZnCO 3中,阴离子CO 32-中C 原子价层电子对个数=3+4+2-322⨯=3且不含孤电子对,根据价层电子对互斥理论判断碳酸根离子空间构型及C 原子的杂化形式分别为平面正三角形、sp 2杂化,故答案为:平面正三角形;sp 2;(5)金属锌的这种堆积方式称为六方最密堆积,该晶胞中Zn 原子个数=12×16+2×12+3=6,六棱柱底边边长为acm ,高为ccm ,六棱柱体积2)×3×c]cm 3,晶胞密度=m V 为:六方最密堆积(A 3型)。
第三章第一节 铁及其化合物-高一化学期末复习(人教版2019必修第一册)(解析版)

第三章铁金属材料第一节铁及其化合物铁及其化合物,是高中阶段学习的非常典型的一种变价金属元素系列,这一部分内容和氧化还原理论联系密切,又和好多的实验物质制备,工业产品生产相关联,所以在实验题和化学工艺流程题中经常见到铁及其化合物的身影,为了好好掌握,还是先看看价类二维图吧!一、铁及其化合物的颜色铁粉是黑色的;铁块是银白色的Fe2+—浅绿色Fe3O4—黑色晶体Fe(OH)2—白色沉淀Fe3+—黄色Fe(OH)3—红褐色沉淀Fe(SCN)3—血红色溶液FeO—黑色粉末Fe2O3—红棕色粉末FeS—黑色固体这部分内容有时候作为基础题考察记忆颜色的准确性,更多的时候是作为一些推断题的突破口。
(2020·浙江高一月考)下列关于Na、Fe及其化合物的说法不正确的是A.Na着火时不能使用泡沫灭火器灭火B.Na2O在空气中久置变为Na2CO3C.Fe2O3常用作油漆、涂料的红色颜料D.铁粉与水蒸气反应生成黑色的氧化亚铁【答案】D【详解】A.Na着火时生成的过氧化钠可以和泡沫灭火器喷出的CO2反应生成O2,使燃烧更旺,故A 正确;B.Na2O在空气中与水反应生成NaOH,NaOH与CO2反应生成Na2CO3,所以Na2O在空气中久置变为Na2CO3,故B正确;C. Fe2O3是红棕色固体,常用作油漆、涂料的红色颜料,故C正确;D. 铁粉与水蒸气反应生成黑色的四氧化三铁,故D错误;答案选D。
二、铁与水蒸气反应的实验探究常温下,铁与水不反应,只有在高温条件下,Fe才会与水蒸气反应。
实验时只要注意以下细节,就能顺利完成。
a、棉花最好是一整块的,揉捏到合适大小后伸入试管底部。
如果只有多块小棉花,则必须沿试管的纵向,用较大的包裹较小的,然后再塞入。
不要把小块棉花简单堆积,因热水沸腾时会使外面的棉花冲出,一旦接触到高温铁粉,一方面使水突然剧烈沸腾,另一方面降低了铁粉的温度,不利于反应。
b、铁粉的用量要较多,铺满中部试管为宜,略有鼓起,最好较为集中,因火焰的加热面积有限(可观察直接加热区域与两端铁粉变化的区别)。
2023北京二十中高三10月月考化学(教师版)

2023北京二十中高三10月月考化 学相对原子质量:H-1 C-12 N-14 O-16 Cu-64 Cl-35.5 Cd-112 Zn-65 Pb-207第一部分本部分共14题,每题3分,共42分。
在每题列出的四个选项中,选出最符合题目要求的一项。
1. 冠醚因分子结构形如皇冠而得名,某冠醚分子c 可识别K +,其合成方法如下。
下列说法错误的是A. 该反应为取代反应B. a 、b 均可与NaOH 溶液反应C. c 核磁共振氢谱有3组峰D. c 可增加KI 在苯中的溶解度2. 下列有关物质性质与用途具有对应关系的是 A. 23Al O 熔点高,可用于做耐高温材料 B. 3NH 显碱性,可用作制冷剂C. 43NH HCO 受热易分解,可用作氮肥D. 2SO 具有氧化性,可用于自来水的杀菌消毒 3. 铅丹(34Pb O 可用作防锈涂料,它与浓盐酸反应的化学方程式为:()22342O Pb O +8HCl =3Pb l +Cl +C 4H 浓↑。
设A N 为阿伏伽德罗常数值。
下列说法不正确的是A. 标准状况下,22.4L 2Cl 溶于水所得溶液中含HClO 分子数为A NB. 1L 121mol L -⋅的浓盐酸与足量34Pb O 反应生成的2Cl 分子数少于1.5A NC. 标准状况下,22.4L 2H O 中,含有H 原子数目大于2A ND. 反应中消耗137g 34Pb O ,转移的电子数目为0.4A N 4. 下列离子方程式正确的是A. 用足量的NaOH 溶液吸收烟气中的SO 2:SO 2+OH -=HSO 3-B. CuSO 4溶液中滴加稀氨水:Cu 2++2NH 3·H 2O=Cu(OH 2↓+2NH 4+C. 用氯化铁溶液蚀刻覆铜板:Fe 3++Cu=Fe 2++Cu 2+D. 将等物质的量浓度的Ba(OH 2和NH 4HSO 4溶液以体积比1:1混合:Ba 2++2OH -+2H ++SO 24-=BaSO 4↓+2H 2O5. 下列实验操作及现象表述错误..的是A. 向NaHCO3溶液中加入AlCl3溶液,产生白色沉淀并有无色气泡生成B. 向Ba(NO32溶液中通入足量的SO2气体,溶液先变浑浊,然后重新变清澈C. 向NH4Cl溶液中滴加NaOH稀溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝D. 化合物FeO(OCH3溶于溶于氢碘酸(HI ,再加CCl4萃取,有机层呈紫红色6. 日光灯中用到的某种荧光粉的主要成分为3W3(ZX42·WY2。
2020届高三化学 全国卷高考化学模拟试题八(全国I)
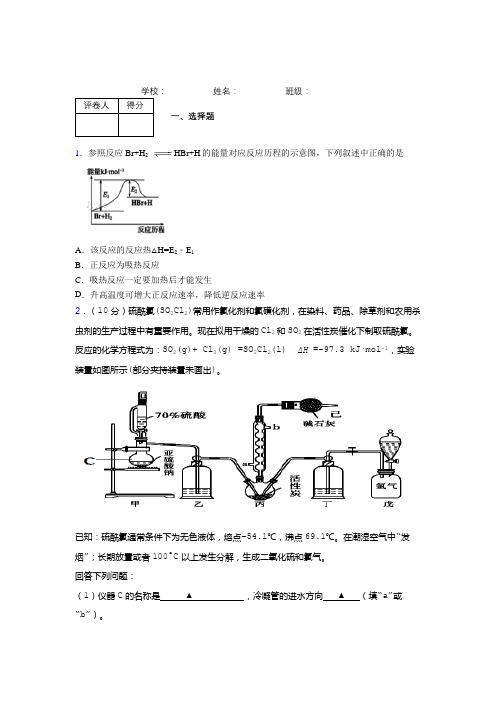
__________ 姓名:__________ 班级:__________评卷人得分一、选择题1.参照反应Br+H2 HBr+H的能量对应反应历程的示意图,下列叙述中正确的是A.该反应的反应热△H=E2﹣E1B.正反应为吸热反应C.吸热反应一定要加热后才能发生D.升高温度可增大正反应速率,降低逆反应速率2.(10分)硫酰氯(SO2Cl2)常用作氯化剂和氯磺化剂,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。
现在拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。
反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =−97.3 kJ·mol−1,实验装置如图所示(部分夹持装置未画出)。
已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。
在潮湿空气中“发烟”;长期放置或者100°C以上发生分解,生成二氧化硫和氯气。
回答下列问题:(1)仪器C的名称是▲ ,冷凝管的进水方向▲ (填“a”或“b”)。
(2)下列操作或描述正确的是▲ 。
A.将70%硫酸换成98.3%硫酸,可以加快制取SO2的速率B.实验中通过观察乙、丁导管口产生气泡的速率相等,可控制两种反应物体积相等C.装置戊上方分液漏斗中最好选用0.10 mol·L-1NaCl溶液,减小氯气的溶解度D.装置己防止污染,又防止硫酰氯变质(3)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯,写出反应方程式:▲ 。
(4)长期储存的硫酰氯会发黄,可能的原因是▲ (用化学方程式和必要的文字加以解释)。
(5)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g 纯净的硫酰氯,则硫酰氯的产率为▲ 。
(产率=×100%)3.下列过程中,共价键被破坏的是A.碘升华B.溴蒸气被木炭吸附C.酒精溶于水D.HCl气体溶于水4.下列叙述正确的是( )A.图I装置中通入N2和O2的作用是相同的B.图II中甲、乙两装置产生喷泉的原理一样C.图III①装置中镁片是原电池的负极,②装置镁片是原电池的正极D.图IV分液漏斗中盛硝酸能证明非金属性:N>C>Si,盛硫酸能证明非金属性:S>C>Si答案5.磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
《几种重要的金属化合物》

• 金属氧化物 • 金属氢氧化物 • 金属盐 • 金属碳化物 • 金属氮化物
01
金属氧化物
定义与性质
定义
金属氧化物是由金属元素和氧元素通 过共价键结合形成的化合物。
性质
金属氧化物通常是固体,具有不同的 颜色和熔点。它们通常是电的绝缘体 或半导体,但在某些条件下可以导电。
部分金属氮化物具有特殊的光学性能,可用于制造高精度光学仪器 和激光器。
耐磨材料
部分金属氮化物具有较高的硬度和耐磨性,可用于制造耐磨耐高温 的机械零件。
THANKS
感谢观看
常见的金属氧化物
氧化铁(Fe2O3)
氧化镁(MgO)
通常称为铁锈,是铁的氧化物,呈红 棕色。
白色粉末,是镁的氧化物,广泛用于 耐火材料和建筑材料。
氧化锌(ZnO)
白色粉末,是锌的氧化物,常用于制 造涂料和防晒霜。
金属氧化物的应用
颜料与涂料
陶瓷与玻璃
一些金属氧化物具有特殊的颜色和稳定性 ,可用于制造颜料和涂料。
金属氢氧化物的应用
化工原料
金属氢氧化物是许多化学 反应的重要原料,如合成 有机物、无机物等。
污水处理
金属氢氧化物可用于中和 酸性废水,处理重金属离 子等污染物。
制药行业
在制药行业中,金属氢氧 化物可用于合成药物中间 体和原料药。
03
金属溶解性
颜色
酸碱性
金属盐是由金属阳离子 和酸根阴离子构成的化 合物。
金属盐具有与相应金属 氧化物或氢氧化物性质 相似,如溶解性、颜色 、酸碱性等。
金属盐的溶解性取决于 金属的活跃度和酸根的 溶解性。一般来说,钾 、钠、铵盐等易溶于水 ,而钙、镁、钡等碱土 金属盐的溶解度则相对 较低。
2024年初升高化学无忧衔接(通用版)衔接点01物质的分类(解析版)

衔接点01 物质的分类初中要求只是了解物质的简单分类方法高中要求1. 了解分类的方法一树状分类法和交叉分类法;2. 理解氧化物的分类及其各类氧化物的性质、制法;3. 了解正盐、酸式盐、碱式盐的概念和形成原因.• 初高考点对接七初中化学盲点区 高中化学纯净物[-谜-混合物-一溶液_浊液无机物-厂金属单质一单质~\L ■非金属单质1-纯净物-「酸-化欲-碱-盐碱的分类_______■氧化物的分凳L —元酸ng 出一二元酸I 多元酸----、按电菠出电离出 __息。
基氧根高球目 一 一兀例L 多元碱「皿: 按酸碱中和费——稣盐「酸性氧化物A 按氧化物性质——碱性氧化物j 两性氧化物-酸的分类wA 盐的分类 W•••♦,初中知识温故tA-回顾一物质的简单分类1.物质的简单分类表「混合物'金属单质单质,非金属单质、稀有气体物质<纯净物<化合物,厂酸碱无机化合物〈盐氧化物I有机化合物回顾二几组重要概念1.混合物和纯净物混合物纯净物宏观由不同种物质组成由一种物质组成微观由不同种分子构成由同种分子构成性质没有固定的组成,各组分保持各自的化学性质。
没有固定的熔点和沸点具有固定的组成,具有固定的熔点、沸点;具有固定的化学性质例如空气是混合物,由氧气、二氧化碳、氮气等组成,含有N2、。
2、C02、田0等不同种分子水是纯净物,由水(H2。
)分子构成;氧气是纯净物,由氧(。
2)分子构成【易错提醒】(1)不要被“洁净、混合”等字眼迷惑,洁净物不一定是纯净物,例如:洁净的空气、干净的矿泉水就是混合物。
(2)不要被物质的名称迷惑,例如:二氧化碳是物质的名称,“氧”“碳”指组成物质的元素,不是两种物质,二氧化碳是纯净物,不是混合物。
2.单质、化合物和氧化物类别单质化合物氧化物概念由回种元素组成的纯净物由不同种元素组成的纯净物由两种元素组成,且其中一种元素是氧元素的化合物判断方法必须是纯净物;只含一种元素必须是纯净物;含两种或两种以上元素必须是化合物举例氮气(N2)、氢气(田)、氧气(02)、铁(Fe)和碳水(H2。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
催化中重要的是非化学计量的N、P型半导体两大类!
非化学计量的氧化物定义:偏离正常分子式的化学计量 比组成. 差别一般<1% 非化学计量的成因:晶体和气相分子的相互作用, 由于金 属离子不足或非金属离子不足造成了晶体的非化学计量
例如:氧化物与气相中的氧的相互作用
当金属氧化物是:非化学计量,或引入杂质 产生 杂质能级(禁带)
MoO3-Bi2O3-Fe2O3 -CoO-K2O-P2O5-SiO2(丙烯腈催化
6
剂)
结构复杂:
组分与组分之间可能相互作用,作用的情况因条件不同而异;
复合氧化物(固熔体,杂多酸,混晶等);
常多相共存,有所谓的活性相概念
例如:Bi2O3-MoO3,就有α-,β-,γ-相,
催化作用与功能
禁带 EF △E
EC EV MgO 禁带较宽 △E > 5 eV
不能使满带电子激发到空带中
半导体
半导体的禁带很窄(0.2~3ev),
在绝对零度时,电子不发生跃迁,与绝缘体相似;
但当温度升高或接受光照时,部分电子从满带激发到空 带上去,空带变成导带, 而满带则因电子移去而留下空穴,在外加电场作用下能 够导电,故称半导体。
在受主能级上有空穴存在。 很容易接受满带中的跃迁的电子,使满带产生正电空穴关 进行空穴导电。又称空穴型半导体
例如单晶Si、单晶Ge、PbS等。
25
本征半导体能带结构
• 晶体中既无施主也无受主,具有电子和空穴两种载流子,其 准自由电子和准自由空穴是在外电场作用下,电子从价带迁
移到导带中产生。
本征半导体在催化领域并不重要,因为化学变化过
程的温度,一般在 300~700 ℃ ,不足以产生电子从 其价带到空带的跃迁。
10
应用
• 金属氧化物(硫化物)催化剂的应用:氧化还原反应 • 金属氧化物:
– 主要催化烃类的选择性氧化,主要应用于有氧参与的氧
化反应 – 部分应用于加氢、脱氢(在氢气中难于还原的氧化物) • 金属硫化物催化剂:主要用于重油的加氢精制,加氢脱硫 (HDS)、加氢脱氮(HDN)、加氢脱金属(HDM)等过 程
氧化物催化剂的工业应用(1)
氧化物催化剂的工业应用(2)
作为氧化作用的氧化物催化剂的类型
① 过渡金属氧化物:晶格氧型,易从晶格中传递出氧给反应 物分子,含有2种以上价态可变的阳离子,且阳离子常交叉互溶, 为非计量化合物 ② 金属氧化物:化学吸附氧型,用于氧化的活性组分为化学 吸附型氧种(分子态、原子态或间隙氧) ③ 原态不是氧化物,是金属:表面吸附氧形成氧化层,如Ag 对乙烯甲醇的氧化,Pt对氨的氧化
(1) 主催化剂组分,对化学反应起催化作用的根本性物质, 单独存在时就有催化活性;是催化剂的必须具备的主体成分;如 丙烯氨氧化制丙烯腈使用的MoO3-Bi2O3催化剂中的MoO3 ( 2 )助催化剂组分,具有提高催化剂活性、选择性和改善催 化剂耐热性、抗毒性、机械强度、寿命等性能的组分,其本身无 活性或者活性很小; MoO3-Bi2O3催化剂中的Bi2O3 (3)载体
上课回顾 金属催化剂化学键
能带模型— d带空穴 价键模型—d% 配位场模型—定域键模型
3.6 金属氧化物和硫化物催化剂及其催化作用
主要内容
1
2 3
概述 半导体的能带结构及其催化活性 氧化物表面的M=O性质与催化剂活 性、选择性的关联
4
5
复合金属氧化物催化剂的结构化学 金属硫化物催化剂及其催化作用
1. 概述
金属氧化物催化剂(复合氧化物)组成
金属氧化物催化剂主要是:
IVB-VIII族和IB,IIB族元素的氧化物
4
元素周期表
57La
镧
89A
58 Ce
59 Pr
60 Nd
61 62 Pm Sm
63 Eu
64 Gd
65 Tb
66 Dy
67 Ho
90
Th
91
Pa
92
U
93
Np
பைடு நூலகம்94
Pu
95
Am
96
Cm
97
Bk
98
Cf
99
Es
c 锕
6 69 70 71Lu 8 Tm Yb 镥 Er 10 10 10 103Lr 0 1 2 5铹
Fm Md No
1. 概述
金属氧化物催化剂组成
催化剂多由两种或多种氧化物组成,且组分中至少有
一种是过渡金属氧化物。
如:V2O5-MoO3,Bi2O3-MoO3, TiO2 -V2O5-P2O5,V2O5-MoO3-Al2O3,
22
半导体:禁带窄,满带电子可激发到空带而导电
0K时半导体不导电。
一定温度下,价带电子跃迁到
EF ee e 空带,空带有自由电子导电,价 带有空穴导电。
空带 满带
导带 满带
半导体分类
半导体分为三类: ⑴ 本征半导体 ⑵ n-型半导体 ⑶ p-型半导体
24
本征半导体
组成计量,不含杂质,具有理想的完整晶体结构、 有电子和空穴两种载流子传导的半导体,
(3)电子从满带跃迁后形成的空穴以与电子相反方向传递电流
(4)禁带宽度为Eg:
金属:Eg=0,
所以导电良好,无禁带。
半导体:Eg=0.2~3e.v.
绝缘体:Eg=5~10e.v. 所以导电很差,禁带较宽。
没有导带 有满带,空带, Ec — 空带最低能级 Ev — 满带最高能级 △E — 能量差
绝缘体
14
二.半导体的能带结构及其催化活性
金属氧化物和硫化物催化剂,大部分是半导体型化合物; 与金属不同,它们的能带结构是不叠加的,形成分开的带(满带 /价带、禁带和空带)
15
能带结构几个概念:
满带、价带、空带→导带、禁带(能量宽度为Eg)。
满带:凡是能被子电子完全充满的能带;
价带:通常是指半导体或绝缘体中,在0K时能被电子占
满的最高能带。
空带:没有填充电子的能带; 导带:凡是能带没有完全被电子充满的; 禁带:在导带(空带)和满带之间没有能级,不能填充 电子,这个区间叫禁带。
16
半导体能带特点:
(1)能带不迭加,形成分开的带
(2)电子(价带中)电子受热或辐射、跃迁到空带,带入的电
子在外电场作用下, 开始导电→导带(原来的空带)
N型、P型半导体
杂质是以原子、离子或集团分布在金属氧化物晶体中,存
在于晶格表面或晶格交界处。
32
N型半导体: 如果杂质能级出现在靠近半导体导带下部称为施主能级。
施主能级的电子容易激发到导带中产生自由电子导电,又称 电子型半导体
E施主能级
33
P型半导体:
如果出现的杂质能级靠近满带上部称为受主能级。
