酸碱盐的定义及分类
酸碱盐的概念及物质的简单分类

精心整理
第七章补充课时
酸碱盐的定义
1.酸盐酸、硫酸、硝酸都能导电,说明HCl 、H 2SO 4、HNO 3
在水溶液中电离生成了能够自由移动的离子。
它们的电离方程式如下: HCl=H ++Cl —
H 2SO 4=2H ++SO 42— HNO 3=H ++NO 3—
由以上式子可以看出,HCl 、HNO 3和H 2SO 4在水溶液里都能电离生成氢离子(H +)。
电离时生成的阳离子全部是氢离子的化合物叫做酸。
HCl 、H 2SO 4、HNO 3都属于酸类。
Cl —、2.碱KOH=K +Ba(OH)2OH —)。
有NH 4+
Ca(OH)2Al(OH)33.盐MgSO 4=BaCl 2由上列各式可以看出,Na 2CO 3、MgSO 4、BaCl 2和NaCl 等物质在水溶液里都能电离出金属离子和酸根离子。
电离时生成金属离子(或铵根离子)和酸根离子的化合物叫做盐。
其中金属离子所带正电荷总数等于酸根离子所带负电荷总数。
盐的结构特点:金属离子(或铵根离子NH 4+)+酸根离子
在日常生活里,我们常常遇到许多种盐。
例如,用作调味和防腐剂的食盐NaCl ,用来制作模型的石膏CaSO 4,用作建筑材料的石灰石和大理石(主要成分为CaCO 3) 用作消毒剂的高锰酸钾。
氯化钠NaCl 碳酸钙CaCO 3水H 2O 碳酸钠
精心整理
精心整理。
酸碱盐讲义
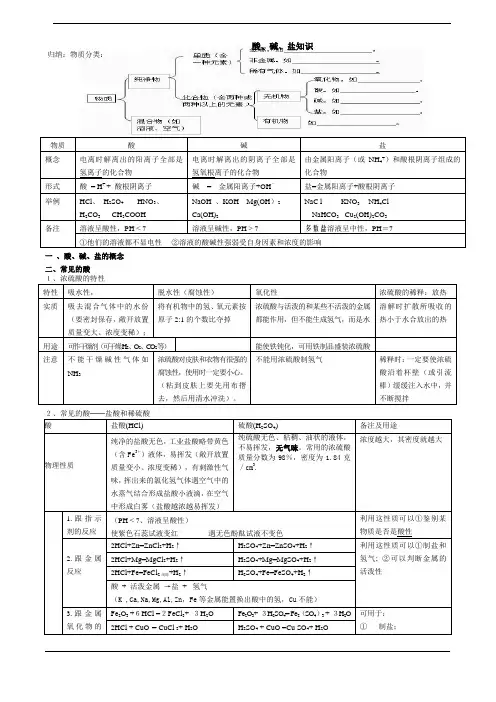
酸、碱、盐知识归纳:物质分类:一、酸、碱、盐的概念二、常见的酸1、浓硫酸的特性B .与排在氢之前的活泼金属反应生成盐和氢气。
金属活动顺序为:K,Ca,Na,Mg,Al;Zn,Fe,Sn,Pb ,(H) Cu,Hg,Ag,Pt,Ar Fe+2AgNO 3=Fe(NO 3)2+2Ag C .与碱性氧化物反应生成盐和水。
D .与碱发生中和反应生成盐和水。
E .与可溶性盐反应生成新盐新酸。
如:H 2SO 4+BaCl 2=2HCl+BaSO 4↓ (白色不溶于稀硝酸的沉淀,常用来检验SO 42-的存在) 。
又如:2HCl+AgNO 3=HNO 3+AgCl ↓(白色不溶于稀硝酸的沉淀,常用来检验Cl -的存在)4. Cl -、SO 2-的检验。
某溶液中滴入AgNO 3产生白色沉淀,是否可以肯定溶液中存在Cl -?某溶液中滴入BaCl 2产生白色沉淀,是否可以肯定溶液中存在S O 42-?不能,如:Na 2CO 3+2AgNO 3=2NaNO 3+Ag 2CO 3↓(白色沉淀), H 2CO 3+ BaCl 2=2HCl+BaCO 3↓(白色沉淀),因此CO 32-遇Ba 2+或Ag +同样产生白色沉淀,不同的是加入硝酸后沉淀消失,原因如下: Ag 2CO 3+2HNO 3=2AgNO 3+CO 2↑+H 2O , BaCO 3 +2HNO 3=Ba(NO 3)2+ CO 2↑+H 2O因此,用Ag +、Ba 2+检验Cl -、SO 4产生白色沉淀后还要用稀硝酸检验沉淀是否消失。
5.溶液的酸碱性可用石蕊、酚酞等酸碱指示剂来区分。
溶液的酸碱度可用PH 试纸来测定(具体方法如何?)。
A 、PH 值表示溶液的酸碱程度。
酸的PH 值<7,PH 值<7的物质呈酸性。
PH 值越小,酸性越强,PH 值为0的物质酸性最强;碱的PH 值>7,PH 值>7的物质呈碱性。
PH 值越大,碱性越强,PH 值为14的物质碱性最强。
初三化学酸碱盐知识点(最全整理版)

初三化学酸碱盐知识点(最全整理版)一、酸性溶液和碱性溶液结论:〔1〕但凡能使紫色石蕊试液变红的溶液都是酸性溶液,并且该溶液不能使无色酚酞试液变色;〔2〕但凡能使紫色石蕊试液变蓝的溶液都是碱性溶液,并且该溶液能使无色酚酞试液变红;〔3〕不能使紫色石蕊试液变色,也不能使无色酚酞试液变色的溶液,我们称为中性溶液。
〔4〕如紫色石蕊试液及无色酚酞等能检验溶液酸碱性的试液,称为酸碱指示剂。
注意:①我们有时候还用蓝色或红色石蕊试纸来检验溶液的酸碱性;②酸性溶液能使蓝色石蕊试纸变红,碱性溶液能使红色石蕊试纸变蓝;③只有可溶性的酸性、碱性物质才能使指示剂变色,变色的是指示剂,而不是该物质。
2.日常生活中常见的酸性物质与碱性物质〔1〕酸性物质:山楂、柠檬、柑橘、西红柿等;〔2〕碱性物质:茶叶碱、烟碱等。
3.区分酸溶液和酸性溶液、碱溶液和碱性溶液注意:酸溶液是指酸的水溶液,酸性溶液是指能使紫色石蕊试液变红的溶液,因此酸溶液一定是酸性溶液,而酸性溶液不一定是酸溶液;同样,碱性溶液不一定是碱溶液,碱溶液一定是碱性溶液。
例如:硫酸铜、氯化铵的水溶液显酸性,而不是酸;纯碱、肥皂的水溶液显碱性,但不是碱。
4.补充知识:酸、碱、盐的概念〔1〕酸:电离时生成的阳离子全部是氢离子的化合物。
如:HCl、HNO3、H2SO4、H2CO3等。
HCl==H++Cl-;H2SO4==2H++SO42-;〔2〕碱:电离时生成的阴离子全部是氢氧根离子的化合物。
如:NaOH、Ca(OH)2等。
NaOH==Na++OH-;Ca(OH)2==Ca2++2OH-;〔3〕盐:电离时生成金属离子〔或铵根离子〕和酸根离子的化合物。
如:NaCl、NH4NO3等。
NaCl==Na++Cl-;NH4NO3==NH4++NO3-;二、溶液的酸碱性的强弱1.酸碱度:用来表示溶液的酸性或碱性的强弱程度。
2.pH试纸用来定量的测定溶液的酸碱度。
溶液的pH值与酸碱性关系:pH=7,溶液呈中性;pH7,溶液呈碱性,且pH越大,碱性越强。
化学酸碱盐知识分类

一、酸的组成、分类、命名
1、酸的组成P4/
由氢元素和酸根组成的化合物。读作:“某酸”、“氢某酸”
2、常见的酸
盐酸、碳酸、硫酸、硝酸、
氢硫酸、醋酸(乙酸)
3、酸的分类与命名
①根据酸中是否含氧元素分
A.含氧酸【“某酸”】
(碳酸、硫酸、硝酸、亚硫酸H2SO3、甲酸HCOOH、乙酸CH3COOH、*柠檬酸、*乳酸等)
(反应物至少有一种可溶,生成物中或者有水、或者有气体、或者有沉淀)
常见化学反应举例:
盐酸与硝酸银溶液、碳酸钙、碳酸钠、碳酸氢钠、碳酸钡、碳酸银反应
硫酸与硝酸钡、氯化钡溶液、碳酸钠、碳酸钾、碳酸铵、碳酸钡反应
4、酸溶液+活泼金属→盐+氢气(置换反应)
常见化学反应举例:
盐酸、硫酸分别与镁、铝、锌、铁反应
2、稀硫酸的化学性质:
①与指示剂作用
[实验]硫酸溶液与石蕊、酚酞作用
②与活泼金属反应
[练习]书写方程式:镁、铝、锌、铁分别与硫酸反应
③与碱反应
[练习]写方程式:氢氧化钠、氢氧化钙、氢氧化钡、氢氧化钾、氨水、氢氧化铁、氢氧化铜分别与硫酸反应
④与盐反应
[实验]硫酸与硝酸钡、氯化钡溶液反应——检验硫酸的方法
[练习]书写方程式:硫酸与碳酸钠、碳酸钾、碳酸铵、碳酸钡反应
⑤与碱性氧化物反应
[实验]硫酸分别与氧化铜、氧化铁反应,观察实验现象,书写方程式
[练习]书写方程式:硫酸与氧化钠、氧化钾、氧化钙、氧化钡反应的方程式
[问]1、如何鉴别盐酸、硫酸?
2、碳酸银能溶于盐酸吗?碳酸钡能溶于硫酸吗?分别写出上述反应的方程式。
[讲述]碱性氧化物与金属氧化物的区别与联系
第十单元酸碱盐定义及分类

写出下列物质的化学式,并指出 它们各属于哪一类化合物:
硫酸钠 碳酸钾 磷酸 硝酸 硝 酸铜 氯化亚铁 氢氧化钡 氢氧化钙
写出下列化合物的名称,并指出它 们各属于哪一类化合物:
Cu(OH)2 CaCO3 MgCl2 Fe(OH)3 NaHCO3 H2SO4 H2CO3 Ca(H2PO4)2
小结:物质的分类
1、碱的定义:在熔融状态或在水溶液 中电离出阴离子全部是氢氧根离子的 化合物叫做碱。
NaOH = Na+ + OH KOH = K+ + OH Ca(OH)2=Ca2+ + 2OH Ba(OH)2=Ba2+ + 2OH
此外,常见的碱还有作为化肥或医药的氨水 (NH3· H2O);作为中和胃酸过多的药物氢氧化铝 [Al(OH)3].
碱= 金属离子/铵根离子+ OH-
二、碱的定义和分类
2、碱的分类
分类依据:根据是否能溶于水
可溶性碱
NaOH KOH Ba(OH)2 NH3· H2O; Ca(OH)2
难溶性碱
Al(OH)3
Cu(OH)2等
二、碱的定义和分类
2、碱的分类
分类依据:根据电离时产生OH-的个数
NaOH = Na+ + OH KOH = K+ + OH Ca(OH)2=Ca2+ + 2OH Ba(OH)2=Ba2+ + 2OH Al(OH)3=Al3+ + 3OH
盐酸:HCl
此外常见的酸还有碳酸(H2CO3) 、磷酸 ( H3 PO4 ) 、氢硫酸( H2 S)、亚硫酸( H2 SO3 ) 等。
酸碱盐定义及构成

酸碱盐定义及构成
酸碱盐是化学中的基础概念,它们的定义和构成如下:
1.酸:酸是能够释放出氢离子(H⁺)的化合物。
在水溶液中,酸会产生氢离子和相应的阴离子。
例如,盐酸( HCl)在水中会解离成氢离子和氯离子。
酸还可以根据其解离程度分为强酸和弱酸。
2.碱:碱是能够释放出氢氧根离子( OH⁻)的化合物。
在水溶液中,碱会产生氢氧根离子和相应的阳离子。
例如,氢氧化钠(NaOH)在水中会解离成氢氧根离子和钠离子。
碱也可以根据其解离程度分为强碱和弱碱。
3.盐:盐是由酸和碱反应产生的化合物,通常由阳离子和阴离子组成。
盐可以是有机或无机的,常见的无机盐如氯化钠( NaCl),它由钠离子和氯离子组成。
盐在水中的溶解性不同,有些易溶于水,如食盐,有些则难溶或不溶。
酸碱盐的反应遵循一定的规律,如酸碱中和反应会产生水和盐,这是化学中的基本反应类型之一。
这些概念不仅在理论上重要,而且在工业、医药、环境科学等领域都有广泛的应用。
5初三科学第五讲酸碱盐定义以及分类(精)
第五讲酸碱盐定义以及分类姓名: 学校: 年级:【知识要点】一、酸1、电离: 物质因溶解或熔化而离解成自由移动离子的过程.2、什么是酸: 电离时生成的阳离子全部是氢离子( H +的化合物.3、酸电离的通式:酸 === H ++ 酸根阴离子.常见的酸有盐酸(HCl,硫酸(H 2SO 4和硝酸(HNO 3等.它们的电离式为: 盐酸: HCI === H ++ Cl - 硫酸:H 2SO 4 == 2 H + + SO 42 -硝酸:HNO 3 === H + + NO 3-二. 酸的分类和命名三、碱1、定义:电离时生成的阴离子全部是OH -的化合物 2、常见的碱有:氢氧化钠(NaOH ;氢氧化钙[Ca(OH2] 四、溶液的酸碱性1、酸碱指示剂:石蕊和酚酞溶液叫酸碱指示剂,也简称指示剂,石蕊和酚酞是两种常用的指示剂,它们在酸碱中的变色情况下表所示: 酸溶液碱溶液中性溶液紫色石蕊溶液变红色变蓝色紫色溶液指示剂无色酚酞溶液不变色(无色变红色无色2、PH 试纸用酸碱指示剂只能指示溶液的酸碱性。
而pH 试纸不仅能显示溶液的酸碱性,还能显示溶液的酸碱性的强弱.pH 值是体现某溶液或物质酸碱度的表示方法。
pH 值分为0-14范围. pH <7,酸性;pH =7,中性;pH >7,碱性强酸:盐酸(HCl 、硫酸(H 2SO 4、硝酸(HNO 3 弱酸:醋酸(CH 3COOH ;碳酸(H 2CO 3 五、盐1、定义:盐是指一类组成里含有金属离子(铵根离子和酸根离子的化合物。
2、常见的盐:碳酸钠(Na 2CO 3;碳酸钙(CaCO 3; 食盐 (NaCl【典型例题】例1、写出盐酸、氢氧化钠、食盐电离时的式子。
、、。
例2、有一瓶无色液体,可能是NaCl 和H 2SO 4选用下列哪种试剂可以鉴别(A .NaOH 溶液B .石蕊试液C .酚酞试液D. KOH例3、如图所示:向实验仪器点滴板的四个井穴(已编号分别滴加氢氧化钠、氢氧化钾、氢氧化钙和碳酸钠四种溶液各三滴,再各加1滴紫色石蕊试液,观察到四种溶液均变为蓝色。
衔接点02 酸碱盐的分类和命名-2020年 初高中衔接化学(解析版)
衔接点02 酸碱盐的分类和命名一、酸的定义、分类和命名1.定义:电离时产生的阳离子全部是氢离子的化合物称之为酸。
概念中的两个关键词:阳离子全部是氢离子、化合物2.分类:A.按一个酸分子完全电离产生的氢离子个数可以分为一元酸、二元酸、三元酸一元酸:盐酸(HCl)、硝酸(HNO3)、CH3COOH二元酸:硫酸(H2SO4)、碳酸(H2CO3)、H2SO3、H2S三元酸:磷酸(H3PO4)B.根据酸是否具有挥发性,可以分成难挥发性酸和挥发性酸难挥发性酸:硫酸、磷酸挥发性酸::盐酸、硝酸、醋酸应用:难挥发性酸制取易挥发性酸H2SO4+2NaCl===△Na2SO4+2HCl↑说明:该反应与温度有关,温度较低时会生成NaHSO4,继续加热和盐酸可以反应生成氯化钠和氯化氢。
C、根据酸产生氢离子的程度可以分为强酸和弱酸强酸:盐酸、硫酸、硝酸弱酸:碳酸、醋酸应用:强酸制取弱酸H2SO4+Na2CO3=Na2SO4+H2O+CO2↑D、根据酸的沸点的高低,可将酸分为高沸点酸和低沸点酸高沸点酸:硫酸、磷酸低沸点酸:盐酸、氢溴酸E、根据酸的组成中是否含有氧元素,可将酸分为含氧酸和无氧酸含氧酸:硫酸、硝酸、碳酸、磷酸无氧酸:盐酸、氢溴酸、氢碘酸、氢氟酸、硫化氢(氢硫酸)3.酸的命名A.含氧酸的命名除去含氧酸中氢氧元素后,用剩下的元素命名该酸,若该酸中化合价较低,可依次用亚×酸、次×酸命名。
如H2SO4、H2SO3分别称硫酸、亚硫酸。
注意:含磷元素的含氧酸命名比较特殊:注意:含氧酸到底是几元酸取决于羟基(—OH)个数,而不是氢原子个数。
如上图亚磷酸、次磷酸、偏磷酸均为一元酸。
磷酸、亚磷酸、次磷酸的命名是根据化合价命名的。
偏磷酸的化学式常简单写成HPO3,但是实际上没有这样的分子的,实际存在的是多聚偏磷酸,常见的有三偏磷酸和四偏磷酸。
B.无氧酸的命名通常称作氢某酸。
如HCl叫做氢氯酸,俗称盐酸;HBr称作氢溴酸;HI称作氢碘酸;H2S称作氢硫酸。
初中化学_酸碱盐的定义及物质分类PPT课件
酸溶液和盐溶液中含有的共同离子是:
碱溶液和盐溶液中含有的共同离子是: 酸和碱的组成中含有的共同元素是:
判断下列物质的类别:
硫酸铜 氢氧化钠 氢氧化钡 氨水 碳酸氢钠 氧化铜
四、物质分类
阅读P83
填写表格
1、判断下列物质哪些是酸?哪些是碱?哪 些是盐?
H2O O2 HCl K2MnO4 MnO2 H2SO4 Ca(OH)2 Fe(OH)3 KNO3 SO3 KCl ZnCl2 NaOH NH3· H2O NH4Cl NaHCO3 Cu2(OH)2CO3
2、下列物质中,含有可以自由移动的 氯离子的是( C ) A.HCl气体 B.NaCl晶体 C.KCl溶液 D.KNO3溶液 3、下列化合物中不属于碱类的是( B. C. ) A.氢氧化钡 Ba(OH)2 B.纯碱 Na2CO3 C.酒精 C2H5OH D.氢氧化钾 KOH
4、写出下列反应的化学方程式,并 判断物质的所属类别(金属单质、非金属单 质、氧化物、酸、碱、盐)
(1)锌与稀硫酸 (2)碳酸钙与稀盐酸 (3)分解高锰酸钾 (4)二氧化碳通入澄清石灰水中 (5)一氧化碳还原氧化铁
5、下图是试验物质导电性的实 验,其中灯泡不亮的是 ( A. )
6、含有下列离子的溶液中,溶 质全部为酸的是 ( B. ) A.H+、Na+、SO42- B.H+、Cl-、NO3- C.OH-、K+、Ba2+ D.Ag+、K+、NO3-
身体健康,学习进步!
HCl是共价化合物,在水溶液中可以离解成自 由移动的氢离子和氯离子,因此盐酸溶液(也 可称做盐酸或氢氯酸)可以导电。 蔗糖、酒精是共价化合物,由分子构成,溶解 于水时以分子形式分散到水中,溶液里不存在 带电的粒子,所以蔗糖溶液和酒精溶液都不导 电。
酸碱盐的分类 范卿平 讲义
酸碱盐的分类范卿平讲义
酸碱盐是一类重要的物质,它们的分类是非常重要的,可以帮助我们更好地理解它们的特性和性质。
首先,我们来看看酸碱盐的分类。
大体上可以分为酸性和碱性,分别是含有酸性阴离子(如H+)和碱性阳离子(如
OH-)的物质,而碱性酸碱盐是含有酸性和碱性离子的物质。
此外,酸碱盐还可以根据其结构分为单酸盐和多酸盐,单酸盐是一种仅含一种酸离子的物质,而多酸盐是一种含有多种酸离子的物质。
其次,看看酸碱盐的性质。
酸碱盐的性质主要取决于它们的结构,比如单酸盐和多酸盐的性质是不同的,单酸盐一般有较强的酸性,而多酸盐的酸性则相对较弱。
此外,酸碱盐的溶解性也不同,单酸盐一般溶解性较好,而多酸盐溶解性则差。
最后,我们来看看酸碱盐的用途。
酸碱盐在日常生活中有着广泛的用途,比如它们可以用作食品添加剂,保持食物的口感和口味;也可以用作清洁剂,用来清洁衣服、地板等;也可以用作碱性洗剂;还可以用作消毒剂,用来杀灭有害的细菌等。
总之,酸碱盐是一类重要的物质,其分类、性质和用途都非常重要,可以帮助我们更好地理解它们的特性和性质,并且可以发挥它们的多种用途。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
班级:组别:姓名:组内评价:教师评价:(等第)
课题:酸、碱、盐的定义及分类
【学习目标】1.了解酸、碱、盐的分类
2.能够根据化学式对该物质进行分类
【重点难点】理解酸,碱,盐的初步概念
【自主学习】教师评价:(等第)
请同学们仔细阅读教材、认真自学,然后回答下例问题:(这部分要求同学
们通过预习来独立完成,如不能独立完成,整理好不明白的问题)
写出下列物质的电离方程式
1.酸H2SO4 HCl HNO3
2.碱NaOH KOH Ba(OH)2
3.盐
Na2SO4
KCl
Ba(NO3)2
观察上面的电离方程式,你能发现酸、碱、盐分别有什么特点吗?
酸:
碱:
盐:
【我的疑问】(通过自学你还有哪些疑问?请记录在这里,以便课堂与同学们讨论交流)
【合作探究】(这部分要求同学们在课堂完成,可以讨论、交流)
4.某物质在水中发生电离产生了H+,该物质一定是酸吗?
5.某物质在水中发生电离产生了OH-,该物质一定是碱吗?
6.我们在判断某物质是酸、碱还是盐时,应该注意哪些问题?
7. 请你将物质进行简单的分类,完成以下空白
1. 以下物质
NaCl 固体、铜棒、铁丝、NaOH 固体、铅笔芯、硫酸铜晶体、稀硫酸、稀盐酸、NH 4Cl 固体 能导电的有
; 固体不能导电,但其水溶液能导电的是 ; 属于酸(溶液则指其溶质)的是 ; 属于碱(溶液则指其溶质)的是 ; 属于盐(溶液则指其溶质)的是。
2. 写出下列物质的化学式,并注明物质的类别。
碳酸 ( );五氧化二磷 ( ); 碳酸钠 ( );氢氧化铝 ( ); 氯化亚铁 ( );硫酸亚铁 ( ); 碳酸钙 ( );氯化铁 ( ); 氢氧化钠 ( );氢氧化镁 ( );
【学习日记】
如:
如:
如:
如:。
