北京化工大学2011——2012学年第一学期 《有机化学》(II)期末考试试卷(A)
高等有机期末考试试卷

《高等有机化学》期末考试试卷2011-2012年度第一学期专业:2011级工程硕士 任课教师:郝文燕 副教授一、选择题(至少有一个正确答案)(每小题2分,共24分) 1.COOH SO 3H OHBrCOOH (a)(b)(c)(d)上述化合物的酸性由强到弱的排列顺序为……………………( D )。
(A ) a>b>c>d; (B ) c>d>b>a; (C ) c>b>a>d; (D ) b>a>c>d 。
2.试剂的亲核活性由强到弱的顺序为…………………………( C )。
(A ) CH 3CH 2- > CH 3O -> (CH 3)2N - > F -; (B ) CH 3CH 2- > (CH 3)2N - > CH 3O -> F -; (C ) F -> CH 3O -> (CH 3)2N - >CH 3CH 2-; (D ) (CH 3)2N - >CH 3CH 2-> CH 3O -> F -。
3.t-BuBr ;(a)(b)(c)(d)i-PrBr ;PhCH 2Br ;发生S N 1反应时的相对速度由大到小的顺序为……………( A )。
(A ) a>b>c>d; (B ) d>c>b>a; (C ) c> a > b >d; (D ) b>a>c>d 。
4.如果亲核取代反应发生了重排反应,则该反应的历程为……( A )。
(A )S N 1; (B )S N 2;(C )说不清; (D )可以为S N 1,也可以为S N 2。
5.发生Diels-Alder 反应的立体选择性为………………………( A )。
(A )加热时,同面/同面允许; (B )光照,为同面/同面允许;(C )加热时,同面/异面允许; (D )加热和光照时都没有立体选择性。
北京化工大学有机波谱分析期末考试卷

北京化工大学2012——2013学年第一学期《有机波谱解析》期末考试试卷(A)课程代码 C H M 3 2 2 0 3 T班级:姓名:学号:题号一二三四总分得分可能用到的部分数据:1、部分官能团的红外波数2、部分氢核和碳核的化学位移3、部分原子的相对原子质量元素原子量相对丰度元素原子量相对丰度元素原子量相对丰度H 1.00783 100.0 16O 15.9949 100.0 33S32.9721 0.75D 2.01410 0.015 17O 16.9991 0.04 34S33.9679 4.2112C 12.00000 98.89 18O 17.9992 0.20 35Cl34.9689 75.73 13C 13.00336 1.11 19F 18.9984 100.00 37Cl36.9659 24.47 14N14.0031 99.63 31P 30.9738 100.00 79Br78.9183 50.69 15N15.0001 0.37 32S 31.9738 95.02 81Br80.9163 49.31一、填空题:(30分,每题3分)1、核磁中,heptet 峰(I =1/2)中每个峰的峰面积比为 。
2、核磁碳谱中,如何鉴别顺-2-丁烯和反-2-丁烯: , 为什么: 。
3、核磁共振碳谱中,进行定量分析的去偶技术为: 。
(填宽带去偶、偏共振去偶、门控去偶、反门控去偶、选择性去偶)4、分子式为C 6H 10ClBr 的化合物,质谱中,其M : M+2: M+4的比例为: 。
5、通过红外光谱,如何区别丙醛和丙酮: 。
6、紫外光谱中,哪一个能级的跃迁,需要能量最低: 。
(一般的能级有σ、π、σ*、π*、n 。
)7、如何通过核磁鉴别如下两非对映异构体 ,简述其具体鉴别过程: 。
rr H 3rr H 3an d8、已知氘元素的I =1,请问用CD 2Cl 2做溶剂测定物质的碳谱时,在54.0 ppm 处溶剂峰被裂分为 几重峰,峰的比例为 。
大学有机化学期末考试题(含三套试卷和参考答案)

一 . 命名以下各化合物或写出结构式(每题 1 分,共 10 分)1.(H3C)2HCC(CH 3)3C CH H2.3-乙基-6-溴-2-己烯-1-醇3.O 4.5. CH 3CHO邻羟基苯甲醛6.苯乙酰胺7.OH8.对氨基苯磺酸9.COOH10.甲基叔丁基醚二. 试填入主要原料,试剂或产物(必需时,指出立体结构),达成以下各反响式。
(每空 2 分,共 48 分)1.CH CHBrKCN/EtOHCH2Cl2.11 / 241 / 242 / 242 / 24高温 、高压①O3+ C12② H 2O Zn 粉3.HBrMgCH = CH 2醚CH 3COC14.+CO 2CH 35.1, B 2H 62, H 2O 2, OH -1, Hg(OAc) 2 ,H 2 O-THF 2, NaBH 46.OOOOO7.CH 2ClNaOH H 2O Cl8.CH 3+ H 2O OH-SN1 历程Cl+9.OCH 3 O C 2 H 5 ONa+ CH 2=CH C 2 H 5 ONaC CH 3O10.① CH 3COCH 3② H 2O H +23 / 243 / 24BrBrZnEtOH11.OH+C CH 3 + Cl 212.CH 3HNO 3Fe,HCl(CH 3CO) 2O( 2)H 2SO 4Br 2NaOHNaNO 2 H 3 PO 2H 2SO 4三 . 选择题。
(每题 2 分,共 14 分)1. 与 NaOH 水溶液的反响活性最强的是()(A). CH 3CH 2COCH 2Br (B). CH 3CH 2CHCH 2Br (C). (CH 3 )3CH 2Br (D). CH 3(CH 2)2CH 2BrCH 32. 对 CH 3Br 进行亲核代替时,以下离子亲核性最强的是: ( )(A). CH 3COO - (B). CH 3CH 2O - (C). C 6H 5O - (D). OH -3. 以下化合物中酸性最强的是()(A) CH 3CCH(B) H 2O (C) CH 3CH 2OH (D) p-O 2NC 6H 4OH(E)CHOH(F) p-CH C H OH6 53 6 44. 以下化合物拥有旋光活性得是: ()COOHA,HOHCH 3B, HCOOHOHCH 3C, (2R, 3S, 4S)-2,4- 二氯 -3- 戊醇5. 以下化合物不发生碘仿反响的是 ( ) A 、 C 65 3、2 5H COCH3B CHOHC 、 CH 3 22D 、 32 3CHCOCHCH CHCOCHCH34 / 244 / 246. 与 HNO 2作用没有 2 生成的是( )A 、H 22 NB 3 2NCONH、CHCH ( NH )COOHC 、C 6 53 D6 52H NHCH、CHNH7. 能与托伦试剂反响产生银镜的是 ( )A 、 CCl 3COOH B、 3C 、 CH CHCOOHClCOOHD、 HCOOH2四 . 鉴识以下化合物(共 6 分)苯胺、苄胺、苄醇和苄溴五 . 从指定的原料合成以下化合物。
《有机化学》期末试卷及答案
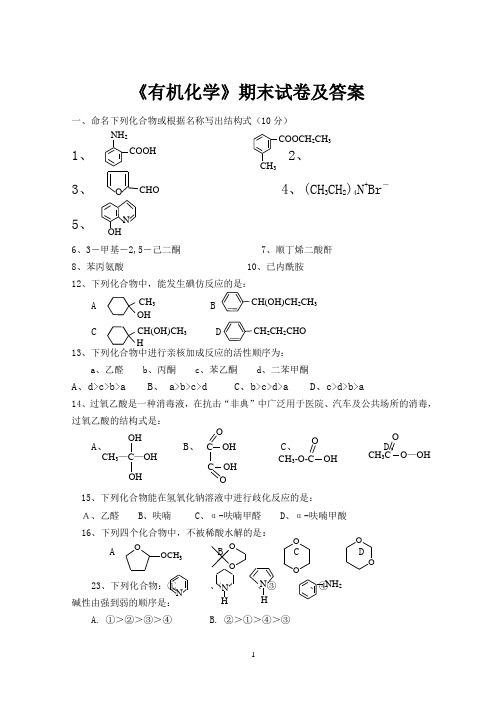
《有机化学》期末试卷及答案10分)1、 2、3、 4、(CH3CH2)4N+Br-5、6、3-甲基-2,5-己二酮7、顺丁烯二酸酐8、苯丙氨酸 10、已内酰胺12、下列化合物中,能发生碘仿反应的是:A BC D13、下列化合物中进行亲核加成反应的活性顺序为:a、乙醛b、丙酮c、苯乙酮d、二苯甲酮A、d>c>b>aB、 a>b>c>dC、b>c>d>aD、c>d>b>a14、过氧乙酸是一种消毒液,在抗击“非典”中广泛用于医院、汽车及公共场所的消毒,过氧乙酸的结构式是:A、 B、 C、 D、15、下列化合物能在氢氧化钠溶液中进行歧化反应的是:A、乙醛 B、呋喃 C、α-呋喃甲醛 D、α-呋喃甲酸16、下列四个化合物中,不被稀酸水解的是:A B C D23、③、④A. ①>②>③>④B. ②>①>④>③2CH(OH)CH2CH3(23CH33OHCH(OH)CH33H 2CH2CH2CHO(23COOCH2CH3CH3O CHOHN NH2OOCH3OOOOCH3—C—OHOHOH OCH3C O—OHOCH3-O-C OHC OHC OHOO浓硝酸+浓硫酸300℃C. ③>④>①>②D. ①>③>②>④ 三、填空完成反应式(每格1分,共20分)28、29、 2 30、31+ RMgX ( ) 32、 CHO+ ( ) CH 2OH33、CHONaOH(浓) ( )+( ) ( )CH 3INHNH2CC O OO+ CH 3CH 2OH ( )H 2O( )(过量)NO 2Fe / HCl ( )( )34、 ( )四、鉴别下列各组化合物(10分) 35、丙 酮丙氨酸 丙酰氯 丙烯腈36、37、 甲酸乙酸 乙醛五、推导结构式(10分)2CH 3ICH 3I( )( )( )( )38、某D 型己醛糖(A ),用HNO 3氧化生成有光学活性的糖二酸(B );(A )经降解得到戊醛糖(C ),(C )经HNO 3氧化生成无光学活性的糖二酸(D );将(C )再进行降解,得到丁醛糖(E ),(E )经HNO 3氧化生成内消旋酒石酸(2,3-二羟基丁二酸)。
北京化工大学高分子材料基础理论试卷附标准答案

北京化工大学2011——2012学年第一学期《高分子材料基础理论》期末考试试卷班级:姓名:学号:分数:一、选择题(多项选择,每题2分,共20分)1 下列聚合物中,碳链聚合物有( )。
A 聚氯乙烯 B聚酰胺 C 聚甲基丙烯酸甲酯 D 聚碳酸酯2 常用高聚物结晶度的测试方法有()。
A 扫描电镜B 差示扫描量热仪DSC C 热膨胀计D X射线衍射3 下列聚合物中,单根高分子链柔顺性最大的是( )。
A 聚氯乙烯B 聚丙烯(全同)C 聚二甲基硅氧烷D 聚苯乙烯4 下列高聚物中本体(不加添加剂)透明的聚合物有()。
A 聚丙烯B 聚氯乙烯C 聚碳酸酯D 聚乙烯5 高分子的远程结构主要包括()。
A 单体单元的化学组成B 高分子的大小C 高分子的形状D 高分子的构象6 下列有关高聚物分子量及分子量分布对材料性能的影响,描述正确的有()。
A 分子量增大,材料的表观粘度增大B 分子量增大,材料的拉伸强度增大C 分子量分布较宽,对改善材料的加工性能有利D 分子量增大,材料的流动性增加7 在挤出和注射成型前必须要进行严格干燥的高聚物有()A 聚乙烯B 聚氯乙烯C 尼龙D 聚甲基丙烯酸甲酯8 能提高高分子材料强度的措施包括()。
A 交联B 降低结晶度C 添加增塑剂D 添加玻璃纤维9 从分子运动观点分析,下列高聚物中抗蠕变能力最强的是( )A 聚苯醚B 聚四氟乙烯C 聚氯乙烯D 聚乙烯10 高聚物的零切粘度越高,说明其( )A 分子间作用力越小B 分子链越柔顺C 分子链越刚硬或者分子间作用力越大D 表观粘度对温度越敏感二填空题(每空1分,共25分)1.高分子化合物是指分子量很高,并由( 1 )连接的一类化合物,分子量通常高达( 2 ),高分子英文表述为( 3 )。
2.根据聚合反应机理,聚合反应可分为两大类,大分子链瞬时形成,延长反应时间对分子量影响不大的聚合反应是( 4 );延长反应时间能提高聚合物分子量的聚合反应是( 5 )。
年基础化学期末考试卷用于合并

北京化工大学2011——2012学年第一学期《基础化学》期末考试试卷所有题目全部答在试卷上一、是非题(判断下列叙述是否正确,正确的在括号中画√,错误的画×)(本大题分10小题,每小题1分,共10分)()1.1.0 ⨯10- 8 mol⋅L-1的HCl溶液,其pH为8.00;()2.任何一对共轭酸碱对均可以组成缓冲溶液;( ) 3. 对零级反应来说,反应速率与反应物浓度无关;()4.某物质的Kɵsp越大,其溶解度也越大;()5. 原电池中负极发生氧化反应,正极发生还原反应;()6.电极电势不具有加和性;()7.EDTA是很多金属离子的螯合剂,在水溶液中是四元弱酸;()8.元素的标准电极电势图: A—B—C—D中,若EɵB/C< EɵA/B, 则B不可能发生歧化反应;()9.某一元弱酸,其浓度越小,其解离度就越大;()10. 由于生成配离子,Ag(Ⅰ)的氧化性增强;二、单项选择题(在下列各题中,选择出符合题意的答案,将其代号填入括号内)(本大题分10小题,每小题2分,共20分)1.下列有关氧化还原反应的表述中,正确的是:(A) 强氧化剂参与的氧化还原反应是不可逆反应,因此无法写出其平衡常数;(B)氧化还原反应也是可逆反应,其平衡常数Kɵ可由公式∆r Gɵm = RT ln Kɵ求得;(C) 氧化还原反应中氧化剂得到的电子数等于还原剂失去的电子数;(D) 原电池中的氧化还原反应在同一处发生。
2.下列物质不是一元酸的是: (A) H 3BO 3(B) H 3PO 2(C) HClO 4(D) H 3PO 33.浓差电池:(-)Zn |Zn 2+(c 1 mol .L -1) || Zn 2+(c 2 mol .L -1) | Zn(+) , 已知V E 76.0/Zn)Zn (2θ-=+,则下列说法正确的是:(A) 为提高电池电动势,可在负极处通入HCl 气体 (B) 为提高电池电动势,可在正极处加入氨水 (C) 若c 1/c 2=104,则电池电动势为0.24V (D) 若c 2/c 1 =104,则电池电动势为0.12V 4.下列关于周期表各族元素论述正确的是: (A) 非金属都是主族元素,金属都是副族元素 (B) VIIA 族元素都是非金属(C) IV A 族与IVB 族元素最外层都只有4个价电子 (D) IA 族与IB 族元素的最高价态为+15.在EDTA 滴定金属离子时,副反应系数α Y 与酸效应系数αY(H)、干扰离子效应系数αY(N)的关系为:(A) αY = αY(H)αY(N) (B) αY = αY(H) + αY(N) (C) αY = αY(H) + αY(N) -1 (D) αY = αY(H)αY(N) -16.下列关于物质中酸性强弱顺序正确的是:(A) HF > HCl > HBr > HI (B) H 4SiO 4 < H 3PO 4 < H 2SO 4 < HClO 4 (C) H 5P 3O 10 < H 4P 2O 7 < H 3PO 4 (D) HClO > HClO 2 > HClO 3 > HClO 47.在H 3PO 4溶液中加入一定量的NaOH 后,其溶液pH 为9.78,则此溶液中下列物种浓度最大的是(已知H 3PO 4的p K ɵa,1=2.15,p K ɵa,2= 7.20, p K ɵa,3= 12.35): (A) H 2PO 4-(B) H 3PO 4(C) PO 43-(D) HPO 42-8.向Mg(OH)2的饱和溶液中加入MgCl 2,使[Mg 2+] 为0.0010mol ⋅L -1,则该溶液的pH 为(已知K ɵsp(Mg(OH)2)=1.8⨯10-11): (A) 8.63 (B) 10.13(C) 3.87 (D) 5.379. 下列物质中能组成碱性缓冲溶液的是:(A) 0.1mol ⋅L -1HOAc 与0.05 mol ⋅L -1NaOH 溶液等体积混合 (B) 0.1 mol ⋅L -1 H 2C 2O 4与0.05 mol ⋅L -1NaOH 溶液等体积混合 (C) 0.1 mol ⋅L -1H 3PO 4与0.05 mol ⋅L -1NaOH 溶液等体积混合 (D) 0.1 mol ⋅L -1H 3PO 4与0.25 mol ⋅L -1NaOH 溶液等体积混合10. 已知K ɵb (NH 3⋅H 2O)=1.8×10-5,欲配制1.0 L pH=10.00、c (NH 3⋅H 2O)=0.10mol ⋅L -1的缓冲溶液,需用(NH 4)2SO 4的物质的量为:(A) 9.0×10-3mol (B)1.8×10-2mol (C) 0.050mol (D) 9.0×10-2mol三、填充题(根据题意,在下列各题的横线处,填上正确的文字,符号或数值)(本大题分10小题,每空1分,共20分)1.NH4HCO3的质子条件式为。
基础化学期末考试卷

(C)分子中具有三中心四电子的大∏键 (D)分子中具有三中心二电子的大∏键 5、已知:E (Cl2/Cl-)=1.36V, E (MnO2/Mn2+)=1.23V,实验室利用 MnO2 与浓盐酸反应制备
Cl2,此时由两电对 MnO2/Mn2+和 Cl2/Cl-组成的原电池的电动势为(
)。
(A)E <0,E<0
。 ;多原子分子
单质有(至少给出 2 个例子)
;巨型分子单质有(至少给出
3 个例子)
;
8、用 EDTA 准确滴定金属离子 M2+的必要条件为_________。
9、[Cu(NH3)3]2+ 的累积稳定常数 β3 与反应[Cu(NH3)2]2+ + NH3 _________ (填“相同”or“不同”)。
(C) CH4 > H2O > NH3 > HF
(D) HF > H2O > NH3> CH4
3、下列物质中,还原性最强的是( )。
(A)MnO4-
(B)CrO42-
(C)CoO(OH)
(D)Fe(OH)2
4、有关 B2H6 分子的叙述正确的是( )。
(A)具有强还原性,燃烧时可放出大量的热
(B)分子结构式为
4、EDTA 在水溶液中是______ 元酸,在水溶液中的形式分别为_______________________。 5、以反应 Cr2O72- + 6Cl- +14H+ = 2Cr3+ + 3Cl2(g) + 7H2O 组成原电池,其标准态的电池符号为
。
6、(NH4)2HPO4 水溶液的质子条件式为 7、常见的小分子单质有(至少给出 5 个例子)
高等有机化学习题与期末考试题库(二)

高等有机化学习题与期末考试题库(二)高等有机化学习题与期末考试题库(二) .....下载可编辑.高等有机化学习题及期末复习一、回答下列问题:(22小题,1-14每题1分,15-22,每题2分,共30分)1.亲核反应、亲电反应最主要的区别是( ) A.反应的立体化学不同 B.反应的动力学不同 C.反应要进攻的活性中心的电荷不同 D.反应的热力学不同2.下列四个试剂不与3-戊酮反应的是( ) A.RMg_ B.NaHSO3饱和水溶液 C.PCl3 D.LiAlH4 3.指出下列哪一个化合物(不)具有旋光性? 4.区别安息香和水杨酸可用下列哪种方法 A.NaOH(aq) B.Na2CO3(aq)C.FeCl3(aq)D.I2/OH-(aq) 5.比较下列化合物的沸点,其中最高的是 6.指出下列哪一个化合物的紫外吸收光谱波长最短( ) 7.下列化合物在常温平衡状态下,最不可能有芳香性特征的是( ) 8.下列含氧化合物最难被稀酸水解的是( ) .. ...下载可编辑. 9.二环乙基碳亚胺(DCC)在多肽合成中的作用是( ) A.活化氨基 B.活化羧基 C.保护氨基 D.保护羧基 10.比较下列化合物在 H 2SO 4 中的溶解度( ) 11.下列关于α-螺旋的叙述,错误的是( ) A.分子内的氢键使α-螺旋稳定 B.减少 R 基团间的不同的互相作用使α-螺旋稳定 C.疏水作用使α-螺旋稳定 D.在某些蛋白质中α-螺旋是二级结构的一种类型 12.比较苯酚(I)、环己醇(II)、碳酸(III)的酸性大小 A.II>I>III B.III>I>II C.I>II>III D.II>III>I 13.1HNMR 化学位移一般在 0.5-11ppm ,请归属以下氢原子的大致位置:A.-CHOB.-CH=CHC.-OCH 3D.苯上 H 14.按沸点由高到低排列的顺序是:()>()>()>()>()。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
北京化工大学2011——2012学年第一学期《有机化学》(II)期末考试试卷(A)专业、班级:姓名:学号:一、用系统命名法命名化合物,必要时标明构型(R/S,顺/反或Z/E)。
每题1分,共12分。
二、选择题(每题只有一个答案,每题1分,共15分。
适用于应化、化工、高材专业重修生)1. 下列化合物中,不能发生Friedel-Crafts烷基化反应的是()A. 苯甲醚B. 硝基苯C. 乙苯D. 苯酚2. 芳香族伯胺发生重氮化反应是在()溶液中进行。
A、强酸性B、中性C、碱性D、强碱性3. 下列化合物中能与土伦试剂发生反应的是()A. 葡萄糖B. 果糖C. 苯乙酮D. 丙酮4. 下列化合物哪一个是酸酐()A. B. C. D.5.下列化合物烯醇式含量最多的是:()A、B、C、D、6. 下列化合物碱性最强的是()A. 苯胺B. 三乙胺C. 乙酰苯胺D. 氨气7. 下列化合物酸性最大的是()A. 邻硝基苯酚;B. 间硝基苯酚;C. 对硝基苯酚;D. 苯酚8. 不能与饱和亚硫酸氢钠反应产生沉淀的是()A、甲醛B、苯乙酮C、2-丁酮D、环己酮9. 下列负离子亲核性性最大的是( )A、B、C、D、10. 下列化合物不能发生碘仿反应的是()A. CH3CHOB. CH3COOHC. CH3CH(OH)CH3D. CH3COCH2CH311. 下列化合物发生醇解反应活性最小的是()A. 乙酰氯B. 乙酸酐C. 乙酰胺D. 乙酸乙酯12. 下列化合物与卢卡斯试剂发生反应,速率最快的是()A、叔丁醇B、1-丙醇C、2-丙醇;D、苄醇13.能使三氯化铁溶液变成蓝紫色的是()A、乙酰丙酮B、甲醇C、丙酮;D、苯甲醇14.根据休克尔规则,下列结构中不具有芳香性的是()A. B. C. D.15. 发生亲核加成反应活性最高的是()A、苯甲醛B、丙烯醛C、丙醛D、丙酮三、完成下列反应(每空1分。
应化学生答第1-14小题,共30分;高材、化工重修生答第1-8及第15-22小题,共36分)四.写出下列反应的反应机理(本大题两个小题都适用于应化专业,总分6分;第2小题适用于高材专业重修生,总分3分。
本大题不适用于化工专业重修生)。
1.2.五、用简单的化学方法鉴别下列化合物1、A. 乙胺 B. 二乙胺 C. 三乙胺 D. 乙酸(3分,本小题仅适用于应化专业)2、A. 丙醛 B. 丙酮 C. 丙醇 D. 异丙醇(3分,本小题适用于高材、化工重修生,应化专业做此题不给分)3、(2分,本小题适用于高材、化工重修生,应化专业做此题不给分)六、结构推断题(共10分。
第1、2、3小题适用于应化专业;高材只适用于第1小题;化工专业重修生只适用于第1、3小题。
具体评分见相应小题后)1、化合物A含有C、H、O、N四种元素,溶于水,不溶于乙醚。
A受热后失去一分子水生成化合物B,B与氢氧化钠水溶液回流反应,放出有气味的气体,残余物酸化后得到一种不含氮的酸性物质C。
C与氢化铝锂反应生成的物质D与浓硫酸共热,得到一个烯烃E,E的相对分子量为70。
E经臭氧化-还原反应后得到一个醛F和一个酮G。
根据以上实验结果推断化合物A到G的构造,并写出各步反应式(5分)。
2、Compound A: C4H8O2. 1H NMR = 1.00 (t, J=7.4 Hz, 3H); 1.65 (sextet, J=7.5 Hz, 2H); 2.31 (t, J=7.4 Hz, 2H); 11.68 (s, 1H) ppm. 13C NMR = 13.4, 18.5, 36.3, 179.6 ppm. (2分)Compound A:3、化合物A的分子式为C6H12O,A能与苯肼作用但不发生银镜反应,A经催化氢化得分子式为C6H14O的B,B与浓硫酸共热得C(C6H12)。
C经臭氧化并水解得D与E。
D能发生银镜反应,但不起碘仿反应,而E能发生碘仿反应而无银镜反应。
写出A~E的结构式及各步反应式。
(3分)七、合成题(共24分):用碳数≤4的烯烃、乙炔、苯、甲苯、乙酰乙酸乙酯或丙二酸二乙酯为原料,无机试剂任选。
(第1-6题适用于应化专业,第3-8适用于高材专业,第4-9适用于化工专业)2.1.3. 4.6.5.7.8.9.北京化工大学2011——2012学年第一学期《有机化学》(II)期末考试参考答案一、用系统命名法命名化合物,必要时标明构型(R/S,顺/反或Z/E)。
每题1分,共12分。
CH 3CH 3H 3CCOOCH 3COOCH 313. 2,3,6-三甲基-4-丙基-辛烷 14. 3-苯基-2-溴-2-戊烯-1-醇 15. (2R,3S )-2-甲基-3-溴-戊醛16. 环氧氯丙烷17.18.二、选择题(每题只有一个答案,每题1分,共15分。
适用于应化、化工、高材专业重修生)1.B2.B3.A4.D5.D6.B7.C8.B9.D 10.B 11.C 12.A(D) 13.A 14.C 15.C三、完成下列反应(每空1分。
应化学生答第1-14小题,共30分;高材、化工重修生答第1-8及第15-22小题,共36分)1.2.3.4.5.6.7.8.9.10.NO 2HOH 2CHOH 2C HOH 2C11.12.13.14.15.16.17.18.19.20.21.22.四.写出下列反应的反应机理(本大题两个小题都适用于应化专业,总分6分;第2小题适用于高材专业重修生,总分3分。
本大题不适用于化工专业重修生)。
1.2.H ++HO(CH 2)4CH=OHOH OH +-H +O OH H +O OH2+O -H 2O+C 2H 5OHO OHC 2H 5+-H +O OC 2H 5五、用简单的化学方法鉴别下列化合物六、结构推断题(共10分。
第1、2、3小题适用于应化专业;高材只适用于第1小题;化工专业重修生只适用于第1、3小题。
具体评分见相应小题后)1.2.H3C H2CCH2OHO3.七、合成题(共24分):用碳数≤4的烯烃、乙炔、苯、甲苯、乙酰乙酸乙酯或丙二酸二乙酯为原料,无机试剂任选。
(第1-6题适用于应化专业,第3-8适用于高材专业,第4-9适用于化工专业)1.2.H3C CH2H2C2H5COOC2H5COOC2HCOOC2H222Cl2ClH2C2H5COOC2H5C HONaCH2ClCH2ClCOOC2HCOOC2HNH3CONH223.324NOSnCl2HClNH乙酸酐NHCOCH3324O2N NHH2OO2N N2+Cl-3H2SO42SnCl2HCl2H3C H3C H3COHH3COHH3C+TM4.CH2CH2SOCl2+CH2CH2ClCH2CH3AlCl324CH2CH3NO2 CH2CH3NO2BrZn,NH4ClCH2CH3NH2BrNaNO2,HClH2OCH2CH3OHBrNaOHCH2CH2ClTM5.CH 2CH 2OH SOCl 2CH 2CH 2Cl H 2SO 4SO 3HOHH 2OHCrO3吡啶Mg CH 2CH 2MgCl HO H 2C CH 3H 2SO 4TM6.+CH 3CH 2CH=CH 2HBr hvCH 3CH 2CH 2CH 2Br Mg ether3CH 2CH 2CH 2MgBrCH 2=CH2O CH 3CH 2CH 2CH 2CH 2CH 2H 2OKMnO 4TM7.CH 3CH 2CH=CH 2B 2H 6CH 3CH 2CH 2CH 2H 2O 2NaCH 3CH 2CH 2CH 2ONaCH 3CH=CH NBS hvBrCH 2CH=CH 2BrCH 2CH=CH 2TM8.CH 3NBS hvCH 2BrH HNaNaNaCH 2CH 2Lindlar cat.H TM9.CH 3Cl 2hvCH 2ClNaCNCH 2+H 2ONaOH TM。
