供应商不合格质量信息反馈表表
质量信息反馈表

分析处理要求:
质量管理部负责人: 年 月 日
□A □B □C □D
要求回答日期:
年 月 日
分析处理
原因分析:
工艺员签名:
技术研发部
处理意见:
技术研发部负责人: 年 月 日 工艺员: 年 月 日
研究/改善
纠正措施:
部门负责人: 年 月 日 执行人: 年 月 日
责任部门
有效性验证
验证结论:
质量管理部负责人: 年 月 日 检验员: 年 月 日
质量管理部
联
络
产品名称
发现者:
电 话:
日 期:
(现场)
确认人
填报人
反
馈
部
门
型号:
生产周期/编号:
பைடு நூலகம்客户
问题产品数量
发生
场所
客户现场
问题陈述:
附:□问题产品 □用户传真 □照片 □其他
(用户)意见/建议:
更换产品
□更换产品 □销账处理□进行书面回复 □其他
受理发
行
受理
编号
受理人:陈迪
(责任)部门调查、确认
质量管理部
服务质量信息反馈表

项目名称
项目负责人
服务类型
服务信息反馈情况
序号
信息反馈项目
服务单位信息反馈意见
1
咨询对象和范围等是否符合合同的约定。
□是 □否
2
对策措施与建议是否符合咨询项目实际、遵循针对性、技术可行性和经济合理性。
□是 □否
3
咨询过程是否公正、客观和独立。
□是 □否
4
咨询服务的质量。
□优秀 □良好 □一般 □较差ቤተ መጻሕፍቲ ባይዱ
5
咨询人员的业务能力。
□优秀 □良好 □一般 □较差
6
咨询人员的服务态度。
□优秀 □良好 □一般 □较差
7
对我公司的整体满意度。
□非常满意 □基本满意 □不满意
对公司和咨询人员的其他意见和建议
委托咨询单位(盖章或签字)
年 月 日
HTQP1001纠正预防措施控制程序

1、目的通过对已发生或潜在性不合格进行原因分析,并采取有效的纠正措施或预防措施,实现不断的质量改进,使类似问题发生可能性减少到最低限度,防止已经发生的不合格品再次发生和潜在不合格发生。
2、适用范围本程序适用于公司不合格过程、不合格品和质量管理体系有关的不合格采取的纠正和预防措施。
3、术语及定义3.1 纠正:为消除已发现的不合格所采取的措施,使其满足规定的要求。
3.2防错:在产品的设计和制造过程中,采用消除错误的技术,防止制造不合格产品。
防错方法一般有:改进工艺、制作固定或专用工装、采用报警装置、目标管理、看板管理、颜色管理等。
3.3 纠正措施:为消除已发现的不合格或其他不期望情况的原因所采取的措施,防止不合格的再发生。
3.4 预防措施:为消除潜在的不合格或其他潜在不期望情况的原因所采取的措施,防止不合格的发生。
3.5潜在不合格:指现在尚未发生,但有趋势或迹象可预期将发生的产品质量/交付/服务等不合格。
4 、职责4.1质量部门:是纠正预防措施的归口管理部门,负责组织纠正和预防措施的制定、跟踪和验证;外部质量信息的收集、反馈和汇总分析;对质量问题及不符合项进行收集和趋势汇总分析。
4.2技术部门:负责纠正、预防措施涉及有关的技术文件的更新。
4.3各部门/车间:负责本部门不合格项的原因分析和纠正预防措施的制定和实施。
参与纠正、预防措施的制定,负责相关措施的实施。
4.4 供应商管理部门:负责督促供方不合格项的原因分析及纠正、预防措施的制定和实施;4.5分管领导:负责纠正、预防措施的批准、协调和监督。
5工作流程描述5.2预防措施流程:5.3工作要点描述6、支持性文件《持续改进程序》《不合格品管理程序》7、记录8程序变更记录。
客户投诉反馈表

客户投诉反馈表
尊敬的客户,
非常感谢您选择我们的产品/服务,并且对我们的工作给予了反馈。
我们非常
重视您的意见和建议,为了更好地改进我们的工作,我们制定了客户投诉反馈表。
请您在下面的表格中填写相关信息,以便我们能够更好地了解您的问题并及时解决。
客户投诉反馈表
1. 姓名:
2. 联系方式:
3. 投诉日期:
4. 产品/服务名称:
5. 投诉内容:
请您详细描述您的投诉内容,包括但不限于以下方面:产品质量、服务态度、
交付时间、售后支持等。
我们将根据您的描述来分析问题所在,并采取相应的措施进行改进。
6. 解决方案:
请您提供您希望我们采取的解决方案。
我们将尽力满足您的要求,并在合理范
围内提供解决方案。
如果您没有特定要求,我们将根据您的投诉内容进行分析,并给出我们认为合适的解决方案。
7. 其他补充信息:
如果您有其他补充信息或者建议,请在此处填写。
我们将认真阅读并考虑您的
意见,以便进一步改进我们的工作。
请您将填写完毕的表格发送至我们的客户服务邮箱(邮箱地址),或者直接回复此邮件。
我们会尽快处理您的投诉,并在3个工作日内给予您答复。
再次感谢您的反馈,我们衷心希望能够给您带来更好的产品和服务。
如果您对我们的工作还有其他意见或建议,也请随时与我们联系。
祝您生活愉快!
此致,
XXX公司。
对供应商反馈意见范文 (3页)

本文部分内容来自网络整理,本司不为其真实性负责,如有异议或侵权请及时联系,本司将立即删除!== 本文为word格式,下载后可方便编辑和修改! ==对供应商反馈意见范文篇一:供应商年度评价表供应商年度评价表供应商名称:供应商代码:评审日期:年月日说明:一、供应商共分为A,B,C,D四级.90分以上为A级供应商,可优先落单; 70~89.5分为B级供应商,可分配部分订单;60~69.5分为C级供应商,限期改善,根据改善效果决定是否继续采购; 60分以下为D级供应商,取消供方资格;二、评分标准1. 此表每年度评审一次。
2. 合格率=(合格批数÷供货批数)×100%3. 交期达成率=(按时交货批数÷供货批数)×100% 4. 品质实际得分=50×合格率 5. 交期得分=20×交期达成率6. 价格得分:高0~5分,偏高6~10分,适中11~15分(以同行业价格比校),由采购部考核。
7. 配合度得分由品质,PMC,采购各分配5分.改善对策分扣分原则不回复质量异常反馈单扣5分;超过要求时间回复每次扣3分;无实际改善效果每次扣5分。
WF-ZYB-010/A篇二:供应商质量处罚通知供应商处罚通知篇三:合格供应商评审及管理办法商城公司合格供应商评审及管理办法第一条、为加强供应商管理,建立合格供应商优选机制,确保公司物资采购和外包服务规范有序,特制定本办法。
第二条、评审对象:商城总公司及各分公司对大额采购以外的物资采购、委托加工(制作)、物业维护保养、保安保洁、花草租赁、车辆维保、保险等服务供应商,其他保持长期合作关系的供应、服务商。
第三条、评审时间:原则上每年度评审一次,特殊情况的可半年度或季度评审。
年度评审在每年3月底之前完成对供应商的年度评审工作,评选出合格供应商进行分类管理并及时更新档案。
第四条、评审人员:公司采购工作领导小组为供应商评审牵头组织机构,具体评审工作由涉及采购的相关公司、部门、专业人员负责实施。
质量信息传递反馈表

质量信息传递反馈表
编号:MLH-ZD-005 【5-1(18】
信息名称:总局关于39批次药品不合格的通告(2017年第193号)
信息来源:国家食品药品监督管理局
收集时间:2017年12月04日
收 集 人:***
信息等级:B类
信息主体:经中国食品药品检定研究院等11家药品检验机构检验,标示为吉林省力胜制药有限公司等19家企业生产的39批次药品不合格。现将相关情况通告如下:
一、不合格产品的标示生产企业、药品品名和生产批号为:
吉林省力胜制药有限公司生产的批号为20160902、20160903、20161002、20161102的安胃片,甘肃佛仁制药科技有限公司生产的批号为150902、151101、160301、170201的安胃片,山西云鹏制药有限公司生产的批号为D150501、D150502、D160201、D160602的安胃片,山西汾河制药有限公司生产的批号为170202的吡拉西坦片,山东仁和堂药业有限公司生产的批号为160601的吡拉西坦片,大同市云岗制药有限公司生产的批号为161214的硫酸庆大霉素颗粒,丹东宏业制药有限公司生产的批号为20160404、20160702的硫酸庆大霉素碳酸铋胶囊,上海全宇生物科技确山制药有限公司生产的批号为1605051的硫酸庆大霉素碳酸铋胶囊,太极集团重庆桐君阁药厂有限公司生产的批号为17030008的龙胆泻肝片,山东齐都药业有限公司生产的批号为1C16120305的羟乙基淀粉130/0.4氯化钠注射液,山东华鲁制药有限公司生产的批号为D17021802、D17012504、D17021601、D16102201、D17012402的羟乙基淀粉130/0.4氯化钠注射液,焦作联盟医用材料股份有限公司生产的批号为20160501的曲安奈德新霉素贴膏,上海金不换兰考制药有限公司生产的批号为20160506的曲克芦丁片,六安华源制药有限公司生产的批号为161120022-A的替硝唑氯化钠注射液,天津儿童药业有限公司生产的批号为20160502的头孢克洛颗粒,焦作市银河药业有限公司生产的批号为20160310、20160405、20160407、20160409、20160506的头孢拉定颗粒,广西邦琪药业集团有限公司生产的批号为160327、160525的头孢拉定颗粒,辽宁丹生生物制药有限公司生产的批号为20160801的胰酶肠溶片,陕西中医学院制药厂生产的批号为160701、17A01的银翘解毒合剂。不合格项目包括含量测定、脆碎度、装量差异、溶出度、微生物限度、可见异物、效价测定、性状等(详见附件)。
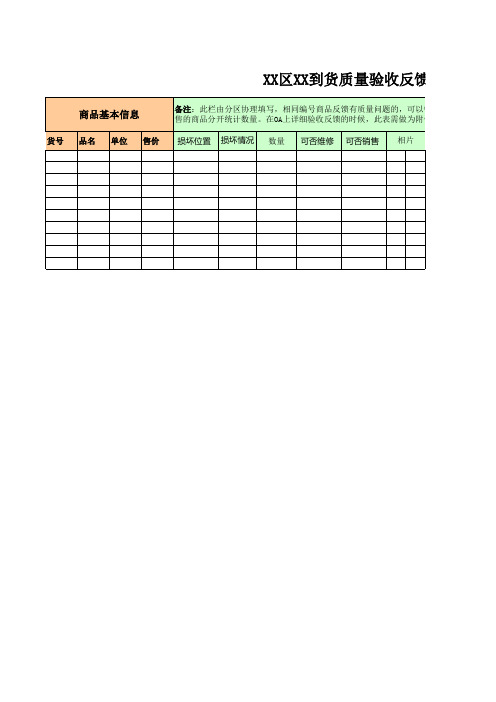
到货质量验收反馈表
问题的,可以销售和不可以销 此表需做为附件上传。 文字性反馈内容
XX区XX到货质量验收反馈表(第二阶段
商品基本信息
货号 品名 单位 售价 备注:此栏由分区协理填写,相同编号商品反馈有质量问题的,可以销售和不可以销 售的商品分开统计数量。在OA上详细验收反馈的时候,此表需做为附件上传。 损坏位置 损坏情况 数量 可否维修 可否销售 相片
验收反馈表(第二阶段)
办公室主任点评 (优+、优、良+、 良、一般、差) 办公室主任签字 (反馈情况是否属实) 仓库解决方案意见
纠正预防措施控制程序

1、目的通过对已发生或潜在性不合格进行原因分析,并采取有效的纠正措施或预防措施,实现不断的质量改进,使类似问题发生可能性减少到最低限度,防止已经发生的不合格品再次发生和潜在不合格发生。
2、适用范围本程序适用于公司不合格过程、不合格品和质量管理体系有关的不合格采取的纠正和预防措施。
3、术语及定义3.1 纠正:为消除已发现的不合格所采取的措施,使其满足规定的要求。
3.2防错:在产品的设计和制造过程中,采用消除错误的技术,防止制造不合格产品。
防错方法一般有:改进工艺、制作固定或专用工装、采用报警装置、目标管理、看板管理、颜色管理等。
3.3 纠正措施:为消除已发现的不合格或其他不期望情况的原因所采取的措施,防止不合格的再发生。
3.4 预防措施:为消除潜在的不合格或其他潜在不期望情况的原因所采取的措施,防止不合格的发生。
3.5潜在不合格:指现在尚未发生,但有趋势或迹象可预期将发生的产品质量/交付/服务等不合格。
4 、职责4.1质量部门:是纠正预防措施的归口管理部门,负责组织纠正和预防措施的制定、跟踪和验证;外部质量信息的收集、反馈和汇总分析;对质量问题及不符合项进行收集和趋势汇总分析。
4.2技术部门:负责纠正、预防措施涉及有关的技术文件的更新。
4.3各部门/车间:负责本部门不合格项的原因分析和纠正预防措施的制定和实施。
参与纠正、预防措施的制定,负责相关措施的实施。
4.4 供应商管理部门:负责督促供方不合格项的原因分析及纠正、预防措施的制定和实施;4.5分管领导:负责纠正、预防措施的批准、协调和监督。
5工作流程描述5.1纠正措施流程:5.2预防措施流程:5.3工作要点描述6、支持性文件《持续改进程序》《不合格品管理程序》7、记录8程序变更记录。
