高中化学奥林匹克竞赛专题练习:有机化合物的合成
完整版)高中化学有机合成练习题

完整版)高中化学有机合成练习题1.香豆素是一类广泛存在于植物中的芳香族化合物,具有光敏性、抗菌和消炎作用。
其核心结构为芳香内酯A,分子式为C9H6O2.该芳香内酯A可通过水解反应转变为水杨酸和乙二酸。
2.设计合理方案从化合物OCCOOH合成化合物O。
方案如下:首先将OCCOOH与HI反应生成乙酸和I2,再将乙酸与苯乙烯在过氧化物催化下进行加成反应,生成化合物D。
化合物D经过还原反应生成化合物E,最后将化合物E与甲醇在酸催化下进行酯化反应,生成化合物O。
3.化合物A经过四步反应可得到常用溶剂四氢呋喃。
其中,化合物A与HBr在室温下反应生成化合物B,化合物B与KMnO4、H+COOH反应生成化合物C,化合物C与NaOH水溶液反应生成化合物D,化合物D与H2/Pd-C反应生成化合物E,化合物E与CH3OH在酸催化下反应生成四氢呋喃。
化合物Y的分子式为C5H12O,其中含有羟基和甲基官能团。
化合物B的反应类型为亲核取代反应,化合物C的反应类型为氧化反应。
4.化合物C的结构简式为C6H5CH=CHCOOH,化合物D 的结构简式为C6H5CHBrCH2CH3,化合物E的结构简式为C6H5CH2CH2OH。
四氢呋喃链状醚类的所有同分异构体的结构简式如下:5.化合物C与NaOH水溶液反应生成苯甲酸和乙二酸,化学方程式为C6H5CH=CHCOOH + NaOH → C6H5COOH + CH3CH2COOH。
注意:原文中有一些明显的格式错误和段落问题,已经被删除或修正。
有机化合物可以与含羰基化合物反应生成醇。
该反应过程如下所示:R2R2R1Br + Mg → R1MgBr → R1CHOMgBr →R1CHOH(△)(其中R1、R2表示烃基)。
有机酸和PCl3反应可以得到羧酸的衍生物酰卤:RCOCl。
苯在AlCl3催化下能与酰卤作用生成含羰基的化合物。
有机物X、Y在医学、化工等方面具有重要的作用,其分子式均为C10H14O,都能与钠反应放出氢气,并均可经上述反应合成,但X、Y又不能从羰基化合物直接加氢还原得到。
高中化学奥林匹克竞赛有机化学的几个基本反应

重排酮肟在酸性条件下发生重排生成烃基酰胺的反应。
1886年由德国化学家.贝克曼首先发现。
常用的贝克曼重排试剂有硫酸、五氯化磷、贝克曼试剂(氯化氢在乙酸-乙酐中的溶液)、多聚磷酸和某些酰卤等。
反应时酮肟受酸性试剂作用,形成一个缺电子氮原子,同时促使其邻位碳原子上的一个烃基向它作分子内 1,2-迁移,其反应过程如下:贝克曼重排是立体专一性反应。
在酮肟分子中发生迁移的烃基及离去基团(羟基)互为反位。
在迁移过程中迁移碳原子的构型保持不变,例如:贝克曼重排反应可用于确定酮类化合物的结构。
工业上利用环己酮肟发生贝克曼重排,大量生-己内酰胺,它是合成耐纶6(见聚己内酰胺)的单体。
亲电取代反应亲电取代反应一种亲电试剂取代其它官能团的化学反应,这种被取代的基团通常是氢,但其他基团被取代的情形也是存在的。
亲电取代是芳香族化合物的特性之一.芳香烃的亲电取代是一种向芳香环系,如苯环上引入官能团的重要方法。
其它另一种主要的亲电取代反应是脂肪族的亲电取代。
亲电加成反应亲电加成反应是烯烃的加成反应,是派电子及实际作用的结果。
派键较弱,派电子受核的束缚较小,结合较松散,因此的作为电子的来源,给别的反应物提供电子。
反应时,把它作为反应底物,及它反应的试剂应是缺电子的化合物,俗称亲电试剂。
这些物质又酸中的质子,极化的带正电的卤素。
又叫马氏加成,由马可尼科夫规则而得名:“烯烃及氢卤酸的加成,氢加在氢多的碳上”。
广义的亲电加成亲反应是由任何亲电试剂及底物发生的加成反应。
在烯烃的亲电加成反应过程中,氢正离子首先进攻双键(这一步是定速步骤),生成一个碳正离子,然后卤素负离子再进攻碳正离子生成产物。
立体化学研究发现,后续的卤素负离子的进攻是从及氢离子相反的方向发生的,也就是反式加成。
如丙烯及的加成:→ 2第一步,电离生成H和离子,氢离子作为亲电试剂首先进攻双键,形成这样的结构:第二步,由于氢已经占据了一侧的位置,溴只能从另外一边进攻。
根据马氏规则,溴及2-碳成键,然后氢打向1-碳的一边,反应完成。
有机化合物的合成 习题

第1节有机化合物的合成习题“绿色化学”对化学反应提出了“原子经济性”(即节约原子)的新概念及要求。
理想原子经济性反应是原料分子中原子全部转化为所要得到的产物中,不产生副反应,实现零排放。
据此,回答1~4题:1.下列反应可能符合这一要求的是①取代反应;②化合反应;③消去反应;④加成反应;⑤水解反应;⑥加聚反应;A.①③⑤B.②④⑥C.①②③D.④⑤⑥2.以下反应中符合绿色化学原理的是A.乙烯与氧气在银催化作用下生成环氧乙烷B.乙烷与氯气制备氯乙烷C.甲苯和氯气为原料,在一定条件下生产一氯甲苯D.乙醇与浓硫酸共热制备乙烯3.下列几种生产乙苯的方法中,原子经济性最好的是(反应均在一定条件下进行)A.+C2H5Cl→-C2H5+HClB.+C2H5OH→-C2H5+H2OC.+CH2=CH2→-C2H5D.-CHBrCH3→-CH=CH2+HBr,-CH=CH2+H2→-C2H5 4.如用CH3C≡CH合成CH2=C(CH3)COOCH3。
欲使原子利用率达到最高,还需要的反应物是A.CO和CH3OH B.CH3OH和H2C.H2和CO2D.CO2和H2O5.从溴乙烷制取1,2-二溴乙烷,下列转化方案中最好的是A.CH3CH2Br CH3CH2OH CH2=CH2CH2BrCH2BrB.CH3CH2Br CH2BrCH2BrC.CH3CH2Br CH2=CH2CH2BrCH3CH2BrCH2BrD .CH 3CH 2BrCH 2=CH 2CH 2BrCH 2Br 6.有机物可通过如下表示的方法制得:,则烃A 应是A .1-丁烯B .2-丁烯C .乙烯D .乙炔7.以乙醇为原料,用下述6种类型的反应:(1)氧化;(2)消去;(3)加成;(4)酯化;(5)水解;(6)加聚,来合成乙二酸乙二酯()的正确顺序是A .(1)(5)(2)(3)(4)B .(1)(2)(3)(4)(5)C .(2)(3)(5)(1)(4)D .(2)(3)(5)(1)(6)8.香兰素是重要的香料之一,它可由丁香酚经多步反应合成。
化学竞赛 有机基础知识与合成.docx

第三讲有机基础知识与合成7月14日1.聚集状态(1)桂:碳原子数小于5的桂都是气体。
(新戊烷是气体,沸点:9.5C)烷桂:Ci 一Cj为气体,05一Ce为液体,C]7以上为固体。
烯绘02—C4为气体,05—018为液体,G9以上为固体。
苯的同系物多数为液体,和苯一样有特殊的香味,其蒸气有毒。
但对二甲苯为固体。
环内烷、环丁烷为气体,环戊烷为液体,高级同系物为固体。
(2)桂的衍生物:CH B CK CH2=CHC1> C2H5CI、HCHO、CHJB T等为气体。
饱和一元醇屮,G —G为酒味液体,5以丄为固体。
饱和一元竣酸屮,G —G为具有强烈酸味和刺激性的流动液体,C4—a为具有无色无臭的油状液体,Go以丄为石蜡状固体。
硝基化合物屮,一硝基化合物为高沸点液体,其余为结晶固体。
酚类、饱和高级脂肪酸、二元竣酸、芳香酸、脂肪、糖类、氨基酸及荼等为固体。
不饱和脂肪酸(如油酸)为液体。
2.溶解性(1)难溶于水:坯类、卤代桂、酯、硝基化合物、高级脂肪酸、多糖、高分子化合物等。
(2)低级醇、醛、竣酸、单糖、二糖、氨基酸、内酮、某些蛋口质溶于水。
(3)乙烘、乙醛微溶于水。
常温下,苯酚微溶于水,70°C以上与水互溶。
(4)难溶于水,且比水轻:烷坯、烯桂、烘炷、CJUC1、汽油、乙醛、苯(0. 8765g / cm')、甲苯(0. 8669 g / cm)、二甲苯、环己烷、乙酸乙酯(0. 9003 g / cm% 油酸及低级酯类、油。
(5)难溶于水,且比水重:漠甲烷(1.6755 g / cm3).混乙烷(1.4604 g / cm3). 漠苯(1.495g / cm3). CCI4、硝基苯、多氯代坯、漠代姪等。
3.最简式相同的(1)CH:乙烘(QHJ、(C」H」)、苯(CeHJ、立方烷(GHJCH?:烯桂(QH」)、环烷桂(CJk)CH20:甲醛(CUO)。
乙酸和甲酸甲酯(GHQ)、乳酸(GHQ)、葡萄糖和果糖(C6H1O O6) C6H1005(W萄糖单元):淀粉和纤维素[(C6H1O O5)J(2)最简式相同的,所含元素的百分含量不变。
全国高中生化学奥林匹克竞赛难题解析

全国高中生化学奥林匹克竞赛难题解析化学是一门既有理论又有实践的学科,对于学生来说,理解和掌握化学知识需要不断的实践和思考。
而在全国高中生化学奥林匹克竞赛中,难题总是充满挑战性,需要考生们具备扎实的理论基础和细致的解题技巧。
本文将针对全国高中生化学奥林匹克竞赛中的部分难题进行解析,帮助读者更好地理解和掌握化学知识。
1. 题目一:化学反应速率与反应机理在化学反应速率与反应机理这一题目中,要求考生解析一个特定的反应过程,包括速率与反应物浓度之间的关系、速率方程的推导过程以及反应机理的解析。
首先,我们可以通过观察实验数据得到速率与反应物浓度的关系。
然后,根据速率与浓度的关系确定速率方程。
最后,可以根据反应物的结构和实验数据来分析反应机理。
2. 题目二:酸碱中和反应的计算酸碱中和反应一直是高中化学教学的重要内容,也是化学奥林匹克竞赛中的常见难题。
这一题目要求考生计算酸和碱的中和反应。
在解题过程中,考生需要根据反应所涉及的化学方程式计算物质的摩尔量,然后根据摩尔比例以及物质的浓度计算所需的体积。
最后,需要根据溶液的中和反应特性和能量变化来推导出最终答案。
3. 题目三:化学平衡与平衡常数化学平衡是化学中一个重要的概念,而计算平衡常数也是化学竞赛中的一道常见题目。
这一题目要求考生分析一个特定的化学平衡过程,确定平衡常数。
在解答此题时,考生需要根据给定的化学方程式,根据反应物和生成物的物质摩尔量之间的关系,利用平衡常数公式计算平衡常数。
同时,还需要了解化学平衡的条件和影响因素,对结果进行分析。
4. 题目四:有机化学反应与合成有机化学反应与合成是化学奥林匹克竞赛中的一大重点。
此题目要求考生通过分析一个有机化合物的结构,确定其合成路径和合成反应的具体步骤。
在解答此题时,考生需要通过对有机化合物结构的分析,确定所需的起始物质和所需反应的类型。
然后,根据有机化学反应规律和合成方法进行步骤的推导和确定。
总结:全国高中生化学奥林匹克竞赛的难题解析是对学生化学知识和解题能力的综合考验。
2023年第37届中国化学奥林匹克竞赛初赛试题及答案

第37届中国化学奥林匹克(初赛)试题(2023年9月3日9:00~12:00)提示:1)凡题目中要求书写反应方程式,须配平且系数为最简整数比。
2)可能用到的常数:法拉第常数 .·-=⨯41F 9648510Cmol 气体常数 . ··--=11R 83145J K mol 阿伏伽德罗常数 .-=⨯231A N 6022110mol 玻尔兹曼常数kB =R/N A第1题(14分,占7%)镓的化合物1-1半导体工业中通过刻蚀制造微纳结构,GaN 是重要的半导体材料,通常采用含氯气体在放电条件下进行刻蚀。
写出利用Ar-Cl 2混合气体放电刻蚀GaN 的化学方程式.1-2金属镓熔点很低但沸点很高其中存在二聚体Ga 。
1990年,科学家将液态Ga 和l 2在甲苯中超声处理,得到了组成为Gal 的物质。
该物质中含有多种不同氧化态的Ga ,具有两种可能的结构,分子式分别为Ga 4I 4(A)和Ga 6I 6(B),二者对应的阴离子分别为C 和D ,两种阴离子均由Ga 和I 构成且其中所有原子的价层均满足8电子。
写出示出A 和B 组成特点的结构笱式并标出Ga 的氧化态,画出C 和D 的结构。
1-3GaI 常用于合成低价Ga 的化合物。
将GaI 与Ar ’Li (Ar ’基如图所示,解答中直接采用简写Ar ’)在-78℃的甲苯溶液中反应,得到晶体E ,E 中含有2个Ga 原子:E 在乙醚溶液中与金属钠反应得到晶体F,X 射线晶体学表明,F 中的Ga-Ga 键长比E 中短0.028nm 。
关于F 中Ga-Ga 的键级历史上曾有过争议,其中一种观点认为,F 中的Ca 价层满足8电子.基于该观点,画出E 和F 的结构式。
第2题(12分,占6%)复盐的组成在NH 4Cl-CuCl-H 2O 体系中,结晶出一种淡蓝色的物质A ,其组成可表示为xNH 4Cl ·CuCl 2·yH 2O 。
高中化学竞赛题-合成有机物
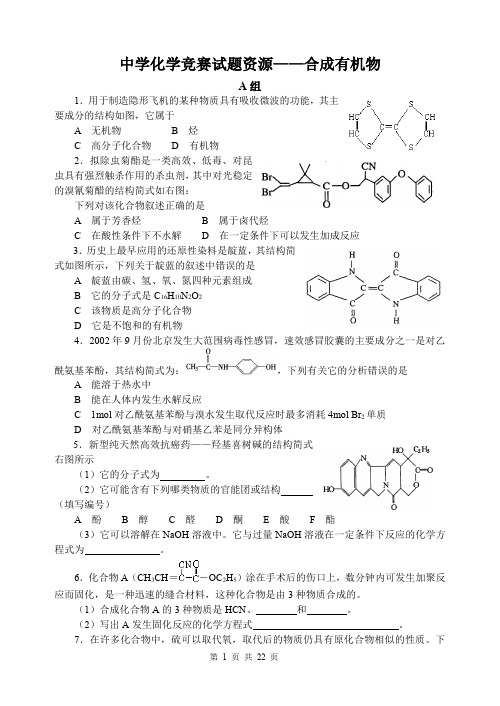
中学化学竞赛试题资源——合成有机物A组1.用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如图,它属于A无机物B烃C高分子化合物D有机物2.拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如右图:下列对该化合物叙述正确的是A属于芳香烃B属于卤代烃C在酸性条件下不水解D在一定条件下可以发生加成反应3.历史上最早应用的还原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的是A靛蓝由碳、氢、氧、氮四种元素组成B它的分子式是C16H10N2O2C该物质是高分子化合物D它是不饱和的有机物4.2002年9月份北京发生大范围病毒性感冒,速效感冒胶囊的主要成分之一是对乙酰氨基苯酚,其结构简式为:,下列有关它的分析错误的是A能溶于热水中B能在人体内发生水解反应C1mol对乙酰氨基苯酚与溴水发生取代反应时最多消耗4mol Br2单质D对乙酰氨基苯酚与对硝基乙苯是同分异构体5.新型纯天然高效抗癌药——羟基喜树碱的结构简式右图所示(1)它的分子式为。
(2)它可能含有下列哪类物质的官能团或结构(填写编号)A酚B醇C醛D酮E酸F酯(3)它可以溶解在NaOH溶液中。
它与过量NaOH溶液在一定条件下反应的化学方程式为。
6.化合物A(CH3CH=-OC2H5)涂在手术后的伤口上,数分钟内可发生加聚反应而固化,是一种迅速的缝合材料,这种化合物是由3种物质合成的。
(1)合成化合物A的3种物质是HCN、和。
(2)写出A发生固化反应的化学方程式。
7.在许多化合物中,硫可以取代氧,取代后的物质仍具有原化合物相似的性质。
下面是两种有机磷农药分子的结构式:杀螟松一六O五我们可以分析得出:这两种农药在使用过程中,不能与物质混和使用,否则会因完全失效的推论。
8.以苯为原料,可通过下列途径制取冬青油和阿司匹林。
请按要求回答:(1)写出流程中方框内物质的结构简式。
(2)写出变化过程中③和⑥的化学方程式,并注明反应条件。
高三化学练习题:有机化合物的合成与反应

高三化学练习题:有机化合物的合成与反应
1. 介绍:
有机化合物的合成与反应是化学领域中的重要研究方向之一。
有机化合物在生活及工业中广泛应用,因此掌握其合成与反应机制对于化学学习具有重要意义。
本文将介绍几个高三化学练习题,涵盖有机化合物的合成与反应等方面知识。
2. 题目一:
已知化合物A为羰基化合物,其分子式为C5H8O,在一定条件下与氨和一种醛反应,生成B和C两个有机化合物:
A + NH3 → B
A + 醛→ C
请推测化合物A的结构,并写出可能的反应机制和产物B、C的结构式。
3. 题目二:
已知丙烯酮(分子式C3H4O)可以与氰化钠发生反应。
请写出该反应的平衡方程式,并解释该反应的机理。
4. 题目三:
某有机化合物D可以被酸性高锰酸钾氧化,生成酮酸E。
请写出该氧化反应的平衡方程式,并说明其中涉及的氧化还原反应机制。
5. 题目四:
已知具有苯环的有机化合物F可以发生取代反应,生成新的有机化合物。
请写出F与溴乙烷反应的平衡方程式,并解释该反应的机理。
6. 题目五:
化合物G是一种脂肪酸,其由甲酸和乙醇酸部分组成。
请写出化合物G的结构式,并解释其在碱性溶液中水解的化学反应。
7. 结论:
通过解答以上高三化学练习题,我们探讨了有机化合物的合成与反应方面的知识。
这些练习题涉及了酰基化合物、取代反应、氧化还原等多个有机化学概念与实践。
通过学习与掌握这些知识,我们可以更好地理解有机化合物的性质与变化,为日后的学习和实践打下坚实基础。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第17讲有机化合物的合成学号姓名得分1、由指定原料及其他必要的无机及有机试剂合成下列化合物:(1)由丙烯合成甘油。
(2)由丙酮合成叔丁醇。
(3)由1-戊醇合成2-戊炔。
(4)由乙炔合成CH3CH2CH2CH2CH2CH2CH 3。
(5)由CH3CH2CH2CHO合成2、试用化学方程式表示以乙烯、为主要原料制备肉桂醛()的过程。
3、用一步或几步反应完成下列甾体化合物的转化。
4、已知苯磺酸在稀硫酸中可以水解而除去磺酸基:又知苯酚与浓硫酸易发生磺化反应:请用化学方程式表示苯、水、溴、铁、浓硫酸及烧碱等为原料,合成的过程。
5、由甲苯为原料,加入必要的有机、无机试剂合成6、以C2H5OH为原料,加入必要的无机试剂合成CH3CH2CH2CH2OH。
7、以BrCH2CH(CH3)2为原料制取2-甲基-1,2-丙二醇。
8、环氧树脂(一种黏合剂)的重要原料是环氧氯丙烷(),试以丙烯为原料加必要的试剂合成之。
9、用你掌握的苯及其衍生物性质的有关知识,写出以最短的流程制备苯甲酸乙酯以及o–、m–、p–氨基苯甲酸反应的化学方程式。
10、请用苯及任选无机试剂合成3,5-二溴硝基苯。
11、以丙二酸二乙酯制备2-苄基丁二酸。
12、请使用不超过4个碳原子的开链有机化合物及任选无机试剂合成2,4-甲基戊酸。
13、(1)写出(CH3)2CHOCH2CH3的两种合成方法,并解释哪种合成法较好;(2)今需合成甲基叔丁基醚[CH3OC(CH3)3],有人用甲醇钠[CH3ONa] 加到叔丁基氯[(CH3)3CCl] 中来制备,未能得到所需产物。
指出在此反应中得到了什么产物?应该怎样合成甲基叔丁基醚?14、动物之间的信息传递除了声音、光电信号外,在低等动物中,如昆虫,还能分泌化学物质作为种群个体之间的通讯工具,这就是所谓“化学通讯”。
棉铃象(一种象鼻虫)的性引诱剂就是这类化学物质。
它是混合物,含有单环萜烯醇E和萜烯醛F和H。
人工合成棉铃象性引诱剂是杀灭这种棉花害虫的绿色农药。
其合成路线如下:O+CH3MgI CuCl2H 3O+A(1) BrZnCH2CO2C2H5(2)3+CO2EtHO(1) KOH23+B(1) (CH3CO)2O23+CO2C2H5+CO2C2H5+C+D(i)(ii)C LiAlH4EMnO2CHO(F)(iii)E LiAlH4GMnO2H问题:分别写出上面以A、B、C、D、E、G、H为代号的各化合物的结构简式。
15、丙炔醇(A)在精细有机合成中是一个重要的化合物,可由乙炔与一分子甲醛反应制得。
在氨基锂等强碱存在下,丙炔醇与卤代烃反应可得到各种取代的丙炔醇,这是制备一元伯醇的方法:HC≡CCH2OH + RBr RC≡CCH2OH化合物B,C,D和E均可以经由上述反应合成CH3(CH2)5CH2 C≡CCH2OH CH3(CH2)5CH2 C≡CCH2 C≡CCH2OHB CCH3(CH2)11CH2OHD E(1)用反应式表示由电石和甲醛以及必要的无机试剂为原料制备A的各步反应,并注明必要的反应条件。
(2)用系统命名法命名化合物B,C,D。
(3)以乙烯、丙烯、乙炔、化合物A以及必要的无机试剂为原料合成B和C,以反应式表示。
(4)由化合物C可以制得D和E,请分别写出反应所需要的条件。
16、用苯乙烯制取,你认为须经过哪些步骤,请写明各步反应属性。
17、化合物A的结构式为:据报道,A可由B与格氏试剂C先进行加成反应,后经氧化、酯化和还原反应等步骤而生成。
(1)请命名化合物A;(2)化合物A有何立体化学现象?为什么?(3)写出化合物B和C的结构式。
(4)写出化合物C的合成路线。
(5)写出B和C加成反应的历程。
(6)写出上述加成反应产物的氧化、酯化及还原等各步反应产物的结构式。
18、化合物A可由苯、异丙醇、醋酸、乙醇及无机试剂合成。
(1)用化学方程式表示A的合成路线。
(2)写出化合物A的各种可能立体异构体(不包括构象异构)的立体表示式。
并指出各异构体是否有光学活性。
(3)给化合物A命名。
19、运用逆合成法设计化合物的合成路线。
所用的有机物不超过4个碳,无机试剂任选。
20、运用逆合成法设计化合物的合成路线。
所用有机物不超过4个碳,无机试剂任选。
参考答案:1、(1)(2)(3)(4)(5)2、①C2H4+HCl→CH3CH2Cl②CH3CH2Cl+NaOH C2H5OH+NaCl③2C2H5OH+O2→2CH3CHO+2H2O④-CH2Br+NaOH-CH2OH+NaBr⑤2-CH2OH+O2→2-CHO+2H2O⑥-CHO+CH3CHO→-CH=CHCHO3、4、5、6、①②7、先发生消去反应生成2-甲基丙烯,再加溴生成2-甲基-1,2-二溴丙烷,然后再将其水解。
8、9、(1)苯甲酸乙酯的合成: 5-CH 3+6KMnO 4+9H 2SO 4→5-COOH +3K 2SO 4+6MnSO 4+14H 2O -COOH +C 2H 5OH −→−+H-COOC 2H 5+H 2O(2)o –氨基苯甲酸的合成:-CH 3 + HNO 3(浓)−−−→−42SO H 浓 + H 2O5 + 6KMnO 4 + 9H 2SO 4→5+3K 2SO 4 + 6MnSO 4 + 14H 2O+ 3H 2SO 4+3Fe →+ 3FeSO 4 + 2H 2Op –氨基苯甲酸的合成:-CH 3 + HNO 3(浓)−−−→−42SO H 浓O 2N --CH 3 + H 2O5O 2N --CH 3+6KMnO 4+9H 2SO 4→5O 2N --COOH+3K 2SO 4+6MnSO 4+14H 2OO 2N --COOH + 3H 2SO 4 + 3Fe →H 2N --COOH + 3FeSO 4 + 2H 2Om –氨基苯甲酸的合成: 5-CH 3 + 6KMnO 4 + 9H 2SO 4→5-COOH + 3K 2SO 4 + 6MnSO 4 + 14H 2O-COOH + HNO 3(浓)−−−→−42SO H 浓 + H 2O+ 3H 2SO 4 + 3Fe →+ 3FeSO 4 + 2H 2O10、11、12、13、(1)①(CH3)2CHONa+BrCH2CH3②(CH3)2CHBr+NaOCH2CH3以①法较好,②得到醚与烯的混合物。
(2)得到了(CH3)2C=CH2,因为叔卤烷遇强碱易消除。
所以用:(CH3)3CONa+CH3Br→(CH3)3COCH3较好。
14、A:O;B:HO CO2H;C:H CO2Et;D:EtO2C H;E:CH2OHH;G:HHOCH2C;H:HOHC15、(1)CaC2+H2O →HC≡CH HC≡CCH2OH(2)B:2–癸炔–1–醇C:2,5–十三碳二炔–1–醇D:(2Z,5Z)–2,5–十三碳二烯–1–醇(3)其中:*(a)CH3(CH2)5CH2Br的制备方法一CH2=CH2CH3CH=CH2+HBr CH3CH2CH2Br CH3CH2CH2MgBrCH3(CH2)3CH2OH CH3(CH2)3CH2Br CH3(CH2)3CH2MgBrCH3(CH2)5CH2OH CH3(CH2)5CH2Br(此法较好)方法二CH3CH2CH2Br+HC≡CH CH3CH2CH2C≡CHCH3CH2CH2CH=CH2CH3(CH2)3CH2Br CH3(CH2)3CH2C≡CHCH3(CH2)3CH2CH=CH2CH3(CH2)5CH2BrB的制备:CH3(CH2)5CH2Br+HC≡CCH2OH CH3(CH2)5CH2C≡CCH2OH(2)C的合成:CH3(CH2)5CH2C≡CCH2OH CH3(CH2)5CH2C≡CCH2BrCH3(CH2)5CH2C≡CCH2Br +HC≡CCH2OH CH3(CH2)5CH2C≡CCH2C≡CCH2OH(4)C+H2 D C+H2 E16、(A)烯烃与Br2亲电加成(B)卤代消去反应(RONa/ROH)(C)末端炔烃活性氢被金属离子取代(D)炔化物(有机金属化合物)与RX发生亲核取代(R-C≡CM为亲核试剂)(E)用Na+NH3作催化剂还原产物为E型(F)过氧酸,或O2+Ag,或N2O2均可使烯烃(C=C)双键氧化成环氧键17、(1)3–羟基–3–氟代甲基–5–羟基戊酸内酯,或4–羟基–4–氟代甲基–2–吡喃酮。
(2)A 有旋光异构(对映异构)现象,因为A 含有手性碳原子;A 也有构象异构现象,因为A 为六元环,FCH 2–和–OH 在空间的位置不同。
(3)B :FCH 2COOC 2H 5,C :CH 2=CH -CH 2MgBr 。
(4)CH 2 = CH –CH 3−−−→−γh Br ;2CH 2 = CH –CH 2Br −−−−−→− 无水乙醚Mg CH 2 = CH –CH 2MgBr (5)(6)A18、(1)(2)(3)2,6-二苯基环己甲醇19、20、。
