九年级化学溶解现象
九年级化学下册《第六章溶解现象-物质在水中的分散-溶解与乳化》知识梳理(含答案)
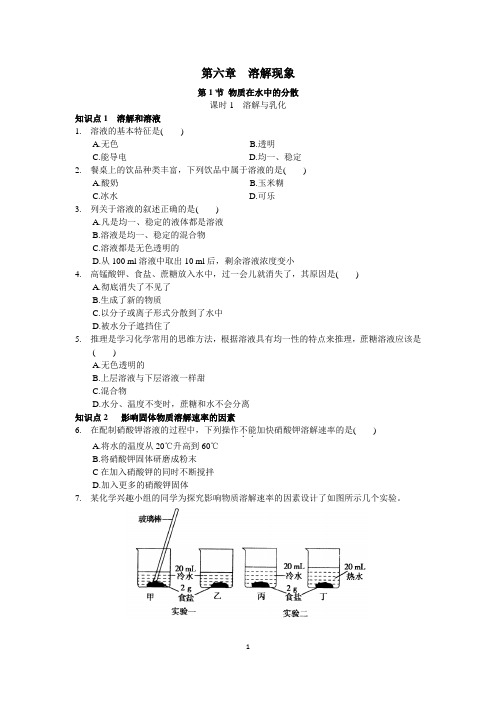
第六章溶解现象第1节物质在水中的分散课时1 溶解与乳化知识点1 溶解和溶液1. 溶液的基本特征是( )A.无色B.透明C.能导电D.均一、稳定2. 餐桌上的饮品种类丰富,下列饮品中属于溶液的是( )A.酸奶B.玉米糊C.冰水D.可乐3. 列关于溶液的叙述正确的是( )A.凡是均一、稳定的液体都是溶液B.溶液是均一、稳定的混合物C.溶液都是无色透明的D.从100 ml溶液中取出10 ml后,剩余溶液浓度变小4. 高锰酸钾、食盐、蔗糖放入水中,过一会儿就消失了,其原因是( )A.彻底消失了不见了B.生成了新的物质C.以分子或离子形式分散到了水中D.被水分子遮挡住了5. 推理是学习化学常用的思维方法,根据溶液具有均一性的特点来推理,蔗糖溶液应该是( )A.无色透明的B.上层溶液与下层溶液一样甜C.混合物D.水分、温度不变时,蔗糖和水不会分离知识点2 影响固体物质溶解速率的因素6. 在配制硝酸钾溶液的过程中,下列操作不能..加快硝酸钾溶解速率的是( )A.将水的温度从20℃升高到60℃B.将硝酸钾固体研磨成粉末C在加入硝酸钾的同时不断搅拌D.加入更多的硝酸钾固体7. 某化学兴趣小组的同学为探究影响物质溶解速率的因素设计了如图所示几个实验。
(1)实验一探究的是对物质溶解速率的影响。
(2)实验二中观察到丁中的食盐比丙中溶解得快,由此得出的结论是。
(3)实验三中观察到.由此得出的结论是固体的颗粒越小,溶解得越快。
知识点3 乳化8. 下列洗涤或除污过程应用乳化原理的是( )A用水清洗沾在手上的蔗糖B.用水洗去盘子上的水果渣C.用洗洁精洗去餐具上的油污D.用稀盐酸清洗长期盛放石灰水的烧杯9. 下列应用与乳化现象无关..的是( )A.用汽油洗去金属表面的油污B.化妆品及乳制饮品的配制C.用洗发水清洗头发上的油脂D.用乳化剂稀释难溶于水的液态农药10. 下列关于溶解和乳化的说法正确的是( )A.利用乳化作用将油污溶解而除去B.向植物油与水的混合物中加入乳化剂,可得到溶液C.用酒精洗去试管中的碘利用了乳化原理D.用肥皂洗衣服利用了乳化原理11. 小刚分别试用以下方法清洗餐具:①只用冷水;②只用热水;③在冷水中加入几滴洗涤剂;④在热水中加入几滴洗涤剂。
九年级化学下册《溶解现象》知识学习总结要点沪教版

九年级化学下册《溶解现象》知识点沪
教版
一、物质在水中的分散
1、将深紫色的高锰酸钾加入水中,你将发现高锰酸钾固体不见了,得到紫红色的液体。
2、将紫色固体碘加入酒精中,你发现碘消失,得到暗黄的液体。
通过实验可以知道高锰酸钾能溶解在水里,碘能溶解在酒精里。
二、溶液组成的表示
1.用溶质的质量分数和溶质的物质的量浓度来表示溶液组成。
溶液的组成:溶质和溶剂。
浓溶液、稀溶液:在一定量的溶剂里所含的溶质多为浓溶液,所含的溶质少为稀溶液。
溶液的“浓、稀”只是溶液组成的一种粗略表示方法。
溶液的“浓、稀”与饱和不饱和无关,即浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
溶液体积与溶液质量的关系:溶液质量=溶液体积×溶液密度。
三、物质的溶解性
1.溶液的定义:一种或几种物质分散在另一种物质中,
形成均一、稳定的混合物叫做溶液。
2,溶液的特征
均一性:是制溶液各部分组成、性质完全相同。
稳定性:是指外界条件不变,溶剂的量不变时,溶液长期放置不会分层也不会析出固体或气体。
初中化学实验现象总结大全

初中化学实验现象总结大全
一、溶解现象
1、溶剂液体蒸发:溶质溶于溶剂,溶剂液体集中在溶剂中,当其扩散到空气中时,溶剂液体随气流而散发,蒸发挥发,从而溶质析出。
2、挥发性溶剂溶质会慢慢挥发:溶质溶于挥发性溶剂,当热量使溶质气化后,慢慢挥发,吸收热量,溶质析出。
3、融化:某些固体溶质在适当的温度下,溶质完全溶解,而溶质析出。
二、结晶现象
1、滴液析出:某种溶质或溶剂沉积到固态表面,使溶质析出,形成滴液状的晶体。
2、霍夫曼析出:在溶液中,溶质有一定比例有规律地移动,形成晶体,叫做霍夫曼析出。
3、沸腾析出:把溶液沸腾一段时间,溶质就会蒸发析出,析出晶体形成沸腾析出。
三、沉淀现象
1、热沉淀:当溶液热度提高时,由于温度升高,溶质的活力增强,溶质析出,形成沉淀物。
2、冷沉淀:把溶液冷却,溶质的活力减弱,溶质沉淀,形成沉淀物。
3、加入试剂沉淀:加入一定的试剂,使溶质的活力减弱,溶质
析出,析出沉淀物。
中考化学第一轮专题复习(第六章 溶解现象)

中考化学第一轮专题复习第六章溶解现象溶液:物质相互分散,形成均一的、稳定的混合物。
1、混合物状态不同:悬浊液:存在固体小颗粒(不均一,不稳定,会形成沉淀)乳浊液:存在液体小颗粒(不均一,不稳定,会分层)※“均一”是指溶液各组成成分和性质完全相同。
※“稳定”是指当条件不变是,长时间放置,溶液中的溶质和溶剂也不会出现分离的现象。
※“颜色”不是判定溶液的标准:如溶液中含有Cu2+会显蓝色;含有Fe2+(亚铁)的溶液显浅绿色;含有Fe3+的溶液显黄色;含有MnO4-的溶液显紫红色。
2、物质的溶解是构成物质的离子或分子分散的过程。
※像氯化钠NaCl、氢氧化钠NaOH等物质溶解是由于在水分子的作用下电离出的阴阳离子。
NaCl = Na+ + Cl-;NaOH = Na+ + OH-※像蔗糖的物质,它们是由分子构成的,溶于水只是其分子脱离晶体表面,分散到水中的道理。
硝酸铵NH4NO3的溶解使溶液温度下降(吸热)3、溶解现象:像氯化钠NaCl等物质的溶解不会造成溶液温度发变化氢氧化钠NaOH、浓硫酸H2SO4、生石灰CaO溶解时放热,造成溶液温度上升。
4、洗洁精能使难溶于水的油以小液滴均匀悬浮在水中形成乳浊液,这称为乳化现象。
乳化的应用:油污清洗、洗涤剂和化妆品的配制、石油开采、污水处理、制剂合成及纺织印染。
※用纯碱、汽油和洗涤剂的水溶液都能除去衣物上的油污,其实它们的原理各不相同:纯碱是与油污中的物质发生化学反应;汽油是将油污溶解;洗涤剂是和油污发生乳化作用。
5、较快溶解物质的方法:⑴用玻璃棒搅拌;⑵提高溶解的水温;⑶使固体变成粉末颗粒6、物质溶于水后,溶液的凝固点下降,沸点升高。
例1、冬天厨房中最易结冰的是(D )A、酱油B、米酒C、食醋D、水※水的凝固点比溶液的低例2、寒冬里,为什么水缸往往会冻裂,而装有腌制食品的水缸却不会冻裂?冰的密度比水小,等质量的水和冰相比,冰的体积大,所以水结冰后体积变大,把水缸撑裂;腌制食品的水形成溶液,溶液的凝固点低,所以不易结冰。
初中化学溶解现象教案

初中化学溶解现象教案
教学内容:溶解现象
教学目标:了解溶解的定义、特点和影响因素,掌握一些实际生活中的有关溶解现象的知识。
教学重点:溶解的定义和特点。
教学难点:影响溶解的因素。
教学准备:实验器材、实验药品、PPT课件。
教学步骤:
第一步:引入
通过简单的实验现象引入本课主题,让学生观察实验现象,并提出问题:为什么溶质会溶解在溶剂中?
第二步:学习
1. 讲解溶解的定义:溶质在溶剂中彻底分散形成溶液的过程称为溶解。
2. 讲解溶解的特点:溶解是一个动力过程,速度快慢取决于溶质与溶剂之间的相互作用。
3. 探究影响溶解的因素:温度、溶质粒子的大小和形状、溶剂性质等因素会影响溶解的速度。
第三步:实验
组织学生进行简单的实验,观察不同条件下溶解过程的状态变化,验证影响溶解速率的因素。
第四步:总结
归纳出影响溶解速率的因素,并进行梳理总结。
第五步:拓展
通过实际生活中的案例,让学生理解溶解现象在日常生活中的应用,并启发学生思考更多的问题。
第六步:作业
布置作业:整理溶解现象相关知识,写出影响溶解速率的因素及其解释。
教学反思:
通过本节课的学习,学生应该能够了解溶解的定义和特点,掌握影响溶解速率的因素,并能够在实际生活中运用所学知识。
在教学中需要引导学生思考,让其能够在学习中得到启发和提高。
九年级化学溶解部分知识点

九年级化学溶解部分知识点溶解是化学中一种常见的物质现象,指的是将固体、液体或气体溶于溶剂中形成溶液的过程。
在九年级化学中,我们需要了解溶解的基本概念、溶解过程中的物质性质变化以及一些关键的知识点。
本文将围绕这些方面进行探讨。
一、溶解的基本概念溶解是指固体、液体或气体溶质与溶剂之间发生相互作用,使溶质分散均匀地分布在溶剂中,形成溶液的过程。
在溶解过程中,溶质的微观粒子与溶剂的微观粒子发生相互作用,以致溶质的微观粒子能够均匀地分散在溶剂中。
二、溶解的物质性质变化1. 固体溶解:固体溶解是指固体溶质与溶剂之间的相互作用。
在固体溶解过程中,溶质的微观粒子逐渐与溶剂的微观粒子分散均匀,与此同时,溶质的粒子间距减小、有序性降低,溶液的熵增加。
2. 液体溶解:液体溶解是指液体溶质与溶剂之间的相互作用。
液体溶解过程相对较为复杂,涉及到溶质与溶剂之间的相互作用力。
对于大多数液体溶解过程,存在着相互溶解的情况,即溶液中既有溶质的分子也有溶剂的分子。
3. 气体溶解:气体溶解是指气体溶质与溶剂之间的相互作用。
溶解气体的实质是气体分子与溶剂分子之间的碰撞,通过相互碰撞而相互溶解。
溶解气体的能力与气体的性质、温度、压强等因素有关。
三、九年级化学溶解部分的知识点1. 溶解度:溶解度指的是在一定温度下,单位溶剂中溶质溶解的最大量。
它与溶质和溶剂之间的相互作用、温度等因素有关。
常用的溶解度单位有g/100g溶剂、mol/L等。
2. 饱和溶液:当在给定的温度下继续向已经饱和的溶液中加入溶质,无法再通过溶解达到更高浓度时,称该溶液为饱和溶液。
饱和溶液中溶质的溶解度等于溶解度的值。
3. 过饱和溶液:在较高温度下溶解较多溶质,然后迅速冷却,也可以得到一个溶液。
在此情况下,溶液中含有超过饱和度的溶质,称为过饱和溶液。
4. 离子溶解:在水溶液中,其溶解过程涉及到离子的形成和断裂。
当固体物质溶解于水中时,其溶质通常以形成个别的离子,溶剂通常以离子形式存在。
九年级化学溶解现象知识点总结
九年级化学溶解现象知识点总结溶解现象是化学中一种重要的物质变化过程,是指固体、液体或气体中的微粒分散在另一种物质中,形成均匀透明的混合物。
以下是九年级化学中关于溶解现象的知识点总结:一、溶解的定义与特点溶解是指溶质的微粒逐渐分散在溶剂中形成溶液的过程。
溶解的特点包括:溶质微粒与溶剂微粒之间的相互作用力,保持永久为弱化学键;溶质微粒在溶剂中自由运动而不聚集;溶质不能被过滤分离,只能靠蒸发得到纯物质。
二、溶解的影响因素1. 温度:温度升高,溶解度一般会增大,但对气体溶解度却相反。
2. 压力(只适用于气体溶解度):压力升高,气体溶解度增大。
3. 溶质与溶剂之间的相互作用力:相互作用力越强,溶解度越大。
4. 溶质与溶剂的粒径:溶质的粒径越小,溶解度越大。
三、溶液的浓度及计算1. 质量分数:溶质的质量与溶液总质量之比。
2. 体积分数:溶质的体积与溶液总体积之比。
3. 摩尔浓度:溶质的摩尔数与溶液总体积之比。
4. 溶解度:在规定温度下,饱和溶液中溶质质量与溶剂质量之比。
四、饱和溶液与过饱和溶液饱和溶液是指在一定温度下,已经溶解了最大量的溶质的溶液。
而过饱和溶液是指在一定温度下,溶质溶解度超过平衡溶解度,在稳定条件下存在溶解度不稳定的现象。
五、溶解的物质状态1. 水溶液:以水为溶剂的溶液,如盐水、糖水等。
2. 液体溶液:由液体溶质溶解于液体溶剂中,如酒精和水的混合物。
3. 气体溶液:由气体溶质溶解于液体溶剂中,如汽水。
六、分离溶液中的溶质与溶剂1. 晶体得到分离:通过蒸发溶剂,使其发生结晶得到溶质。
2. 沉淀得到分离:通过加入反应剂使溶质发生反应,沉淀得到分离。
3. 蒸馏:通过将溶液加热至溶剂的沸点,使溶剂蒸发得到分离。
七、溶解现象在日常生活中的应用1. 调味品:食盐、白糖等溶于水中,增添食物的味道。
2. 药物:药物以溶解的形式进入人体,发挥治疗作用。
3. 清洁剂:洗衣液、洗洁精等能将污渍溶解,起到清洁作用。
初中化学物质的溶解性课件PPT
衣物干洗原理:
利用清洁剂或挥发性的有机溶剂,除掉衣 服上的污渍.目前主要是利用四氯乙烯等 干洗剂溶解衣服上不易溶于水的油脂等污 迹.
一杯水中能不能无限制的溶解某种物质?
饱和溶液和不饱和溶液的概念:
饱和溶液:一定温度下、一定量的溶剂里,不能 再溶解某种溶质的溶液,叫做这种溶质的饱和溶液
溶解性与 温度 有关。
探究:物质溶解性的影响因素
合作实验四
将雪碧到在杯子里,观察现象 ____有_气__泡____实验表明: __气_体_也__能_溶__解_在__液_体_中_____
进一步实验发现:液体的温度越 高,气体的溶解能力越弱。
学以致用
1、大家都有喝过可乐,那么 你知道喝下冰冷的可乐以后为 什么会打嗝?
3.同一种物质在同一溶剂中的溶解性与温度有关
4.气体物质的溶解性还与温度、压强有关
小结: 综上所述: 物质的溶解性
1、与溶__质_性__质__(_或溶质的种类()这是内因)
和_溶__剂_性__质__(或溶剂的种类) 有关
2、同时也受温__度__ 的影响
(气体物质的溶解性还与温度、压强有关)
(这是外因)
A.溶液中溶质质量增加 B.溶液质量不变
C.固体质量增加
D.固体质量减少
3.将热的饱和的硝酸钾溶液100g降温至常温时, 没有发生变化的是( A )
A.溶液的质量
B.溶液里溶质的质量
C.溶液里溶剂的质量 D.溶质的溶解度
4.下列措施中,不能使不饱和溶液转变为饱和溶液的
是( D ) A.蒸发溶剂 B.增加溶质 C.改变温度 D.加快搅拌
答,因为冰冷的可乐进入人体后 温度升高,气体溶解能力下降, 二氧化碳而逸出,所以打嗝。
第7章 探索溶解现象第1节 物质在水中的溶解 (课件)2024-2025九下化学沪教
A.可乐
B.自制西瓜汁
C.冰水
D.绿豆汤
[解析] 自制西瓜汁和绿豆汤不均一、不稳定,久置后发生沉降,
不属于溶液;冰水是纯净物,不属于溶液;可乐中含有蔗糖等物质,
具有均一性和稳定性,属于溶液。
3.衣服上的污垢、头发上的油脂难溶于水,通常需要使用洗衣粉、 洗发剂清洗,这与乳化作用有关。
乳化与乳化作用 (1)乳化:如果在油和水的混合物中加入一些洗洁精,振荡后, 油能以很小的液滴的形式均匀悬浮在水中形成乳浊液,这种现象称 为乳化。
于水中
物质在
水中的 分散形
分子或离子
细小固体颗粒 小液滴
式
溶液
悬浊液
乳浊液
不均一、不稳 不均一、不
宏观特 均一、稳定,久置后不分
定,久置后发生 稳定,久置
征
层
沉降
后分层
实例
蔗糖水、碘酒
泥浆、CO2通入 油与水的混 澄清石灰水后形
合物 成的浊液
相同点
都是混合物
典例1 [重庆中考] 食堂里的下列饮品中属于溶液的是( A )
2.溶液导电的条件
特别提醒 1.溶液不一定都能导电,如蔗糖溶液、酒精溶液等不能导电。 2.常见的导电物质可以是金属单质,如铁、铜等,因为其中存在能 够自由移动的电子;也可以是某些溶液,如氯化钠溶液、稀硫酸等。
典例3 下列物质的水溶液不能导电的是( B )
A.氯化钠
B.蔗糖
C.硫酸
D.氢氧化钠
[解析]
硝酸铵固体
溶解或稀释时放热,溶液温度升高
溶解时热量变化不明显,溶液温度 没有明显变化
氢氧化钠固体 氯化钠固体
典例2 某同学往如图所示的烧杯中
加入一种固体物质,轻轻搅拌后,粘在
九年级化学下册 第6章 溶解现象 6.3 物质的溶解性(1)课件
第五页,共十四页。
资料(zīliào)
呢绒、毛、丝绸等高级衣料用水洗会引起皱 缩、变形和损伤,或不易洗净,故常采用干洗 的方法。干洗剂(xǐ jì)是由易挥发的有机溶剂,表 面活性剂和少量水(或不加水)及乳化剂组成 的。有机溶剂的作用是溶解衣物上的油污(常用 的有轻石油烃和氯代烃),表面活性剂能防止 溶于溶剂的污垢微粒再沉积。干洗剂尽管对清 洁油性污渍非常有效,但对水溶性污渍的去污 效果却不明显。
不饱和溶液
3、检验饱和溶液方法:
取样,加入少量该溶质,观察能否继续溶解。
4、浓溶液和稀溶液: ⑴饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液;
⑵相同温度,同一溶质的溶液,
饱和溶液比不饱和溶液要浓一些。
第十三页,共十四页。
内容 总结 (nèiróng)
第6章 溶解现象。胡萝卜如果生吃,其中的β-胡萝卜素只有25%被吸收,如果用食用油烹调后,则 能吸收95%,你知道吸收效率高低的道理吗。β-胡萝卜素在水中溶解性小,在食用油中的溶解性大。
的溶质多。
√ (6)浓溶液一定是饱和溶液,稀溶液一定是不饱和溶液。
(7)在相同温度下,食盐的饱和溶液比它的不饱和溶液要浓。
√ (8)60℃时的硝酸钾饱和溶液,当温度降低到20℃时,其它条件不变,该
溶液还是饱和溶液 。
第十页,共十四页。
1、下列因素不会影响(yǐngxiǎng)物质溶解性的是( )
A.溶质的性质
第六页,共十四页。
干洗不是什么神秘的事,它只是用溶剂来去除油垢或 污渍。由于溶剂中几乎不含任何水分,所以称之为干洗 。干洗的溶液可以溶解及去除衣物上的油垢,例如羊毛 及丝类的天然纤维,水洗后很可能会缩水、变形及褪色 ,但是干洗就可以处理得很好。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
牛牛文档分 享│ 易混易淆扫描 易混易淆扫描 牛牛文档分 享│ 易混易淆扫描
牛牛文档分 享│ 易混易淆扫描
牛牛文档分 享│ 真题归类示例 真题归类示例 牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 知识网络构建 知识全息整合 牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
│ 真题归类示例 牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 易混易淆扫描 易混易淆扫描 牛牛文档分 享│ 易混易淆扫描
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 物质的溶解性
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 易混易淆扫描
牛牛文档分 享│ 易混易淆扫描
牛牛文档分 享│ 真题归类示例 真题归类示例 牛牛文档分 享│ 真题归类示例
牛牛文档分 享Leabharlann库文档分 享│ 真题归类示例 牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享 牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 考点全息整合
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享│ 真题归类示例
牛牛文档分 享
