高分子化学第三章
高分子化学 第三章

第三章参考答案2.下列烯类单体适于何种机理聚合?自由基聚合,阳离子聚合或阴离子聚合?并说明理由。
解:①.氯乙烯,适于自由基聚合。
Cl-就是吸电子基团,有共轭效应,但均较弱②.偏二氯乙烯,适于自由基聚合,但也可进行阴离子聚合。
两个Cl-原子的共同作用使其可进行两种聚合。
③.丙稀腈,适于自由基聚合与阴离子聚合。
CN-基就是强吸电子基团,并有共轭效应。
④.2-腈基丙稀腈,适于阴离子聚合。
两个CN-基的吸电子基团倾向过强,只能阴离子聚合。
⑤. 丙稀,由于烯丙基效应,使其易向单体转移,不能进行自由基聚合。
一般采取配位聚合的方式合成聚合物。
⑥. 异丁烯,适于阳离子聚合。
3CH -就是供电子基团,且与双键有超共轭效应,而且两个3CH -的共同作用,使其可以阳离子聚合。
⑦. 苯乙烯,适于自由基聚合,阳离子与阴离子聚合。
因为共轭体系π电子容易极化并易流动。
⑧. 四氟乙烯,适于自由基聚合。
F -原子体积小,结构对称。
⑨. 2-腈基丙烯酸酯,适于阴离子聚合与自由基聚合。
CN -基与COOR -两个吸电子基团使其易于阴离子聚合,同时又具有共轭效应,可进行自由基聚合。
⑩. 异戊二烯,适于自由基聚合,阳离子与阴离子聚合。
因为共轭体系π电子容易极化并易流动。
3. 判断下列烯类能否进行自由基聚合,并说明理由。
解:①. CH 2=C(C 6H 5)2 偏二苯乙烯,不能。
因为二苯基的空间位阻过大,只能形成二聚体。
②. ClHC=CHCl 1,2-二氯乙烯,不能。
因为单体结构对称,1,2-二取代又具有较大的空间位阻。
③. CH 2=C(CH 3)C 2H 5 2-甲基丁烯,不能。
由于双键上的电荷密度过大,不利于自由基的进攻,且易转移生成稳定的烯丙基自由基。
④. CH 3CH=CHCH 3 2-丁烯,不能。
因为单体结构对称,空间位阻较大,且易生成烯丙基自由基。
⑤. CH 2=CHOCOCH 3 丙烯酸甲酯,能。
酯基有弱的吸电子效应及共轭效应。
高分子化学第三章

(二)阴离子聚合
在链式聚合反应中,活性中心为阴离子的聚 合反应。常用的引发剂有碱金属、丁基锂等亲核 试剂。
阴离子聚合反应的通式可表示如下:
A B M BM A M M n
其中B-为阴离子活性中心,A+为反离子,一般 为金属离子。与阳离子聚合不同,阴离子聚合中 ,活性中心可以是自由离子、离子对,以及处于 缔合状态的阴离子。
酸根的亲核性不能太强,否则会与活性中心结合成 共价键而终止,如HCl
CH3 CH A X
A CH3 CH
X
不同质子酸的酸根的亲核性不同
氢卤酸的X-亲核性太强,不能作为阳离子聚合引发剂, 如HCl引发异丁烯
(CH3)3C Cl
(CH3)3C Cl
HSO4- H2PO4-的亲核性稍差,可得到低聚体。 HClO4,CF3COOH,CCl3COOH的酸根较弱,可生成高聚 物。
Lewis酸引 发
傅-克(俗称Friedel-Grafts催化剂)反应中的各种
金属卤化物,都是电子的接受体,称为Lewis酸。
从工业角度看,是阳离子聚合最重要的引发剂。
Lewis酸包括: 金属卤化物:
BF3 , AlCl3, SnCl4 , TiCl4, SbCl5, PCl5, ZnCl2 金属卤氧化物:
离子聚合:活性中心是离子的聚合。
根据中心离子电荷性质的不同 阳离子聚合 阴离子聚合
离子聚合的理论研究开始于五十年代:
1953年,Ziegler在常温低压下制得PE 1956年,Szwarc发现了“活性聚合物”
多数烯烃单体都能进行自由基聚合,但是 离子聚合却有极高的选择性。 原因: 离子聚合对阳离子和阴离子的稳定性要求 比较严格。
3 高分子化学第三章课堂复习

解:氯乙烯悬浮聚合时所得聚氯乙烯的分子量与引发剂浓度关系不大。分子量主要由 单体链转移来决定,所以聚氯乙烯的分子量主要由温度控制。
氯乙烯悬浮聚合是非均相本体聚合,在转化率较低时易出现反应自动加速。如选用高 活性引发剂,引发剂浓度随反应的进行显著下降。这样正常聚合速率的衰减与自动加速所 造成的速率上升互相补偿使反应可匀速进行。但聚合的后期,高活性引发剂浓度降得很低, 正常聚合速率得衰减不能由自动加速部分来补偿,通过加入中活性引发剂提高引发剂浓度, 使反应温度得控制,在较短时间内完成反应都有了保证。
降低其分子量,则应加入硫醇等链转移剂。在 50C 时,丁二烯链自由基对正辛硫醇的转移
常数 C,高达 16。加入少量硫醇即可显著地降低聚丁二烯的分子量。
6
例 4:已知在苯乙烯单体中加入少量乙醇进行聚合时,所得聚苯乙烯的分子量比一般本体 聚合要低,但当乙醇量增加到一定程度后,所得到的聚苯乙烯的分子量要比相应条件下本 体聚合所得的要高,试解释之。 答:加少量乙醇时,聚合反应还是均相的,乙醇的链转移作用会使其分子量下降。当乙醇 量增加到一定比例后,聚合反应是在不良溶剂或非溶剂中进行,出现明显的自动加速现象, 从而造成产物的分子量反而比本体聚合的高。
(CH3)2C CH2CH n-1CH2CH(OCOCH3) CN OCOCH3
甲醇转移终止
(CH3)2C CH2CH CH2CH(OCOCH3)+CH3OH CN OCOCH3
CHOH+(CH3)2C CH2CH nH CN OCOCH3
2.甲醇转移引发,岐化终止 甲醇转移引发
高分子化学-第3章 自由基聚合
3. 4
聚合物的平均聚合度
1、动力学链长和聚合度
(1)动力学链长υ (kinetic chain length)的定义
每个活性种从引发阶段到终止阶段所消耗单体分子数。无 链转移时,动力学链长为增长速率和引发速率的比。 依据稳态时引发速率等于终止速率,则动力学链长可表 示为增长速率与终止速率的比: 即为单体消耗速率与
自由基产生(或消失) 速率之比
3. 4
聚合物的平均聚合度
如将稳态时的自由基浓度 入上式,可得下式:
,代
3. 4
聚合物的平均聚合度
若自由基聚合反应由引发剂引发时,
引发速率Ri = 2 f kd[I],则:
3. 4
聚合物的平均聚合度
可知动力学链长与引发速率存在以下关系:
1) 动力学链长与单体浓度的一次方成正比,与 引发剂浓度平方根成反比。 2) 说明了在自由基聚合体系中,增加引发剂用 量虽然可以提高聚合速率,但又使聚合物相对分子 质量降低。由此说明引发剂在自由基聚合中的重要
(1)温度对聚合速率的影响
总聚合速率常数k与温度T(K)遵循Arrhenius经验公式: 由前面推导可知: k=Ae-E/RT
k=kp(kd/kt)1/2
因此:
3.5 影响自由基聚合反应的因素
从而可知,总活化能E=(Ep-Et/2)+Ed/2
由Ep、 Et和Ed的大小可以得到总活化能E约为83 kJ/mol,为正值,表明温度升高,速率常数增大k增大。
3.5 影响自由基聚合反应的因素
1. 链自由基的双基终止过程的三步曲:
1) 链自由基的平移;
2) 链段重排,使活性中心靠近;
3) 双基相互反应而使链终止。
第二步(链段重排)是 控制步骤,受体系粘度 影响显著。
高分子化学课件第三章 自由基共聚合

m1= d[M1] = k11[M1*][M1] + k21[M2*][M1] (i)
m2 d[M2]
k12[M1*][M2] + k22[M2*][M2]
第三章 自由基共聚合
(3)假设共聚反应是一个稳态过程,即总的活性中心的浓 度[M1*+M2*]恒定,[M1*]和[M2*]的消耗速率等于[M1*]和 [M2*]的生成速率,并且 M1* 转变为M2*的速率等于M2*转 变为M1*的速率;
二元共聚合的理论研究较系统深入,而三元及三元以上共 聚合复杂,理论研究很少,但实际应用的例子颇多。ABS, SBS
三元以上聚合,一般以两种单体确定主要性质,另外单体 改性。
二元共聚物根据两单体单元在分子链上的排列方式可分四 类:
第三章 自由基共聚合
(1)无规共聚物(random copolymer) 两种单体单元的排列没有一定顺序,A单体单元相邻的单
第三章 自由基共聚合
四种竞争链增长反应:
k11 M1* + M1
k12 M1* + M2
k21 M2* + M1
k22 M2* + M2
M1* R11 = k11[M1*][M1]
M2* R12 = k12[M1*][M2]
M1*
R21 = k21[M2*][M1]
M2* R22 = k22[M2*][M2]
若含一段A链与一段B链,如~AAAAAAA-BBBBBBBBBB~, 称AB型二嵌段共聚物;如果是由一段A链接一段B链再届一 段A链,如~AAAAAA-BB~BBB-AAAAAAA~,则称ABA型 三嵌段共聚物;若由多段A链和多段B链组成,则称(AB)n型 多嵌段共聚物。
第三章 自由基共聚合
高分子化学导论第3章_自由基聚合机理及分子量链转移
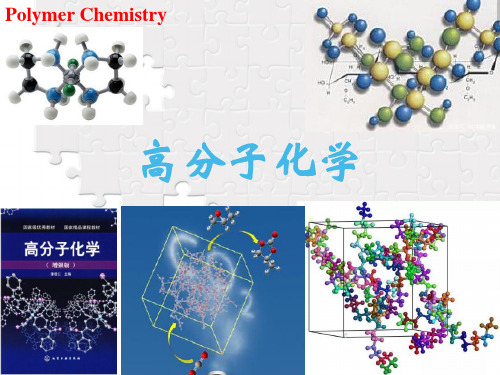
链转移与链终止反应
链转移 自由基与其他非自由基分子的反应
链终止 自由基与自由基的反应
引发 增长
E (kJ/mol)
k
特点
Ed:105~150 Ei: 21~34
Ep=20~34
kd: 10- 4~10- 6s-1 慢引发 kp=102~104l/mol·s 快增长
终止 Et=8~21
kt=106~108l/mol·s 速终止
如:过氧化乙酰环己烷磺酰(ACSP)
2) 无机过氧化物——过硫酸盐 过硫酸钾,过硫酸铵
O
O
KO S O O S OK
O
O
O 2 KO S O
O
K2S2O8
2KSO4
水溶性引发剂
可单独使用,还可与适当的还原剂构成氧化 还原体系,在室温或更低温度下引发聚合
3. 氧化-还原体系引发剂
由氧化剂与还原剂组合在一起,通过电子转移 反应(氧化-还原反应),产生自由基而引发单 体进行聚合 特点: 活化能低,可在室温或更低温度下引发聚合 引发速率快,即活性大 种类多
歧化终止的结果:
Xn与链自由基中的单体单元数相同。
每个大分子只有一端为引发剂残基,
另一端为饱和或不饱和(两者各半)。
终止方式与单体种类、聚合条件有关 St:偶合终止为主 MMA:>60℃歧化终止为主
< 60℃两种终止方式均有
链终止的特点: Et(终止活化能)很低,8-21KJ/mol Rt(终止速率)极高 双基终止受扩散控制
均裂(homolysis) 共价键上一对电子分属两个基团,带独 电子的基团呈中性,称为自由基
RR
2R
异裂(heterolysis) 共价键上一对电子全部归属于某一基团, 形成阴离子,另一缺电子的基团,称做阳 离子
高分子化学第三章 自由基聚合

• 链转移反应前后,自由基的数目未变。
35
1. 向单体转移
· ~~CH2-CH + CH2=CH Cl Cl
· ~~CH=CH + CH3-CH Cl Cl
• 注意CH2=CHCl单体
36
2. 向溶剂或链转移剂转移
X ~~CH2CH · + YS X ~~CH2CHY + S ·
• 溶剂:
• 链转移剂:有较强的链转移能力的化合
1 2
[I ]
1
2
[M ] (3—35式)
注意本方程的适用范围
73
二、温度对聚合速率的影响
• 阿累尼乌斯公式:K=Ae–Ea/RT
其中:K=kp(kd/kt)½ 则:Ea=Ep+Ed/2–Et/2
74
一般情况下: Ep≈29kJ•mol–1, Ed≈126kJ•mol–1 Et≈17kJ•mol–1
10
一、 聚合的可能性
• 主要取决于双键上取代基的空间 效应
11
1.烯类单体: CXY=CMN
(1)一取代( CH2=CHX)
可均聚合
12
(2)二取代
(CH2=CXY、CHX=CHY) (a)1,1——二取代:一般不考虑空 间位阻效应,可均聚合。
注意:CH2=C(Ar)2只能形成二聚体
13
(b)1,2——二取代
54
2.半衰期
[I] ln = Kd t [I0]
• 60℃
ln2 t½ = K d
(3—17)
t½ >6h,低活性引发剂 1h< t½ <6h,中活性引发剂 t½ <1h,高活性引发剂
55
3. 引发效率
高分子化学第三章自由基聚合

①由条件a得单体浓度[M]=0.877×103/104=8.53mol·L-1 ,条 件b得引发剂浓度 [I]=0.109%×0.887×103/242=4.0×10-
3mol·L-1
②60 ℃苯乙烯为100%双基偶合终止,当聚合度=2460,则动
力学 链长为R1p230. Rp
Ri 2f kd[I]
• 阻聚常数见课本P98表3-26 • 阻聚效果:
DPPH > FeCl3 > 苯醌> 硝基苯Fra bibliotek计算题
1、甲基丙烯酸甲酯进行聚合,试由⊿H和⊿S来计算77℃、 127℃、177℃、227℃ 时的平衡单体浓度,从热力学上 判断聚合能否正常进行。
解:ln[M]e=⊿H/RT-⊿S/R,且⊿H=-56500 ⊿S=-117.2 当T=350K时,ln[M]e=⊿H/RT-⊿S/R=-5.32
20、链转移反应对支链的形成有何影响?聚乙烯的长支链 和短支链,以及聚氯乙烯的支链是如何形成的?
答:自由基向大分子转移,在大分子链上形成活性点, 引发单体增长,形成支链,聚乙烯的长支链是分子间 转移的结果,而短支链则是分子内转移的结果。
M x+C H 2 C H X
M x H +C H 2 C
M M n C H 2 C
-3760<0,可以进行; 而当T=500K时,⊿G=⊿H-T⊿S=-
56500+117.2×500=2100>0,不能进行。
8、以过氧化二苯甲酰作引发剂,苯乙烯聚合时各基元反应的活化 能较为从E50d=℃12增5k至J·m60o℃l-1以,及E从p=8302.℃6k增J·m至o9l-01 ,℃聚Et=合10速kJ率·m和ol聚-1 ,合试度比的 变化。光引发的情况又如何?
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(1)无规共聚物
单体单元 M2
单体单元 M1 命名:在单体间插入-CO-表示,例如 聚(丁二烯—CO—苯乙烯)
由自由基共聚得到的多高为分子此化学类第产三章物,如Vc—VAc共聚物。
(2)交替共聚物
两种单体单元严格呈交替排列
命名:在单体间插入-alt-表示, 如聚(苯乙烯-alt-马来酸酐)
高分子化学第三章
(4)接枝共聚物
主链
支链
命 名: 主链在前,中间插入 -g- 或 -graft- 表示, 例如聚丁二烯-g-聚苯乙烯,或聚(丁二烯-g-苯乙 烯)或(丁二烯/苯乙高分烯子化)学第接三章枝共聚物
如ABS树脂,SB为主链,A为支链(亦可AB为主 链,S为支链)。
无规和交替共聚物为均相体系,可由一般共聚反 应制得。 嵌段和接枝共聚物往往呈非均相,由特殊反应制 得,另行讨论。
由一段M1链段与一段M2链段构成的嵌段共聚物,称 为AB型嵌段共聚物。如苯乙烯-丁二烯(SB)嵌段共聚 物。由两段M1链段与一段M2链段构成的嵌段共聚物。称 为ABA型嵌段共聚物。如苯乙烯-丁二烯-苯乙烯(SBS) 嵌段共聚物。由n段M1链段与n段M2链段交替构成的嵌段 共聚物,称为(AB)n型嵌段共聚物。
高分子化学第三章
2) 链增长反应
M1* M2*
M1
四种 链增长反应
M2
高分子化学第三章
2) 链增长反应(M1* ,M2* ,M1, M2)
M*1 + M1 k11
M*1 , R11= k11[ M*1][ M1]
M*1 + M2 k12
M*2 , R12= k12[ M*1][ M2]
M*2 + M1 k 21
高分子化学第三章
R + M 1 k i1
RM1
R i,1
链引发
R + M2
k i2
RM2
R i,2
M 1 + M 1 k11
M1
R 1 1 = k 1 1 [ M 1 ] [ M 1 ](3-1)
链增长
M 1 + M 2 k12 M 2 + M 1 k21
M2
R 1 2 = k 1 2 [ M 1 ] [ M 2 ] (3-2)
高分子化学第三章
(2)扩大单体的原料来源
某些单体不能均聚,但能与其他单体共聚, 从而增加了聚合物的品种。
例如马来酸酐是1, 2取代单体,不能均聚。但 与苯乙烯或醋酸乙烯能很好共聚,是优良的织物 处理剂和悬浮聚合分散剂。
1, 2-二苯乙烯也不能均聚,但能与马来酸酐 共聚。产物严格交替。
(3)理论研究
[ CH2 CH CH CH ]n
CC OOO
CH CH + CH CH
[ CH CH CH CH ]n
CC OOO
CC OOO
高分子化学第三章
(3)嵌段共聚物
较长的 M1 链段
较长的 M2 链段
可以是二嵌段、三嵌段或多嵌段的, 如AB型、ABA型、ABC型和(AB)n型等
命名: 用-b-或-block-表示, 例如聚(苯乙烯-b-丁二烯)或(苯乙烯 /丁二烯)高嵌分子化段学第共三章聚物
3 三、自由基共聚(P76)
共聚合反应的特征 自由基共聚反应机理
竞聚率与共聚物组成关 系
控制共聚物组成的方法
高分子化学第三章
共聚合反应的特点和意义
1 共聚合及其共聚物的概念
由一种单体进行的聚合,称为均聚。产物称为 均聚物。由两种或两种以上单体共同参与的聚合反 应,称为共聚合。产物含有两种或两种以上单体单 元,称为共聚物。 。
M1
R 2 1 = k 2 1 [ M 2 ] [ M 1 ](3-3)
M 2 + M 2 k22
M2
R 2 2 = k 2 2 [ M 2 ] [ M 2 ](3-4)
M*1 , R21= k21[ M2*][ M1]
M*2 + M2 k22
M2* , R22= k22[ M2*][ M2]
高分子化学第三章
3) 链终止反应(M1*,M2*)
M*1 + M*1 +
M1* kt11 高分子 Rt11= k t11[ M*1]2 M*2 k t12 高分子 Rt12= k t12[ M*1] [ M2*]
高分子化学第三章
自由基共聚合反应机理P78
自由基共聚合反应的基元反应与均聚相同, 也可分为链引发、链增长、链终止三个阶段。二 元共聚涉及两种单体,因此有两种链引发、四种 链增长和三种链终止。
高分子化学第三章
(1) 链引发反应(两种单体)
K i1
单体1 或 2
或 K i2
R*M1 k i1RM 1* R*M2k i 2RM 2*
高分子化学第三章
交替共聚物 M1、M2两单元严格相间
M 1 M 2 M 1 M 2 M 1 M 2 M 1 M 2 M 1 M 2 M 1 M 2 M 1
实际上,这可看成无规共聚物的一种特例。如 苯乙烯—马来酸酐共聚物是这类产物的代表。 也可由自由基共聚得到。
CH2 CH + CH CH
CC OOO
高分子化学第三章
主单体
典型的共聚性能和主要性能
乙烯
乙酸乙烯酯
增加柔性,软塑料, 可作聚氯乙烯共混料
乙烯
丙烯
破坏结晶性,增加柔性和弹性,乙丙橡胶
异丁烯
异戊二烯
引入双键供交联用,丁基橡胶
丁二烯
苯乙烯
增加强度,耐磨耗,通用丁苯橡胶
丁二烯
丙烯腈
增加耐油性,丁腈橡胶
苯乙烯
丙烯腈
共聚合反应可用于研究单体、自由基、阴离 子和阳离子的活性,了解单体活性与聚合物结构 之间的关系,控制共聚物的组成与结构,设计合 成新的聚合物。
高分子化学第三章
2 共聚物的类型与命名P77
根据大分子链的微观结构,共聚物有下列四 种类型:
1) 无规共聚物 2) 交替共聚物 3) 嵌段共聚物 4) 接枝共聚物
提高抗冲强度,增韧塑料
氯乙烯
乙酸乙烯酯
增加塑性和溶解性能,塑料和涂料
四氟乙烯
全氟丙烯
破坏结构规整性,增加柔性,特种橡胶
甲基丙烯酸甲酯
苯乙烯
改善流动性和加工性能,模塑料
丙烯腈
丙烯酸甲酯衣康酸 改善柔软性和染色性能,合成纤维
高分子化学第三章
1、研究共聚合的意义P76 (1)改性
均聚物数量有限。共聚后,可改变大分子的 结构和性能,扩大应用范围。是高分子材料的重 要改性方法。 举例: 乙烯和丙烯都是塑料。将乙烯和丙烯共聚合,得 到的是乙丙橡胶。 聚苯乙烯是一种脆性材料。将其与丙烯腈共聚, 可得到优良的抗冲性、耐热性、耐油性和耐化学 腐蚀性的材料。 将丁二烯与苯乙烯无规共聚,可得到丁苯橡胶; 而进行嵌段共聚,则得到SBS热塑性弹性体。
