化学方程式计算习题_2
(化学)九年级化学化学方程式的计算常见题型及答题技巧及练习题(含答案) (2)

(化学)九年级化学化学方程式的计算常见题型及答题技巧及练习题(含答案)一、中考化学方程式的计算1.硝酸铵是农业生产中常用的化学肥料。
为测定某含有少量NaNO 3的硝酸铵样品中 NH 4NO 3的纯度,取2.0g 该硝酸铵样品于容器中,滴入5.0g 20%的NaOH 溶液。
反应过程中放出的氨气质量及加入的NaOH 溶液的质量的关系如图所示:完成有关计算:(1)样品中硝酸铵的质量是____________ g 。
(2)所得溶液中 NaNO 3的质量分数是___________(保留一位小数)。
【答案】1.6 31.5% 【解析】 【分析】(1)从图中可看出氢氧化钠溶液滴加到4克时硝酸铵恰好完全反应,根据参加反应的氢氧化钠的质量求出硝酸铵的质量,即可解答;(2)根据参加反应的氢氧化钠的质量求出生成的硝酸钠的质量,用生成的硝酸钠的质量+原有的硝酸钠的质量为所得溶液中硝酸钠的质量;用样品的质量+所加氢氧化钠溶液的质量-氨气的质量(氨气的质量可根据氢氧化钠的质量求出)为所得溶液的质量;再根据溶质质量分数计算公式即可求出所得溶液中硝酸钠的质量分数。
【详解】(1)设2.0g 样品中含NH 4NO 3的质量为x 。
43332NH NO NaOH NaNO NH H O 4g 20%+=++8040x↑⨯48g 0x =4020%⨯ x= 1.6g答:样品中硝酸铵的质量是1.6g 。
(2)反应生成 NaNO 3的质量为 y ,反应生成的NH 3的质量为z 。
43332NH NO NaOH N +=++408517y aNO NH H O40%zg 2↑⨯404g 20%=85y ⨯ 404g 20%=17z ⨯ y= 1.7g z= 0.34g反应后所得溶液中NaNO 3的质量分数为=1.7g+(2g-1.6g)100%=31.5%2g+5g-0.34g⨯ 答:所得溶液中 NaNO 3的质量分数是31.5%。
【点睛】做本道题时要将4克氢氧化钠溶液和5克氢氧化钠溶液区分清,不能乱用,参加反应的氢氧化钠溶液的质量是4克,所加的氢氧化钠溶液的质量是5克。
(化学)化学化学方程式的计算练习题20篇及解析

(化学)化学化学方程式的计算练习题20篇及解析一、中考化学方程式的计算1.将一定质量的金属锌投入到100g稀硫酸中,恰好完全反应,放出气体的质量与反应时间的关系如图所示。
试求:(1)完全反应后生产氢气的质量为___________g。
(2)所用硫酸溶液的溶质质量分数_________。
(计算结果精确到0.1%)。
【答案】0.4 19.6%【解析】【分析】【详解】(1)由图可知,完全反应后生成氢气的质量为0.4g;(2)设所用硫酸溶液的溶质质量分数为x2442Zn+H SO=ZnSO+H982100gx0.4g98100gx =20.4gx=19.6%答|所用硫酸溶液的溶质质量分数为19.6%。
2.某研究性学习小组为测定铜锌合金中铜的质量分数,进行如下实验:取合金 10g,向其中不断加入稀硫酸,产生的气体与所加稀硫酸的质量关系如图所示:求:合金中铜的质量分数______。
【答案】67.5%【解析】【分析】铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气,根据图示数据可以得出生成氢气的质量,根据氢气的质量可以计算出锌的质量,进一步计算出铜锌合金中铜的质量分数。
【详解】由图示数据可知,当加入20g 稀硫酸时,合金中的锌恰好反应完全,产生0.1g 氢气。
设参加反应的锌的质量为ag 。
2442n +H SO nSO H 652ag0.1g Z Z =+↑ 65a =20.1,解得a=3.25g 则合金中铜的质量为10g-3.25g=6.75g ,合金中铜的质量分数=6.75g 10g×100%=67.5%, 答:合金中铜的质量分数为67.5%。
3.一同学取来某品牌的钾肥(主要成分硫酸钾,还含少量的氯化钾)共200克,投入到908克的氯化钡溶液中恰好完全反应。
经过滤后得到硫酸钡沉淀233克和氯化钾的不饱和溶液。
请帮他计算:(注明:K 2SO 4+ BaCl 2= BaSO 4↓+2KCl )(1)氯化钾的相对分子质量是_______。
【化学】 化学方程式的计算练习题(含答案)经典

【化学】 化学方程式的计算练习题(含答案)经典一、中考化学方程式的计算1.碳酸氢钠用于焙制糕点,在270℃时分解:323222NaHCO Na C ΔO H O CO ++↑。
现取3NaHCO 16.8g ,在敞口容器中加热到质量不再改变为止,减少的质量为( ) A .4.4gB .6.2gC .8.8gD .10.6g【答案】B【解析】【分析】【详解】根据题意可知,在敞口容器中加热到质量不再改变为止,剩余物质为固体碳酸钠。
此题为固体的差量计算,设减少的质量为x 。
323222NaHCO Na CO +H O +CO 1681066216.8g x ↑△固体减少的质量16816.8g =62xx=6.2g2.铝被称为“年轻的金属”,工业上用电解氧化铝的方法制取金属铝。
反应的化学方程式为2Al 2O 3通电 4Al +3O 2↑。
请计算生成1.08t 金属铝,理论上需要氧化铝的质量是多少____?【答案】2.04t【解析】【分析】【详解】解:设生成1.08t 金属铝,理论上需要氧化铝的质量为x 2322Al O 4Al +3O 204108x 1.08t↑通电 204x =108 1.08tx=2.04t答:生成1.08t 金属铝,理论上需要氧化铝的质量为2.04t 。
3.我国科学家实现电催化高效分解硫化氢制氢技术,反应的化学方程式为H 2S 一定条件S ↓ +H 2 .请计算生产 3吨 H 2,理论上需要 H 2S 多少吨?【答案】51吨【解析】【分析】【详解】解:设理论上需要H 2S 的质量为x22S +H 342x3tH S ↓一定条件34x =23tx=51 t答:理论上需要H 2S 51吨。4.某工厂需要16kg 氧气作原料,若用电解水的方法制取这些氧气,消耗水的质量是_________?(要求写出计算过程)【答案】18kg【解析】【分析】【详解】设消耗水的质量为x2222H O2H +O 3632x 16kg↑↑通电 36x =3216kgx=18kg答:消耗水的质量是18kg 。
化学方程式的计算练习题(含答案)

化学方程式的计算练习题(含答案)一、中考化学方程式的计算1.请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:计算稀盐酸中溶质质量。
【答案】7.3g【解析】【分析】【详解】根据质量守恒反应前后物质总质量不变可得二氧化碳的质量等于12g+100g+100g-207.6g=4.4g设稀盐酸中溶质质量为x3222CaCO2HCl=CaCl CO H O7344x 4.4g73x=,x=7.3g44 4.4g++↑+答:稀盐酸中溶质质量7.3g【点睛】根据质量守恒,求出二氧化碳质量,根据二氧化碳质量求稀盐酸中溶质质量2.波尔多液是一种运用广泛的农药,由熟石灰和硫酸铜配制而成。
某工厂用以下反应:2Cu+O2+2H2SO4=2CuSO4+2H2O 来生产硫酸铜,若要制得 40kg 硫酸铜。
试计算:(1)硫酸铜中铜元素质量分数是_____。
(2)若恰好消耗稀硫酸的质量是 200kg,则该稀硫酸溶质的质量分数是多少_____?【答案】40% 12.25%【解析】【分析】【详解】(1)CuSO4中Cu元素质量分数=6464100%=100%=40% 6432416160⨯⨯++⨯。
(2)设消耗的硫酸的质量为x 。
22442H SO 2CuSO 2Cu O 2=2982160x 40kg2H O+++⨯⨯ x 29840kg 2160⨯=⨯ x=24.5kg则稀硫酸溶质的质量分数=24.5kg 100%=12.25%200kg⨯。
3.向 100 克 MgCl 2 和 HCl 的混合溶液中,逐滴加入 10%的氢氧化钠溶液,反应情况,如图所示。
(1)当滴加氢氧化钠溶液的质量至 N 点时所得溶液的 pH 值为_______(填编号); A 大于 7 B 等于 7 C 小于 7(2)通过计算,确定 M 点时所得溶液中溶质的质量分数,写出计算过程____。
【答案】A 9.2%(详见解析)【解析】【分析】向 100 克 MgCl 2 和 HCl 的混合溶液中,逐滴加入 10%的氢氧化钠溶液,氢氧化钠先与盐酸反应,等盐酸完全反应后再与氯化镁反应。
化学方程式的计算练习题40道

化学方程式的计算练习题40道化学方程式的计算练习题40道一、根据化学方程式进行计算1、在一个有6克氧气的密闭容器中,有5克铁粉和足量的硫,加热使之充分反应,问生成多少克固体混合物?2、现有10克氢气和氧气混合气体,点燃使之充分反应,得到5克水蒸气,问原来混合气体中各成分的质量?3、欲制得100千克碳酸钙含量为80%的石头灰,需要煅烧含碳酸钙含量为85%的石灰石多少千克?4、在一定条件下,11.2克金属钠与氧气完全反应,生成16.6克氧化物,求氧化物的化学式。
5、现有硫酸铜溶液20千克,其中含铜的质量分数为6%,现欲采用电解的方法除去其中的水分,问需要除去的水分质量为多少千克?(设水的质量分数为99%)二、物质的量在化学方程式计算中的应用6、在39千克过氧化氢溶液中,加入0.5千克二氧化锰,充分反应后可以得到多少摩尔氧气?61、在标准状况下,11.2升一氧化碳和13.2升氢气混合,充分反应后得到多少克产物?611、一定量的乙醇在氧气不足的情况下燃烧,得到二氧化碳、一氧化碳和水的总质量为50.4克,其中水的质量为25.2克,求二氧化碳的质量。
6111、在一个密闭容器中,有适量铜与一定量氧气反应,生成氧化铜的质量为16克,问消耗氧气的质量为多少?三、有关溶液的计算10、在20℃时,将33克食盐放入100克水中,充分溶解后得到溶液。
已知在该温度下,食盐在水中的溶解度为36克,求所得溶液的质量分数。
101、将58.5克食盐全部溶于200克水中,求该食盐溶液的质量分数。
1011、在20℃时,将40克硝酸钾溶于100克水中,已知在该温度下,硝酸钾在水中的溶解度为60克,求所得溶液的质量分数。
四、综合计算13、工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。
现称取纯碱样品12克,全部溶解在94.7克水中。
当加入稀盐酸73克时,恰好完全反应。
生成的气体全部逸出,所得溶液质量为170.2克。
计算反应后所得溶液中溶质的质量分数。
化学方程式计算练习题

化学方程式计算练习题1. 计算下列化学反应中,如果生成物中二氧化碳的质量为44g,那么需要多少质量的碳酸钙反应?CaCO3 → CaO + CO2↑2. 某化学反应中,甲烷和氧气反应生成二氧化碳和水,如果甲烷的质量为16g,计算生成的二氧化碳的质量。
CH4 + 2O2 → CO2 + 2H2O3. 铁与稀硫酸反应生成硫酸亚铁和氢气,若生成的氢气质量为2g,计算反应中消耗的铁的质量。
Fe + H2SO4 → FeSO4 + H2↑4. 铜与硝酸银溶液反应生成硝酸铜溶液和银,若生成的银质量为216g,计算反应中消耗的铜的质量。
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag5. 碳酸氢铵受热分解生成氨气、水和二氧化碳,若生成的二氧化碳质量为88g,计算反应中消耗的碳酸氢铵的质量。
NH4HCO3 → NH3↑ + H2O + CO2↑6. 硫酸铜与氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,若生成的氢氧化铜质量为98g,计算反应中消耗的硫酸铜的质量。
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO47. 锌与稀盐酸反应生成氯化锌和氢气,若生成的氢气质量为0.2g,计算反应中消耗的锌的质量。
Zn + 2HCl → ZnCl2 + H2↑8. 碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,若生成的二氧化碳质量为22g,计算反应中消耗的碳酸钠的质量。
Na2CO3 + 2HCl → 2NaCl + H2O + CO2↑9. 镁条在空气中燃烧生成氧化镁和氮气,若生成的氧化镁质量为60g,计算反应中消耗的镁的质量。
2Mg + O2 → 2MgO10. 硫酸和氢氧化钡反应生成硫酸钡沉淀和水,若生成的硫酸钡沉淀质量为233g,计算反应中消耗的硫酸的质量。
H2SO4 + Ba(OH)2 → BaSO4↓ + 2H2O。
化学方程式习题

化学方程式习题化学方程式是化学反应中物质转化和化学变化的描述方式。
掌握好化学方程式的书写和解析对于化学学习非常重要。
本文将提供一些化学方程式的习题,帮助读者加深对化学方程式的理解和运用。
习题一:简单的化学反应方程式1. 将氢气与氧气反应生成水的化学方程式是什么?答案:2H2 + O2 → 2H2O2. 苯酚与多氯联苯反应生成二苯胺的化学方程式是什么?答案:C6H5OH + C12H10Cl6 → 2C12H11N + 6HCl习题二:配平化学方程式1. 铝与氧气反应生成氧化铝的化学方程式中,配平下列方程式:Al + O2 → Al2O3答案:4Al + 3O2 → 2Al2O32. 氢气与氧气反应生成水的化学方程式中,配平下列方程式:H2 + O2 → H2O答案:2H2 + O2 → 2H2O习题三:酸碱中和反应1. 氢氧化钠与盐酸反应生成水和氯化钠的化学方程式是什么?答案:NaOH + HCl → H2O + NaCl习题四:氧化还原反应1. 氧化镁与铝反应生成氧化铝和镁金属的化学方程式是什么?答案:2Mg + Al2O3 → 2Al + 3MgO2. 二氧化硫氧化为三氧化硫的化学方程式是什么?答案:2SO2 + O2 → 2SO3习题五:沉淀反应1. 硫酸钙与氯化钠反应生成氯化钙和硫酸钠的化学方程式是什么?答案:CaSO4 + 2NaCl → CaCl2 + Na2SO42. 硝酸银与氯化钠反应生成氯化银和硝酸钠的化学方程式是什么?答案:AgNO3 + NaCl → AgCl + NaNO3习题六:燃烧反应1. 丙烯燃烧生成二氧化碳和水的化学方程式是什么?答案:C3H6 + 4O2 → 3CO2 + 3H2O习题七:还原反应1. 氧化铁还原生成铁的化学方程式是什么?答案:Fe2O3 + 3H2 → 2Fe + 3H2O2. 二氧化锰还原生成锰的化学方程式是什么?答案:MnO2 + 4HCl → MnCl2 + 2H2O + Cl2通过以上习题,读者可以更好地理解和掌握化学方程式的书写与解析。
根据化学方程式计算习题带答案
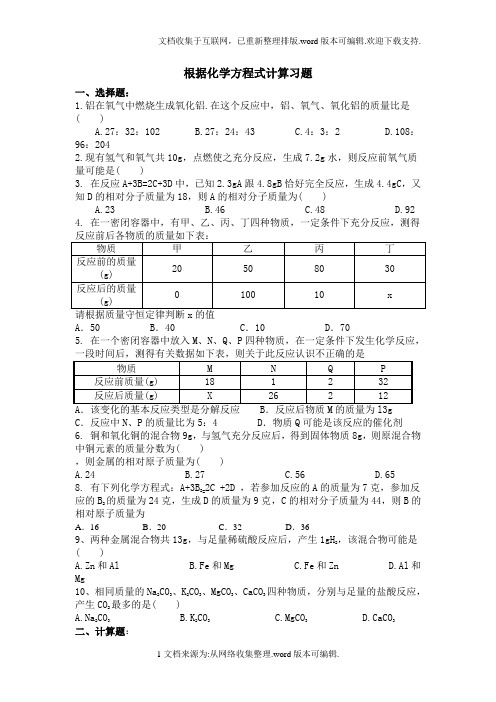
根据化学方程式计算习题一、选择题:1.铝在氧气中燃烧生成氧化铝.在这个反应中,铝、氧气、氧化铝的质量比是( )A.27:32:102B.27:24:43C.4:3:2D.108:96:2042.现有氢气和氧气共10g,点燃使之充分反应,生成7.2g水,则反应前氧气质量可能是( )3. 在反应A+3B=2C+3D中,已知2.3gA跟4.8gB恰好完全反应,生成4.4gC,又知D的相对分子质量为18,则A的相对分子质量为( )A.23B.46C.48D.924. 在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得A.50 B.40 C.10 D.705. 在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,C.反应中N、P的质量比为5:4 D.物质Q可能是该反应的催化剂6. 铜和氧化铜的混合物9g,与氢气充分反应后,得到固体物质8g,则原混合物中铜元素的质量分数为( ),则金属的相对原子质量为( )A.24B.27C.56D.658. 有下列化学方程式:A+3B2=2C +2D ,若参加反应的A的质量为7克,参加反应的B2的质量为24克,生成D的质量为9克,C的相对分子质量为44,则B的相对原子质量为A.16 B.20 C.32 D.369、两种金属混合物共13g,与足量稀硫酸反应后,产生1gH2,该混合物可能是( )A.Zn和AlB.Fe和MgC.Fe和ZnD.Al和Mg10、相同质量的Na2CO3、K2CO3、MgCO3、CaCO3四种物质,分别与足量的盐酸反应,产生CO2最多的是( )A.Na2CO3B.K2CO3C.MgCO3D.CaCO3二、计算题:1. 宇航员在太空舱中,往往可利用自己呼出的二氧化碳与过氧化钠粉末作用来获得所需的氧气,并合理处理呼出的二氧化碳。
(反应方程式为2Na2O2+2CO2===2Na2CO3+O2)假如某宇航员在某次太空飞行中预计消耗氧气480kg,则该宇航员应在太空舱中至少准备多少克过氧化钠。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学方程式计算习题
一.已知反应物(或生成物)的质量求生成物(反应物)的质量
1.某实验室中需要5g氧气。
若用电解水的方法制取这些氢气,需要消耗水多少克?
2.把干燥、纯净的氯酸钾和二氧化锰的混合物15.5g装入大试管中,加热制取氧气。
待反应完全后,将试管冷却、称量,得到10.7g固体物质。
计算:①制得的氧气多少克?②剩余固体中各物质质量?
二.反应物过量的计算:
3.实验室用5g锌和5mL的稀硫酸反应制取氢气,反应完全后称得剩余的锌粒为3.7g,问可以生成氢气多少克?
三.混合物的计算:
4.某高锰酸钾样品含高锰酸钾的质量分数为80%,求加热7.9g该样品可生成O2多少克?
四.讨论法:
5.40g氢气和氧气的混合气体在点燃后经充分反应后生成了36g的水,求原混合气体中氢气和氧气的质量比为多少?
五.关系式法:
6.(1)54g的水在通电的条件下分解放出的氧气和多少克的氯酸钾完全反应后生成的氧气的质量相同?
(2)54g的水在通电的条件下分解放出的氢气和多少克的锌与足量的稀硫酸反应后放出的氢气的质量相同?六.差量法:
7.用氢气还原10g氧化铜样品,反应一段时间后,剩余固体的质量为8.4g,求反应生成的铜的质量为?(CuO
+H2Cu+H2O)
8.将8g铁钉投入硫酸铜溶液中,一段时间后,将铁钉取出,称得铁钉的质量为8.8g,求参加反应的铁的质量?
练习试题:
1.实验室用28g的铁与100g足量稀盐酸充分反应后最多可以得到多少克的氢气?
2.某炼钢厂日产含杂质5%的生铁3000t,该炼钢厂每天需含Fe2O3质量分数为85%的赤铁矿石多少吨?(计算结果保留整数)
3.加热分解多少克高锰酸钾所得到的氧气的质量与122.5g氯酸钾分解放出的氧气的质量相同?
4.镁易被空气中的氧气氧化成氧化镁。
现有一卷标签上标明120g的镁带,称其质量为136g(假设除镁被氧化外,没有发生其他任何变化,且氧化是均匀的)。
(1)试计算被氧化的镁的质量是多少克?
(2)称取上述变质的镁带6.8g加入到足量的盐酸溶液中反应,试计算反应产生氢气的质量是多少克?5.某学生称取一定质量的氯酸钾装入试管中加热后有氧气放出,几分钟后停止加热,冷却后称得残留在试管中的物质的质量为8.84g,接着向试管中加入0.1g二氧化锰,继续加热到不再产生氧气时,最后称得剩下的残留物的质量为6.06g,求未加入二氧化锰时,氯酸钾的分解率是多少?(注:分解率是已分解的该物质的质量与原有的该物质的质量之比)
6海南省] 黄铜是铜和锌的合金,在20g黄铜样品中加入足量稀盐酸使其完全反应,生成氢气0.2g,求样品中铜的质量。
例:把氯酸钾和二氧化锰的混合物15.5g放入大试管中加热,充分反应后冷却、称量,剩余固体质量为10.7g。
剩余固体里有哪些物质?各多少克?(已知相对原子质量:K 39 Cl 35.5 O 16)
解法一:常规法
根据质量守恒定律,氧气的质量为:15.5 g-10.7 g=4.8 g
设:剩余固体中含氯化钾质量为X
二氧化锰的质量为:10.7 g -7.45 g =3.25 g
答:剩余固体中含氯化钾质量为7.45g,二氧化锰的质量为3.25 g。
分析:本题已知反应物(是混合物)的质量,由于是充分反应,反应后的剩余固体里没有氯酸钾,二氧化锰是
催化剂,其质量在化学反应前后不变。
所以剩余固体里的成分是氯化钾和二氧化锰的混合物。
在反应:2KClO
3
2KCl + 3O
2↑中,根据质量守恒定律,反应前KClO
3
与反应后KCl质量之差等于氧气的质量。
然后根据氧气质量
计算氯化钾的质量,最后求二氧化锰的质量(切忌:列比例求二氧化锰质量)。
特点:已知一种生成物质量或一种参加反应的反应物质量,代入化学方程式列比例即可求出化学方程式中另外所有反应物或生成物的质量。
你来试一试?
①(2006年重庆中考题)煤炭中往往含有硫,直接燃烧产生的二氧化硫会污染环境。
计算含硫400 g的煤炭燃烧时产生二氧化硫的质量。
②将氯酸钾与0.1 g二氧化锰混合加热制取氧气,当收集到所需氧气后停止加热,冷却称量剩余固体4.04 g,
继续加热至完全反应,又收集到0.96 g氧气,求原混合物中氯酸钾的质量。
解法二:量差法
设:剩余固体中含氯化钾质量为X
二氧化锰的质量为:10.7g -7.45g =3.25g
答:剩余固体中含氯化钾质量为7.45g,二氧化锰的质量为3.25g。
分析:先找准反应前后固体质量之差等于氧气质量。
将其相对分子质量列在△m(表示某一反应前后同一种状态质量的改变量)正下方,然后将本题反应前固体15.5g与反应后固体10.7g之差代入,即可求出化学方程式中另外所有反应物或生成物的质量。
特点:已知化学反应前后某一种状态(指固、液或气三态)质量的改变量,先找准化学方程式里这种状态的改变量,然后代入本题这种状态的改变量,列比例即可求出化学方程式中另外所有反应物或生成物的质量。
你来试一试?
①加热31.6 gKMnO
4
,反应一段时间后停止加热,冷却称量,剩余固体质量为30g 。
计算(1)产生氧气多少克?(2)剩余固体中有哪些物质?各多少克?
②实验室用H
2还原CuO,当m克CuO部分变红时停止加热,冷却后停止通H
2
,称得残留固体物质为n克,实
验中用去W克H
2,生成a克H
2
O,则得到Cu的质量为
解法三:关系式法
根据质量守恒定律,氧气的质量为:15.5 g-10.7 g=4.8 g
设:剩余固体中含氯化钾质量为X
2KCl~3O
2
↑
149 96
X 4.8 g
二氧化锰的质量为:10.7g -7.45g =3.25g
答:剩余固体中含氯化钾质量为7.45 g,二氧化锰的质量为3.25 g。
分析:由方程式已知量(O
2)和未知量(KCl)的关系式为:2KCl~3O
2
↑,本题将已知量氧气代入,列比例即可
求出未知量氯化钾的质量。
关系式省去了化学方程式中无关物质的质量,使得运算过程得以简化。
特点:找准题目中已知量和未知量之间的关系式。
特别要注意化学式前的化学计量数,其数值由化学方程式来确定。
关系式法常常用于多步反应的计算。
你来试一试?
①利用高锰酸钾制取氧气,并将氧气跟铜反应制取氧化铜,现要制取8g氧化铜需高锰酸钾多少克?
②加热KClO
3和MnO
2
的混合物制O
2
,将产生的O
2
用于红磷燃烧的实验,若要制30gP
2
O
5
,需KClO
3
的质量至少
是多少克?
解法四:元素守恒法
设:剩余固体中含氯化钾质量为X
参加反应的氯酸钾质量为y
由化学方程式:2KClO
3 2KCl + 3O
2
↑知:
根据质量守恒定律,氧气的质量为:15.5g-10.7g=4.8g
根据氧元素质量守恒:
y·=4.8g
y=12.25g
根据钾元素质量守恒:
12.25g×=X·
X=7.45g
二氧化锰的质量为:10.7g -7.45g =3.25g
答:剩余固体中含氯化钾质量为7.45g,二氧化锰的质量为3.25g
分析:本题已知氧气的质量,根据KClO
3和O
2
中氧元素质量的相等关系,可求出KClO
3
质量,再根据KClO
3
和KCl
中钾元素(或氯元素)质量的相等关系,可求出KCl的质量,最后算出MnO
2
的质量。
特点:找准化学反应前后化学式中某一种元素质量的相等关系。
由于省略无关的化学式和一些元素,使得计算过程大大化简。
对于一些较复杂的化学方程式的计算,运用该法显得特别简单。
它适用于一切化学反应的计算。
①某有机物在6.4gO
2中完全燃烧生成4.4gCO
2
和3.6gH
2
O,通过计算说明该有机物中是否含有氧元素?
②一定质量的甲烷(CH
4)在O
2
不完全的条件下燃烧,得到CO、CO
2
和H
2
O,其总质量为11.2克,若其中水的
质量为5.4g,生成CO
2
的质量是多少克?。
