第四章酰化反应答案
第四章 烃化反应

H2C N N
+
ROH
H3C N N OR
N2
CH3OR
R = Ar 或 R' C 酸 O 酚
OMe OMe OH OMe OH OH
过量CH2N2
2 mol CH2N2
COOMe
COOMe
COOH
什么情况下为过量? 1 mol CH2N2
OH OH
羧酸比酚更易于反应
COOMe
DCC催化酚醇偶联 催化酚醇偶联
b
R H
OH
H H Nu
过渡态时 C- O断 裂 少 - 断
位阻小
H2SO4
Ph O
* CH2OH Ph 2h
OMe
+ +
Ph
* CH2OMe
OH
+
MeOH CH3ONa 2h
Ph
90% * CH2OH
OMe
10% * CH2OMe
OH
Ph
25%
75%
由于产物中含羟基,如果环氧乙烷过量,就可形成聚醚, 由于产物中含羟基,如果环氧乙烷过量,就可形成聚醚,故 甲醇必须过量
多卤化物与醇钠反应,得到多醚化产物: 多卤化物与醇钠反应,得到多醚化产物:
CHCl3
+ 3 RONa CCl3NO2 + 4 RONa
CH(OR)3 C(OR)4
原酸酯 四烷氧基甲烷
Cl
EtOH/NaOH
NO2
OEt
(95.6%) 转化率70%
NO2
4.1.1.2 芳磺酸酯作烃化剂
芳磺酸酯的应用比硫酸酯(有毒 广 是很好的离去基团。 芳磺酸酯的应用比硫酸酯 有毒)广,且OTs是很好的离去基团。 有毒 是很好的离去基团
药物合成反应 第四章 酰化反应

O CHCl2 H2O
CHO
Vilsmeier甲酰化反应 芳香化合物、杂环化合物及活泼烯烃化合物用二取代 甲酰胺及氧氯化磷处理得到醛类的反应称Vilsmeier甲酰化 反应。是芳香环的甲酰化反应最普通的方法。
POCl3 R1 R1 + ArCHO ArH + N C H NH R2 R2 O
机理
B: PhCOCl
CH3COCHCOOC2H5 COPh
PhCOOH + CH2
X -CN -H -CN
X DEPC/Et3N/DMF X PhCOCH Y r.t. Y
Y -COOC2H5 -NO2 -CN 收率 93.4% 85.5% 92.8% 96.8%
-COOC2H5 -COOC2H5
(2). 酮及羧酸衍生物的-位C-酰化 Claisen酯缩合反应 含有-氢的酯在醇钠等碱性缩合剂作用下发生缩合作 用,失去一分子醇得到酮酯的反应称为Claisen酯缩合反应。
N CH3.I
C O + ( CH2 )n O
n=5 (89%) n=11 (69%)
N O CH3
(3) 羧酸三硝基苯酯
O R''OH+ R-C-OH + Cl
O2N NO2
O R-C-OR''
O2N
O R C O
O2N NO2
难 于 分 离 ,所 以 三 种 物 质 一 起 加 入
O2N
酸酐为酰化剂
73%
COOH
CH3
+
H3C
C
CH3
OH
(CF3CO)2O
COOBu-t
混合酸酐的应用 ②羧酸-磺酸混合酸酐
(整理)羧酸与胺的缩合酰化反应

羧酸与胺的缩合酰化反应王露化工与制药专业 1105班学号110150151指导教师刘雪凌老师摘要合成是制药的基本方法,也是很重要的方法,人类对药物的需求很大,要不断的创新、研发新药,合成是其中必不可少的方法,本文介绍了常见合成酰胺的方法,合成酰胺通用的方法是先活化羧基,然后再与胺反应得到酰胺。
其中羧酸与胺的反应是合成酰胺的重要方法【5】。
这一反应是一个平衡反应,采用过量的反应物之一或除去反应中生成的水,均有利于平衡向产物方向转移。
除去水的方法通常是在反应物中加入苯或甲苯进行共沸蒸馏【1】。
关键词:合成酰化活化前言药物对于我们任何一个人来说都不陌生,而且离不开。
现在药物的种类有很多,但还是有一些疾病无法治疗,所以我们需要不断的研发新药,而合成又是制药的基本领域和方法,所以我们需要学习、了解具体的合成方法【3】。
常见合成酰胺的方法➢羧酸与胺的缩合酰化反应➢氨或胺与酰卤的酰化反应➢氨或胺与酸酐的酰化反应➢其他缩合方法➢酯交换为酰胺➢氰基转化为酰胺羧酸与胺的缩合酰化反应1羧酸和胺的直接缩合反应羧酸与胺的反应是合成酰胺的重要方法: 这一反应是一个平衡反应,采用过量的反应物之一或除去反应中生成的水,均有利于平衡向产物方向转移。
除去水的方法通常是在反应物中加入苯或甲苯进行共沸蒸馏。
例如将a-羟基乙酸及苄胺于90℃共热,并蒸出生成的水及过量的苄胺,则生成a-羟基乙酰基苄胺【7】:90o C1.1混合酸酐法1.1.1混合酸酐法(一)氯甲酸酯法:主要应用羧酸与氯甲酸乙酯或异丁酯反应生成混合酸酐,而后再与胺反应得到相应的酰胺。
这一反应如果酸的a-位位阻大或者连有吸电子基团,有时会停留在混合酸酐这一步。
但加热可以促使其反应;这一反应也可用于无取代酰胺的合成。
ClCOOEt, NEt3 CHCl3, -20~5o C, 1.5h NH3 (gas) rt, 30min91%NMM, DMFr.t.33%1.1.2混合酸酐法 (二)羰基二咪唑:应用羰基二咪唑(CDI)与羧酸反应得到活性较高的酰基咪唑,许多酰基咪唑有一定的稳定性,有时可以分离出来。
第4章 烷基化反应和酰基化反应.

含活泼亚甲基氢的化合物如乙酰乙酸乙酯、丙二酸 二乙酯、2,4-戊二酮等与卤代烷的C-烷化反应可用于制 备其α-H被烃基取代的衍生物。
H C2H5ONa + H C COOC2H5
C4H9 C H COOC2H5
R'OR'OH
RHC O
CH2
[RCHCH2OR'] O-
RCHCH2OR' + R'OOH
高级脂肪醇能加成环氧乙烷生成高级脂肪醇聚氧乙烯醚型 非离子表面活性剂:
ROH + n H2C O CH2 RO (CH2CH2O )n H
高级脂肪酸也能加成环氧乙烷生成酯类聚氧乙烯型非离子表 面活性剂,是一种性能优良的乳化剂:
ROH + NaOH RO-Na+ + XAlk RO-Na+ + H2O ROAlk + NaX
在氢氧化钾和相转移催化剂聚乙二醇-400存在下,酚类与卤 代烷的反应非常顺利,如:
OH + CH3 I + KOH 聚乙二醇-
CH2Cl2,H2O
OCH3
+ KI + H2 O
用氯乙酸做烷基化剂可用于制备苯氧乙酸类的化合物。
O C
O Cl
<
H3C
C
Cl
4.4.1 用羧酸的N-酰化 用羧酸对胺类化合物进行酰化是合成酰胺的重要方法,反应有 水生成,是一个可逆反应,其酰化反应通式为:
R'NH2 + RCOOH R'NHCOR + H2O
酰化反应

-
-
R带吸电子基团 利于进行反应;R带给电子不利于反应; R的体积若庞大,则亲核试剂对羰基的进攻有位阻,不利于反应进行; R为芳基时,由于芳基与N原子或O原子的共轭效应,使N原子或O原子 上的云密度降低而反应活性下降,所以RNH2>ArNH2;ROH>ArOH 。
10
概 述 催化
酸碱催化
碱催化作用是可以使较弱的亲核试剂H-Nu转化成亲核性较强的 亲核试剂Nu-,从而加速反应。 酸催化的作用是它可以使羰基质子化,转化成羰基碳上带有更 大正电性、更容易受亲核试剂进攻的基团,从而加速反应进行。
16
第一节 氧原子的酰化反应
一 醇的氧酰化
b.催化剂
(1)质子酸催化法: 常用浓硫酸,氯化氢气体,磺酸,四氟硼酸等
O R C OH H+ OH R C OH OH R C OH
1) 羧酸为酰化剂
各种质子酸都具有各自卑优点和缺点。
17
第一节 氧原子的酰化反应
一 醇的氧酰化
1) 羧酸为酰化剂
浓硫酸具有催化能力强、性质稳定、价廉等优势,其缺 点是有一定的氧化性、易发生磺化、脱水、脱羧等副反应, 所以一般不饱和酸、羟基酸、甲酸、草酸、丙酮酸等不宜采 用之。 无水氯化氢具有催化能力强、无氧化性、价廉等优势,其 缺点是易发生加成、卤代等副反应,另外对反应设备的有一 定腐蚀性和易对环境造成一定的污染。一般不饱和酸(醇)、 叔醇等不易采用之。 对甲苯磺酸具有浓硫酸的一切优点,且无氧化性,在有机 溶剂中的溶解度较大,不易发生磺化副反应等优点,尤其是在 使用共沸带水等反应条件时更为适用,但其缺点是价格比较贵, 一般用于复杂结构的酯的制备中。
O C X
当然还有(硫代)异氰酸酯[R-N=C=O(S)]等.
药物合成反应 第四章 酰化反应

Et O RCOOH R NH2 Et O
O P
Et3N/DMF
O N BDP
N N Nr.t.20minRCOHR二、氮原子上的酰化反应
2.影响因素
(1)催化剂 为加快酰化反应的速度,有时需加入少量强酸 作为催化剂。
RCOOH H RC OH OH OH H RC OH OH R NH2 R C N R
羧酸是一个弱酰化剂,对于弱碱性氨基化合物若直接用 羧酸酰化较为困难,反应中可加入缩合剂以提高反应活性。 活性磷酸酯类是近年发展较快的一类N-酰化偶合剂,这 些试剂在反应中可迅速转化成相应的酯类活性中间体与胺反 应生成酰胺。
二、氮原子上的酰化反应
此类试剂由于具有活化能力强,反应条件温和,光学活 性化合物不发生消旋化等特点,广泛应用于肽类或β-内酰胺 类化合物的合成中。如苯并三唑基磷酸二乙酯(BDP)
间接酰化法
(1)间接亲电酰化
N(CH3)2 [ R2N CH Cl ] . OPOCl2 - HOPOCl2 N(CH3)2 CH Cl H2O N(CH3)2 CHO R2NH HCl NR2
间接酰化法
(2)间接亲核酰化
HS HS R 、C R S S S S O H2O/HgCl2 R C C4H9Li S S
- H2O
O R C NHR H
OH H
二、氮原子上的酰化反应
(2)胺的结构 羧酸作为酰化剂一般用于碱性较强的胺类,氨基氮原子 上的电子云密度愈大,空间位阻愈小,则反应活性愈强。胺 类化合物酰化反应的活性:伯胺>仲胺;脂肪胺>芳香胺。 在芳香族胺类化合物中,芳环上有给电子基团时,反应活性 增强;反之,有吸电子基团时,则反应活性下降。
C C C O
H N N H C O
第四章 酰化反应 答案
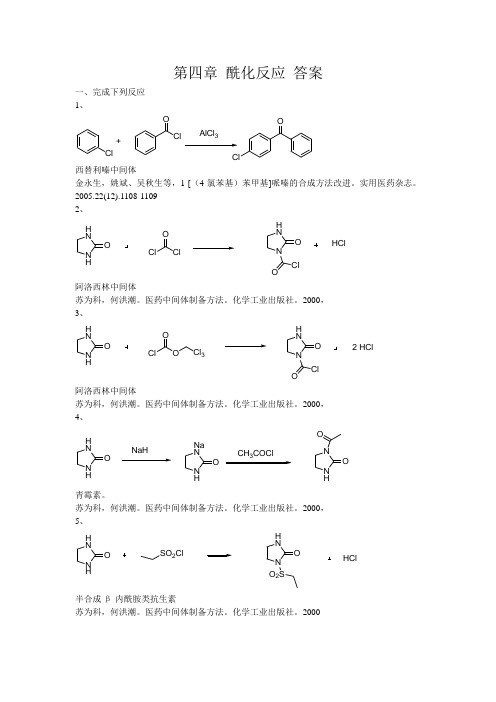
第四章 酰化反应 答案一、完成下列反应 1、ClClClOO+AlCl 3西替利嗪中间体金永生,姚斌、吴秋生等,1-[(4-氯苯基)苯甲基]哌嗪的合成方法改进。
实用医药杂志。
2005.22(12).1108-1109 2、 N HH NO ClO ClN H NO ClOHCl阿洛西林中间体苏为科,何洪潮。
医药中间体制备方法。
化学工业出版社。
2000, 3、 N HH NO ClO ON H NO ClO2 HClCl 3阿洛西林中间体苏为科,何洪潮。
医药中间体制备方法。
化学工业出版社。
2000, 4、 N HH NO NaHN HNa NO CH COClN HNO O青霉素。
苏为科,何洪潮。
医药中间体制备方法。
化学工业出版社。
2000, 5、 N HH NO SO 2ClN H NO O 2SHCl半合成β-内酰胺类抗生素苏为科,何洪潮。
医药中间体制备方法。
化学工业出版社。
20006、OOO3C OCH 2CH 2COOH芬不芬章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,1340 7N HS CH3C O O CCH O NS COCH 3乙酰丙嗪8NH 2COOHNHCOCH 3COOH安眠酮章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,13 9N N SH 2NSHCH3C O CCH 3O N N S HN SHCOCH 3乙酰唑胺章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,14 10 NH 2OHCH3C O O CCH O NHCOCH 3OH嘧啶苯芥章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,15 11 NH 23NHCOCH 3磺胺类药物章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,17 12NH2 F3CCl2NHCOClF3CClCH3CN卤卡班章思规。
实用精细化学品手册(有机卷)下。
2015酰化反应

反应机理:
RCOOH + C6H11N C NC6H11 C6H11 N C N C6H11 H RCOO NHC6H11 O RCOOH R C O C NC6H11 O C NHC6H11 O + RCOO R C O C NHC6H11 A O C6H11NHCNHC6H11
A
R'OH
R
O R' + H
酰化反应
酰化反应
定义:有机化合物分子中引入酰基的反应称为酰化 反应。主要发生在碳、氧、氮、硫等原子上。 用途:活性化合物的必要官能团 结构修饰和前体药物 羟基、胺基等基团的保护 类型:直接酰化 间接酰化
Page 2
直接酰化反应类型
亲电酰化反应 亲核酰化反应 自由基酰化反应
-H RCO2R'
Page 9
氨基的酰化:
O R' + H N R C OH R''
RCOO NH2R'R'' O R C OH NH R' R'' O R C N R' R''
羧酸与胺 需高温脱水 催化剂:可用DCC、DIC等缩水剂(活化羧酸)
Page 10
COOH NH2 N H CH3OH SOCl2 N H COOMe DCC/Et3N/CH2Cl2 COOH N H HN O
用量:至少是底物的一倍以上(?)
Page 32
催化剂的选择:
以酰氯、乙酸酐为酰化剂时,多用Lewis酸为催化剂如AlCl3、 FeCl3、TiCl4、ZnCl2
O C Cl F + AlCl3 NH2 O C F
NH2
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第四章 酰化反应 答案一、完成下列反应 1、ClClClOO+AlCl 3西替利嗪中间体金永生,姚斌、吴秋生等,1-[(4-氯苯基)苯甲基]哌嗪的合成方法改进。
实用医药杂志。
2005.22(12).1108-1109 2、 N HH NO ClO ClN H NO ClOHCl阿洛西林中间体苏为科,何洪潮。
医药中间体制备方法。
化学工业出版社。
2000, 3、 N HH NO ClO ON H NO ClO2 HClCl 3阿洛西林中间体苏为科,何洪潮。
医药中间体制备方法。
化学工业出版社。
2000, 4、 N HH NO NaHN HNa NO CH COClN HNO O青霉素。
苏为科,何洪潮。
医药中间体制备方法。
化学工业出版社。
2000, 5、 N HH NO SO 2ClN H NO O 2SHCl半合成β-内酰胺类抗生素苏为科,何洪潮。
医药中间体制备方法。
化学工业出版社。
20006、OOO3C OCH 2CH 2COOH芬不芬章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,1340 7N HS CH3C O O CCH O NS COCH 3乙酰丙嗪8NH 2COOHNHCOCH 3COOH安眠酮章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,13 9N N SH 2NSHCH3C O CCH 3O N N S HN SHCOCH 3乙酰唑胺章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,14 10 NH 2OHCH3C O O CCH O NHCOCH 3OH嘧啶苯芥章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,15 11 NH 23NHCOCH 3磺胺类药物章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,17 12NH2 F3CCl2NHCOClF3CClCH3CN卤卡班章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,1438 13NHNH2OOO N NHOO6-羟基-2-苯基-3-哒酮章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,1509 14O COCl +O CO2CHCOOCH2CH2CH(CH3)2 (CH3)2CHCH2CHCOOCH2OH呋布西林苏为科,何潮洪。
医药中间体制备方法。
化学工业出版社。
2001,671 15NH2CF32CH3NHCOClCF3间三氟甲苯异氰酸脂制备章思规。
实用精细化学品手册(有机卷)下。
化学工业出版社。
1996,1357 16COOH NO2HOCH CH N(C H)xylene O2N ONO盐酸普鲁卡因制备尤启冬。
药物化学。
化学工业出版社。
2005,89 醇的O-酰化17CH3NH2 CH3ClCH2COClCH3NHCH3ClO盐酸利多卡因制备尤启冬。
药物化学。
化学工业出版社。
2005,96 胺的N-酰化18H 3H 2+H 3COOEt 3N,DMFH 3CO依托咪酯尤启冬。
药物化学。
化学工业出版社。
2005,89 胺的N-酰化 19NHCH 3CClO ClCH 2COCl C 6H 12N CClO COCH 2Cl CH 3地西泮尤启冬。
药物化学。
化学工业出版社。
2005,114 胺的N-酰化 20F+ClClO3FClO氟哌啶醇尤启冬。
药物化学。
化学工业出版社。
2005,139 苯环的C-酰化 21OHAC 2OOHCOCH 3对乙酰氨基酚尤启冬。
药物化学。
化学工业出版社。
2005,176 苯环的C-酰化 22OHOH O +H 3COCH 3OO H SO O OHOOCH 3阿司匹林尤启冬。
药物化学。
化学工业出版社。
2005,179 酚的O-酰化 23H 3CONHNHSO 3NaClCOClN H 3COC NHO SO 3Na Cl吲哚美辛尤启冬。
药物化学。
化学工业出版社。
2005,187 胺的N-酰化 24N HClCl ClCH 2COClNO ClCl双氯芬酸钠尤启冬。
药物化学。
化学工业出版社。
2005,189 胺的N-酰化和苯环的C-烃化 25H 3CCH 3CH COCl 3H 3CCH 3CH 3O布洛芬尤启冬。
药物化学。
化学工业出版社。
2005,192 苯环的C-酰化 26H 3COCH 3CH 2COClAlCl 3H 3COCH 3O萘普生尤启冬。
药物化学。
化学工业出版社。
2005,193 芳环的C-酰化 27HO HOPOCl 3,ClCH 2COOHHO HOCCH 2ClO肾上腺素尤启冬。
药物化学。
化学工业出版社。
2005,240 苯的C-酰化 28H 3CSClO CH 3O H NOHOH 3CSNOCH 3OOHO卡托普利尤启冬。
药物化学。
化学工业出版社。
2005,283 胺的N-酰化 29、HC CHClClO 3ClClO替卡西林Tetrahydro,1984,70: 1555-1558 炔烃的碳酰化 30、N S NH 2OOOOC 2H 5OH HNS N HOO胺磺噻唑胺Bombas L. J Am Chem Soc. 1945,67,671 氮原子上的酰化反应 31、 SO O OSOCH 3COOH头孢西丁,头孢三唑Hartough H B, et al. J Am Chem Soc,1947,69:1102 碳原子上的酰化反应 32、 OO O OOOCH 3COOHH 3PO 4头孢呋辛,头孢呋辛酯Howard D,et al. J Am Chem Soc,1947,69:3093 碳原子上的酰化反应33、合成新型头孢菌素中间体3-乙酰基-2-咪唑烷酮-1-甲酰氯的合成 1)光气法NH NO TMSClNNNO OOTMS N ClTMSClNNO OTMS ClClO NNO OCOCl2)双光气法NH NO OClOO NNO OCOCl 2N22N2HCl3)光气法NH N O OCl 3ONNO OCOCl 3O 3HClCCl 3O 3苏为科。
3-取代基-1-氯甲酰基-2-咪唑烷酮,系列产品合成的研究报告。
杭州浙江大学,1995 Kong H B,Schrock W, Metzger K G .GB1392850 Michael P,et al. EP3992,1979 .33、COOHSOCl 23O盐酸塞庚啶尤启冬。
药物化学。
化学工业出版社。
2005,362 苯的C-酰化34、西维菌杀虫剂的合成OHCoCl 2NaOH TolOClO22NaOHO N HOHaynes, et al.,Contrib.Boye Thompson Inst.,1957,18,507 (1)氧原子上的酰化反应,酚的O-酰化 (2)氮原子上的酰化反应35、卡马西平的合成N HCOCl 2TolN 2ClO N ClOBr-HBrN ClO3C 2H 5OHN NH 2ODavis,M.A.et al.,J.Med.Chem.1964,7,88(1)氮原子上的酰化反应,光气为酰化剂 36、COOH H 2NNH 2I I I32COOHNHNH III OO泛影酸诊断用药J.Am.Chem.Soc.,1956,78,3210氮原子上的酰化反应,醋酐为酰化剂 37、N N HOEt 2NClO N N OO吡喹酮尤启冬。
药物化学。
化学工业出版社。
2005,395 胺的N-酰化 38Cl Cl F3CH 3COCl F ClCl C OCH 3环丙沙星尤启冬。
药物化学。
化学工业出版社。
2005,421 苯的C-酰化 39OHAlCl 3HOO枸橼酸氯米芬尤启冬。
药物化学。
化学工业出版社。
2005,565 苯的C-酰化 40 OO 2NHC CHCOOHPCl 5OO 2NHC CHCOCl呋喃丙胺王汝龙,原正平。
化工产品手册-药物。
化学工业出版社。
2005,190 羧羟基卤置换反应 41NH 2COOH2NHCOCH 3COOH甲喹酮王汝龙,原正平。
化工产品手册-药物。
化学工业出版社。
2005,270 胺的N-酰化,以酸酐为酰化剂42、氧原子的酰化反应 醇的氧酰化 羧酸为酰化剂 镇痛药盐酸呱替啶的合成CH 3OH/C 6H 6/△HCl(gas)NHO ON OOHCl闻韧,药物合成反应,化学工业出版社。
115 43、氧原子的酰化反应 醇的氧酰化 羧酸为酰化剂 局部麻醉药盐酸普鲁卡因的合成HOCH 2CH 2N(C 2H 5)2/二甲苯HCl(gas)45℃,2hOHO O 2NOO O 2NNOOO 2NNHCl闻韧,药物合成反应,化学工业出版社。
11544、氧原子的酰化反应 醇的氧酰化 羧酸酯为酰化剂 局麻药丁卡因C 2H 5ONa △N HOO HONN HOO NC 2H 5OH闻韧,药物合成反应,化学工业出版社。
118 45、氧原子的酰化反应 醇的氧酰化 羧酸酯为酰化剂32CH Br60-80℃,45minO COH ONHOO COH ONO COH ONBr 77%闻韧,药物合成反应,化学工业出版社。
118 46、氧原子的酰化反应 醇的氧酰化 羧酸酯为酰化剂 抗胆碱药格隆溴胺(胃长宁)的合成Na 3·BrOHOONOHOH OONOHO O N闻韧,药物合成反应,化学工业出版社。
11947、氧原子的酰化反应 醇的氧酰化 酸酐为酰化剂 镇痛药阿法罗定(安那度尔)的合成①(C 2H 5CO)2O/Py/△OH N·HClON OO闻韧,药物合成反应,化学工业出版社。
120 48、氮原子上的酰化反应 脂肪氨-N 酰化 羧酸为酰化剂消炎痛ClCOCl +N HH 3COCH 2COOHCH 3N H 3COCH 2COOH CH 3ClCO闻韧,药物合成反应,化学工业出版社。
13549、氮原子上的酰化反应 脂肪氨-N 酰化 羧酸酯为酰化剂 巴比妥类通用方法H 2NC H 2NO R'R C COOEt +NH C C C NH C R R OO O '闻韧,药物合成反应,化学工业出版社。
13650、氮原子上的酰化反应 脂肪氨-N 酰化 羧酸酯为酰化剂 舒比利H 2NO 2SOCH 3C ONO 2NO 2O N H 2CH 2N C 2H 5+H 2NO 2SOCH 3C O N H 2CH NC 2H 5闻韧,药物合成反应,化学工业出版社。
136 51、醇的酰化羧酸为酰化剂 镇痛药盐酸呱替啶的合成 52、醇的酰化羧酸为酰化剂局部麻醉药盐酸普鲁卡因的合成CH 3OH/C 6H 6/△HCl(gas)N COOH N CO 2Et HCl(gas)Fe/HCl 45℃,2hO 2NCOOH 22252O 2N OO NH 2NO ON53、醇的酰化羧酸酯为酰化剂 丁卡因54、醇的酰化羧酸酯为酰化剂抗胆碱药溴美喷酯(宁胃适)的合成55、醇的酰化酸酐为酰化剂镇痛药阿法罗定(安那度尔)的合成56、氮原子上的酰化反应羧酸酯为酰化剂 巴比妥类药物合成通法 57、碳原子上的酰化反应 羰基α位C-酰化 活性亚甲基化合物的C-酰化HOCH 2CH 2N(C 2H 5)2C 2H 5ONa △t-BuHN O Ot-BuHN O O N Et Et CH CH ONa60-80℃,45min (77%)HO O O+NHO HO O ONMeBr HO O ON BrN OH CH 3CH 3①(C 2H 5CO)2O/Py/△②HCl(gas)N OCOC 2H 5CH 3CH 3·HClH 2N NH 2O R'RCOOEt COOEt +NH R R O O O'氯苯乙酮(氯喘定的合成中间体)的制备58、碳原子上的酰化反应 羰基α位C-酰化 酮及羧酸衍生物的α-C 酰化 苯基丙二酸二乙酯(苯巴比妥中间体)的合成59、扑热息痛(对羟基乙酰苯胺)的合成(一种解热镇痛药),其制备经过乙酰基化反应60、OHOHCOCH 3苯环上的酰化,F-C 酰化反应 普罗帕酮王汝龙,原正平。
