SMP01-025文件管理
QP-04(I0)文件控制2007-5-22

质量管理系统程序
Kuni-Stars Company Limited
名称:QP-04 发行日期:
文 件 控 制 版次: I0 第5页共10页
(2)发文(质量记录除外)部门负责销毁所有回收的旧版文件,但旧版文件原稿需 由发文部门保存并加盖“作废文件”红色印章,保存期为一年。(特殊情况如 为了追溯、参考之用,文件保管部门可适当延长保存期限)
具体编号方式参照EP-5.1-01
(备注:对原有CMC、MC等部门代号的QP(S)文件和表格在修改之前仍继续有效,本版次《文件控 制》程序发行后制定的相关QP(S)文件和表格不再使用上述部门的部门代号作为文件编号和表格编 号。对原文件或表格一旦有修改时,必须将原文件编号或表格编号改成现属部门统一编号。)
Q S- Model A
制
Quality System 产品的 工程表
定
质 量 系 统 型号
版本号
的 工作指示书
工 程 文
件 《产品/部品分解图》
W I - Model A
Working 工作
Indication
指
示
产品的 指示书
型号
版本号
P / P F – Model A
《成形条件基准表》
Product 产品
4.0 职责:
4.1 由SM部门负责监督此程序的执行。
4.2 由Kuni-Stars之各部门共同负责实施相关程序。
4.3 各部门文员负责本部门文件的收/发和管理。
5.0 程序:
文件控制程序LM-QP-01
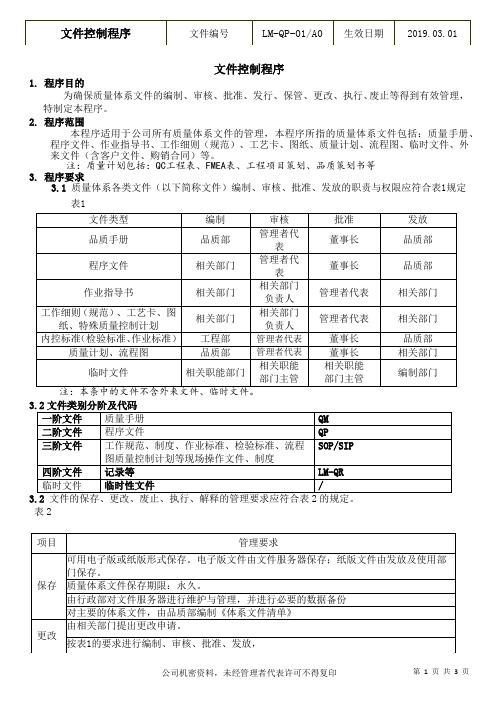
文件控制程序1. 程序目的为确保质量体系文件的编制、审核、批准、发行、保管、更改、执行、废止等得到有效管理,特制定本程序。
2. 程序范围本程序适用于公司所有质量体系文件的管理,本程序所指的质量体系文件包括:质量手册、程序文件、作业指导书、工作细则(规范)、工艺卡、图纸、质量计划、流程图、临时文件、外来文件(含客户文件、购销合同)等。
注:质量计划包括:QC工程表、FMEA表、工程项目策划、品质策划书等3. 程序要求3.1质量体系各类文件(以下简称文件)编制、审核、批准、发放的职责与权限应符合表1规定表1表23.3.1 外来标准国际、国家、行业和地方标准及企业标准,法律法规外来文件等,由品质部批准采用和统一购入,并以电子版或纸质副本发放相关部门。
品质部负责上述文件的更新。
此类文件保存期限:永久。
3.3.2 外来顾客文件顾客标准、图样等外来顾客文件等,由品质部接受,以纸版或电子版形式保管,并负责此类文件的更新及确保其有效性。
此类文件保存期限:不少于3年。
3.3.3 外来供方文件外购原辅材料、设备等的技术文件,如设备操作说明书等,由采购部接受并发放给相关使用或维护部门,由使用或维护部门保存。
注:设备操作说明书等外来供方文件可由设备部保存原件,使用部门保存副件。
此类文件保存期限:永久。
3.4 临时文件相关部门根据需要可编制与体系有关的暂行或临时文件,临时文件可由有关部门编制和发放。
如无特殊说明,临时文件有效期为1年,1年后自动失效。
技术部也可根据体系运行情况终止临时文件的施行。
3.5 文件的编号3.5.1 除外来文件、临时文件外,文件应由编制部门编号;外来文件可使用原编号,不必另行编号;临时文件可不用编号。
3.5.2 编号方法A.质量手册+数字),版本号,从A0开始(每个文件修改3次后升版本); 01至99;QM 品质手册LM:公司代码B.程序文件+数字),版本号,从A0开始(每个文件修改3次后升版本); 01至99;位大写字母: QP 程序文件代码LM:公司代码C.各类说明书、作业指导书、制度、规范、标准等三阶文件+数字)从A0开始(每个文件修改3次后升版本);位数字:流水号,从01至99;位大写字母;标准用SIP、其余均用SOP代码位大写字母:部门代号(工程部:EN、生产中心:PR、QC、销售部:MK、行政部:MN、采购部:PH、客PM、仓库:ST、财务部:CA、市场部:MK)LM:公司代码5记录LM-QR-A01/A0 《受控文件清单》。
ISMS-01-02文件控制程序

ISMS-01-02文件控制程序变更履历目录1.目的确保生产经营全过程的有效策划、运行和控制所需的文件、资料(包括外来文件)受控,对质量、环境、安全管理体系(以下简称综合管理体系)运行有关的文件、资料进行有效控制。
2.范围适用于综合管理体系运行有关的文件、资料,包括外来文件,如法律法规、技术标准、相关提供的文件、规章制度等。
3. 职责3.1信息安全工作小组是综合管理手册、程序文件的归口管理部门;负责手册、程序文件的编制,环境、安全管理体系覆盖的程序文件及有关的法律法规及其它要求的收集、更新。
3.2技术部是技术文件及外来技术文件的归口管理部门;负责产品标准的获取、更新、贯彻执行;技术文件的发放、回收、保留、并做好相关记录。
3.4 行政部门负责外来行政类及政策类文件的收集及公司外部公文的发放工作,负责外来文件的收集、发放、保存,并做好相关记录。
3.5规定了信息安全管理手册、策略文件、方针目标文件由信息安全小组以及有关部门共同编写,总经理审批、发布。
3.6程序文件和各类三层文件由相关责任部门编写,各部门领导参与审核,管理者代表批准、发布4. 工作程序4.1文件分类4.1.1文件分为:管理文件、技术文件、外来文件管理文件分为:手册、程序文件、管理制度(包括管理制度及管理标准)、记录表单等。
4.1.2 外来文件1)国家、行业、地方颁发的适用的法律法规、政策等文件;2)有关标准(如产品标准,国际标准等)、国家和行业技术标准、产品图样和规范;3)顾客提供的知识产权保护(如图样、规范等);4.2 文件的编制和收集1)手册、程序文件由体系中心负责编制、更改,各部门协助。
按文件编码规定编号。
2) 管理制度、管理标准由归口部门编制,部门主管审核,有关责任部门会签后报体系中心编号、标准化检查后,报归口负责人批准。
3) 技术类文件由相关业务部门编写并按编号规则编号,部门负责人审核,部门主管副总经理批准,各部门负责将文件相关信息登记到部门【受控文件清单】中。
SMP-QA-001.01 文件管理规程

1 目的规范文件的管理,制定公司cGMP 文件的分类、编号、格式,起草、审核、批准、培训、生效、发放、收回、销毁、保存、复审等程序。
2 范围适用于艾康睿公司所有的cGMP 文件。
3 职责(1) 质量保证部(QA ):负责cGMP 文件的所有管理过程。
(2) 各部门:负责本部门相关文件的起草、修订、审核、培训、收发与保管、执行。
4 程序4.1 分类公司的cGMP 文件主要包括以下几类:(1) 管理文件各部门的系统管理规程,英文缩写SMP (Standard Management Procedure )。
(2) 标准文件标准操作规程,英文缩写SOP (Standard Operating Procedure ),指一切涉及药品生产和 质量的书面标准程序,例如仪器使用的SOP ,检验规程、工艺规程等。
(3) 记录文件作为管理文件或标准文件的附件,提示性的描述各文件中规定应填写的内容,例如台帐、 批检验记录、批生产记录等。
记录文件应遵循本规程的管理原则,同时按照《记录管理规 程》(SMP-QA-002)的具体规定进行管理。
(4) 验证文件指验证方案、报告及验证相关文件。
验证文件应遵循本规程的管理原则,同时按照《验证 管理规程》(SMP-QA-019)的具体规定进行管理。
(5) 其他cGMP 文件,英文缩写OT (Other cGMP files ) 主要用于年度计划类或图表类文件。
4.2 编号文件编号由QA 负责编制。
4.2.1 管理文件SMP-部门代号-流水号.版本号SMP (Standard Management Procedure ):管理规程 部门代号:颁发部门: QA文件名称: 文件管理规程 生效日期:2014.11.20 文件编号: SMP-QA-001.01 前版本:新编起草人: 审核人: 批准人: 日期:日期:日期:分发部门:QA 生产部 QC 工程部 仓库 EHS 采供部 销售部(1)QA(Quality Assurance),质量保证部(2)PD(Production Department),生产部(3)QC(Quality Control),质量控制部(4)ED(Engineering Department),工程部(5)SD(Storage Department),仓库(6)EHS,安全、健康、环保部流水号:从001开始递增的3位数字;版本号:从01开始递增的2位数字。
SP-01 文件控制程序

1、目的对品质系统的文件和资料进行控制,规范其批准、发布、归档、更改及回收处理的方法。
2、范围适用于工厂的品质系统文件、外来文件、表格。
3、参考无4、定义4.1 外来文件---指外来的标准、参考资料,客户提供的图纸、工程标准/规范等。
4.2 主本文件---指保存在文件控制中心的品质系统文件、外来文件、表格等的原件。
4.3 受控文件---受更新控制的文件。
5、权责5.1 文件编制人5.1.1 确保所编制的文件符合ISO9001:2008标准和工厂实际运作的要求;5.1.2 文件的格式符合规定;5.1.3 文件按规定的流程审批并交给文控员进入文件发布流程。
5.2 文控员5.2.1 提供新增文件的文件编号;5.2.2 提供待修改文件的现行修订号;5.2.3 审查文件格式和审批程序是否符合本程序的规定;5.2.4 按规定的流程发放文件;5.2.5 按要求组织回收和处理作废文件;5.2.6 编制、修改(需要时)主本文件清单;5.2.7 管理和检查品质系统文件。
5.3 各相关部门5.3.1 签收受控文件并归档;5.3.2 按文件控制中心的要求退回作废文件;5.3.3 确保本部门的文件完整、有序。
6、程序6.1 文件的编制6.1.1 文件之编制或修改由各使用部门自行根据需要起草或修改文件。
6.1.2 新文件编制前,文件编制人须向文控员申请文件编号:首先说明文件的类型,由文控员根据文件清单确定可用的文件编号,给文件编制人使用。
6.1.3 修改文件时,由文件编制人向文控员索取现行文件的主本和修订号,然后进行修改。
6.1.4 文件须符合ISO9001:2008标准和工厂实际运作的要求。
6.1.5 文件编制人须注明文件修订日期、预定的生效日期并签名。
6.2 文件编号6.2.1 本公司文件编号一般是AA-BB型。
6.2.1.1 AA表示文件类别,以字母表示。
其中:QM表示质量手册SP表示程序文件WI表示作业指导书QI表示进料检验规范QO表示最终检验规范6.2.1.2 BB表示同类文件的顺序号,以数字表示。
QP-001文件管理程序
5.3.2第四级表单格式经核准后,原稿保存并发行一份给原申请部门,使用时由使用部门自行影印或请购印制;如表单发行新版时,可不填写《文件分发、回收、销毁记录表》。
5.2文件制订、修订、废止的制作
ISO文件包括质量手册,程序文件,三级文件,表格等的制订、修订或废止时,由主办及相关部门人员或指定人员按各类文件之标准格式拟定后,填写《文件申请单》经管理代表批准后,依次编号,并附《文件分发、回收、销毁记录表》注明发行部门及份数,由综合管理部发行实施。
5.3文件发放、回收
5.5.3电子文档管理:各部门电子文档自行保存并定期备份,防止文件丢失。
6.相关文件:无。
7.相关表单
序号
相关记录
保存期限
备注
1
外来文件一览表
长期
随时更新
2
文件分发、回收、销毁记录表
一年
3
文件申请单
一年
8.附件
8.1附件一:“受控文件”章
8.2附件二:“外来文件”章
8.3附件三:“作废文件”章
4.4指导书文件:标准作业书、细则、规范、通则等文件,为本公司第三级文件。
4.5制造文件:作业指导书等为公司第三级文件。
4.6外来文件:从公司以外获得的标准、规范或文件及设备相关说明书、操作介绍等属第三级文件。
4.7记录:校验记录、检验记录、测试记录及执行第二、第三级所衍生的记录资料等为本公司第四级文件。
QP-01文件管理程序
文 件 名 称 页 次 20XX.05.08
质量/HSF/环境文件管理程序 第 3 页 共 15 页 条 款 号 Q4.2.3+E4.4.5
过程输入
过程输出
过程绩效
1.ISO9001:2008 要求。 2.ISO14001:2004 要求 3.IECQ HSPM QC080000:2012 要求 4.顾客及相关方要求(含外来文件) 。 5.新项目及各种更改。 6.各部门运作的实况。 7.持续改进的内容。
文 件 编 号 版 本/修 订 号
流程 目标
文 件 名 称 页 次 20XX.05.08
作业方法描述
质量/HSF/环境文件管理程序 第 7 页 共 15 页 条 款 号 Q4.2.3+E4.4.5
输出 职责 信息 时效/反馈
XXX-QP-01 A/2 生 效 日 期
输入
文件识 别管制 (续)
编号说明: 第 1--3 码,表示和宏公司,缩写为 DNS; 第 4--5 码,表示表单的等级编号:QR(质量/HSF 记录) 、ER(环境 记录) 第 6--7 码,表示程序文件等级代号:QP、EP; 第 8--9 码,表示出自程序文件的流水号:01、02、03„„; 第 10--11 码,表示质量记录的流水号:01、02、03„„; 例:DNS/QR-QP01-01,表示从和宏公司第一份质量/HSF 程序文件中 衍生的第 1 份质量/HSF 记录。 DNS/ER-EP03-02,表示从和宏公司第三份环境程序文件中衍生 的第 2 份环境记录。 5.1.7.6 从各职能部门 A 类作业指导文件中衍生的表格、记录, 编号由 13 码组成,格式如下, (B、C、D、E 技术类指导文件中不产 生表格) 1.部门代码; □ □ □/□ □--□ □-- □ □ □ □--□ □ 2.文件编号规定; 1 2 3 4 5 6 7 8 9 10 11 12 13 3.文件编号格式; 编号说明: 4.文件版本、版次。 第 1--3 码,同上,和宏公司缩写:DNS 第 4--5 码,表示表单的等级编号:QR(质量/HSF 记录) 、ER(环境 记录) 第 6--7 码,表示职能部门代码; 第 8--9 码,表示作业指导文件的等级代号:WI; 第 10、11 码,表示 A 类作业指导文件的流水号:01、02、03„„; 仅从 A 类作业指导文件 第 12、13 码,表示质量/HSF 记录的流水号:01、02、03„„; 例:DNS/QR-QM-WI02-01,表示从和宏厂品管部 A 类第 2 份作业指导 文件中衍生的第 1 份表格。 5.1.7.7 表格、表单的编号,统一标注于左下角。 5.1.8 文件版本、版次规定 5.1.8.1 质量/HSF 手册、程序文件、作业指导书初版时,皆为 A/0(A 版 0 次) ,版本号以大写字母 A、B、C、„„顺推,版次以 0、 1 .文件、记 录的编号方 法; 2. 版 本 版 次 的识别; 3. 《作业指导 书》 4.《技术文件 编码规则》 1.体系科主 管/专员/文 控员 2.各相关部 门文员及使 用文件的人 员
文件管理使用手册
文件管理使用手册一、用户种类及各用户可进行的操作1.普通用户(非研工部以上权限用户):查看及下载文件(表格)2.研工部及研工部以上权限用户:查看及下载文件(表格);添加文件(表格);清空临时文件。
二、流程:1.普通用户打开首页即可查看及下载(表格)2.研工部及研工部以上权限用户:登录系统—〉进入文件管理页面—〉执行相应操作三、详细说明:1.查看及下载文件(表格)首页查看及下载文件(表格)如下图红框内所示,点击文字即可下载文件。
首页显示四条信息所有文件列表页面:进入“所有文件列表”页面点击文字链接出现以下界面,点击“保存”即可下载文件。
2.管理文件管理文件包括添加,删除文件.第一步:登录系统。
只有研工部管理员和超级管理员才能使用此功能。
方式一:首页登陆:方式二:在登录页面登录:当您不具备使用权限时,系统会自动转到登陆页面。
点击“确定”后转到登录页面。
输入用户名和密码,即可登录系统。
第二步:进入文件管理。
研工部:点击“研工部”进入研工部导航页面研工部导航页面文件管理页面:图:文件管理删除文件:如上图所示:点击“删除”后会弹出提示框:如下:点击“确定”即可删除文件;点击“取消”放弃操作。
添加文件:如图:文件管理中所示1.点击浏览选择所需上传文件:2.输入文件名字3.点击“添加”完成操作,操作成功,系统会提示:清空临时文件:临时文件为系统运行时产生的一些EXCEL文件及图片文件,为了系统更快的运行,请定期清空临时文件:方法:点击“清空”按钮即可。
如果成功,系统会提示:。
ISO17025:2023实验室-文件管理程序
ISO17025:2023实验室-文件管理程序1. 引言本文件旨在指导实验室在符合ISO :2023质量管理体系要求下进行文件管理。
文件管理是实验室管理中不可或缺的一部分,能够确保组织的文件得到有效的组织、存储、保护和维护。
2. 范围这份文件管理程序适用于所有ISO:2023认证的实验室,包括实验室内的所有文件、资料和记录。
它涵盖了文件的创建、审查、批准、发布、存储、保护、访问和维护过程。
3. 文件创建在创建实验室文件时,应遵循以下步骤和原则:- 确定文件的目的和范围;- 审查现有的相关文件,以避免重复或冲突;- 编写文件的内容,并确保准确、清晰、简洁;- 确定文件的格式和结构;- 让文件经过相关人员的审查、讨论和批准;- 文件版本控制,确保对文件进行跟踪和管理。
4. 文件审查和批准在文件创建完成后,应进行审查和批准,确保文件的准确性和完整性。
- 审查文件的内容,验证其与实验室要求的符合程度;- 由相关管理人员批准文件,并记录批准日期;- 在文件中标志文件的审查和批准状态。
5. 文件发布已审查和批准的文件应及时发布给相关用户和部门,以确保文件的有效性和适用性。
- 使用适合的传递方式将文件发送给相关人员;- 确保文件在接收方处得到确认和理解;- 文件发布日期应记录在文件中。
6. 文件存储和保护文件的存储和保护是确保文件完整和保密性的重要措施。
- 确定适当的存储介质和环境,以确保文件的安全性和可访问性;- 制定访问权限和保密级别,确保只有授权人员可以访问和修改文件;- 定期备份文件,以防止意外的数据丢失;- 识别和监控文件的存储位置,以确保文件的完整性和时效性。
7. 文件访问和维护为了有效管理和维护文件,应确保文件的适当访问和维护。
- 规定文件访问的程序和要求,确保文件只能被授权人员访问;- 实施文档变更管理,确保文件的更新和准确性;- 监测文件使用情况和反馈,及时解决发现的问题;- 定期审查和验证文件的有效性和适用性。
COP025设备管理程序
COP025设备管理程序为确保采设备始终处于优胜的运行状况,以进步工作效力、降低消费,特制订并履行本法度榜样。
2.有用范畴:本法度榜样有用于公司硬件举措措施、设备评判和操纵方法,及设备爱护、检修、筹划设备操纵。
3.引用文件:3.1 ISO9002/ 6.3差不多举措措施 7.6监督和测量装配的操纵3.2 ISO14001 /4.4.6运行操纵 4.5.1监督和测量3.3《治理手册》4.职责:4.1 临盆部负责设备的更新筹划,设备修理及保养,临盆部经理负责筹划的审核。
4.2 行政部负责情形体系计量检测设备的治理和同一送检。
4.3技质部负责质量测量设备的治理和同一送检。
4.4财务部经理负责设备合同的审核,总经理负责赞成。
4.5各部分负责本部分设备的日常爱护、保养。
5.法度榜样要求:5.1设备更新改革5.1.1 各部分应在12月20日编制下一年度设备添置和更新改革筹划报临盆部。
5.1.2 临盆部汇总落后行可行性分析,提出下年度设备更新改革筹划,须临盆部经理核定,报董事长审批。
5.1.3 依照货比三家原则,临盆部、财务部负责设备的购买。
5.2.4 关于零碎设备的购买,由各部分提出版面申报,经临盆部签订可行性看法后,报董事长审批。
5.1.5 设备到厂后,由临盆部分通知应用部分一路开箱验收。
5.1.6 验收主辅机、附件、备件、随机对象等与装箱单、合同内容是否相符,验收设备及其附件、备件在运转搬运过程中的无缺情形,验收有关技巧文件、说明书、合格证等材料是否齐备。
5.1.7 验收合格后,由临盆部归档储存全部图文材料,并向应用部分的设备治理人员供给原始图文材料的复印件,由临盆部负责安装和调试。
5.1.8 设备安装完毕,由临盆部、应用部分及其它有关部分参加试车验收,验收合格由临盆部填写“设备验收单”,交介入部分负责人签字承认。
5.2设备爱护、保养及检查5.2.1 重要设备,如空调、配电、锅炉、发电机等设备详见各设备操作规范。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一部分
文件
管理规程
河南雪樱花制药有限公司
目录
1.文件管理规程
2.文件总目录
3.文件分类、编码管理规程
4.文件的编制与格式管理规程
5.文件的起草、会稿、审核及批准管理规程
6.文件编制(修订)申请单
7.文件会稿记录
8.文件编制(修订)记录
9.文件复制记录
10.文件的颁布、回收、归档及销毁管理规程
11.文件发放记录
12.文件回收记录
13.文件归档记录
14.文件销毁记录
15.文件落实情况检查管理规程
16.文件实施情况检查反馈表
17.整改计划反馈表
18.工作标准编制管理规程
19.产品工艺规程编制规程
20.记录的编制规程
21.批生产记录的编制规程
22.批包装记录的编制规程
23.批记录的管理规程
24.批记录归档记录
25.标准操作规程(SOP)的编制及管理规程SMP01-001-00 SMP01-002-00 SMP01-003-00 SMP01-004-00 SMP01-005-00 SMP01-005-a-00 SMP01-005-b-00 SMP01-005-c-00 SMP01-005-d-00 SMP01-006-00 SMP01-006-a-00 SMP01-006-b-00 SMP01-006-c-00 SMP01-006-d-00 SMP01-007-03 SMP01-007-a-03 SMP01-007-b-03 SMP01-008-03 SMP01-009-00 SMP01-010-00 SMP01-011-00 SMP01-012-00 SMP01-013-00 SMP01-013-a-00 SMP01-014-00
26.标准管理规程(SMP)的编制及管理规程
27.生产指令的编制规程
28.包装指令的编制规程
29.原料质量标准的编制规程
30.辅料质量标准的编制规程
31.包装材料质量标准的编制规程
32.成品、中间品质量标准的编制规程
33.检验操作规程的编制规程
34.产品制造过程监控管理规程的编订规程
35.包装过程监控管理规程的编订规程
36.清洁规程的编制及管理规程SMP01-015-00 SMP01-016-00 SMP01-017-00 SMP01-018-00 SMP01-019-03 SMP01-020-03 SMP01-021-00 SMP01-022-00 SMP01-023-00 SMP01-024-00 SMP01-025-00
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程
文件编制(修订)申请单
文件会稿记录
文件编制(修订)记录
编号:SMP01-005-c-00
文件复制记录
标准管理规程
标准管理规程
编号:SMP01-006-a-00
编号:SMP01-006-b-00
编号:SMP01-006-c-00
文件销毁记录
编号:SMP01-006-d-00
文件实施情况检查反馈表
注:本表由检查组人员填写,一式三份,一份交被查单位,一份交职能管理部门,一份交公司行政事务
部。
整改计划反馈表
编号:SMP01-007-b-00
注:本表由被查单位填写,一式三份,一份报公司行政事务部,一份报职能管理部门,一份本单位留存。
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程
标准管理规程。
