最新总结-红外光谱频率与官能团特征吸收峰分析
红外光谱频率与官能团特征吸收峰总结表

内弯曲振动的倍频或组频吸收),是进一步确定取代苯的重要旁证。
苯 670cm-1(S) 单取代苯 770~730 cm-1(VS),710~690 cm-1(S)
1,2-二取代苯 770~735 cm-1(VS)
1,3-二取代苯 810~750 cm-1(VS),725~680 cm-1(m~S)
1,4-二取代苯 860~800 cm-1(VS) 五、卤化物
1、σC=O 1750~1735 cm-1 处出现(饱和酯 σC=O 位于 1740cm-1 处),受相邻基 团的影响,吸收峰的位置会发生变化。
2、σC-O 一般有两个吸收峰,1300~1150 cm-1,1140~1030 cm-1 十一、酰卤
σC=O 由于卤素的吸电子作用,使 C=O 双键性增强,从而出现在较高波数处, 一般在~1800cm-1 处,如果有乙烯基或苯环与 C=O 共轭,,会使 σC=O 变小,一 般在 1780~1740cm-1 处。 十二、酸酐
1、σC=O 由于羰基的振动偶合,导致 σC=O 有两个吸收,分别处在 1860~1800 cm-1 和 1800~1750 cm-1 区域,两个峰相距 60 cm-1。 2、σC-O 为一强吸收峰,开链酸酐的 σC-O 在 1175~1045 cm-1 处,环状酸酐 1310~1210 cm-1 处。 十三、酰胺
σ C C 出现在 2140—2100 cm-1,二元取代炔烃在 2260—2190 cm-1,当两个取
代基的性质相差太大时,炔化物极性增强,吸收峰的强度增大。当
处
于分子的对称中心时,σ C为C红外非活性。 3、σ C C H 炔烃变形振动发生在 680—610 cm-1。
四、芳烃
芳烃的红外吸收主要为苯环上的 C-H 键及环骨架中的 C=C 键振动所引起。
红外光谱频率与官能团特征吸收峰总结表

三、炔烃
在 IR 光谱中,炔烃基团很容易识别,它主要有三种特征吸收。
1、σC C H 该振动吸收非常特征,吸收峰位置在 3300—3310 cm-1,中等强度。 σN-H 值与 σC-H 值相同,但前者为宽峰、后者为尖峰,易于识别。
2、σ C C 一般
C C键的伸缩振动吸收都较弱。一元取代炔烃 RC CH
σ C C 出现在 2140—2100 cm-1,二元取代炔烃在 2260—2190 cm-1,当两个取
代基的性质相差太大时,炔化物极性增强,吸收峰的强度增大。当
处
于分子的对称中心时,σ C为C红外非活性。 3、σ C C H 炔烃变形振动发生在 680—610 cm-1。
四、芳烃
芳烃的红外吸收主要为苯环上的 C-H 键及环骨架中的 C=C 键振动所引起。
1、σC=O 1750~1735 cm-1 处出现(饱和酯 σC=O 位于 1740cm-1 处),受相邻基 团的影响,吸收峰的位置会发生变化。
2、σC-O 一般有两个吸收峰,1300~1150 cm-1,1140~1030 cm-1 十一、酰卤
σC=O 由于卤素的吸电子作用,使 C=O 双键性增强,从而出现在较高波数处, 一般在~1800cm-1 处,如果有乙烯基或苯环与 C=O 共轭,,会使 σC=O 变小,一 般在 1780~1740cm-1 处。 十二、酸酐
随着卤素原子的增加,σC-X 降低。如 C-F(1100~1000 cm-1);C-C(l 750~700 cm-1);C-Br(600~500 cm-1);C-I(500~200 cm-1)。此外,C-X 吸收峰的频率 容易受到邻近基团的影响,吸收峰位置变化较大,尤其是含氟、含氯的化合物变 化更大,而且用溶液法或液膜法测定时,常出现不同构象引起的几个伸缩吸收带。 因此 IR 光谱对含卤素有机化合物的鉴定受到一定限制。 六、醇和酚 醇和酚类化合物有相同的羟基,其特征吸收是 O-H 和 C-O 键的振动频率。 1、 σO-H 一般在 3670~3200 cm-1 区域。游离羟基吸收出现在 3640~3610 cm-1, 峰形尖锐,无干扰,极易识别(溶剂中微量游离水吸收位于 3710 cm-1)。OH 是 个强极性基团,因此羟基化合物的缔合现象非常显著,羟基形成氢键的缔合峰一 般出现在 3550~3200 cm-1。
官能团化合物的红外(FTIR)吸收峰特征总结
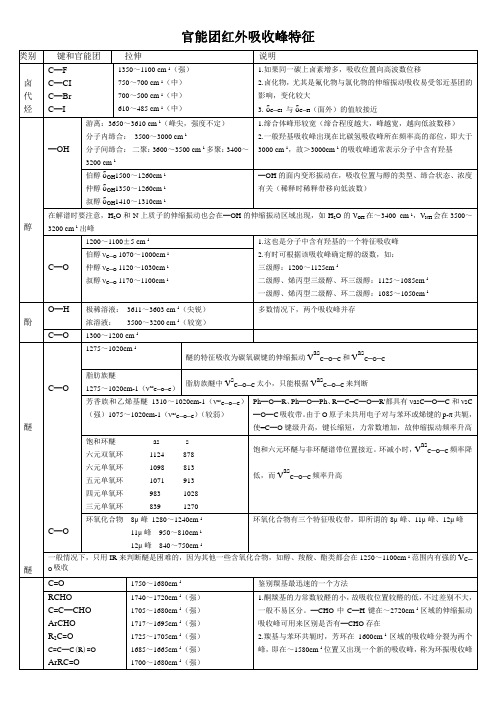
OH
气相(游离):≈3550cm-1
液/固(二缔合体):3200~2500cm-1(宽而散,以3000cm-1为中心。此吸收在2700~2500cm-1常有几个小峰,因为此区域其他峰很少出现,故对判断羧酸很有用,这是由于伸缩振动和变形振动的倍频及组合频引起)
羧酸
C=O
RCOOH:单体:1770~1750cm-1二缔合体:≈1710cm-1
CH2=CH━COOH:单体:~1720cm-1二缔合体:≈1690cm-1;ArCOOH:单体:1770~1750cm-1二缔合体:~1745cm-1
1.二缔合体C=O的吸收,由于氢键的影响,吸收位置向低波数位移
2.芳香羧酸,由于形成氢键及与芳环共轭两种影响,更使C=O吸收向低波数方向位移
NH2的面内变形振动:即酰胺Ⅱ带。此吸收较弱,并靠近νC=O。一般在1655~1590cm-1。
νC━N谱带:在1420~1400cm-1内有一个很强碳氮键伸缩振动的吸收带。在其它酰胺中也有此吸收。
NH2的摇摆振动吸收:伯酰胺在~1150cm-1有一个弱吸收,在750~600cm-1有一个宽吸收。
仲酰胺
官能团红外吸收峰特征
类别
键和官能团
拉伸
说明
卤代烃
C━F
C━CI
C━Br
C━I
1350~1100 cm-1(强)
750~700 cm-1(中)
700~500 cm-1(中)
610~485 cm-1(中)
1.如果同一碳上卤素增多,吸收位置向高波数位移
2.卤化物,尤其是氟化物与氯化物的伸缩振动吸收易受邻近基团的影响,变化较大
C━N
1º ≈1400cm-1(中)
主要官能团的红外吸收峰频率特征

νC━O━C在1330~1050cm-1有两个吸收带,即νasC=O和νsC━O━C。其中νasC=O在1330~1150cm-1,峰强大且宽,在酯的红外光谱中常为第一强峰。酯的νasC=O与结构有关。
内酯的νC=O与环的大小及共轭基团和吸电子取代基团的连接位置有关。羰基与双键个共轭时,νC=O频率减小;内酯的氧原子与双键连接时νC=O增大。α,β-不饱和内酯和γ-内酯常有两个νC=O吸收带,在~1780,~1755 cm-1附近。这是羰基的α位的δCH(881cm-1附近附近)的倍频与νC=O发生费米共振的结果。
仲酰胺
νNH吸收:在稀溶液中伯酰胺在有一个很尖的吸收,在仪器分辨率很高时,可以分裂为相似的双线,是由于顺反异构产生。在压片法或浓溶液中,仲酰胺的νNH可能会出现几个吸收带,这是由于顺反两种异构产生的靠氢键连接的多聚物所致。
νC=O:即酰胺Ⅰ带。仲酰胺在1680~1630cm-1有一个强吸收是νC=O,叫酰胺Ⅰ带。
δNH和νC━N之间偶合造成酰胺Ⅱ带和酰胺Ⅲ带。酰胺Ⅱ带在1570~1510cm-1。酰胺Ⅲ带在1335~1200cm-1。
其它:在和附近还会有酰胺的Ⅳ、Ⅴ、Ⅵ带,但应用上不如前面谱带那么重要
叔酰胺
叔酰胺的氮上没有质子,其唯一的特征谱带是νC=O,在1680~1630cm-1。
在955~915cm-1有一特征性宽峰,是酸的二聚体中OH···O=的面外变形振动引起的,可用于确认羧基的存在
νC=O高于酮的νC=O,这是OH的作用结果
羧酸盐中的━COO-无νC=O吸收。COO-是一个多电子的共轭体系, ,两个C=O振动偶合,故在两个地方出现其强吸收,其中反对称伸缩振动在1610~1560cm-1;对称伸缩振动在1440~1360cm-1,强度弱于反对称伸缩振动吸收,并且常是两个或三个较宽的峰。
红外的基团频率和特征吸收峰

物质的红外光谱是其分子结构的反映,谱图中的吸收峰与分子中各基团的振动形式相对应。
多原子分子的红外光谱与其结构的关系,一般是通过实验手段得到。
这就是通过比较大量已知化合物的红外光谱,从中总结出各种基团的吸收规律。
实验表明,组成分子的各种基团,如O-H、N-H、C-H、C=C、C=OH和C C等,都有自己的特定的红外吸收区域,分子的其它部分对其吸收位置影响较小。
通常把这种能代表及存在、并有较高强度的吸收谱带称为基团频率,其所在的位置一般又称为特征吸收峰。
一、基团频率区和指纹区(一)基团频率区中红外光谱区可分成4000 cm-1 ~1300 cm-1和1800cm-1 (1300 cm-1 )~ 600 cm-1两个区域。
最有分析价值的基团频率在4000 cm-1 ~ 1300 cm-1 之间,这一区域称为基团频率区、官能团区或特征区。
区内的峰是由伸缩振动产生的吸收带,比较稀疏,容易辨认,常用于鉴定官能团。
在1800 cm-1 (1300 cm-1 )~600 cm-1 区域内,除单键的伸缩振动外,还有因变形振动产生的谱带。
这种振动与整个分子的结构有关。
当分子结构稍有不同时,该区的吸收就有细微的差异,并显示出分子特征。
这种情况就像人的指纹一样,因此称为指纹区。
指纹区对于指认结构类似的化合物很有帮助,而且可以作为化合物存在某种基团的旁证。
基团频率区可分为三个区域:(1)4000 ~2500 cm-1 X-H伸缩振动区,X可以是O、H、C或S 等原子。
O-H基的伸缩振动出现在3650 ~3200 cm-1 范围内,它可以作为判断有无醇类、酚类和有机酸类的重要依据。
当醇和酚溶于非极性溶剂(如CCl4),浓度于0.01mol. dm-3时,在3650 ~3580 cm-1处出现游离O-H基的伸缩振动吸收,峰形尖锐,且没有其它吸收峰干扰,易于识别。
当试样浓度增加时,羟基化合物产生缔合现象,O-H基的伸缩振动吸收峰向低波数方向位移,在3400 ~3200 cm-1 出现一个宽而强的吸收峰。
的总结红外光谱频率与官能团特征吸收峰解读汇报
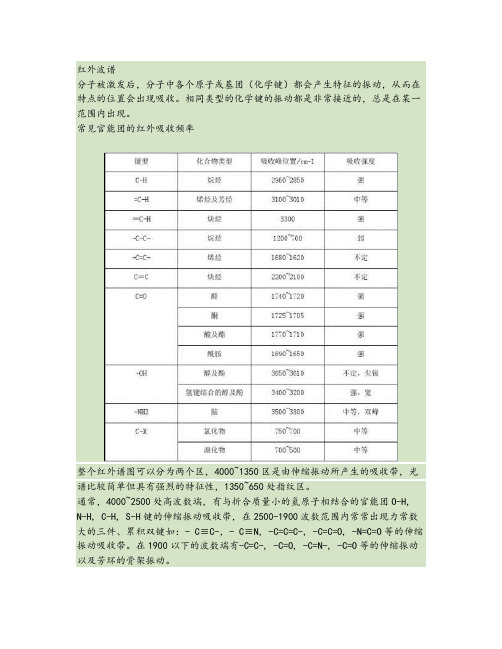
红外波谱分子被激发后,分子中各个原子或基团(化学键)都会产生特征的振动,从而在特点的位置会出现吸收。
相同类型的化学键的振动都是非常接近的,总是在某一范围内出现。
常见官能团的红外吸收频率整个红外谱图可以分为两个区,4000~1350区是由伸缩振动所产生的吸收带,光谱比较简单但具有强烈的特征性,1350~650处指纹区。
通常,4000~2500处高波数端,有与折合质量小的氢原子相结合的官能团O-H, N-H, C-H, S-H键的伸缩振动吸收带,在2500-1900波数范围内常常出现力常数大的三件、累积双键如:- C≡C-,- C≡N, -C=C=C-, -C=C=O, -N=C=O等的伸缩振动吸收带。
在1900以下的波数端有-C=C-, -C=O, -C=N-, -C=O等的伸缩振动以及芳环的骨架振动。
1350~650指纹区处,有C-O, C-X的伸缩振动以及C-C的骨架振动,还有力常数较小的弯曲振动产生的吸收峰,因此光谱非常复杂。
该区域各峰的吸收位置受整体分子结构的影响较大,分子结构稍有不同,吸收也会有细微的差别,所以指纹区对于用已知物来鉴别未知物十分重要。
有机化学有机化合物红外吸收光谱σ伸缩振动,δ面内弯曲振动,γ面外弯曲振动一、烷烃饱和烷烃IR光谱主要由C-H键的骨架振动所引起,而其中以C-H键的伸缩振动最为有用。
在确定分子结构时,也常借助于C-H键的变形振动和C-C键骨架振动吸收。
烷烃有下列四种振动吸收。
1、σC-H在2975—2845 cm-1范围,包括甲基、亚甲基和次甲基的对称与不对称伸缩振动2、δC-H在1460 cm-1和1380 cm-1处有特征吸收,前者归因于甲基及亚甲基C-H的σas,后者归因于甲基 C-H的σs。
1380 cm-1峰对结构敏感,对于识别甲基很有用。
共存基团的电负性对1380 cm-1峰位置有影响,相邻基团电负性愈强,愈移向高波数区,例如,在CH3F中此峰移至1475 cm-1。
官能团化合物的红外(FTIR)吸收峰特征总结

六元双氧环1124 878
六元单氧环1098 813
五元单氧环1071 913
四元单氧环983 1028
三元单氧环839 1270
饱和六元环醚与非环醚谱带位置接近。环减小时,νasC━O━C频率降低,而νasC━O━C频率升高
环氧化合物8μ峰1280~1240cm-1
11μ峰950~810cm-1
酯
C=O
1735cm-1(强)
1.在1300~1050cm-1区域有两C━O伸缩振动吸收,其中波数较高的吸收峰比较特征,可用于酯的鉴定
2.芳香酯在1605~1585cm-1区域还有一个特征的环振吸收峰
>C=C━COOR或ArCOOR的C=O吸收因与C=C共轭移向低波数方向,在≈1720cm-1区域━COOC=C<或RCOOAr结构的C=O则向高波数方向位移,在≈1760cm-1区域吸收
环酮中νC=O随张力的增大波数增大
α二酮R━CO━CO━R'在1730~1710cm-1有一强吸收。β二酮R━CO━CH2━CO━R'有酮式和烯醇式互变异构体。酮式中因两个羰基偶合效应,在在1730~1690cm-1有两个强吸收;烯醇式中在1640~1540cm-1出现一个宽且很强的吸收
C━CO━C面内弯曲振动
12μ峰840~750cm-1
环氧化合物有三个特征吸收带,即所谓的8μ峰、11μ峰、12μ峰
一般情况下,只用IR来判断醚是困难的,因为其他一些含氧化合物,如醇、羧酸、酯类都会在1250~1100cm-1范围内有强的νC━O吸收
醛、酮
醛、酮
C=O
1750~1680cm-1
鉴别羰基最迅速的一个方法
RCHO
C━O
最新总结-红外光谱频率与官能团特征吸收峰分析
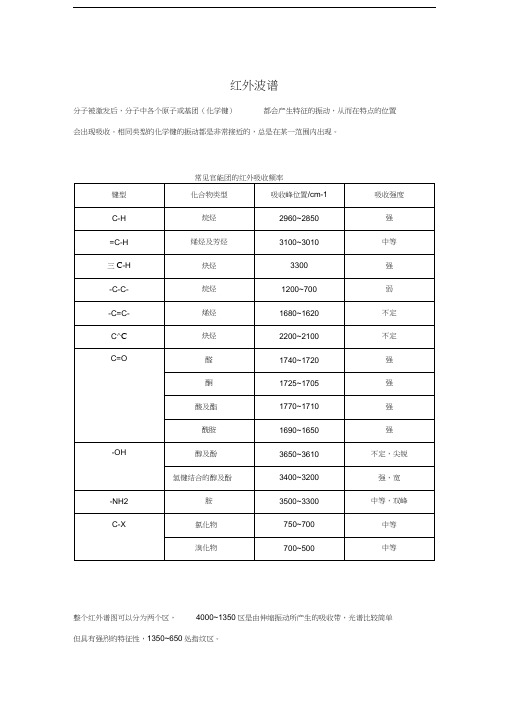
红外波谱分子被激发后,分子中各个原子或基团(化学键)都会产生特征的振动,从而在特点的位置会出现吸收。
相同类型的化学键的振动都是非常接近的,总是在某一范围内出现。
整个红外谱图可以分为两个区,4000~1350区是由伸缩振动所产生的吸收带,光谱比较简单但具有强烈的特征性,1350~650处指纹区。
通常,4000~2500 处高波数端,有与折合质量小的氢原子相结合的官能团O-H, N-H, C-H, S-H键的伸缩振动吸收带,在2500-1900 波数范围内常常出现力常数大的三件、累积双键如:-y, - gN, -C=C=C-,-C=C=O,-N=C=O等的伸缩振动吸收带。
在1900以下的波数端有-C=C-, -C=O, -C=N-, -C=O 等的伸缩振动以及芳环的骨架振动。
1350~650指纹区处,有C-O, C-X的伸缩振动以及C-C的骨架振动,还有力常数较小的弯曲振动产生的吸收峰, 因此光谱非常复杂。
该区域各峰的吸收位置受整体分子结构的影响较大, 分子结构稍有不同, 吸收也会有细微的差别, 所以指纹区对于用已知物来鉴别未知物十分重要。
有机化学有机化合物红外吸收光谱C伸缩振动,S面内弯曲振动,丫面外弯曲振动一、烷烃饱和烷烃IR光谱主要由C-H键的骨架振动所引起,而其中以C-H键的伸缩振动最为有用。
在确定分子结构时,也常借助于C-H键的变形振动和C-C键骨架振动吸收。
烷烃有下列四种振动吸收。
1、(T C-H在2975—2845 cm-1范围,包括甲基、亚甲基和次甲基的对称与不对称伸缩振动2、S C-H在1460 cm-1和1380 cm-1处有特征吸收,前者归因于甲基及亚甲基C-H 的(T as,后者归因于甲基C-H的(T s。
1380 cm-1峰对结构敏感,对于识别甲基很有用。
共存基团的电负性对1380 cm-1峰位置有影响,相邻基团电负性愈强,愈移向高波数区,例如,在CH3F中此峰移至1475 cm-1。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
红外波谱分子被激发后,分子中各个原子或基团(化学键)都会产生特征的振动,从而在特点的位置会出现吸收。
相同类型的化学键的振动都是非常接近的,总是在某一范围内出现。
整个红外谱图可以分为两个区,4000~1350区是由伸缩振动所产生的吸收带,光谱比较简单但具有强烈的特征性,1350~650处指纹区。
通常,4000~2500 处高波数端,有与折合质量小的氢原子相结合的官能团O-H, N-H, C-H, S-H键的伸缩振动吸收带,在2500-1900 波数范围内常常出现力常数大的三件、累积双键如:-y, - gN, -C=C=C-,-C=C=O,-N=C=O等的伸缩振动吸收带。
在1900以下的波数端有-C=C-, -C=O, -C=N-, -C=O 等的伸缩振动以及芳环的骨架振动。
1350~650指纹区处,有C-O, C-X的伸缩振动以及C-C的骨架振动,还有力常数较小的弯曲振动产生的吸收峰, 因此光谱非常复杂。
该区域各峰的吸收位置受整体分子结构的影响较大, 分子结构稍有不同, 吸收也会有细微的差别, 所以指纹区对于用已知物来鉴别未知物十分重要。
有机化学有机化合物红外吸收光谱C伸缩振动,S面内弯曲振动,丫面外弯曲振动一、烷烃饱和烷烃IR光谱主要由C-H键的骨架振动所引起,而其中以C-H键的伸缩振动最为有用。
在确定分子结构时,也常借助于C-H键的变形振动和C-C键骨架振动吸收。
烷烃有下列四种振动吸收。
1、(T C-H在2975—2845 cm-1范围,包括甲基、亚甲基和次甲基的对称与不对称伸缩振动2、S C-H在1460 cm-1和1380 cm-1处有特征吸收,前者归因于甲基及亚甲基C-H 的(T as,后者归因于甲基C-H的(T s。
1380 cm-1峰对结构敏感,对于识别甲基很有用。
共存基团的电负性对1380 cm-1峰位置有影响,相邻基团电负性愈强,愈移向高波数区,例如,在CH3F中此峰移至1475 cm-1。
异丙基1380 cm-1裂分为两个强度几乎相等的两个峰1385 cm-1、1375 cm-11 1 1叔丁基1380 cm 裂分1395 cm 、1370cm两个峰,后者强度差不多是前者的两倍,在1250 cm-1、1200 cm-1附近出现两个中等强度的骨架振动。
3、(T C-C在1250—800 cm-1范围内,因特征性不强,用处不大。
4、丫C-H分子中具有一(CH2)n—链节,n大于或等于4时,在722 cm-1有一个弱吸收峰,随着CH2个数的减少,吸收峰向高波数方向位移,由此可推断分子链的长短。
二、烯烃烯烃中的特征峰由C=C-H键的伸缩振动以及C=C-H键的变形振动所引起。
烯烃分子主要有三种特征吸收。
1、(T C=C-H烯烃双键上的C-H键伸缩振动波数在3000 cm-1以上,末端双键氢\ 1zC=CH 2 在3075—3090 cm 有强峰最易识别。
2、(T C=C吸收峰的位置在1670—1620 cm-1。
随着取代基的不同,c C=C吸收峰的位置有所不同,强度也发生变化。
3、S C=C-H烯烃双键上的C-H键面内弯曲振动在1500—1000 cm-1,对结构不敏感,用途较少;而面外摇摆振动吸收最有用,在1000- 700 cm-1范围内,该振动对结构敏感,其吸收峰特征性明显,强度也较大,易于识别,可借以判断双键取代情况和构型。
1 1RHC=CH2 995~985cm (=CH, S) 915~905cm-1(=CH2, S)R1R2C=CH2 895~885 cm-1(S)12 112 i(顺)-R CH=CHR ~690 cm-(反)-R CH=CHR 980~965 cm-(S)R1R2C=CHR3840~790cm-1(m)三、炔烃在IR光谱中,炔烃基团很容易识别,它主要有三种特征吸收。
1、co三C-H 该振动吸收非常特征,吸收峰位置在3300- 3310 cm-1,中等强度。
c N-H值与c C-H值相同,但前者为宽峰、后者为尖峰,易于识别。
2、 c gc —般C三C键的伸缩振动吸收都较弱。
一元取代炔烃RC CHc C三C 出现在2140—2100 cm-1,二元取代炔烃在2260— 2190 cm-1,当两个取代基的性质相差太大时,炔化物极性增强,吸收峰的强度增大。
当处于分子的对称中心时,c c三为红外非活性。
3、C C三C-H炔烃变形振动发生在680—610 cm-1。
四、芳烃芳烃的红外吸收主要为苯环上的C-H键及环骨架中的C=C键振动所引起。
芳族化合物主要有三种特征吸收。
1、 c Ar-H芳环上C-H吸收频率在3100~3000 cm-1附近,有较弱的三个峰,特征性不强,与烯烃的c C=C-H频率相近,但烯烃的吸收峰只有一个。
2、 c C=C芳环的骨架伸缩振动正常情况下有四条谱带,约为1600, 1585, 1500, 1450 cm-1,这是鉴定有无苯环的重要标志之一。
13、S Ar-H芳烃的C-H变形振动吸收出现在两处。
1275— 960 cm为S Ar-H,由于吸收较弱,易受干扰,用处较小。
另一处是900—650 cm-1的S A「-H吸收较强,是识别苯环上取代基位置和数目的极重要的特征峰。
取代基越多,S Ar-H频率越高,见表3-10。
若在1600- 2000 cm-1之间有锯齿壮倍频吸收(C-H面外和C=C面内弯曲振动的倍频或组频吸收),是进一步确定取代苯的重要旁证。
苯670cm-1(S) 单取代苯770~730 cm-1(VS), 710~690 cm-1(S)1.2- 二取代苯770~735 cn< (VS)1 11.3- 二取代苯810~750 cm (VS) ,725~680 cm-(m~S)1,4- 二取代苯860~800 cm-1(VS)五、卤化物随着卤素原子的增加,(TC-X 降低。
如C-F (1100~1000 cm1); C-Cl (750~700 cm-1); C-Br (600~500 cm-1); C-I (500~200 cm-1)。
此外,C-X 吸收峰的频率容易受到邻近基团的影响,吸收峰位置变化较大,尤其是含氟、含氯的化合物变化更大,而且用溶液法或液膜法测定时,常出现不同构象引起的几个伸缩吸收带。
因此IR 光谱对含卤素有机化合物的鉴定受到一定限制。
六、醇和酚醇和酚类化合物有相同的羟基,其特征吸收是0-H和C-O键的振动频率。
1、T 0-H一般在3670~3200 cm-1区域。
游离羟基吸收出现在3640~3610 cm-1, 峰形尖锐,无干扰,极易识别(溶剂中微量游离水吸收位于3710 cm-1)。
OH是个强极性基团,因此羟基化合物的缔合现象非常显著,羟基形成氢键的缔合峰一般出现在3550~3200 cm-1。
1,2-环戊二醇顺式异构体P47-1 -10.005mol/L (CCI4)3633 cm-(游离),3572 cm-(分子内氢键)。
-1 -1 -10.04 mol/L (CCI4)3633 cm-(游离),3572 cm-(分子内氢键)~3500cm-(分子间氢键)。
2、T C-O和S O-H C-O键伸缩振动和O-H面内弯曲振动在1410—1100 cm-1处有强吸收,当无其它基团干扰时,可利用T C-O 的频率来了解羟基的碳链取代情况(伯醇在1050cm-1,仲醇在1125cm-1,叔醇在1200cm-1,酚在1250cm-1)。
七、醚和其它化合物醚的特征吸收带是C-O-C不对称伸缩振动,出现在1150~1060cm1处,强度大,C-C 骨架振动吸收也出现在此区域,但强度弱,易于识别。
醇、酸、酯、内酯的T C-O 吸收在此区域,故很难归属。
八、醛和酮醛和酮的共同特点是分子结构中都含有(C=O),T C=O在1750~1680cm<范围内,吸收强度很大,这是鉴别羰基的最明显的依据。
临近基团的性质不同,吸收峰的位置也有所不同。
羰基化合物存在下列共振结构:C=O 键有着双键性强的A 结构和单键性强的B 结构两种结构。
共轭效应将 使C C=O 吸收峰向低波数一端移动,吸电子的诱导效应使(T C=O 的吸收峰向高波数 方向移动。
a , B 不饱和的羰基化合物,由于不饱和键与C=O 的共轭,因此C=O 键的吸收峰向低波数移动RCH=CHCOR'-1er C =O 1685~1665cm苯乙酮对氨基苯乙酮对硝基苯乙酮-1-1-11691cm 1677cm 1700cm般在2700~2900cn <区域内,通常在~2820 cm -1、~2720 cm -1附近各有一个中等强度的吸收峰,可以用来区别醛和酮。
九、羧酸1、T O -H 游离的O-H 在~3550 cm -1,缔合的O-H 在3300~2500 cm -1,峰形宽而散,强度很大。
2、 T C =O 游离的C=O 一般在~1760 cm -1附近,吸收强度比酮羰基的吸收强度大, 但由于羧酸分子中的双分子缔合,使得 C=O 的吸收峰向低波数方向移动,一般 在1725~1700cm 1,如果发生共轭,贝U C=O 的吸收峰移到1690~1680 cni 1。
3、 T C -O 一般在1440~1395 cmi 1,吸收强度较弱。
4、 S O -H 一般在1250 cm -1附近,是一强吸收峰,有时会和 T C -O 重合。
十、酯和内酯1、 T C =O 1750~1735 cm 1处出现(饱和酯T C =O 位于1740cm -1处),受相邻基团 的影响,吸收峰的位置会发生变化。
1 12、 T C-O 一般有两个吸收峰,1300~1150 cm ,1140~1030 cm -十、酰卤T C =O 由于卤素的吸电子作用,使C=O 双键性增强,从而出现在较高波数 处,一般在~1800cm _1处,如果有乙烯基或苯环与 C=O 共轭,,会使T C =O 变小,般在 1780~1740cm -1 处。
十二、酸酐 1、 C C=O 由于羰基的振动偶合,导致C C=O 有两个吸收,分别处在1860~1800 cm -1 和 1800~1750 cm -1 区域,两个峰相距 60 cm -1。
2、 C C-O 为一强吸收峰,开链酸酐的 C C-O 在 1175~1045 cm -1 处,环状酸酐 1310~1210RCHClCOR' -11745~1725cm i'(T C=O (Tcm-1处。
十三、酰胺1、 C C=O酰胺的第谱带,由于氨基的影响,使得 C C=O向低波数位移,伯酰胺1690~1650 cm1,仲酰胺1680~1655 cm-1,叔酰胺1670~1630 cm-1。
2、 C N-H一般位于3500~3100 cm-1,伯酰胺游离位于~3520 cm-1和~3400 cm-1,形成氢键而缔合的位于~3350 cm-1和~3180 cm-1,均呈双峰;仲酰胺游离位于~3440 cm-1,形成氢键而缔合的位于~3100 cm-1,均呈单峰;叔酰胺无此吸收峰。
