化学方程式计算题型汇总
化学方程式计算专题
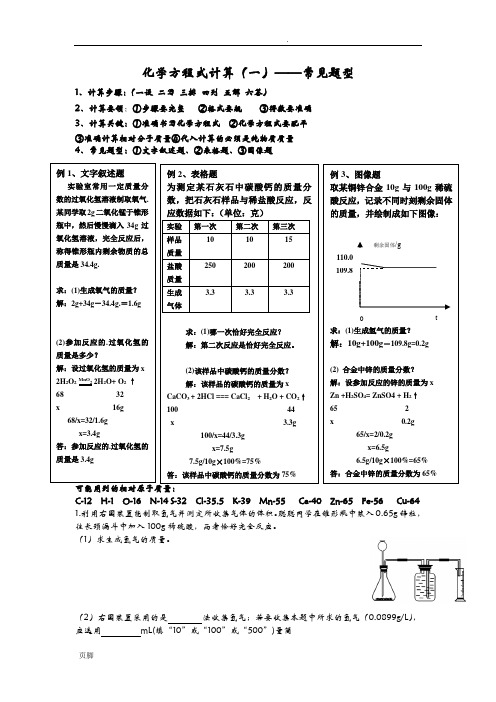
化学方程式计算(一)——常见题型1、计算步骤:(一设 二写 三排 四列 五解 六答)2、计算要领:①步骤要完整 ②格式要规 ③得数要准确3、计算关键:①准确书写化学方程式 ②化学方程式要配平 ③准确计算相对分子质量④代入计算的必须是纯物质质量4、常见题型:①文字叙述题、②表格题、③图像题24、专题练习C-12 H-1 O-16 N-14 S-32 Cl-35.5 K-39 Mn-55 Ca-40 Zn-65 Fe-56 Cu-64 1.利用右图装置能制取氢气并测定所收集气体的体积。
聪聪同学在锥形瓶中装入0.65g 锌粒,往长颈漏斗中加入100g 稀硫酸,两者恰好完全反应。
(1)求生成氢气的质量。
(2)右图装置采用的是 法收集氢气;若要收集本题中所求的氢气(0.0899g/L ),应选用 mL(填“10”或“100”或“500”)量筒 例1、文字叙述题 实验室常用一定质量分数的过氧化氢溶液制取氧气.某同学取2g 二氧化锰于锥形瓶中,然后慢慢滴入34g 过氧化氢溶液,完全反应后,称得锥形瓶内剩余物质的总质量是34.4g.求:(1)生成氧气的质量? 解:2g+34g-34.4g.=1.6g(2)参加反应的.过氧化氢的质量是多少?解:设过氧化氢的质量为x2H 2O 2MnO 2 2H 2O+ O 2 ↑ 6832x 16g68/x=32/1.6gx=3.4g答:参加反应的.过氧化氢的质量是3.4g例2、表格题为测定某石灰石中碳酸钙的质量分数,把石灰石样品与稀盐酸反应,反应数据如下:(单位:克)实验 第一次第二次 第三次样品 质量 101015盐酸 质量 250200200生成 气体3.33.33.3求:(1)哪一次恰好完全反应? 解:第二次反应是恰好完全反应。
(2)该样品中碳酸钙的质量分数? 解:该样品的碳酸钙的质量为x CaCO 3 + 2HCl === CaCl 2 + H 2O + CO 2↑ 100 44 x 3.3g100/x=44/3.3gx=7.5g7.5g/10g ×100%=75%答:该样品中碳酸钙的质量分数为75% 例3、图像题取某铜锌合金10g 与100g 稀硫酸反应,记录不同时刻剩余固体的质量,并绘制成如下图像:求:(1)生成氢气的质量?解:10g+100g -109.8g=0.2g(2) 合金中锌的质量分数? 解:设参加反应的锌的质量为x Zn +H 2SO 4= ZnSO4 + H 2↑ 65 2 x 0.2g65/x=2/0.2g x=6.5g6.5g/10g ×100%=65%答:合金中锌的质量分数为65% 剩余固体/gt109.8 0110.02、某同学为了测定黄铜屑(由锌和铜形成的合金)样品组成。
初中化学方程式计算题题型汇总(最新整理)

初中化学方程式计算题题型汇总初中化学计算的主要内容如下: (一)有关化学式的计算 用元素符合来表示物质组成的式子叫做化学式。
本知识块的计算关键是抓住这一概念,理解概念的含义,并要深刻理解化学式中各符号及数字的意义,处理好部分与整体之间的算术关系。
1.计算相对分子质量。
相对分子质量是指化学式中各原子的相对原子质量的总和。
通过化学式可以计算出该物质的相对分子质量,也可以通过相对分子质量,求某物质的化学式。
在计算的过程中应注意化学式前面的数字(系数)与相对分子质量及元素符号右下角的数字与相对原子质量之间的关系是“相乘”不是“相加”;若计算结晶水合物的相对分子质量时,化学式中间的“·”与结晶水的相对分子质量之间是“相加”不是“相乘”。
例计算5CuSO4·5H2O的相对分子质量总和。
5CuSO4·5H2O=5×[64+32+16×4+5×(1×2+16)]=5×[160+5×18]=1250 2.计算化合物中各元素的质量比 宏观上物质是由元素组成的,任何纯净的化合物都有固定的组成,这样可以计算化合物中所含元素的质量比。
计算的依据是所含元素的质量比,等于微观上每个分子(即化学式)中各种原子的个数与其原子量的乘积之比。
例计算氧化铁中铁元素和氧元素的质量比。
氧化物的化学式:Fe2O3,则 Fe∶O=56×2∶16×3=112∶48=7∶3 3.计算化合物中某元素的质量分数 宏观上化合物中某元素的质量分数等于微观上化合物的每个分子中,该元素的原子的相对原子质量总和与化合物的相对分子质量之比,即: 化合物中某元素质量比=×100% 例计算硝酸铵(NH4NO3)中,含氮元素的质量分数。
w(N)=×100%=35% (二)有关化学方程式的计算 化学方程式是用化学式表示化学反应的式子,这样,化学方程式不仅表达了物质在质的方面的变化关系,即什么是反应物质和什么是生成物质,而且还表达物质在量的方面的变化关系,即反应物质和生成物质的质量关系,同时包括反应物质和生成物质的微粒个数关系,这是有关化学方程式计算的理论依据。
利用化学方程式的简单计算(题型)

利用化学方程式的计算一、质量比的计算1.丁酸乙酯(C6H12O2)是无色、具有菠萝香味的液体, 常用作食品、饮料的调香剂。
下列正确的()A.丁酸乙酯是由20个原子构成的B.丁酸乙酯中碳元素的质量分数为27.6%C.丁酸乙酯中碳、氢、氧元素的质量比为18: 3: 8D.一个丁酸乙酯分子中, 碳、氢、氧原子的个数比为3:6:22.电解水得到氢气和氧气的质量比为()A.4: 8B.1: 8C.2: 1D.1: 163.磷在氧气中燃烧生成五氧化二磷的化学反应方程式中磷、氧气、五氧化二磷的质量比是()A.31: 16: 142B.4: 5: 2C.124: 160: 284D.31: 32: 71解析: 体会求物质中各元素质量比和化学方程式中求各物质质量比的区别。
二、“相同质量”的计算4.相同质量的下列各种物质, 经完全分解后, 制得氧气质量最多的是()A.HgOB.KMnO4C.H2OD.H2O25、相同质量的下列物质分别在氧气中完全燃烧, 消耗氧气最多的是()A.CB.H2C.FeD.P解析:设相同质量的各物质质量为1g, 方便计算。
三、过量问题6.4g碳在8g氧气中充分燃烧后, 生成二氧化碳的质量是()A.22gB.44gC.11gD.12g7、16克H2与196克 O2充分反应, 求生成水的质量。
第次以后, 生成氧化镁的质量不再增加。
为什么会出现这种情况?解析: 两个已知量, 莫急于代入计算, 需先判断哪个物质过量有剩余, 应用充分反应的量代入计算。
四、反应前后固体质量减少9、15g氯酸钾和二氧化锰的混合物, 充分加热后剩余10.2g固体物质, 则原混合物中二氧化锰的质量为()A.10.2gB.2.75gC.4.8gD.10g10、实验室用加热10g高锰酸钾的方法制取氧气, 实验完毕, 剩余固体为9.2g, 通过计算确定9.2g固体物质中含有那些物质?它们的质量各是多少?11.为测定某石灰石样品中碳酸钙的含量, 取样品10.0g于烧杯中加入稀盐酸50.0g, 恰好完全反应(杂质不反应), 反应后烧杯中物质的总质量为56.7g。
化学方程式计算题型汇总

化学方程式计算题型汇总题型一1、加热分解12.25克氯酸钾,可得到多少克的氧气?同时生成氯化钾多少克? 题型二实验室有不纯的氯酸钾样品,把该样品与1g 二氧化锰混合加热制取氧气(杂质不参加反应),充分反应后,固体混合物质量变化如下所示(1)生成氧气的质量为 g ;(2)样品中氯酸钾的质量分数是多少? 题型三在含少量NaCl 的某纯碱(碳酸钠)样品26.5g 中加入盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示.(提示:相关反应为:Na 2CO 3+2HCl=2NaCl+H 2O+CO 2↑)计算当恰好完全反应时:(1)产生的二氧化碳的质量是 克 (2)此纯碱样品中碳酸钠的质量分数 题型四实验室用氯酸钾和二氧化锰的混合物制取氧气,某次实验中固体的质量变化如图:反应前固体总质量 反应后固体总质量13.5g 8.7g(1)生成氧气的质量是g,剩余的固体混合物中二氧化锰的质量是g;(2)求参加反应的氯酸钾的质量.题型五氢化钙(CaH2)是有机合成的还原剂,遇水发生化学反应,生成氢氧化钙和氢气.为了测定某样品中氢化钙的含量,进行了如图所示实验,请计算:(反应原理:CaH2+2H2O═Ca(OH)2+2H2↑)(1)生成氢气的质量是g.(2)该样品中氢化钙的质量分数题型六某兴趣小组为了测定铜锌合金(不含有其它杂质)中锌的质量分数,取出10g合金样品放入试管中,加入足量稀硫酸充分反应后,溶液中还剩余部分固体,试管中物质总质量减少0.2g,请回答:样品中锌的质量分数是多少?(Zn + H2SO4=== ZnSO4+ H2↑ )题型七某同学为了测定某黄铜样品(主要含有铜和锌,其他成分忽略不计)中铜的质量分数,取10g样品加入100g稀硫酸中,充分反应后,称量剩余物的质量为109.8g,求:(Zn + H2SO4=== ZnSO4 + H2↑ )(1)生成氢气的质量;(2)计算黄铜样品中铜的质量分数.题型八小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:(CaCO3高温 CaO+ CO2↑)(1)完全反应后生成二氧化碳的质量是g.(2)求珍珠粉中碳酸钙的质量分数.题型九小华同学取某地石灰石(主要成分是碳酸钙)样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成其他的总质量如表所示:(CaCO3+2HCl==CaCl2+H2O+CO2↑ )(1)m的值为g.(2)石灰石样品中碳酸钙的质量.题型十某纯碱样品中混有少量的氯化钠,为了测定样品的纯度,小明准确称取样品12.0g,并将60g稀盐酸等分四次加入,每次产生气体情况如下表,请回答下列问题:(Na2CO3+2HCl=2NaCl+H2O+CO2↑)(1)m的值是;(2)产生CO2的总质量是;(3)纯碱样品中的Na2CO3的质量分数是多少?(计算结果保留1位小数).。
化学方程式的计算练习题40道

化学方程式的计算练习题40道化学方程式的计算练习题40道一、根据化学方程式进行计算1、在一个有6克氧气的密闭容器中,有5克铁粉和足量的硫,加热使之充分反应,问生成多少克固体混合物?2、现有10克氢气和氧气混合气体,点燃使之充分反应,得到5克水蒸气,问原来混合气体中各成分的质量?3、欲制得100千克碳酸钙含量为80%的石头灰,需要煅烧含碳酸钙含量为85%的石灰石多少千克?4、在一定条件下,11.2克金属钠与氧气完全反应,生成16.6克氧化物,求氧化物的化学式。
5、现有硫酸铜溶液20千克,其中含铜的质量分数为6%,现欲采用电解的方法除去其中的水分,问需要除去的水分质量为多少千克?(设水的质量分数为99%)二、物质的量在化学方程式计算中的应用6、在39千克过氧化氢溶液中,加入0.5千克二氧化锰,充分反应后可以得到多少摩尔氧气?61、在标准状况下,11.2升一氧化碳和13.2升氢气混合,充分反应后得到多少克产物?611、一定量的乙醇在氧气不足的情况下燃烧,得到二氧化碳、一氧化碳和水的总质量为50.4克,其中水的质量为25.2克,求二氧化碳的质量。
6111、在一个密闭容器中,有适量铜与一定量氧气反应,生成氧化铜的质量为16克,问消耗氧气的质量为多少?三、有关溶液的计算10、在20℃时,将33克食盐放入100克水中,充分溶解后得到溶液。
已知在该温度下,食盐在水中的溶解度为36克,求所得溶液的质量分数。
101、将58.5克食盐全部溶于200克水中,求该食盐溶液的质量分数。
1011、在20℃时,将40克硝酸钾溶于100克水中,已知在该温度下,硝酸钾在水中的溶解度为60克,求所得溶液的质量分数。
四、综合计算13、工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。
现称取纯碱样品12克,全部溶解在94.7克水中。
当加入稀盐酸73克时,恰好完全反应。
生成的气体全部逸出,所得溶液质量为170.2克。
计算反应后所得溶液中溶质的质量分数。
化学方程式计算题

化学方程式计算题第一篇:化学方程式计算题(一)1. 将2.5 mol 的铁和1.5 mol 的硫磨碎混合,然后使之彻底反应,形成化合物 FeS。
请写出该反应的化学方程式,并计算反应后全部反应物被消耗完所生成的 FeS 的物质量。
解答:化学方程式: 2Fe + S -> FeS根据化学方程式可知,1 mol 的反应产物 FeS 的摩尔质量为 56 g/mol。
因此,2.5 mol 的铁完全反应后,生成 FeS 的质量为:2.5 mol × 56 g/mol = 140 g2. 将1 mol 的氯化铝与1 mol 的硫酸反应,生成铝硫酸和氯气。
请写出该反应的化学方程式,并计算反应后生成的氯气的体积(假设理想气体行为)。
解答:化学方程式:2AlCl3 + 3H2SO4 -> Al2(SO4)3 + 6HCl 根据化学方程式可以确定,该反应中 2 mol 的 AlCl3 会生成 6 mol 的 HCl。
假设气体的体积与摩尔数成正比,因此在该反应中,生成的 HCl 气体体积为:2 mol of AlCl3 : 6 mol of HCl = 1 mol : 3 mol即 1 mol 的 AlCl3 反应后生成 3 mol 的 HCl。
因此,1 mol 的 AlCl3 反应后生成的 HCl 气体体积为3 倍,即 3 mol。
3. 当 1 L 的乙炔(C2H2)气体与氧气(O2)完全反应时,生成的二氧化碳(CO2)和水(H2O),该反应发生在一定的压力和温度条件下。
请写出该反应的化学方程式,并计算反应后产生的 CO2 的体积。
解答:化学方程式:2C2H2 + 5O2 -> 4CO2 + 2H2O根据化学方程式可知,2 mol 的 C2H2 在完全反应后会生成 4 mol 的 CO2。
假设气体的体积与摩尔数成正比,因此在该反应中,生成的 CO2 气体体积为:2 mol of C2H2 : 4 mol of CO2 = 1 mol : 2 mol即 1 mol 的 C2H2 反应后生成 2 mol 的 CO2。
化学化学方程式的计算题20套(带答案)及解析
化学化学方程式的计算题20套(带答案)及解析一、中考化学方程式的计算1.洁厕灵是常用的陶瓷清洗液,某同学对某品牌洁厕灵的有效成分含量进行探究。
向一锥形瓶中加入100 g 该品牌的洁厕灵,再加入足量的溶质质量分数为8%的NaHCO 3溶液120 g ,反应结束后溶液的总质量是215.6 g 。
试计算下列问题:(知识卡片)①洁厕灵有效成分是HCl ,洁厕灵中其它成分均不跟NaHCO 3反应。
②HCl 和NaHCO 3反应的化学方程式为HCl+NaHCO 3=NaCl+H 2O+CO 2↑(1) 产生的二氧化碳质量为_________克。
(2) 该品牌洁厕灵中HCl 的质量分数是多少?_____(写出计算过程) 【答案】4.4 3.65% 【解析】【分析】盐酸和碳酸氢钠反应生成氯化钠、水和二氧化碳,由质量守恒定律可知,反应物的总质量等于生成物的总质量,减少的是生成的气体或沉淀的质量。
【详解】(1) 由质量守恒定律可知,反应物的总质量等于生成物的总质量,减少的是生成的气体或沉淀的质量,故产生的二氧化碳质量为100g+120g-215.6g=4.4g 。
(2) 设100 g 该品牌洁厕灵中HCl 的质量为x322HCl +NaHCO =NaCl +H O +CO 36.544x4.4g↑36.544=x 4.4gx=3.65g该品牌洁厕灵中HCl 的质量分数为:3.65g100%=3.65%100g⨯答:该品牌洁厕灵中HCl 的质量分数为3.65%。
【点睛】=100%⨯溶质质量溶质质量分数溶液质量2.某造纸厂排放的废水中含有Na 2CO 3和NaOH 。
为测定废水中Na 2CO 3的质量分数,取50g 废水样品于烧杯中,将40g 稀盐酸分成4等份分4次缓慢加入到烧杯中,产生气体质量与稀盐酸溶液的质量关系如图曲线所示。
回答下列问题:(1)请仔细分析如图数据,完成下表实验记录: 实验次数 123 4 稀盐酸的质量(g ) 10 101010生成气体质量(g )____ ____ ____(2)上述生成气体________ g 。
初三化学 化学方程式计算习题全
初三化学化学方程式计算习题全化学方程式的计算是初三化学学习中的重要内容,它不仅能帮助我们理解化学反应的本质,还能在实际问题中解决物质的定量关系。
以下是为大家精心准备的一系列化学方程式计算习题。
一、基础类型1、实验室用分解过氧化氢的方法制取氧气。
若要制取 16 克氧气,需要分解多少克过氧化氢?解:设需要分解过氧化氢的质量为 x。
2H₂O₂= 2H₂O + O₂↑68 32x 16g68/x = 32/16gx = 34g答:需要分解 34 克过氧化氢。
2、工业上用煅烧石灰石(主要成分是 CaCO₃)的方法制取生石灰(CaO)和二氧化碳。
若要制取56 吨生石灰,需要分解多少吨石灰石?解:设需要分解石灰石的质量为 y。
CaCO₃= CaO + CO₂↑100 56y 56t100/y = 56/56ty = 100t答:需要分解 100 吨石灰石。
二、含有杂质的计算3、某赤铁矿样品 10 克,经实验分析知其含氧化铁(Fe₂O₃)8 克,求该赤铁矿样品中氧化铁的质量分数。
解:氧化铁的质量分数=(8g÷10g)×100% = 80%答:该赤铁矿样品中氧化铁的质量分数为 80%。
4、用含杂质 20%的石灰石 100 克与足量的稀盐酸反应,能生成多少克二氧化碳?解:石灰石中碳酸钙的质量= 100g×(1 20%)= 80g设生成二氧化碳的质量为 z。
CaCO₃+ 2HCl = CaCl₂+ H₂O + CO₂↑100 4480g z100/80g = 44/z答:能生成 352 克二氧化碳。
三、多步反应的计算5、用一氧化碳还原氧化铜制取铜。
若要制取 64 克铜,需要一氧化碳的质量是多少?同时生成二氧化碳的质量是多少?解:设需要一氧化碳的质量为 a,生成二氧化碳的质量为 b。
CuO + CO = Cu + CO₂28 64 44a 64g b28/a = 64/64g 64/64g = 44/ba = 28gb = 44g答:需要一氧化碳的质量是 28 克,同时生成二氧化碳的质量是 44 克。
化学方程式计算题型总结
甲 10
乙 10
丙 20
100 120 100 2 2 12
9、一表面氧化的镁24克与150克稀盐酸恰好完全
反应,共放出氢气0.16克,求此稀盐酸的质量分
数?
10.碳酸钠和氯化钠的固体的混合物13.3克,与45.5
克稀盐酸恰好完反应,反应得到T℃的氯化钠的饱
和溶液54.4克,没有晶体析出,求
(1)生成二氧化碳的质量.
14、将氯化钠和碳酸钠的混合物33.8克放入125克
有关化学方程式的计算题型总结
1.含杂质30%的铁粉16克,跟足量稀硫酸反应
(杂质不反应)可生成氢气多少克?
2、100克石灰石加热分解共放出2.2克二氧化
碳,求此石灰石中含碳酸钙的质量分数?
3、50克10%的氢氧化钠溶液能中和多少克硫酸?
4、8克碳和8克氧气反应,共生成多少二氧化碳?
5、98克10%的硫酸与80克20%的氢氧化钠溶液 反应,生成多少克硫酸钠?
稀盐酸中,恰好完全反应,得氯化钠溶液150克(无
晶体析出),计算
(1)原混合物中碳酸钠质量为多少克。
16、若21.2克碳酸钠与87.6克盐酸恰好完全反应,
计算 (1)原盐酸溶液的质量分数; (2)反应后所得溶液的溶质质量分数。
17、甲、乙、丙三位同学分别取铁粉和铜粉的均 匀混合物与某稀硫酸反应,所得数据如下:计算 (1)金属混合物中铁的质量分数 (2)甲制得硫酸亚铁的质量 (3)该稀硫酸中溶质的质量分数 取用金属混合物的质量(克) 取用稀硫酸的质量(克) 反应后过滤得到的干燥固体 的质量(克)
6、6.2克氧化钠溶于100克水中,所得溶液的溶质
质量分数是多少?
7、50克10%的氢氧化钠溶液恰好能与100克硫
化学方程式计算常见题型(含答案)
化学方程式计算常见题型一、填空题(共7道,每道10分)1.某干燥剂含氧化钙的质量分数是80%(吸水原理为CaO+H2O=Ca(OH)2,杂质不吸水),理论上14g干燥剂能吸收水的质量为____g。
(相对原子质量:H-1,O-16,Ca-40)答案:3.6解题思路:要求吸收水的质量,可根据所给的干燥剂中的氧化钙的质量来求,需注意,化学反应中各物质均为纯净物,计算时需将不纯物的质量换算成纯净物的质量。
14 g干燥剂中氧化钙的质量为14g×80%=11.2g。
设14 g干燥剂能吸收水的质量为x。
则试题难度:知识点:化学方程式的计算2.某工厂煅烧石灰石生产生石灰(反应的化学方程式为CaCO3CaO+CO2↑),若生产200 t含氧化钙84%的生石灰,需要含碳酸钙75%的石灰石的质量为____t。
(相对原子质量:C-12,O-16,Ca-40)答案:400解题思路:要求所需石灰石的质量,可根据生成物(CaO)的质量求反应物的质量,需注意,化学反应中各物质均为纯净物,计算时需将不纯物的质量换算成纯净物的质量。
根据题意可知生成物氧化钙(CaO)的质量为200t×84%=168 t。
设需要含碳酸钙(CaCO3)75%的石灰石的质量为x,则需要的碳酸钙的质量为75%x。
试题难度:知识点:化学方程式的计算3.某兴趣小组取150 g过氧化氢溶液在3 g二氧化锰的作用下反应,反应一段时间后测得容器中剩余物质的总质量为149.8 g。
试计算:(相对原子质量:H-1,O-16)(1)生成氧气的质量为____g。
(2)生成水的质量为____g。
答案:3.2, 3.6解题思路:涉及到的化学方程式为2H2O22H2O+O2↑。
(1)反应前容器中物质的总质量为150g+3 g=153 g,反应后容器中总质量为149.8g,减少的质量即为放出氧气的质量,则氧气的质量为153g-149.8 g=3.2 g。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
化学方程式计算题型汇总
题型一
1、加热分解12.25克氯酸钾,可得到多少克的氧气?同时生成氯化钾多少克?
题型二
实验室有不纯的氯酸钾样品,把该样品与1g二氧化锰混合加热制取氧气(杂质不参加反应),充分反应后,固体混合物质量变化如下所示
(1)生成氧气的质量为Array
g;
(2)样品中氯酸钾的质量分数是
多少?
题型三
在含少量NaCl的某纯碱(碳酸钠)样品26.5g中加入盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示.(提示:相关反应为:Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰
好完全反应时:
(1)产生的二氧化碳的质量是克
(2)此纯碱样品中碳酸钠的质量分数
题型四
实验室用氯酸钾和二氧化锰的混合物制取氧气,某次实验中固体的质量变化如图:
(1)生成氧气的质量是g,剩余的固体混合物中二氧化锰的质量是g;(2)求参加反应的氯酸钾的质量.
题型五
氢化钙(CaH2)是有机合成的还原剂,遇水发生化学反应,生成氢氧化钙和氢气.为了测
定某样品中氢化钙的含量,进行了如图所示实验,请计算:
(反应原理:CaH2+2H2O═Ca(OH)2+2H2↑)
(1)生成氢气的质量是g.
(2)该样品中氢化钙的质量分数
题型六
某兴趣小组为了测定铜锌合金(不含有其它杂质)中锌的质量分数,取出10g合金样品放
入试管中,加入足量稀硫酸充分反应后,溶液中还剩余部分固体,试管中物质总质量减少0.2g,请回答:样品中锌的质量分数是多少?(Zn + H2SO4 === ZnSO4 + H2↑ )
题型七
某同学为了测定某黄铜样品(主要含有铜和锌,其他成分忽略不计)中铜的质量分数,取10g样品加入100g稀硫酸中,充分反应后,称量剩余物的质量为109.8g,求:(Zn + H2SO4 === ZnSO4 + H2↑ )
(1)生成氢气的质量;
(2)计算黄铜样品中铜的质量分数.
题型八
小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5g珍珠粉样品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
(CaCO3高温CaO+ CO2↑)
(1)完全反应后生成二氧化碳的质量是g.
(2
题型九
小华同学取某地石灰石(主要成分是碳酸钙)样品12g进行测定实验,现将100g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),充分反应后测得生成其他的总质量如表所示:(CaCO3+2HCl==CaCl2+H2O+CO2↑ )
(1
m
的值为g.(2石灰石样品中碳酸钙的质量.
题型十
某纯碱样品中混有少量的氯化钠,为了测定样品的纯度,小明准确称取样品12.0g,并将60g 稀盐酸等分四次加入,每次产生气体情况如下表,请回答下列问题:
(Na2CO3+2HCl=2NaCl+H2O+CO2↑)
(1)m的值是;
(2)产生CO2的总质量是;
(3)纯碱样品中的Na2CO3的质量分数是多少?(计算结果保留1位小数).。
