工程热力学实验一
工程热力学实验

工程热力学实验
工程热力学实验是一种通过实验手段研究热力学问题的方法。
在这种实验中,通常会使用一些设备和仪器,如热力计、压力计、温度计等,来测量和记录热力学参数,例如压力、温度、热功、热容等。
在实验中,通常会选择一些代表性的系统或过程进行研究,例如理想气体的等温膨胀、绝热膨胀、等压过程等,以及一些实际工程中常见的热力学问题,如锅炉、汽轮机、制冷系统等。
通过对这些系统或过程的实验研究,可以深入了解它们的热力学特性,为实际工程应用提供重要的参考和支持。
为了保证实验的准确性和可靠性,工程热力学实验需要进行一系列的实验设计和实验操作,如实验设备的校准和调试、实验数据的记录和处理、实验结果的分析和验证等。
同时,还需要注意实验安全和环保,做好实验废物的处理和管理工作。
总之,工程热力学实验是一种非常重要的热力学研究方法,它为实际工程应用提供了可靠的理论基础和实验支持。
工程热力学实验指导书

热能与动力工程专业工程热力学实验指导书编写教师:商福民能源动力学院热工实验室实验一 空气定压比热的测定一、实验目的比热是理想气体十分重要的热力性质。
气体定压比热的测定是工程热力学的基本实验之一。
实验中涉及温度、压力、热量(电功)、流量等基本量的测量。
本实验将通过流通量热法使学生掌握测定空气平均定压质量比热的基本方法,以加深对比热理论的理解,增强热物性实验研究方面的感性认识,促进理论联系实际,培养分析问题和解决问题的能力。
二、实验原理让空气连续而稳定地(即所谓稳定流动)流经一个特制的加热器,在加热器中空气被加热,温度升高,比容变大,流速加快,而压力只有一小部分消耗在摩阻上,当流动阻力相对工质压力而言很小时,若加热器入口压力恒定,则我们就可以近似地认为空气是定压流动。
当空气流速和温度都达到稳定后,若加热器对外热损失很小而忽略不计,则加热器内热源的放热全部被空气吸收(注意:必须是当达到稳定流动时才如此,因为温度等不稳定,说明有一部分热量储存在加热器本体内)。
此热平衡关系可用下式表示:)(1221t t mc Q tt p -=式中:t 1、t 2 —加热器入、出口空气温度,℃;m —空气的质量流量,kg/s ;21tt p c —空气在t 1、t 2范围内的平均定压质量比热,J/(kg·K);Q —加热器内热源单位时间内的放热,W 。
如上所述21tt p c 待求,而Q 、t 1、t 2、m 大小均可在实验中测出,方法如下:1.t 1、t 2大小由温度计直接读得。
2.111RT V p m =,式中T 1、p 1为加热器入口空气温度T 1=t 1+273.15和绝对压力p 1=p g +p b (Pa ),p g 和p b 大小由U 型管压力计和大气压力计读得(注意单位的统一)。
空气的容积流量V (m 3/s )大小由流量计上直接读取(m 3/h )(注意单位的换算)。
3.本实验用的是电加热器,电热源是一只电热丝,因而其放热量Q=IU(W)。
工程热力学实验报告

水的饱和蒸汽压力和温度关系实验报告水的饱和蒸汽压力和温度关系一、实验目的1、通过水的饱和蒸汽压力和温度关系实验,加深对饱和状态的理解。
2、通过对实验数据的整理,掌握饱和蒸汽P-t关系图表的编制方法。
3、学会压力表和调压器等仪表的使用方法。
二、实验设备与原理4 5 6 71. 开关2. 可视玻璃3. 保温棉(硅酸铝)4. 真空压力表(-0.1~1.5MPa)5. 测温管6. 电压指示7. 温度指示8. 蒸汽发生器9. 电加热器10. 水蒸汽11.蒸馏水12. 调压器图 1 实验系统图物质由液态转变为蒸汽的过程称为汽化过程。
汽化过程总是伴随着分子回到液体中的凝结过程。
到一定程度时,虽然汽化和凝结都在进行,但汽化的分子数与凝结的分子数处于动态平衡,这种状态称为饱和态,在这一状态下的温度称为饱和温度。
此时蒸汽分子动能和分子总数保持不变,因此压力也确定不变,称为饱和压力。
饱和温度和饱和压力的关系一一对应。
二、实验方法与步骤1、熟悉实验装置及使用仪表的工作原理和性能。
2、将调压器指针调至零位,接通电源。
3、将调压器输出电压调至 200V,待蒸汽压力升至一定值时,将电压降至 30-50V保温(保温电压需要随蒸汽压力升高而升高),待工况稳定后迅速记录水蒸汽的压力和温度。
4、重复步骤3,在 0~4MPa(表压)范围内实验不少于 6次,且实验点应尽量分布均匀。
5、实验完毕后,将调压器指针旋回至零位,断开电源。
6、记录室温和大气压力。
四、数据记录1. 绘制 P -t 关系曲线将实验结果绘在坐标纸上,清除偏离点,绘制曲线。
五、实验总结19.0235.0544.8657.9669.0180.2492.0699.79y = 35.834x 0.81241030507090110130012345饱和蒸汽P-t 关系图温度/°c压力/Mpa仪器编号 1(R134a ) 大气压力 B /MPa0.10室温 /℃23 实验次数饱和压力MPa饱和温度 ℃误差压力表读数 P’绝对压力 P =P’+B温度读数 t’对应压力 P1温度读数 t’绝对压力 P 对应温度 tΔt =t -t’ΔP =P1-P1 无 0.568 0.537 18 19.02 -1.02 -0.35% -0.031 -5.77% 2 无 0.897 0.862 34 35.05 -1.05 -0.34% -0.035 -4.06%3 无 1.165 1.13 44 44.86 -0.86 -0.27% -0.035 -3.10% 4 无 1.614 1.603 58 57.96 0.04 0.01% -0.011 -0.69% 5 无 2.088 2.023 68 69.01 -1.01 -0.30% -0.065 -3.21% 6 无 2.667 2.633 80 80.24 -0.24 -0.07% -0.034 -1.29% 7 无 3.3943.379 92 92.06 -0.06 -0.02% -0.015 -0.44% 8无43.8979899.79-1.79-0.48%-0.103-2.64%用双对数坐标纸绘制水的饱和蒸汽压力-温度曲线,曲线近似成一条直线。
工程热力学实验指导书(三个实验)

工程热力学课程实验指导书兰州理工大学2006年6月实验1空气定压比热测定实验指导书一、实验目的1.掌握气体比定压热容的测量原理及其操作方法;2.掌握本实验中测温、测压、测热、测流量的方法;3.掌握由基本数据计算比热值的方法;4.分析实验产生误差的原因及减小误差的可能途径。
二、实验装置如图1.1所示,本实验装置由风机、流量计、比热仪主体、调压器和功率表等组成。
实验时,被测空气由风机经流量计送入比热仪主体,经加热、均流、旋流、混流后流出。
比热仪主体构造如图1.2所示,由多层杜瓦瓶、电热器、均流阀、绝缘垫、旋流片、混流网、出口温度计等组成。
气体的流量由节流阀调节,比热仪出口温度由电加热器输入功率来控制。
比热仪可测200℃以下气体的定压比热。
图1.1 比热仪全套装置图1.2 比热仪主体三、实验原理根据气体平均定压比热定义,当气体在定压加热过程中温度由t1升到t2时,其平均定压比热可以由下式确定:21,21|()ptp m tmQcq t t=-J/(kg.℃)式中:Q p-湿空气在定压加热过程中的吸热量J/sq m-湿空气的质量流量kg/s湿空气是干空气和水蒸气的混合物,当湿空气中水蒸气含量较少,分压力较低时,水蒸气可以当作理想气体处理。
显然,当已知湿空气中水蒸气的吸热量Q v时,干空气的定压比热可由下式确定:21,,21|()p v t pm a t m a Q Q c q t t -=- J /(kg.℃)式中: Q p -湿空气在定压加热过程中的吸热量 J /s Q v -水蒸气的吸热量 J /s q m ,a -干空气的质量流量 kg /s由1t 加热到2t 的平均定压比热则可表示为:()212112,212t t t p m t a bt dt t t ca bt t ++==+-⎰ 若以(t 1+t 2)/2为横坐标,21,t p mt c 为纵坐标,如图3所示,则可根据不同温度范围的平均比热确定截距a 和斜率b,从而得出比热随温度变化的计算式。
华北电力《工程热力学》实验指导01气体定压比热容实验

《工程热力学》实验指导工程热物理教研室二O年月1.实验总体目标通过实验能更好地理解工程热力学的一些现象和结论。
学习一些实验仪器的使用方法。
学习实验数据的处理方法。
2.适用专业热能与动力工程、建筑环境与设备工程、核科学与核工程3.先修课程高等数学、大学物理4.实验课时分配5.实验环境实验室环境干净整洁,水电齐全,能够满足实验的要求。
在醒目的地方有实验原理的说明,便于教师讲解和学生熟悉实验的步骤。
6.实验总体要求通过实验能够帮助学生更好地理解工程热力学的一些基本原理。
指导教师要提前做好准备,提高实验的效率。
学生要提前预习实验的内容和要求(特别是注意事项),以免发生危险和损坏实验设备。
按指导教师的要求书写实验报告,及时上交。
7.本实验的重点、难点及教学方法建议本实验的重点是气体定压比热容实验、二氧化碳压缩综合实验和喷管实验,这三个实验都是综合性实验,涉及到水浴的使用,真空泵的使用,表压力及真空度和绝对压力的关系,等等,需要大家对工程热力学的基本内容有清楚的了解。
难点是在临界温度下定温压缩二氧化碳时不好把握,绘出来的图和理想压缩有较大的差别,另外,如何通过间接方法求出二氧化碳的比体积也有一些技巧。
教学方法:学生提前预习,做实验之前老师提问;学生仔细观察指导教师的演示;实验室对学生开放,一次没有做成功,或者想更好地掌握实验技巧的学生,可以跟指导教师预约时间另做。
实验一气体定压比热容实验 (3)实验二二氧化碳综合实验 (7)实验三空气在喷管内流动性能测定实验 (8)实验四饱和蒸汽压力和温度关系实验 (11)实验一气体定压比热容实验一、实验目的1 .了解气体比热容测定装置的基本原理和构思。
2 .熟悉本实验中测温、测压、测热、测流量的方法。
3 .掌握由基本数据计算出比热值和比热公式的方法。
4 .分析本实验产生误差的原因及减小误差的可能途径。
二、实验类型综合性实验三、实验仪器实验所用的设备和仪器仪表由风机、流量计、比热仪本体、电功率调节测量系统共四部分组成,实验装置系统如图1-1所示。
工程热力学实验讲义
第一章 工程热力学§1-1 空气绝热指数的测定实验一、实验目的通过测量绝热膨胀和定容加热过程中空气的压力变化,计算空气绝热指数。
理解绝热膨胀过程和定容加热过程以及平衡态的概念。
二、实验原理气体的绝热指数定义为气体的定压比热容与定容比热容之比,以K 表示,即p vc k c =。
本实验利用定量空气在绝热膨胀过程和定容加热过程中的变化规律来测定空气的绝热指数K 。
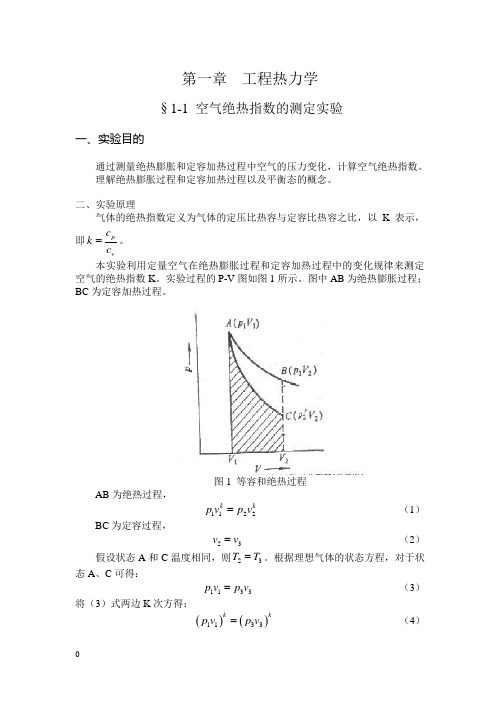
实验过程的P-V 图如图1所示。
图中AB 为绝热膨胀过程;BC 为定容加热过程。
图1 等容和绝热过程AB 为绝热过程,1122k kp v p v = (1) BC 为定容过程,23v v = (2)假设状态A 和C 温度相同,则23T T =。
根据理想气体的状态方程,对于状态A 、C 可得:1133p v p v = (3)将(3)式两边K 次方得:()()1133kkp v p v = (4)由(1)、(4)两式得,1132kp p p p ⎛⎫=⎪⎝⎭,再两边取对数,得: 1213ln ln p p k p p ⎛⎫ ⎪⎝⎭=⎛⎫ ⎪⎝⎭(5)因此,只要测出A 、B 、C 三状态下的压力123,,p p p 且将其代入(5)式,即可求得空气的绝热指数k 。
三、实验装置空气绝热指数测定仪由刚性容器,充气阀、排气阀和U 型差压计组成,如图2所示。
空气绝热指数测定仪以绝热膨胀和定容加热两个基本热力过程为工作原理,测出空气绝热指数。
整个仪器简单明了,操作简便,有利于培养学生运用热力学基本和公式从事实验设计和数据处理的工作能力,从而起到巩固和深化课堂教学内容的实际效果。
图2 空气绝热指数测定装置示意图1-有机玻璃容器;2-进气及测压三通;3 U 型压力计;4 -气囊;5-放气阀门。
四、实验步骤实验对装置的气密性要求较高。
因此,在实验开始时,应检查其气密性。
通过充气阀对刚性容器充气,使U 型压差计的水柱h ∆达到2200mmH O 左右,记下h ∆值,5分钟后再观察h ∆值,看是否发生变化。
热流技术基础实验(二)——热工综合实验

装置由风机、流量计、比热仪主体、电功率调节、热电偶测温电路及测量系统等四部分 组成(如图 2-1 所示)。
图 2-1 实验装置
比热仪主体如(图 2-2)所示。 实验时,被测空气(也可以时其它空气)由风机经流量计送入比热仪主体,经加热、均流、 旋流、混流后流出。在此过程中,分别测定:空气在流量计出口处的干、湿球温度(t0,tw);气
14第二章热工综合实验第一节实验概述一工程热力学实验在本实验中主要研究热力学的基本现象通过研究饱和水蒸气的pt关系测定空气的定压比热两个实验掌握常用热工参数的测试方法了解空气水等介质的热力学性质
陕西科技大学机电工程学院实验指导书
1
前言
实验教学是热工教学过程的重要环节,它不仅可以巩固和加深对课本知识的理解,更重 要的是通过有计划、有目的的实验教学,可以训练学生的动手能力,培养学生的工程实践技 能,提高学生的科学素质。
蒸汽发生器
配汽管 光管
镀铬管 锯末保温管
玻璃丝保温管
翅片管 涂黑管
玻璃量筒
二、 实验装置:
图 3-1
传热综合实验台结构如(图 3-1)所示。
三、 实验步骤
1、 检查设备是否完好。 2、 蒸汽发生器装水,通电自动加热,达到实验蒸汽压力(0.2~0.4MPa)和温度。 3、 打开配汽管上和玻璃量筒下的所有开关,慢慢供气,预热和排空系统。
图 1-1
4
陕西科技大学机电工程学院实验指导书
升至一定值时,将电压降至 20~50V 保温,待工况稳定后迅速记录下水蒸气的压力和温 度。重复上述实验,在 0~1.0Mpa(表压)范围内实验不少于 6 次,且实验点应尽量分布 均匀。 4、 实验完毕后,将调压指针旋回零位,并断开电源。 5、 记录室温和大气压力。
气体定压比热测定实验

干气体定压比热测定实验干气体定压比热的测定是工程热力学的基本实验之一。
实验中涉及温度、压力、热量(电功)、流量等基本量的测量;计算中用到比热及混合气体(混空气)方面的知识。
一、实验目的1. 了解实验装置的基本原理和结构。
2. 熟悉温度、压力、热量、流量等基本量的测量方法。
3. 掌握由基本数据计算出比热值和求得比热公式的方法。
4. 分析产生误差的原因及减小误差的途径。
二、实验原理本实验测定的是干空气的定压质量比热,而不是定压容积比热。
时,1kg气体温度升高1K时所吸收的热量,;时,1Nm3气体温度升高1K时所吸收的热量,。
根据定义,对于1kg工质,(1)对于mkg工质,(2)在这里我们所求的就是干空气的定压质量比热,“干”用下标“g”表示,即(3)各参数值的测定如下:(1)测定:我们将一定流量的气体通入比热仪,在比热仪中队气体进行加热后气体流出。
这样,气体进入比热仪与流出比热仪就存在了温度差,只要我们在比热仪进口设置温度计和出口设置温度计,即可求出。
(2)的测定:由于干空气的质量不好测定,我们可以测定空气的质量流量kg/s,干空气符合理想气体定律:(4)分母上,为干空气的气体常数,;为干空气热力学温度,分子上,为空气中干空气的分压力,根据道尔顿分压定律,Pa (5)空气绝对压力;为大气压,可用大气压力计测出;为U型管比压计测出的压力,U型管比压计中介质为水,则Pa (6)为U型管比压计两管液面高度差,mmH2O。
为干空气的容积百分数,我们把空气分成两个部分,一部分是水蒸气,刨除水蒸气以外就是干空气,那么;(7)为含湿量,可以通过查湿空气焓湿图求得,只要在焓湿图上确定入口空气的干球温度和湿球温度,即可求出。
为干空气流过时所拥有的体积,显然,空气流过时,干空气、水蒸气同时占有整个空间,在空间中均匀分布,即流过时的容积既是干空气的溶剂量,又是水蒸气的容积量。
我们用湿式流量计进行测定:(8)10升是指流量计指针转5圈的容积量,为转5圈所用的时间。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
工程热力学实验一
二氧化碳临界状态观测及p-v-t关系测定实验
[实验目的]
1、了解CO2临界状态的观测方法,增加对临界状态概念的感性认识。
2、增加对课堂所讲的工质热力状态、凝结、汽化、饱和状态等基本概念的理解。
3、掌握CO2的p-v-t关系的测定方法,学会用实验测定实际气体状态变化规律的方法和技巧。
4、学会活塞式压力计,恒温器等热工仪器的正确使用方法。
[实验设备及原理]
整个实验装置由压力台、恒温器和实验台本体及其防护罩等三大部分组成(如图一所示)。
图一试验台系统图
试验台本体如图二所示。
其中:1—高压容器;2
—玻璃杯;3—压力机;4—水银;5—密封填料;6
—填料压盖;7—恒温水套;8—承压玻璃杯;9—CO2
空间;10—温度计。
对简单可压缩热力系统,当工质处于平衡状态
时,其状态参数p、v、t之间有:
F(p,v,t)=0 或t=f(p,v) (1)
本实验就是根据式(1),采用定温方法来测定
CO2的p-v-t关系,从而找出CO2的p-v-t关系。
实验中,压力台油缸送来的压力由压力油传入高
压容器和玻璃杯上半部,迫使水银进入预先装了CO2
气体的承压玻璃管容器,CO2被压缩,其压力通过压
力台上的活塞杆的进、退来调节。
温度由恒温器供给
的水套里的水温来调节。
实验工质二氧化碳的压力值,由装在压力台上的
压力表读出。
温度由插在恒温水套中的温度计读出。
比容首先由承压玻璃管内二氧化碳柱的高度来测量,
而后再根据承压玻璃管内径截面不变等条件来换算
图二实验台本体
得出。
[实验内容]
1、测定CO2的p-v-t关系。
在p-v坐标系中绘出低于临界温度(t=20℃)、临界温度(t=31.1℃)和高于临界温度(t=50℃)的三条等温曲线,并与标准实验曲线及理论计算值相比较,并分析其差异原因。
2、测定CO2在低于临界温度(t=20℃、27℃)饱和温度和饱和压力之间的对应关系,
并与图四中的t s -p s 曲线比较。
3、观测临界状态
(1)临界状态附近气液两相模糊的现象。
(2)气液整体相变现象。
(3)测定CO 2的p c 、v c 、t c 等临界参数,并将实验所得的v c 值与理想气体状态方程和范德瓦尔方程的理论值相比较,简述其差异原因。
[实验步骤]
1、按图一装好实验设备,并开启实验本体上的日光灯(目的是易于观察)。
2、恒温器准备及温度调节:
(1)、把水注入恒温器内,至离盖30~50mm 。
检查并接通电路,启动水泵,使水循环对流。
(2)、把温度调节仪波段开关拨向调节,调节温度旋扭设置所要调定的温度,再将温度调节仪波段开关拨向显示。
(3)、视水温情况,开、关加热器,当水温未达到要调定的温度时,恒温器指示灯是亮的,当指示灯时亮时灭闪动时,说明温度已达到所需要恒温。
(4)、观察温度,其读数的温度点温度与设定的温度一致时(或基本一致),则可(近似)认为承压玻璃管内的CO 2的温度处于设定的温度。
(5)、当需要改变实验温度时,重复(2)~(4)即可。
注意:当初始水温高于实验设定温度时,应加冰进行调节。
3、作好实验的原始记录:
(1)设备数据记录:
仪器、仪表名称、型号、规格、量程、等。
(2)常规数据记录:
室温、大气压、实验环境情况等。
(3)测定承压玻璃管内CO 2质量不便测量,而玻璃管内径或截面积(A )又不易测准,因而实验中采用间接办法来确定CO 2的比容,认为CO 2的比容ν与其高度是一种线性关系。
具体方法如下:
a )已知CO 2液体在20℃,9.8MPa 时的比容ν(20℃,9.8Mpa )=0.00117 M 3/㎏。
b )实际测定实验台在20℃,9.8Mpa 时的CO 2液柱高度Δh 0(m )。
(注意玻璃管水套上刻度的标记方法)
c ) ∵kg m m A h /00117.0=)9.8Mpa ℃,20(
30=∆ν ∴ )/(00117
.020m kg K h A m =∆= 其中:K ——即为玻璃管内CO2的质面比常数。
所以,任意温度、压力下CO2的比容为:
K
h A m h ∆=∆=/ν (m 3/kg ) 式中, Δh=h-h 0
h ——任意温度、压力下水银柱高度。
h 0——承压玻璃管内径顶端刻度。
4、测定低于临界温度t=20℃时的等温线。
(1)将恒温器调定在t=20℃,并保持恒温。
(2)压力从4.41Mpa 开始,当玻璃管内水银柱升起来后,应足够缓慢地摇进活塞螺杆,以保证等温条件。
否则,将来不及平衡,使读数不准。
(3)按照适当的压力间隔取h 值,直至压力p=9.8MPa 。
(4)注意加压后CO 2的变化,特别是注意饱和压力和饱和温度之间的对应关系以及液化、汽化等现象。
要将测得的实验数据及观察到的现象一并填入表1。
(5)测定t=20℃、27℃时其饱和温度和饱和压力的对应关系。
5、测定临界参数,并观察临界现象。
(1)按上述方法和步骤测出临界等温线,并在该曲线的拐点处找出临界压力c p 和临界比容c v ,并将数据填入表1。
(2)观察临界现象。
a )整体相变现象
由于在临界点时,汽化潜热等于零,饱和汽线和饱和液线合于一点,所以这时汽液的相互转变不是象临界温度以下时那样逐渐积累,需要一定的时间,表现为渐变过程,而这时当压力稍再变化时,汽、液是以突变的形式相互转化。
b )汽、液两相模糊不清的现象
处于临界点的CO 2具有共同参数(p,v,t ),因而不能区别此时CO 2是气态还是液态。
如果说它是气体,那么,这个气体是接近液态的气体;如果说它是液体,那么,这个液体又是接近气态的液体。
下面就来用实验证明这个结论。
因为这时处于临界温度下,如果按等温线过程进行,使CO 2压缩或膨胀,那么,管内是什么也看不到的。
现在,我们按绝热过程来进行。
首先在压力等于7.64Mpa 附近,突然降压CO 2状态点由等温线沿绝热线降到液区,管内CO 2出现明显的液面。
这就是说,如果这时管内的CO 2是气体的话,那么,这种气体离液区很接近,可以说是接近液态的气体;当我们在压缩之后,突然膨胀CO 2时,这个液面又立即消失了。
这就告诉我们,这时CO 2液体离气区也是非常接近的,可以说是接近气态的液体。
既然此时的CO 2既接近气态又接近液态,所以,能处于临界点附近。
可以这样说:临界状态究竟如何,就是饱和汽、液分不清。
这就是临界点附近,饱和汽、液模糊不清的现象。
6、测定高于临界温度t=50℃时的定温线。
将数据填入原始记录表2。
[实验数据记录]
1、当时当地大气压:p b= ; 室温:t 0= ;
2、管内CO 2质面比常数的标定: h 0= , △h 0= ,
)/(00117.020m kg h K ∆== ;
[实验结果处理和分析]
1、按表1的数据,如图三在p-v 坐标系中画出三条等温线。
2、 将实验测得的等温线与图三所示的标准等温线比较,并分析它们之间的差异及原因。
3、将实验测得的饱和温度与压力的对应值与图四给出的t s -p s 曲线相比较。
4、将实验测定的临界比容c ν与理论计算值一并填入表2,并分析它们之间的差异及其原因。
3
5。
