低密度聚乙烯药用包装膜、袋质量标准(企业标准范本)
聚酯低密度聚乙烯药品包装用复合膜、袋(YBB)参考模板

国家药品监督管理局国家药品包装容器(材料)标准(试行)YBB00182002聚酯/低密度聚乙烯药品包装用复合膜、袋Laminated Films and Pouches (PET/LDPE) for Pharmaceutical Packaging本品系指聚酯(PET)与聚乙烯(LDPE)通过黏合剂复合而成的膜。
本品的袋系将上述膜通过热合的方法制成。
本标准适用于固体药品包装用的复合膜、袋。
【外观】取本品适量,照药品包装用复合膜、袋通则(试行)(YBB00132002)外观项下的方法检查,应符合规定。
【鉴别】红外光谱取本品适量,采用内表面反射方法,照分光光度法(中华人民共和国药典2000年版附录IV C)测定,PET及LDPE层应分别与对照图谱基本一致。
【阻隔性能】水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GB1037-88的规定进行。
试验时LDPE层向湿度低的一侧,试验温度(38±2)℃,相对湿度(90±5)%,不得过5.5(g/m2·24h)。
氧气透过量照塑料薄膜和薄片气体透过性试验方法压差法(GB/T1038—2000)的规定进行。
试验时LDPE层向氧气低压侧,试验温度为23℃±2℃,不得过1500cm3/( m2·24h·0.1Mpa).【机械性能】PET层与LDPE层剥离强度照药品包装用复合膜、袋通则(试行)(YBB00132002)内层与次内层剥离强度项下的方法检查,纵、横向剥离强度平均值不得低于1.0N/15mm。
【热合强度】膜除另有规定外,裁取100mm×100mm试片四片,将任意两个试片LDPE面叠合,置热封仪上进行热合,热合温度145℃-160℃,压力0.2-0.3Mpa,时间1秒。
从热合的中间部位各裁取3条15mm宽的试样,进行试验。
试样应在温度23℃±2℃,相对湿度50%±5%的环境中,放置4小时以上,并在上述条件下进行试验。
007药用低密度聚乙烯膜、袋质量标准
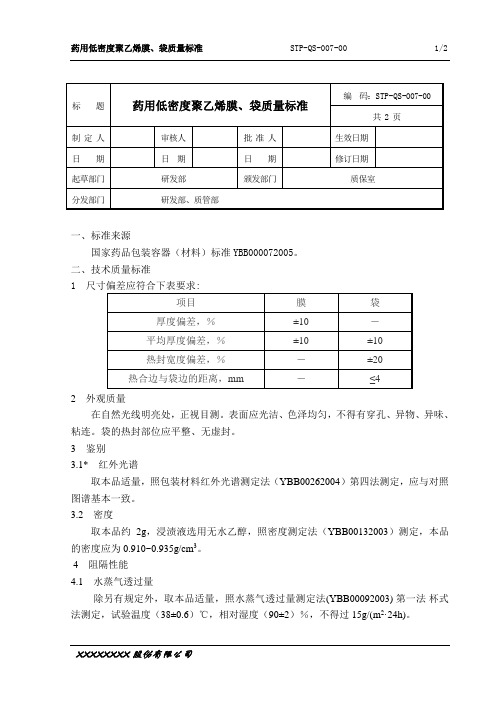
一、标准来源国家药品包装容器(材料)标准YBB000072005。
二、技术质量标准1 尺寸偏差应符合下表要求:2 外观质量在自然光线明亮处,正视目测。
表面应光洁、色泽均匀,不得有穿孔、异物、异味、粘连。
袋的热封部位应平整、无虚封。
3 鉴别3.1* 红外光谱取本品适量,照包装材料红外光谱测定法(YBB00262004)第四法测定,应与对照图谱基本一致。
3.2 密度取本品约2g,浸渍液选用无水乙醇,照密度测定法(YBB00132003)测定,本品的密度应为0.910~0.935g/cm3。
4 阻隔性能4.1 水蒸气透过量除另有规定外,取本品适量,照水蒸气透过量测定法(YBB00092003) 第一法杯式法测定,试验温度(38±0.6)℃,相对湿度(90±2)%,不得过15g/(m2·24h)。
4.2 氧气透过量除另有规定外,取本品适量,照气体透过量测定法 (YBB00082003) 第一法测定,试验温度(23±2)℃,不得过4000cm3/(m2·24h·0.1Mpa)。
5 机械性能5.1 拉伸强度取本品适量,照拉伸性能测定法(YBB00112003)测定,试验速度(空载):300mm/min±30mm/min,试样为Ⅰ型。
纵向、横向拉伸强度平均值均不得低于10MPa。
5.2 断裂伸长率取本品适量,照拉伸性能测定法(YBB00112003)测定,试验速度(空载):300mm/min±30mm/min,试样为Ⅰ型。
厚度小于0.05mm的膜,纵向、横向断裂伸长率平均值均不得低于130%;厚度大于0.05mm的膜,纵向、横向断裂伸长率平均值均不得低于200%。
6 热合强度6.1 膜除另有规定外,裁取100mm×100mm膜片四片,将任意两个膜片叠合,置热封仪上进行热合,热合温度130℃~150℃,压力0.2MPa,时间1秒。
药用低密度聚乙烯袋内控质量标准

药用低密度聚乙烯袋内控质量标准程
1. 目的:建立药用低密度聚乙烯袋内控质量标准,保证产品质量。
2. 应用范围:药用低密度聚乙烯袋的使用、采购和检验。
3. 责任人:采购部经理、采购员生、产部经理、生产管理员、质量部经理、质检中心主任、QA、QC
4.编制依据:
国家药品监督管理局国家药品包装容器(材料)标准(试行)YBB00072005 适用于以低密度聚乙烯树脂(LDPE)为主要原料采用流诞法、吹割法生产的药用薄膜,及2此薄膜通过热封制成的袋。
本品适用于非无菌固体原料药的包装。
内容:
5.质量标准
7.检验:按《药用低密度聚乙烯袋检验标准操作规程》进行检验。
8.用途:。
药用低密度聚乙烯袋质量标准

建立药用低密度聚乙烯袋的质量标准,以确保其质量。
2.
质量管理科、中心化验室、检验员。
4.
YBB00072005。
5.
物料编码:HB-02
限度要求:
项目
质量标准
规格尺寸
长度1050mm,偏差±15mm;宽度700mm,偏差±10mm;厚度0.08 mm,偏差±0.01mm。
外观
表面应光洁、色泽均匀,不得有穿孔、异物、异味、粘连。袋的热封部位应平整、无虚封。
炽灼残渣
不得过0.1%
重金属
不得过1ppm
易氧化物
二者消耗之差不得过1.5ml
不挥发物
与其空白残渣之差应不得过30.0mg
微生物限度
1.细菌数不得过1000个/100cm2;
2.霉菌、酵母菌数不得过100个/100cm2;
3.大肠埃希菌不得检出。
类别:药用内包材
贮存及注意事项:距热源不少于1米。
贮存期:二年。
用途:利福平内包装用。
检验操作规程编号:《ZL-SOP-059》
6.
编号
修订简述
生效日期
YBB00072005-2015药用低密度聚乙烯塑料膜、袋

药用低密度聚乙烯膜、袋Yaoyong Dimidu Jyixi Mo、DaiLDPE Films and Pouches for Pharmaceutical Packaging本标准适用于低密度聚乙烯树脂(LDPE)为主要原料采用流涎法、吹制法生产的药用薄膜,以及由此薄膜通过热封制成的袋。
本品适用于非无菌固体原料药的包装。
【外观】取本品适量,在自然光线明亮处,正视目测。
表面应光洁、色泽均匀,不得有穿孔、异物、异味、粘连。
袋的热封部位应平整、无虚封。
【鉴别】 *(1)红外光谱取本品适量,照包装材料红外光谱测定法(YBB00262004-2015)第四法测定,应与对照图谱基本一致。
(2)密度取本品约2g,浸渍液选用无水乙醇,照密度测定法(YBB00132003-2015)测定,本品的密度应为0.910~0.935g/cm3【阻隔性能】水蒸气透过量取本品适量,照水蒸气透过量测定法(YBB00092003-2015)第一法实验条件B测定,不得过15g/(m2*24h)。
氧气透过量取本品适量,照气体透过量测定法(YBB00082003-2015)第一法或第二法测定,不得过4000cm3/(m2*24h*0.1MPa)。
【机械性能】拉伸强度取本品适量,照拉伸性能测定法(YBB00112003-2015)测定,试验速度(空载):300mm/min±30mm/min,试样为Ⅰ型。
纵向、横向拉伸强度平均值均不得低于10MPa。
断裂拉伸率取本品适量,找拉伸性能测定法(YBB00112003-2015)测定,试验速度(空载):300mm/min±30mm/min,试样为Ⅰ型。
厚度小于等于0.05mm的膜,纵向、横向断裂拉伸长率平均值均不得低于130%;厚度大于0.05mm的膜,纵向、横向断裂拉伸长率平均值均不得低于200%。
【热合强度】(膜)截取100mm×100mm得膜片四片,将任意两个膜片叠合,置热封仪上进行热合,热合温度130~150℃,压力0.2MPa,时间1秒。
药品包装用复合膜质量标准
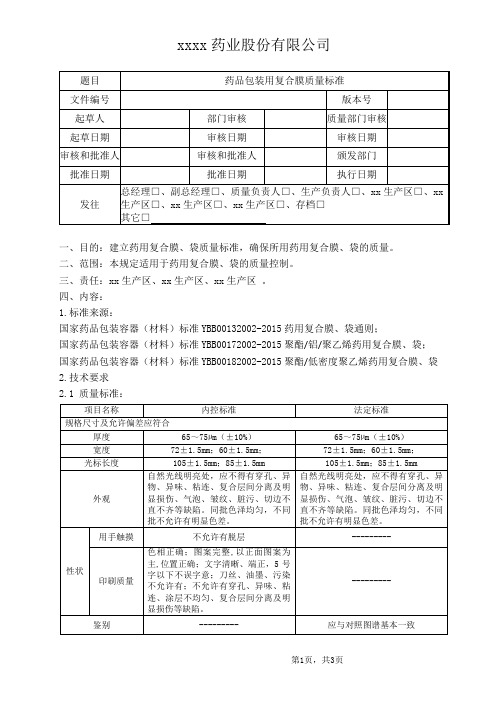
xxxx药业股份有限公司
一、目的:建立药用复合膜、袋质量标准,确保所用药用复合膜、袋的质量。
二、范围:本规定适用于药用复合膜、袋的质量控制。
三、责任:xx生产区、xx生产区、xx生产区。
四、内容:
1.标准来源:
国家药品包装容器(材料)标准YBB00132002-2015药用复合膜、袋通则;
国家药品包装容器(材料)标准YBB00172002-2015聚酯/铝/聚乙烯药用复合膜、袋;国家药品包装容器(材料)标准YBB00182002-2015聚酯/低密度聚乙烯药用复合膜、袋2.技术要求
2.1 质量标准:
2.2不同缺陷的允许限度:
3.贮存条件:用药用低密度聚乙烯袋密封,保存于清洁,通风处。
4.相关标准操作规程:药用复合膜、袋检验操作规程(SOP-ZL-JG(BC)-005)、物料取样标准操作规程(SOP-ZL-QA-001)。
5.企业统一指定的物料名称:药用复合膜、袋。
6.内部使用的物料代码:详见产品所对应的药用复合膜、袋物料代码。
7.经批准的供应商:见合格供应商目录。
8.印刷包装材料的实样或样稿:见包装材料样稿。
9.注意事项:标准中未明确的项目,以包材标准样张为准,每批产品需与标准样张进行核对。
10.复验期:执行“物料有效期及复验期管理规程(SMP-WL-008)”相关规定。
11.文件附件:共0份。
12.修订及变更历史:。
药用包装材料质量标准

(一)聚酯/铝/聚乙烯药品包装用复合膜、袋来源国家药品监督管理局YBB00172002本品系指聚酯(PET)与铝箔(Al)及聚乙烯(PE)通过黏合剂复合而成的膜。
本品的袋系将上述膜通过热合的方法制成。
本标准适用于固体药品包装用的复合膜、袋。
[外观]取本品适量,照药品包装用复合膜、袋通则(试行)(YBB00132002)外观项下的方法检查,应符合规定。
[鉴别]红外光谱取本品适量,采用内表面反射方法,照分光光度法(中华人民共和国药典2000年版附录ⅣC)测定,PET及PE层应分别与对照图谱基本一致。
[阻隔性能]水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GBl037-88)的规定进行。
试验时PE 层向湿度低的一侧,试验温度(38±2)℃,相对湿度(90±5)%,不得过0.5(g/m2·24h)。
氧气透过量照塑料薄膜和薄片气体透过性试验方法压差法(GB/T 1038-2000)的规定进行。
试验时PE层向氧气低压侧,试验温度为(23±2)℃,不得过0.5cm3/(m2·24h·0.1MPa)。
[机械性能] PE层与A1层剥离强度照药品包装用复合膜、袋通则(试行)(YBB00132002)内层与次内层剥离强度项下的方法检查,纵、横向剥高强度平均值均不得低于2.5N/15mm。
[热合强度]膜除另有规定外,裁取100mm×100mm试片四片,将任意两个试片PE面叠合,置热封仪上进行热合,热合温度150℃~170℃,压力0.2~0.3MPa,时间1秒。
从热合的中间部位各裁取3条15mm宽的试样,进行试验。
试样应在温度23℃±2℃,相对湿度50%±5%的环境中,放置4小时以上,并在上述条件下进行试验。
以热合部位为中心线,打开呈180度,把试样的两端夹在试验机的两个夹具上,试样轴线与上下夹具中心线相重合,并松紧适宜,夹具间距离为50mm,试验速度为(300±30)mm/min,读取试样断裂时的最大载荷,平均值不得低于12N/15mm。
药用低密度聚乙烯袋内控质量标准

药用低密度聚乙烯袋内控质量标准程
1. 目的:建立药用低密度聚乙烯袋内控质量标准,保证产品质量。
2. 应用范围:药用低密度聚乙烯袋的使用、采购和检验。
3. 责任人:采购部经理、采购员生、产部经理、生产管理员、质量部经理、质检中心主任、QA、QC
4.编制依据:
国家药品监督管理局国家药品包装容器(材料)标准(试行)YBB00072005 适用于以低密度聚乙烯树脂(LDPE)为主要原料采用流诞法、吹割法生产的药用薄膜,及2此薄膜通过热封制成的袋。
本品适用于非无菌固体原料药的包装。
内容:
5.质量标准
7.检验:按《药用低密度聚乙烯袋检验标准操作规程》进行检验。
8.用途:。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
低密度聚乙烯药用包装膜、袋质量标准
1 范围
Q/ T.03.07.001-2011.1适用于我公司所购低密度聚乙烯药用包装膜、袋的质量控制。
2 规范性引用文件
下列文件对于本文件的应用是必不可少的。
凡是注日期的引用文件,仅注日期的版本适用于本文件。
凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
本标准依据国家药包材质量标准YBB00072005《药用低密度聚乙烯膜、袋》制订
Q/ T.00.00.001 标准的结构与编写
Q/ M.12.06.010 质量标准编写要求
GB/T 2828.1-2003 逐批检查计数抽样程序及抽样表(适用于连续批的检查)
3 产品信息
3.1产品名称:低密度聚乙烯药用包装膜、袋
3.2 规格:袋
3.3 产品编码:见物料分类及编码管理规程
3.4 取样方法:Q/ M.12.03.010
3.5包装:内层:塑料袋,外层:瓦楞纸箱
3.6 贮藏:置通风干燥处
3.7 复验期:36个月
4 技术要求及检验方法
4.1 外观
取本品适量,在自然光线明亮处,正视目测。
表面应光洁、色泽均匀,不得有穿孔、异物、异味、粘连。
袋的热封部位应平整、无虚封。
4.2 水蒸气透过量
取本品适量,照水蒸气透过量测定法(YBB00092003)第一法(杯式法)测定,试验温度(38±0.6)℃,相对湿度(90±2)%,不得过15g/(m2·24h)。
4.3 氧气透过量
取本品适量,照气体透过量测定法(YBB00082003)第一法测定,试验温度(23±2)℃,不得过4000cm3/(m2·24h·0.1Mpa)。
4.4 拉伸强度
取本品适量,照拉伸性能测定法(YBB00112003)测定,试验速度(空载):300mm/min±30mm/min,纵向、横向拉伸长度平均值不得低于10Mpa。
4.5 热合强度
4.5.1 膜裁取100mm×100mm膜片四片,将任意两个膜片叠合,置热封仪上进行热合,热合温度130℃~150℃,压力0.2MPa,时间1秒。
照热合强度测定法(YBB00122003)测定,热合强度平均值不得低于7.0N/15mm。
4.5.2 袋从袋的热合强度部位裁取试样,照热合强度测定法(YBB00122003)测定,热合强度平均值不得低于7.0N/15mm。
4.6炽灼残渣
取本品5.0g精密称定,置于已恒重的坩锅,缓缓炽灼至完全炭化,再于550℃灼烧至恒重,遗留残渣不得过0.1%。
4.7溶出物试验
取样品适量,分别取本品内表面积600cm2(分割成长3cm,宽0.3cm的小片)三份置具塞锥形瓶中,加水(70℃±2℃)、65%乙醇(70℃±2℃)、正己烷(58℃±2℃)200ml浸泡2小时后取出,放冷至室温,
低密度聚乙烯药用包装膜、袋质量标准内部资料Q/T 03.07.001-2011.1
用同批试验用溶剂补充至原体积作为供试液,以同批水、65%乙醇、正己烷为空白液,备用。
重金属
精密量取水浸液20ml,加醋酸盐缓冲液(pH3.5) 2ml,依法检查(中华人民共和国药典2010年版二部附录Ⅷ H第一法),含重金属不得过百万分之一。
易氧化物
精密量取水浸液20ml,精密加入高锰酸钾滴定液(0.002mol/L)20ml与稀硫酸1ml,煮沸3分钟,迅速冷却,加入碘化钾0.1g,在暗处放置5分钟,用硫代硫酸钠滴定液(0.01mol/L)滴定,滴定至近终点时,加入淀粉指示液0.25ml,继续滴定至无色,另取水空白液同法操作,二者消耗滴定液之差不得过1.5 ml。
不挥发物
分别取水、65%乙醇、正己烷浸出液与空白液各100ml置于已恒重的蒸发皿中,水浴蒸干,105℃干燥2小时,冷却后精密称定,水不挥发物残渣与其空白残渣之差应不得过30.0 mg;65%乙醇不挥发物残渣与其空白残渣之差不得过30.0 mg;正己烷不挥发物残渣与其空白残渣之差不得过30.0 mg。
4.8 微生物限度
取试样用开孔面积为20cm2的消毒过的金属模板压在内层面上,将无菌棉签用氯化钠注射液稍沾湿,在板孔范围内擦抹5次,换1支棉签再擦抹5次,每个位置用2支棉签共擦抹10次,共擦抹5个位置100 cm2。
每支棉签抹完后立即剪断(或烧断),投入盛有30ml无菌生理水的锥型瓶(或大试管)中。
全部擦抹棉签投入瓶中后,将瓶迅速摇晃1分钟,即得供试液。
取提取液照微生物限度法(中华人民共和国药典2010年版二部附录Ⅺ J)测定。
细菌数不得过1000个/100cm2,霉菌、酵母菌数不得过100个/100cm2,大肠埃希菌不得检出。
4.9 异常毒性**
取试样500cm2,剪碎,加入氯化钠注射液50ml,110℃湿热灭菌30分钟后取出,冷却备用,静脉注射液,依法测定(中华人民共和国药典2010年版二部附录Ⅺ C),应符合规定。
5 检验规则
5.1 袋按逐批检查计数抽样程序及抽样表(GB/T2828.1-2003)规定进行。
检查水平、合格质量水平见表1 。
5.2 带“**”的项目,每年检验一次。
───────────────────────────────────────────────────
第2页共2页。
