钙钛矿结构大作业
钙钛矿太阳能电池构造

钙钛矿太阳能电池构造钙钛矿太阳能电池是一种新型的太阳能电池技术,具有高效能转化、低成本、易制备等优点,被广泛认为是未来太阳能电池的发展方向之一。
本文将从钙钛矿太阳能电池的构造、工作原理和应用前景等方面进行介绍。
一、钙钛矿太阳能电池的构造钙钛矿太阳能电池由多个层次的结构组成,主要包括透明导电玻璃基底、导电层、钙钛矿层、电解质层、电子传输层和反射层等。
其中,透明导电玻璃基底用于支撑电池结构并透过太阳光;导电层用于收集电荷并输送电流;钙钛矿层是光吸收层并产生电子和空穴对;电解质层用于电子和空穴的传输;电子传输层用于收集电子;反射层用于提高光的利用效率。
二、钙钛矿太阳能电池的工作原理钙钛矿太阳能电池的工作原理是基于光电效应。
当太阳光照射到钙钛矿层上时,光子的能量被转化为电子和空穴对。
这些电子和空穴对会在电场的作用下分离,电子被导电层收集,而空穴则由电解质层传输到反射层。
导电层和反射层之间形成了电势差,使电子在电子传输层中流动,从而产生电流。
这样,光能被转化为电能。
三、钙钛矿太阳能电池的应用前景由于钙钛矿太阳能电池具有高效能转化、低成本、易制备等优点,其在太阳能领域具有广阔的应用前景。
首先,钙钛矿太阳能电池的效率较高,已经超过了传统硅基太阳能电池,能够更有效地利用太阳能资源。
其次,钙钛矿太阳能电池的制备工艺相对简单,成本较低,有望实现大规模生产。
此外,钙钛矿材料可用于柔性电子器件的制备,有很大的应用潜力。
四、钙钛矿太阳能电池的挑战与改进方向尽管钙钛矿太阳能电池具有巨大的潜力,但其也面临一些挑战。
首先,钙钛矿材料对湿度和氧气敏感,对环境要求较高,稳定性有待提高。
其次,钙钛矿太阳能电池在长时间使用后会出现性能衰减,寿命仍然较短,需要进一步改进。
此外,钙钛矿材料中存在铅等有毒元素,对环境和人体健康造成一定的风险。
为了克服这些挑战,科研人员正在不断努力。
一方面,他们致力于改进钙钛矿材料的稳定性,寻找更稳定的替代材料,提高太阳能电池的使用寿命。
钙钛矿器件结构

钙钛矿器件结构钙钛矿(perovskite)是一种晶体结构,具有ABX3的化学式。
其中A、B、X分别代表阳离子、阳离子和阴离子。
钙钛矿具有较高的光吸收系数和载流子迁移率,因此被广泛应用于太阳能电池、光电探测器等器件中。
本文将介绍钙钛矿器件的结构。
一、钙钛矿太阳能电池结构钙钛矿太阳能电池是一种新型的高效能源转换器件。
其结构一般由透明导电玻璃基底、导电氧化物电极、钙钛矿吸收层、电子传输层和金属电极组成。
1. 透明导电玻璃基底:作为太阳能电池的底部支撑材料,具有高透明度和导电性,能够增强钙钛矿吸收层对光的吸收,并将光能转化为电能。
2. 导电氧化物电极:常用的导电氧化物有氧化锡(SnO2)等。
它具有良好的导电性和光透过性,能够提供电子传输通道,并且能够提高钙钛矿吸收层的稳定性。
3. 钙钛矿吸收层:钙钛矿吸收层是太阳能电池的关键部分,具有良好的光吸收性能和电子传输性能。
它通常由有机无机杂化钙钛矿材料制备而成,如CH3NH3PbI3等。
光照射到钙钛矿吸收层上时,光子被吸收后会激发出电子-空穴对,并通过电子传输层和导电氧化物电极流向外部电路。
4. 电子传输层:电子传输层常用的材料有二氧化钛(TiO2)等。
它具有良好的电子传输性能,能够有效地将钙钛矿吸收层中的电子输送到导电氧化物电极上。
5. 金属电极:金属电极通常由铝(Al)或银(Ag)等材料制成,用于收集电子并将其引出器件。
金属电极具有良好的导电性和稳定性。
二、钙钛矿光电探测器结构钙钛矿光电探测器是一种高灵敏度的光电转换器件,广泛应用于光通信、光传感等领域。
其结构一般由基底、阳极、钙钛矿吸收层和电子传输层组成。
1. 基底:基底一般由硅(Si)等材料制成,用于支撑器件结构并提供机械强度。
2. 阳极:阳极常用的材料有铂(Pt)等。
阳极具有良好的导电性,能够有效地收集光生电荷并将其引出器件。
3. 钙钛矿吸收层:钙钛矿吸收层用于吸收入射光并产生电子-空穴对。
光子被吸收后,会激发出电子-空穴对,并通过电子传输层和阳极流向外部电路。
钙钛矿结构大作业

钙钛矿结构大作业钙钛矿结构及其典型功能材料一.摘要。
介绍了钙钛矿结构的几何构型,并以一些典型的钙钛矿结构化合物为例阐述了其对理想结构的偏离往往会产生一些新的性能。
介绍了一些应用较广的钙钛矿材料,并对其结构与性能的关系进行了一些论述。
最后,简要介绍了它们的应用。
二.主要内容。
1.钙钛矿结构。
图1[1]钙钛矿最初是指CaTiO3,理想的钙钛矿结构属于立方晶系,空间群Pm3m,通式是ABO3,典型的晶胞如上图所示。
A位于立方体的8个角点上(图1(a))或立方体的体心(图1(b));而B则位于体心(图1(a))或立方体的8个角点上(图1(b));O位于6个面心(图1(a))或12个棱边的中点(图1(b))。
整个晶体可以看成由氧八面体共顶点连接形成,各氧八面体之间的空隙由A位原子占据,A和B的配位数分别是12和6。
共顶连接使氧八面体网络之间的空隙比共棱、共面连接时要大,允许较大尺寸离子填入,即使产生大量晶体缺陷,或者各组成离子的尺寸与几何学要求有较大出入时,仍然能够保持结构稳定;并有利于氧及缺陷的扩散迁移。
通常A离子比较大以便和O一起密堆积,B离子的半径要适合八面体配位。
三种离子半径满足以下关系:r A+r O=t?2(r B+r O),式中t为可变因子,在0.77~1.1范围时才以钙钛矿型存在,理想结构只在t接近1或高温情况下出现,多数结构是它的不同畸变形式,这些畸变结构在高温时转变为立方结构。
2.几种典型的钙钛矿结构功能材料。
理想的钙钛矿晶体是绝缘体,所有的格点均被占据并被强烈的离子键牢固地束缚在格点上,因此,它们十分坚硬,熔点高,也是各向同性的。
但是,对理想晶体结构的偏离产生的各种变体往往具有各向异性并伴随着新性能的出现。
其性能范围覆盖:铁电体、顺电体、压电体、反铁电体、绝缘体、半导体、快离子导体、金属导体和超导体。
1)BaTiO3的相变及压电、铁电材料常温下BaTiO3为四方相,但在降温过程中,其要发生立方-四方-斜方-三方的相变。
钙钛矿的晶体结构

钙钛矿的晶体结构钙钛矿是一种重要的无机化合物,其晶体结构具有特殊的性质和应用潜力。
本文将详细介绍钙钛矿的晶体结构,并探讨其物理和化学特性。
晶体结构概述钙钛矿是一类具有ABX3化学式的化合物,其中A和B是金属离子,X是阴离子。
典型的钙钛矿晶体结构由氧化物离子组成的立方晶格中,A位于晶格的正中心,B 位于晶格的顶点位置,X位于晶格的面心位置。
A位和B位的离子通常是正离子,它们的尺寸和电荷应当满足特定的条件,以保持整个晶体结构的稳定性。
X位的离子通常是负离子,如氧、氯等。
这种晶体结构的排列方式使得钙钛矿具有一定的稳定性和功能性。
钙钛矿的晶体结构特点钙钛矿的晶体结构具有以下几个重要特点:1. 高度对称性钙钛矿的晶体结构属于立方结构,具有高度的对称性。
其空间群一般为立方晶系或斜方晶系,如在立方晶系下的空间群有Pm-3m、Fm-3m等。
这种高度的对称性使得钙钛矿晶体具有一些特殊的物理和化学性质。
2. 离子间较短的键长由于钙钛矿晶体结构中A、B两种离子的尺寸适配和排列方式的密集性,导致A和B之间的键长相对较短。
这种较短的键长有助于增强钙钛矿的化学稳定性和电子传导性能。
3. 多样的金属氧配位数钙钛矿晶体结构中的B位金属离子通常具有多样的氧配位数。
这种多样性使得钙钛矿能够容纳多种离子,从而扩展了其应用领域。
4. 可控的晶体结构调控由于钙钛矿晶体结构的特殊性,我们能够通过不同的合成方法和控制条件来调控其晶体结构。
这种可控性为钙钛矿的制备和应用提供了更多可能性。
钙钛矿的物理和化学特性钙钛矿的晶体结构赋予其一些特殊的物理和化学特性,对于材料科学和能源领域有着重要的应用价值。
1. 铁电性和铁磁性钙钛矿中的部分化合物具有铁电性和铁磁性。
铁电性是指材料在外加电场作用下产生的电偶极矩,而铁磁性是指材料在外加磁场作用下表现出的磁性。
这些性质使得钙钛矿在信息存储和传感器等领域具有广泛的应用。
2. 光电性和光催化性钙钛矿中的部分化合物具有良好的光电性和光催化性能。
(完整版)钙钛矿结构示意图
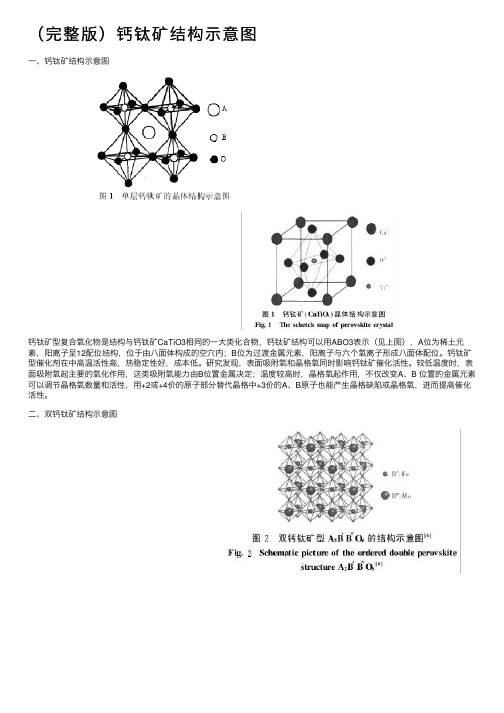
(完整版)钙钛矿结构⽰意图⼀、钙钛矿结构⽰意图钙钛矿型复合氧化物是结构与钙钛矿CaTiO3相同的⼀⼤类化合物,钙钛矿结构可以⽤ABO3表⽰(见上图),A位为稀⼟元素,阳离⼦呈12配位结构,位于由⼋⾯体构成的空⽳内;B位为过渡⾦属元素,阳离⼦与六个氧离⼦形成⼋⾯体配位。
钙钛矿型催化剂在中⾼温活性⾼,热稳定性好,成本低。
研究发现,表⾯吸附氧和晶格氧同时影响钙钛矿催化活性。
较低温度时,表⾯吸附氧起主要的氧化作⽤,这类吸附氧能⼒由B位置⾦属决定;温度较⾼时,晶格氧起作⽤,不仅改变A、B 位置的⾦属元素可以调节晶格氧数量和活性,⽤+2或+4价的原⼦部分替代晶格中+3价的A、B原⼦也能产⽣晶格缺陷或晶格氧,进⽽提⾼催化活性。
⼆、双钙钛矿结构⽰意图近年来,双钙钛矿型氧化物得到了越来越⼴泛的关注,双钙钛矿的通式可表⽰为A2B’B’’O6,标准的A2B’B’’O6型氧化物可以看作是由不同的BO6⼋⾯体规则的相间排列⽽成。
⼀般情况下B′和B″是不同的过渡⾦属离⼦,其晶体结构如图2所⽰。
A2B’B’’O6结构双层钙钛矿型复合氧化物呈NaCl型结构相见排列。
多数情况下双层钙钛矿氧化物结构也将发⽣畸变,它的结构⼀般由离⼦⼤⼩、电⼦组态和离⼦间相互作⽤等决定,⽽且双钙钛矿结构中B’O6和B’’O6⼋⾯体的稳定性对整个结构的稳定性起着很重要的作⽤,B′位、B″位离⼦相应的氧化物越稳定,则钙钛矿结构越稳定。
双钙钛矿型复合氧化物的制备近年已成为材料科学的重要发展⽅向。
从理论⾓度上看,双钙钛矿氧化物材料可以提供更加丰富的变换组合,给研究者提供了⼴阔的研究空间。
Sr2FeMoO6属于典型的A2B’B’’O6结构氧化物,其理想形式为Fe3+和Mo5+分别有序地占据B′和B″位置,FeO6⼋⾯体和MoO6⼋⾯体在三维空间以共⾓顶的⽅式相间排列组成三维框架,Sr2+则填充在由8个⼋⾯体所围成的空隙的中⼼位置,如上图所⽰。
实际上,由于占据A位、B′位及B″位的Sr2+、Fe3+、Mo5+并不是像标准⽴⽅双钙钛矿结构那样完全匹配,因此,在常温下其结构并⾮为⽴⽅对称,⽽是沿c轴⽅向有⼀个拉伸,畸变为四⽅对称结构。
钙钛矿电池结构

钙钛矿电池结构钙钛矿材料是近几年新兴的重要的储能材料。
它具有强烈的吸附性能和高耐蚀性,在储能领域具有广阔的潜力。
钙钛矿电池是一种新型钙钛矿电池,它利用钙钛矿材料作为电极材料,实现电池的蓄电功能。
钙钛矿电池结构主要由正极、负极和电解液三部分组成。
正极由复合钙钛矿材料(CaTiO3)和碳素材料组成,具有高耐蚀性,能从电解液中吸附有机物,在电解液中形成等离子体,使得电池的容量大大增加。
负极也利用钙钛矿材料,成分类似于正极电极材料;不同的是,它将金属钒(V)螯合在正的掺杂钒上,由于该材料的良好电学性能和超高的吸附力,使其具有较高的储能容量,可以将大部分外加的电流转换成化学能。
电解液大部分由水和有机溶液组成。
钙钛矿电池工作原理是,电解液将有机物流入正极电极材料等离子体中,形成燃料供给正极,正极电极材料产生放电反应,电解液中的金属钒被转化为钒酸,钒酸流入负极,由于负极材料的良好电学性能和超高的吸附力,使其能够将大多数电流转换成化学能,从而实现电池的蓄电功能。
钙钛矿电池的主要优势在于高自放电率,低充电损耗和高容量。
对于有机物质,它具有优良的吸附性能,能有效减少放电损失;而电池容量则比传统锂电池、钴酸锂电池更高,具有更好的储能性能。
除此之外,钙钛矿电池具有高安全性,可在较高温度下维持安全性。
它的安全极限温度为150℃,而其他传统储能电池的安全极限温度通常都要比它低得多。
因此,钙钛矿电池具有更高的操作安全性,可以在更高的温度下长时间运行,能有效延长电池的使用寿命。
总之,钙钛矿电池是一种新型储能电池,具有高自放电率、低充电损耗、高容量、高安全性等优点。
钙钛矿电池以其优良的性能和良好的应用前景,有望在实际应用中获得较为广泛的使用。
钙钛矿建模

利用第一性原理对甲胺碘铅进行结构模拟及性能研究目录摘要 (2)关键词 (2)一、绪论 (2)1.1钙钛矿太阳电池的结构与原理 (2)1.2CH3NH3PbX3钙钛矿的结构和性能 (3)1.3选题的意义 (4)二、CH3NH3PBI3钙钛矿结构的构建 (4)2.1CH3NH3PbI3钙钛矿的主要参数 (4)2.2建立几何模型 (5)2.2.1建立晶格 (5)2.2.2添加原子 (5)2.3利用Reflex模块进行粉末衍射图谱 (6)三、对晶体进行优化结构 (7)3.1结构优化 (7)3.1.1参数设置 (8)3.1.2运行结果显示 (8)3.2能量计算 (9)3.2.1参数设置 (9)3.2.2运行结构显示 (10)3.3计算结果分析 (11)四、CH3NH3PbI3钙钛矿几何结构延伸 (12)4.1Sn的掺杂对钙钛矿电池的能带结构的影响 (13)4.1.1Reflex粉末衍射图 (13)4.1.2几何优化 (14)4.1.3能量计算 (15)4.1.4计算结果分析 (16)4.2掺杂CH3NH3PbI3钙钛矿的几何机构及其分析 (17)4.2.1Reflex粉末衍射图 (18)4.2.2几何优化 (19)4.2.3能量计算 (19)4.2.4计算结果分析 (21)五、结论 (22)六、致谢 (22)参考文献 (22)摘要钙钛矿型甲胺碘铅薄膜太阳能电池因其结构简单、制备成本低廉等优点吸引了科研工作者的关注。
其光电转换效率在近5年内从3.8%迅速提高到15%以上,高于非晶硅的太阳电池效率,被Science评选为2013年十大科学突破之一。
本文主要是用Material Studio通过对CH3NH3PbI3钙钛矿建立晶体模型后,利用第一性原理对有机金属钙钛矿CH3NH3PbI3及其延伸结构进行结构模拟、能带分析和性能研究。
关键词:第一性原理 ; CH3NH3PbI3钙钛矿; 能带结构一、绪论1.1钙钛矿太阳电池的结构与原理钙钛矿是指CaTiO3,化学式是CaTiO3,是一种立方晶系的氧化物,是俄国化学家佩罗夫斯基发现的。
钙钛矿晶体结构

钙钛矿晶体结构
钙钛矿晶体结构是一类复杂的多相固体体系,也被称为带非晶-晶形态的压缩费米子
能带材料(CMR)。
这类体系具有特殊的结构特点,如其电容器、磁性和非线性电子性质。
从其结构上看,它包括三组元素:钙、钛和副元素。
其中,钙原子是体系中以六元组方式
排列的面心立方晶格;钛原子以宽带形式充满六元素单元;而副原子则穿插在两者之间。
这样,当外加外界施加电场、压力或温度等刺激时,从钙和钛间的局域电荷分布会发生变化,从而改变物质的共同特性。
钙钛矿晶体的核心特征在于原子(或分子)的相互作用,即交互耦合。
即使在体系中
钙和钛组成的面心立方晶格和副元素可能对原子间立体交互相当弱,但在整体结构上仍具
有特定的火焰反射和散射等结构性质,这就是什么它吸引了如此多研究者的原因。
另外,晶体的不断发展也为钙钛矿体系的研究提供了一些有趣而有用的物理效应,如
无紫外细节的传输,材料本身的热传播和精密的热传导,这些特性都使其成为制备功能材
料的理想基础。
在最近的研究中,基于不同形态的钙钛矿材料及其特性的研究和制备,为新一代复杂
体系及其功能性能开发提供了重要思路和创新空间,满足了用于多目标实际应用、新型电
子材料设计和宏观应用等方面的需求。
总的来说,钙钛矿晶体结构在研究方面处于前沿,其原子间的复杂相互作用为电子、光、磁、力学和机械等费米子效应研究带来了新的思路和可能性,从而发现复杂材料系统
中更多的新物性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
钙钛矿结构及其典型功能材料
一.摘要。
介绍了钙钛矿结构的几何构型,并以一些典型的钙钛矿结构化合物为例阐述了其对理想结构的偏离往往会产生一些新的性能。
介绍了一些应用较广的钙钛矿材料,并对其结构与性能的关系进行了一些论述。
最后,简要介绍了它们的应用。
二.主要内容。
1.钙钛矿结构。
图1[1]
钙钛矿最初是指CaTiO3,理想的钙钛矿结构属于立方晶系,空间群Pm3m,通式是ABO3,典型的晶胞如上图所示。
A位于立方体的8个角点上(图1(a))或立方体的体心(图1(b));而B则位于体心(图1(a))或立方体的8个角点上(图1(b));O位于6个面心(图1(a))或12个棱边的中点(图1(b))。
整个晶体可以看成由氧八面体共顶点连接形成,各氧八面体之间的空隙由A位原子占据,A和B的配位数分别是12和6。
共顶连接使氧八面体网络之间的空隙比共棱、共面连接时要大,允许较大尺寸离子填入,即使产生大量晶体缺陷,或者各组成离子的尺寸与几何学要求有较大出入时,仍然能够保持结构稳定;并有利于氧及缺陷的扩散迁移。
通常A离子比较大以便和O一起密堆积,B离子的半径要适合八面体配位。
三种离子半径满足以下关系:r A+r O=t•2(r B+r O),式中t为可变因子,在0.77~1.1范围时才以钙钛矿型存在,理想结构只在t接近1或高温情况下出现,多数结构是它的不同畸变形式,这些畸变结构在高温时转变为立方结构。
2.几种典型的钙钛矿结构功能材料。
理想的钙钛矿晶体是绝缘体,所有的格点均被占据并被强烈的离子键牢固地束缚在格点上,因此,它们十分坚硬,熔点高,也是各向同性的。
但是,对理想晶体结构的偏离产生的各种变体往往具有各向异性并伴随着新性能的出
现。
其性能范围覆盖:铁电体、顺电体、压电体、反铁电体、绝缘体、半导体、快离子导体、金属导体和超导体。
1)BaTiO3的相变及压电、铁电材料
常温下BaTiO3为四方相,但在降温过程中,其要发生立方-四方-斜方-三方的相变。
主要原因为A)Ti4+-O2-间距大(2.005A),故氧八面体间隙大,因而Ti4+离子能在氧八面体中震动。
B)降温过程中,Ti4+由于热涨落,偏离一方,结构发生畸变,使一些钙钛矿晶体结构中正、负电荷中心不重合,形成偶极矩,产生自发极化。
在一些钙钛矿ABO3型晶体中,在一定的温度下由于B离子半径较小会发生B、O离子的相互运动。
形成离子半径失配的变体,在外力或者外电场的作用下会产生铁电压电性能。
或者在离子取代过程中会产生一些偏离化学分子式的变体,改变其铁电压电性能。
通过置换掺杂发展了一系列钙钛矿结构压电陶瓷材料,主要代表如下:
Pb(Ti,Zr)O3 (PZT);
Pb(BⅡ1/3Nb2/3)O3(BⅡ=Mg、Co、Zn、Cd、Mn、Ni);
Pb(BⅢ1/2Nb1/2)O3(BⅢ=Sb、Y);
Pb(BⅡ1/2W1/2)O3(BⅡ= Mg、Co、Cd )
Pb(BⅡ1/2Te1/2)O3(BⅡ= Mg、Ni、Co、Mn);
Pb(BⅡ1/3Nb2/3)O3(BⅡ= Mn、Ni)
Pb(BⅢ1/2BⅤ1/2)O3(BⅡ= Fe、Cr;;BⅤ=Nb、Ta);
(Pb1-x La x)(Zr y T iz)1-x/4O3(PLZT) 图2[3]其在高密度信息存储、变压器、探测器、换能器、陶瓷滤波器,压力计等方面具有重要应用。
2)YBCO体系及高T C的超导体
自1986年,在La2-x Ba x CuO4[2]多相体系中发现超导现象至今,人们为开发它的实际应用进行了大量的研究工作。
其中YBCO系列超导体是高温超导材料中研究最多、应用最广的超导体之一,受到普遍关注。
YBa2Cu3O7 - x[3]也是钙钛矿结构,其结构如图2所示,晶胞由3个立方体组成,上、下立方体的体心位置由Ba离子占据,中间立方体的体心则由Y离子占据,而Cu离子占据立方体角点位置。
此时由于氧缺位,偏离化学配比,发生了Cu离子的变价,产生了Cu-O 四面体层状结构,产生了超导特性。
超导体在电力传输、高场磁体、磁悬浮列车、高速超导开关及超高速超导计算机等方面有重要应用,但今后研究不同的结构以提高超导体的临界温度,超导机理的研究仍是大家共同追寻的话题。
3)CMR材料[4]
所谓磁电阻效应就是物质在磁场作用下电阻率发生变化的现象。
而庞磁阻效应主要是指具有钙钛矿结构的混合价氧化物,如L a1-x Ca x MnO3,[R1-x A x MnO3 ,
R是La3+,Pr3+,Nd3+,Eu3+,(also Bi3+),A是Ca2+,Sr2+,Ba2+,(also Pb2+)]在外加磁场时,会发生顺磁-铁磁转变,其电阻率在T C快速下降的现象。
在L a1-x Ca x MnO3中,二价的Ca离子掺入A位置换3价La离子,导致氧空位的产生,引起氧八面体变形,Mn3+离子在八面体中的畸变使Mn-O键长不均匀,一边长一边短,在一个属于Mn3+占据的轨道和邻近Mn4+空轨道间产生强交换作用,导致面内形成铁磁性排列,而且电子从高自旋的Mn3+离子转移到邻近Mn4+离子。
因此这种材料不仅具有铁磁性,而且具有导电性。
磁电阻材料的应用主要有以下几个方面:巨磁电阻磁头、磁电阻随机存储器磁电阻传感器。
4)其它钙钛矿系功能材料[5]
a.在气体吸附方面,常用LaM03(M—Cr、Mn、Fe、Co、Ni)[6]钙钛矿化合物,合成B位缺陷的化合物,以改善其吸附性能。
b.在光催化方面,常通过对钙钛矿化合物的掺杂改性,以加大化合物的非计
量比,增加相应结构中氧空位的含量,提高钙钛矿的催化性能。
c.钙钛矿化合物在燃料电池、锂离子电池、气敏材料、非线性光学等方面也
有重要应用。
总之,我们可以通过对钙钛矿结构基本化学相进行正离子掺杂,使其产生正离子或负离子偏离化学计量、正离子构型畸变、混合价、晶体缺陷等从而出现一些新的性能,但今后我们还应加强对其结构和机理的深入研究,以便发展新型材料。
[7]
三.参考文献。
[1] Appl. Phys. Lett. Mater.: Special Topic on Perovskites (2014)
[2] Bednorz, J.G.; Müller, K.A.; Z. Phys. B, 1986, 64, 189
[3] Pissas, M.; Sanakis, Y.; Psycharis, V.; Simopoulos, A.; Devlin, E.; Ren, Z. A.; Shen, X.L.; Che,
G. C.; Zhao, Z. X. Superconductor Science & Technology 2008, 21
[4]J. Wang, et al., Science, 299, 1719 (2003); N. Hur, et al., Nature (London),429, 392 (2004); N. Hill and A. Filippetti, J. Magn. Magn. Mater., 242-245, 976 (2002);C. Ederer and N. A. Spaldin, “A new route to magnetic ferroelectrics”, Nature Mater.,3, 849 (2004); W. Eerenstein, N. D. Mathur & J. F. Scott, “Multiferroic andmagnetoelectric materials”, Nature (London), 442, 759 (2006); N. Hill, “Why Are Thereso Few Magnetic Ferroelectrics?”, J. Phys. Chem., B 104, 6694 (2000)
[5] Hwang D W,Cha K Y,Kim J,et a1.Ind Eng Chem Res,2003,42(6):1184;Rao C N R,Vidyasagar K,et a1.Indian J Chem Sect A,1984,23(A):265;杨秋华,傅希贤,王俊珍,等.催化学报,1999,20(5):521;桑丽霞,傅希贤,白树林,等.感光科学与光化学,2001,19(2):109
[6] Kremenic G,Nieto J M L,et a1.J Chem SOc Faraday Trans,1985,81:939
[7]高西汉.压电与声光[J].1994.04。
