钠镁铝铁及其化合物方程式和离子方程式锦集
高一上四大基本金属元素钠镁铝铁单质及其化合物化学和对应离子方程式总结
NO3- + 2+
Fe3+ + 3H2O
Fe(OH)3(胶体) + 3H+
Cl2 少量: 6FeBr2 + 3Cl2 == 2FeCl3 +4FeBr3 Cl2 过量:2FeBr2+ 3Cl2 == 2FeCl3 + 2Br2
2Fe2+ + Cl2 == 2Fe3+ + 2Cl2Fe2+ + 4Br- + 3Cl2 == 2Fe3+ + 2Br2 + 6Cl-
Al2O3+3H2SO4=Al2(SO4)3+3H2O Al2O3 + 6HCl == 2AlCl3 + 3H2O Al2O3 + 6H+ == 2Al3+ + 3H2O Al2O3+2NaOH=2NaAlO2+H2O Al2O3 + 2OH- == 2AlO2- + H2O AlCl3 + 4NaOH = NaAlO2+ 3NaCl +2H2O Al3+ + 4OH- == AlO2- + 2H2O NaAlO2 + 4HCl == AlCl3 + NaCl+2H2O AlO2- + 4H+ == Al3+ + 2H2O NaAlO2 + HCl + H2O == Al(OH)3↓+ NaCl AlO2- + H+ + H2O == Al(OH)3↓ 2NaAlO2 + CO2 + 3H2O ==2 Al(OH)3↓+ Na2CO3 2AlO2-+ CO2 + 3H2O ==2 Al(OH)3↓+ CO32NaAlO2 + CO2 + 2H2O == Al(OH)3↓+ NaHCO3 AlO2- + CO2 + 2H2O == Al(OH)3↓+HCO3AlCl3+3NaAlO2+ 6H2O=4Al(OH)3↓+3NaCl Al3+ + 3AlO2- + 6H2O== 4Al(OH)3↓
金属+非金属化学方程式整理(全)

金属+非金属化学方程式整理(全)-CAL-FENGHAI-(2020YEAR-YICAI)_JINGBIAN2金属化学方程式整理一、钠、镁、铝及其化合物1、 钠暴露在空气中4Na+O 2==2Na 2O ; 钠在空气中点燃:2Na+O 2 == Na 2O 22、 2Na+2H 2O==2NaOH +H 2↑3、 2Na+2HCl==2NaCl +H 2↑4、 钠投入硫酸铜溶液中:2Na+2H 2O==2NaOH +H 2 ↑ CuSO 4+2NaOH==Cu(OH)2↓+Na 2SO 4 总:2Na+2H 2O+CuSO 4== Cu(OH)2↓+Na 2SO 4 +H 2 ↑5、 Mg+2HCl==MgCl 2+H 2↑ ( Mg+2H +==Mg 2++H 2 ↑ ) 2Al+6HCl ==2AlCl 3+3H 2↑ ( 2Al+6H +==2Al 3++3H 2 ↑ )6、 2Al+2NaOH+2H 2O ==2NaAlO 2+3 H 2↑( 2Al+2OH -+2H 2O ==2AlO 2-+3 H 2↑ )7、 2Na 2O 2+2H 2O==4NaOH+O 2↑ ( 2Na 2O 2+2H 2O==4Na ++4OH -+O 2↑) 8、 2Na 2O 2+2CO 2==2Na 2CO 3+O 29、 Na 2O + 2HCl == 2NaCl + H 2O ( 说明Na 2O 是碱性氧化物 ) 10、2Na 2O 2 + 4HCl==4NaCl + 2H 2O + O 2↑ ( Na 2O 2不是碱性氧化物 ) 11、Na 2CO 3 + 2HCl == 2NaCl + H 2O + CO 2↑ ( CO 32- +2H + == H 2O + CO 2↑) 12、NaHCO 3 + HCl== NaCl + H 2O + CO 2↑ ( HCO 3- + H + == H 2O + CO 2↑) 13、2NaHCO 3= Na 2CO 3+H 2O+CO 2↑14、Al 2O 3 + 6HCl == 2AlCl 3 + 3H 2O ( Al 2O 3 + 6H +== 2Al 3++ 3H 2O ) 15、Al 2O 3 + 2NaOH = 2NaAlO 2 + H 2O ( Al 2O 3 + 2OH - ==2AlO 2- + H 2O ) 16、AlCl 3 + 3NH 3·H 2O== Al(OH)3↓+ 3NH 4Cl (实验室制氢氧化铝)Al 3++3NH 3· H 2O== Al(OH)3↓+3NH 4+17、Al(OH)3+3HCl==AlCl 3+3H 2O ( Al(OH)3+3H +== Al 3++3H 2O ) 18、Al(OH)3+NaOH==NaAlO 2+2H 2O ( Al(OH)3+OH - ==AlO 2-+2H 2O )△△△319、2Al(OH)3 == Al 2O 3+3H 2O 20、少量CO 2通入NaOH 溶液:2NaOH+ CO 2== Na 2CO 3+ H 2O ( 2OH -+ CO 2==CO 32-+ H 2O ) 21、足量CO 2通入NaOH 溶液:NaOH+ CO 2== NaHCO 3 ( OH -+ CO 2==HCO 3- ) 22、少量NaOH 加入AlCl 3溶液:AlCl 3+3NaOH== Al(OH)3↓+3NaCl ( Al 3++3OH - ==Al(OH)3↓ ) 23、足量NaOH 加入AlCl 3溶液:AlCl 3+4NaOH== NaAlO 2+3NaCl+2 H 2O ( Al 3++4OH - == AlO 2-+2H 2O ) 24、Na 2CO 3 与NaHCO 3相互转化Na 2CO 3+ H 2O+ CO 2==2NaHCO 3 (CO 32-+ H 2O+ CO 2== 2HCO 3-) NaHCO 3+NaOH== Na 2CO 3+ H 2O (HCO 3-+ OH - == CO 32-+ H 2O )25、氯碱工业(电解饱和食盐水):2NaCl +2 H 2O==== 2NaOH +H 2↑+Cl 2↑ 26、侯氏(侯德榜)制(纯)碱法(饱和食盐水中先通氨气,再通二氧化碳) ①NaCl +NH 3+H 2O+ CO 2==NaHCO 3↓+NH 4Cl ②2NaHCO 3=== Na 2CO 3+H 2O+CO 2↑ 二、铁及其化合物1、Fe+2HCl==FeCl 2+H 2↑ ( Fe +2H +=Fe 2++H 2↑) Fe+CuSO 4==FeSO 4+Cu ( Fe +Cu 2+=Fe 2++Cu )2、FeO+2HCl=FeCl 2 +H 2O ( FeO +2H +=Fe 2++H 2O )3、Fe 2O 3+6HCl=2FeCl 3 +3H 2O ( Fe 2O 3+6H +=2Fe 3++3H 2O )4、Fe 3O 4+8HCl=FeCl 2 +2FeCl 3+4H 2O ( Fe 3O 4+8H += Fe 2++2Fe 3++4H 2O )5、Fe 2? + 2OH ? = Fe(OH)2?6、Fe 3? + 3OH ? = Fe(OH)3?电解△47、4Fe(OH)2+O 2+2H 2O=4Fe(OH)3 (现象:白色沉淀迅速变成灰绿色,最后变为红褐色)8、2Fe(OH)3 == Fe 2O 3+3H 2O9、Fe(OH)2+2HCl=FeCl 2 +2H 2O ( Fe(OH)2 +2H +=Fe 2++2H 2O ) 10、Fe(OH)3+3HCl=FeCl 3+3H 2O ( Fe(OH)3 +3H +=Fe 3++3H 2O )11、Fe 3? +3SCN ?=Fe(SCN)3 (现象:溶液呈红色。
铁、钠、铝知识点和方程式总结

钠铝及重要化合物知识点小结(★为必背方程式)一、钠及其化合物(一)钠 Na1、单质钠的物理性质:钠质软、银白色、熔点低、密度比水的小但比煤油的大。
★2、单质钠的化学性质: ① 钠与O 2反应常温下:4Na + O 2=2Na 2O ★(新切开的钠放在空气中容易变暗)加热时:2Na + O 2==Na 2O 2 ★(钠先熔化后燃烧,发出黄色火焰,生成淡黄色固体Na 2O 2。
)钠在空气中的变化过程:Na ―→Na 2O ―→NaOH ―→Na 2CO 3·10H 2O (结晶)―→Na 2CO 3(风化),最终得到是一种白色粉末。
一小块钠置露在空气中的现象:银白色的钠很快变暗(生成Na 2O ),跟着变成白色固体(NaOH),然后在固体表面出现小液滴(NaOH 易潮解),最终变成白色粉未(最终产物是Na 2CO 3)。
② 钠与H 2O 反应2Na +2H 2O =2NaOH +H 2↑ ★离子方程式:2Na ++2H 2O =2Na ++2OH -+H 2↑(注意配平)实验现象:钠浮在水面上,熔成小球,在水面上游动,有哧哧的声音,最后消失,在反应后的溶液中滴加酚酞,溶液变红。
“浮——钠密度比水小;游——生成氢气;响——反应剧烈;熔——钠熔点低;红——生成的NaOH 遇酚酞变红”。
③ 钠与盐溶液反应如钠与CuSO 4溶液反应,应该先是钠与H 2O 反应生成NaOH 与H 2,再和CuSO 4溶液反应,有关化学方程式: 2Na +2H 2O =2NaOH +H 2↑ CuSO 4+2NaOH =Cu(OH)2↓+Na 2SO 4 总的方程式:2Na +2H 2O +CuSO 4=Cu(OH)2↓+Na 2SO 4+H 2↑实验现象:钠熔成小球,在液面上四处游动,有蓝色沉淀生成,有气泡放出K 、Ca 、Na 三种单质与盐溶液反应时,先与水反应生成相应的碱,碱再和盐溶液反应④ 钠与酸反应:2Na +2HCl =2NaCl +H 2↑(反应剧烈) 离子方程式:2Na +2H +=2Na ++H 2↑3、钠的存在:以化合态存在。
高三复习资料:铝、镁及其化合物方程式和离子方程式锦集

课前作业4:1.镁在空气中燃烧2Mg + O 2 2MgO 3Mg +N 2 Mg 3N 2 2Mg + CO 2 2MgO + C 2.镁能溶解在氯化铵溶液中Mg + 2NH 4Cl = MgCl 2 + H 2↑+ NH 3↑ Mg + 2NH 4+ = Mg 2+ + H 2↑+ NH 3↑3.铝是活泼金属,为什么可以直接存放在空气中,用简单的文字和方程式说明: 4Al+3O 2=2Al 2O 3 在铝的表面形成致密的氧化铝薄膜,将铝和空气隔绝。
4.铝与盐酸反应、铝与氢氧化钠溶液反应2Al+6HCl = 2AlCl 3+3H 2↑ 2Al+6H + = 2Al 3++3H 2↑2Al+2NaOH+2H 2O = 2NaAlO 2+3H 2↑ 2Al+2OH -+2H 2O =2AlO 2-+3H 2↑ 5.铝在高温条件下与氧化铁(或FeO 、Fe 3O 4、Fe 2O 3、MnO 2、Cr 2O 3)反应2Al +Fe 2O 3 Al 2O 3 + 2Fe 6.氧化铝分别与盐酸、氢氧化钠溶液反应Al 2O 3+6HCl =2AlCl 3+3H 2O Al 2O 3+6H +=2Al 3++3H 2OAl 2O 3+2NaOH =2NaAlO 2+H 2O Al 2O 3+2OH -=2AlO 2-+H 2O (一般金属氧化物都不与碱反应,Al 2O 3特别,应引起注意)课前作业5:1.氢氧化铝分别与盐酸、氢氧化钠溶液反应Al(OH)3+3HCl=AlCl 3+3H 2O Al(OH)3+3H +=Al ++3H 2OAl(OH)3+NaOH=NaAlO 2+2H 2O Al(OH)3+OH -=AlO 2-+2H 2O2.氯化铝(硫酸铝)溶液中加入少量(或过量)的氢氧化钠溶液少量NaOH :AlCl 3+3NaOH =Al(OH)3↓+3NaCl Al 3++3OH - =Al(OH)3↓ 过量NaOH :AlCl 3+4NaOH =NaAlO 2+3NaCl Al 3++4OH - =AlO 2-+2H 2O 3.氯化铝(硫酸铝)溶液中加入少量(或过量)的氨水AlCl 3+3NH 3·H 2O=Al(OH)3↓+3NH 4Cl Al 3++3NH 3·H 2O=Al(OH)3↓+3NH 4+ 4.偏铝酸钠溶液中加入少量(或过量)的盐酸 (Al(OH)3制备方法之一) 少量盐酸:NaAlO 2+HCl+H 2O =Al(OH)3↓+NaCl AlO 2-+H ++H 2O =Al(OH)3↓ 过量盐酸:NaAlO 2+4HCl =AlCl 3+NaCl+2H 2O AlO 2-+4H +=Al 3++2H 2O 5.偏铝酸钠溶液中通入少量(或过量)的二氧化碳 (Al(OH)3制备方法之一) 少量CO 2:2NaAlO 2+CO 2+3H 2O =2Al(OH)3↓+Na 2CO 32AlO 2-+CO 2+3H 2O =2Al(OH)3↓+CO 32-过量CO 2:NaAlO 2+CO 2+2H 2O =Al(OH)3↓+NaHCO 3AlO 2-+CO 2+2H 2O =Al(OH)3↓+HCO 3-6.氯化铝溶液和偏铝酸钠溶液(Al 3+与HCO 3-、CO 32-、S 2-、HS -) (Al(OH)3制备方法之一) AlCl 3 + 3NaAlO 2 + 6H 2O = 4 Al(OH)3↓+3NaCl Al 3++ 3AlO 2-+ 6H 2O = 4Al(OH)3↓ 其他双水解的方程式和离子方程式自己做!7.偏铝酸钠溶液和碳酸氢钠溶液混合NaAlO 2+NaHCO 3+H 2O =Al(OH)3↓+Na 2CO 3 AlO 2-+HCO 3-+H 2O =Al(OH)3↓+CO 32-8.用简单的文字说明和离子方程式描述明矾可以净水的理由 明矾溶于水后电离出Al 3+发生水解生成吸附性很强的Al(OH)3胶体,吸附杂质达到净水目的:Al 3++3H 2O Al(OH)3胶体+3H + 点燃 点燃 点燃 高温。
高中化学方程式钠铝,铁全部

钠及其化合物的化学方程式一、钠1、钠在氧气中燃烧:2Na+O2Na2O22、钠在氯气中燃烧:2Na+Cl22NaCl3、钠常温条件下和氧气反应:4Na+O22Na2O4、钠和硫共热:2Na+S Na2S5、钠和水反应:2Na+2H2O2NaOH+H2↑6、钠和稀盐酸反应:2Na+2HCl2NaCl+H2↑7、钠投入到硫酸铜溶液中:2Na+CuSO4+2H2O Na2SO4+Cu(OH)2↓+H2↑8、向氯化铝溶液中加入少量的钠:6Na+2AlCl3+6H2O6NaCl+2Al(OH)3↓+3H2↑9、向氯化铝溶液中加入足量的钠:4Na+AlCl3+2H2O NaAlO2+3NaCl+2H2↑10、钠在高温条件下与四氯化钛反应:4Na+TiCl44NaCl+Ti二、氧化钠1、氧化钠和水反应:Na2O+H2O=2NaOH2、氧化钠与二氧化碳反应:Na2O+CO2Na2CO33、氧化钠与盐酸反应:Na2O+2HCl2NaCl+H2O4、向硫酸铜溶液中加入氧化钠:Na2O+CuSO4+H2O Cu(OH)2↓+Na2SO45、向氯化铝溶液中加入少量的氧化钠:3Na2O+2AlCl3+3H2O2Al(OH)3↓+6NaCl6、向氯化铝溶液中加入足量的氧化钠:2Na2O+AlCl3NaAlO2+3NaCl三、过氧化钠1、过氧化钠与水反应:2Na2O2+2H2O4NaOH+O2↑2、过氧化钠与二氧化碳反应:2Na2O2+2CO22Na2CO3+O2↑3、过氧化钠与盐酸反应:2Na2O2+4HCl4NaCl+2H2O+O2↑4、向硫酸铜溶液中加入过氧化钠:2Na2O2+2CuSO4+2H2O===2Cu(OH)2↓+2Na2SO4+O2↑5、向氯化铝溶液中加入少量的过氧化钠:6Na2O2+4AlCl3+6H2O4Al(OH)3↓+12NaCl+3O2↑6、向氯化铝溶液中加过量的过氧化钠:2Na2O2+AlCl3+2H2O NaAlO2+3NaCl+O2↑7、过氧化钠与硫酸亚铁溶液反应:4Na2O2+4FeSO4+6H2O4Fe(OH)3↓+4Na2SO4+O2↑四、氢氧化钠1、铝与氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑2、氯气通入氢氧化钠溶液中:Cl2+2NaOH NaCl+NaClO+H2O3、氯气通入热的浓氢氧化钠溶液中:3Cl2+6NaOH5NaCl+NaClO3+3H2O4、硫和氢氧化钠溶液共热:3S+6NaOH2Na2S+Na2SO3+3H2O5、硅溶于氢氧化钠溶液中:Si+2NaOH+H2O Na2SiO3+2H2↑6、氧化铝溶于氢氧化钠溶液中:Al2O3+2NaOH2NaAlO2+H2O7、向氢氧化钠溶液中通入少量的二氧化碳:2NaOH+CO2Na2CO3+H2O8、向氢氧化钠溶液中通入过量的二氧化碳:NaOH+CO2NaHCO39、向氢氧化钠溶液中通入少量的二氧化硫:2NaOH+SO2Na2SO3+H2O10、向氢氧化钠溶液中通入过量的二氧化硫:NaOH+SO2NaHSO311、五氧化二磷与氢氧化钠溶液反应:P2O5+6NaOH2Na3PO4+3H2O12、二氧化氮和氢氧化钠溶液反应:2NO2+2NaOH NaNO2+NaNO3+H2O13、一氧化氮、二氧化氮和氢氧化钠溶液反应:NO+NO2+2NaOH2NaNO2+H2O14、将二氧化硅溶于氢氧化钠溶液中:2NaOH+SiO2Na2SiO3+H2O15、三氧化硫和氢氧化钠溶液反应:SO3+2NaOH Na2SO4+H2O16、盐酸和氢氧化钠溶液反应:HCl+NaOH NaCl+H2O17、醋酸和氢氧化钠溶液反应:CH3COOH+NaOH CH3COONa+H2O18、向氢氧化钠溶液中通入少量的硫化氢:H2S+2NaOH Na2S+2H2O19、向氢氧化钠溶液中通入足量的硫化氢:H2S+NaOH NaHS+H2O20、硫酸和氢氧化钠溶液反应:H2SO4+2NaOH Na2SO4+2H2O21、磷酸溶液氢氧化钠溶液反应:H3PO4+3NaOH Na3PO4+3H2O22、将氢氧化铝溶于氢氧化钠溶液中:Al(OH)3+NaOH NaAlO2+2H2O23、向硝酸银溶液中加入氢氧化钠溶液:AgNO3+NaOH AgOH ↓+NaNO324、向硫酸铜溶液中加入氢氧化钠溶液:CuSO4+2NaOH Na2SO4+Cu(OH)2↓25、向氯化铁溶液中加入氢氧化钠溶液:FeCl3+3NaOH Fe(OH)3↓+3NaCl26、向氯化铝溶液中加入少量氢氧化钠溶液:AlCl3+3NaOH Al(OH)3↓+3NaCl27、向氯化铝溶液中加入足量氢氧化钠溶液:AlCl3+4NaOH NaAlO2+3NaCl+2H2O28、向氯化铵溶液加入氢氧化钠溶液,加热:NH4Cl+NaOH NaCl+NH3↑+H2O29、向碳酸氢铵溶液中加入少量氢氧化钠溶液共热:NH4HCO3+NaOH NaHCO3+NH3↑+H2O30、向碳酸氢铵溶液中加入足量氢氧化钠溶液共热:NH4HCO3+2NaOH Na2CO3+NH3↑+2H2O31、碳酸氢钠溶液与氢氧化钠溶液混合:NaHCO3+NaOH Na2CO3+H2O32、向碳酸氢钙溶液中加入少量氢氧化钠溶液:Ca(HCO3)2+NaOH CaCO3↓+NaHCO3+H2O33、向碳酸氢钙溶液中加入过量氢氧化钠溶液:Ca(HCO3)2+2NaOH CaCO3↓+Na2CO3+2H2O34、向碳酸氢镁溶液中加入少量的氢氧化钠溶液:Mg(HCO3)2+2NaOH Mg(OH)2↓+2NaHCO335、向碳酸氢镁溶液中加入过量的氢氧化钠溶液:Mg(HCO3)2+4NaOH Mg(OH)2↓+Na2CO3+2H2O五、氯化钠1、氯化钠溶液与硝酸银溶液混合:NaCl+AgNO3AgCl↓+NaNO32、氯化钠固体和浓硫酸共热:NaCl+H2SO4Na2SO4+2HCl↑3、电解饱和的氯化钠溶液:2NaCl+2H2O2NaOH+H2↑+Cl2↑4、电解氯化钠的熔融液:2NaCl2Na+Cl2↑六、碳酸钠1、碳酸钠溶液与澄清石灰水反应:Na2CO3+Ca(OH)2CaCO3↓+2NaOH2、碳酸钠溶液与氯化钡溶液混合:Na2CO3+BaCl2BaCO3↓+2NaCl3、碳酸钠溶液呈碱性:Na2CO3+H2O NaHCO3+NaOH4、碳酸钠溶液滴入少量的盐酸:Na2CO3+HCl NaHCO3+NaCl5、碳酸钠溶液滴入足量的盐酸:Na2CO3+2HCl2NaCl+CO2↑+H2O6、碳酸钠溶液中加入醋酸:Na2CO3+2CH3COOH2CH3COONa+CO2↑+H2O7、碳酸钠溶液中通入二氧化碳气体:Na2CO3+CO2+H2O2NaHCO38、向饱和的碳酸钠溶液中通入二氧化碳气体:Na2CO3+CO2+H2O2NaHCO39、碳酸钠溶液与氯化铝溶液混合:3Na2CO3+2AlCl3+3H2O2Al(OH)3↓+6NaCl+3CO2↑10、碳酸钠溶液与氯化铁溶液混合:3Na2CO3+2FeCl3+3H2O2Fe(OH)3↓+6NaCl+3CO2↑七、碳酸氢钠1、碳酸氢钠溶液呈碱性:NaHCO3+H2O H2CO3+NaOH2、碳酸氢钠溶液滴入盐酸:NaHCO3+HCl NaCl+CO2↑+H2O3、碳酸氢钠溶液滴入醋酸:NaHCO3+CH3COOH CH3COONa+CO2↑+H2O4、碳酸氢钠溶液与氯化铝溶液混合:3NaHCO3+AlCl3Al(OH)3↓+3NaCl+3CO2↑5、碳酸氢钠溶液与氯化铁溶液混合:3NaHCO3+FeCl3Fe(OH)3↓+3NaCl+3CO2↑6、碳酸氢钠溶液与氢氧化钠溶液混合:NaHCO3+NaOH Na2CO3+H2O7、碳酸氢钠溶液中加入过量氢氧化钙溶液:NaHCO3+Ca(OH)2 =CaCO3↓+NaOH+H2O8、碳酸氢钠溶液中加入少量氢氧化钙溶液: 2NaHCO3+Ca(OH)2 =CaCO3↓+Na2CO3+2H2O9、碳酸氢钠受热分解:2NaHCO3Na2CO3+CO2↑+H2O铝及其化合物的化学方程式一、铝1、铝在氧气中燃烧:4Al+3O22Al2O32、铝在氯气中燃烧:2Al+3Cl22AlCl33、铝和硫共热:2Al +3S Al 2S 34、铝与稀硫酸反应:2Al +3H 2SO4Al 2(SO 4)3 +3H 2 ↑5、铝和氢氧化钠溶液反应:2Al +2NaOH +2H 2O2NaAlO 2+3H 2 ↑6、铝和浓硫酸共热:2Al +6H 2SO 4Al 2(SO 4)3 +3SO 2 ↑+6H 2O7、铝和浓硝酸共热:Al +6HNO 3Al(NO 3)3 +3NO 2 ↑+3H 2O8、铝和稀硝酸反应:Al +4HNO3Al(NO 3)3 +NO ↑+2H 2O8、铝和硝酸银溶液反应:Al +3AgNO3Al(NO 3)3 +3Ag 9、铝与硫酸铜溶液反应:2Al +3CuSO4Al 2(SO 4)3 +3Cu10、铝和氧化铁高温下反应:2Al +Fe 2O 3Al 2O 3+2Fe 11、铝和四氧化三铁高温共热:8Al +3Fe 3O 44Al 2O 3+9Fe 12、铝和氧化铜高温共热:2Al +3CuO Al 2O 3+3Cu 13、铝和二氧化锰高温共热:4Al +3MnO 22Al 2O 3+3Mn二、氧化铝1、氧化铝与稀硫酸反应:Al 2O 3+3H 2SO4Al 2(SO 4)3 +3H 2O2、氧化铝与氢氧化钠溶液反应:Al 2O 3+2NaOH 2NaAlO 2+H 2O3、电解氧化铝的熔融液:2Al 2O34Al +3O 2 ↑三、氢氧化铝1、氢氧化铝与稀硫酸反应:2Al(OH)3 +3H 2SO 4Al 2(SO 4)3 +6H 2O2、氢氧化铝与氢氧化钠溶液反应:Al(OH)3 +NaOHNaAlO 2+2H 2O3、加热氢氧化铝:2Al(OH)3 Al 2O 3+3H 2O四、硫酸铝1、硫酸铝溶液与氯化钡溶液混合:Al 2(SO 4)3 +3BaCl 22AlCl 3+3BaSO 4 ↓2、硫酸铝的水溶液呈酸性:Al 2(SO 4)3+6H 2O2Al(OH)3 +3H 2SO 43、硫酸铝溶液中加入少量的氢氧化钠溶液:Al 2(SO 4)3 +6NaOH 3Na 2SO 4+2Al(OH)3 ↓4、向硫酸铝溶液中加足量的氢氧化钠溶液:Al 2(SO 4)3 +8NaOH2NaAlO 2+3Na 2SO 4+4H 2O冰晶石电解5、向硫酸铝溶液中加入少量的氢氧化钡溶液:Al2(SO4)3+3Ba(OH)22Al(OH)3↓+3BaSO4↓6、向硫酸铝溶液中加入足量的氢氧化钡溶液:Al2(SO4)3+4Ba(OH)2Ba(AlO2)2+3BaSO4↓+4H2O7、向明矾溶液中加入少量的氢氧化钡溶液:3Ba(OH)2+2KAl(SO4)22Al(OH)3↓+3BaSO4↓+K2SO48、向明矾溶液中加入足量的氢氧化钡溶液:KAl(SO4)2+2Ba(OH)2KAlO2+2BaSO4↓+2H2O9、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO410、向硫酸铝溶液中加入碳酸钠溶液:Al2(SO4)3+3Na2CO3+3H2O2Al(OH)3↓+3Na2SO4+3CO2↑11、向硫酸铝溶液中加入碳酸氢钠溶液:Al2(SO4)3+6NaHCO32Al(OH)3↓+3Na2SO4+6CO2↑12、向硫酸铝溶液中加入硫化钠溶液:Al2(SO4)3+3Na2S+6H2O2Al(OH)3↓+3Na2SO4+3H2S ↑13、向硫酸铝溶液中加入硫氢化钠溶液:Al2(SO4)3+6NaHS+6H2O2Al(OH)3↓+3Na2SO4+6H2S ↑14、向硫酸铝溶液中加入硅酸钠溶液:Al2(SO4)3+3Na2SiO3+6H2O2Al(OH)3↓+3Na2SO4+3H2SiO3↓15、向硫酸铝溶液中加入偏铝酸钠溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O AI(OH)3+NaOH2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O Al(OH)3↓+NaCl↓3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl NaCl+AlCl3+2H2O4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O2Al(OH)3↓+Na2CO35、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O Al(OH)3+NaHCO36、向偏铝酸钠溶液中加入硫酸铝溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓7、向偏铝酸钠溶液中加氯化铵:NaAlO2+NH4Cl+H2O Al(OH)3↓+NaCl+NH3↑8、向偏铝酸钠溶液中加入氯化铁溶液:3NaAlO2+FeCl3+6H2O3Al(OH)3↓+Fe(OH)3↓+3NaCl铁及其化合物的化学方程式一、铁1、铁在氧气中燃烧:3Fe+2O2Fe3O42、铁在氯气中燃烧:2Fe+3Cl22FeCl33、常温条件下铁锈的形成:4Fe+3O2+2H2O2[Fe2O3·H2O]4、高温条件铁与氧气反应:2Fe+O22FeO5、铁和硫共热:Fe+S FeS6、铁与水蒸气在高温条件下反应:3Fe+4H2O Fe3O4+4H27、铁与稀硫酸反应:Fe+H2SO4FeSO4+H2↑8、少量的铁与浓硫酸共热:2Fe+6H2SO4Fe2(SO4)3+3SO2↑+6H2O9、过量的铁与浓硫酸共热:Fe+2H2SO4FeSO4+SO2↑+2H2O10、少量的铁与浓硝酸共热:Fe+6HNO3Fe(NO3)3+3NO2↑+3H2O11、过量的铁与浓硝酸共热:Fe+4HNO3Fe(NO3)2+2NO2↑+2H2O12、少量的铁与稀硝酸反应:Fe+4HNO3Fe(NO3)3+NO↑+2H2O13、过量的铁与稀硝酸反应: 3Fe+8HNO33Fe(NO3)2+2NO ↑+4H2O14、铁与硫酸铜溶液反应:Fe+CuSO4FeSO4+Cu15、铁与硝酸银溶液反应:Fe+2AgNO3Fe(NO3)2+2Ag16、铁与氯化铁溶液反应:Fe+2FeCl33FeCl2二、氧化亚铁1、氧化亚铁在空气中加热:6FeO+O22Fe3O42、氧化亚铁与一氧化碳高温反应:FeO+CO Fe+CO23、氧化亚铁与铝粉在高温下反应:3FeO+2Al Al2O3+3Fe4、氧化亚铁与稀硫酸反应:FeO+H2SO4FeSO4+H2O5、氧化亚铁与浓硫酸反应:2FeO+4H2SO4Fe2(SO4)3+SO2↑+4H2O6、氧化亚铁与浓硝酸反应:FeO+4HNO3Fe(NO3)3+NO2↑+2H2O7、氧化亚铁与稀硝酸反应:3FeO+10HNO33Fe(NO3)3+NO ↑+5H2O三、四氧化三铁1、四氧化三铁与铝粉高温下反应:8Al+3Fe3O44Al2O3+9Fe2、四氧化三铁与一氧化碳高温下反应:Fe3O4+4CO3Fe+4CO23、四氧化三铁溶于稀盐酸:Fe3O4+8HCl FeCl2+2FeCl3+4H2O4、四氧化三铁溶于浓硫酸:2Fe3O4+10H2SO43Fe2(SO4)3+SO2↑+10H2O5、四氧化三铁溶于浓硝酸:Fe3O4+10HNO33Fe(NO3)3+NO2↑+5H2O6、四氧化三铁溶于稀硝酸:3Fe3O4+28HNO39Fe(NO3)3+NO ↑+14H2O6、四氧化三铁溶于氢碘酸:Fe3O4+8HI3FeI2+I2+4H2O四、氧化铁1、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe2、一氧化碳和氧化铁高温下反应:Fe2O3+3CO2Fe+3CO23、氧化铁溶液稀盐酸:Fe2O3+6HCl2FeCl3+3H2O4、氧化铁与氢碘酸反应:Fe2O3+6HI2FeI2+I2+3H2O五、氢氧化亚铁1、氢氧化亚铁与稀硫酸反应:Fe(OH)2+H2SO4FeSO4+2H2O2、氢氧化亚铁与浓硫酸反应:2Fe(OH)2+4H2SO4Fe2(SO4)3+SO2↑+6H2O3、氢氧化亚铁与浓硝酸反应:Fe(OH)2+4HNO3Fe(NO3)3+NO2↑+3H2O4、氢氧化亚铁与稀硝酸反应:3Fe(OH)2+10HNO33Fe(NO3)3+NO↑+8H2O5、氢氧化亚铁在空气中被氧化:4Fe(OH)2+O2+2H2O4Fe(OH)36、氢氧化亚铁隔绝空气加热:Fe(OH)2FeO+H2O7、氢氧化亚铁在空气中加热:4Fe(OH)2+O22Fe2O3+4H2O六、氢氧化铁1、氢氧化铁与稀硫酸反应:2Fe(OH)3+3H2SO4Fe2(SO4)3+6H2O2、氢氧化铁溶于氢碘酸:2Fe(OH)3+6HI2FeI2+I2+6H2O3、加热氢氧化铁:2Fe(OH)3Fe2O3+3H2O七、氯化亚铁1、铝与氯化亚铁溶液反应:2Al+3FeCl22AlCl3+3Fe2、锌与氯化亚铁反应:Zn+FeCl2ZnCl2+Fe3、氯化亚铁暴露在空气中变质:12FeCl2+3O2+6H2O8FeCl3+4Fe(OH)3↓4、酸化的氯化亚铁溶液中通入氧气:4FeCl2+O2+4HCl4FeCl3+2H2O5、氯化亚铁溶液中通入氯气:2FeCl2+Cl22FeCl36、氯化亚铁溶液中加入溴水:6FeCl2+3Br24FeCl3+2FeBr37、氯化亚铁溶液呈酸性:FeCl2+2H2O Fe(OH)2+2HCl8、氯化亚铁溶液中加入氢氧化钠溶液:FeCl2+2NaOH Fe(OH)2↓+2NaCl9、氯化亚铁溶液中加入氨水:FeCl2+2NH3·H2O Fe(OH)2↓+2NH4Cl10、氯化亚铁溶液中加入偏铝酸钠溶液:FeCl2+2NaAlO2+4H2O Fe(OH)2↓+2Al(OH)3↓+2NaCl11、氯化亚铁溶液中加入硝酸银溶液:FeCl2+2AgNO3Fe(NO3)2+2AgCl↓12、氯化亚铁溶液中加入硫化钠溶液:FeCl2+Na2S FeS↓+2NaCl13、硫酸亚铁溶液与浓硫酸反应:2FeSO4+2H2SO4Fe2(SO4)3+SO2↑+2H2O14、硝酸亚铁溶液与浓硝酸反应:Fe(NO3)2+2HNO3Fe(NO3)3+NO2↑+H2O15、硝酸亚铁溶液与稀硝酸反应:3Fe(NO3)2+10HNO33Fe(NO3)3+NO ↑+5H2O16、酸化的氯化亚铁被过氧化氢所氧化:2FeCl2+H2O2+2HCl2FeCl3+2H2O17、过氧化钠与氯化亚铁溶液反应:4Na2O2+4FeCl2+6H2O4Fe(OH)3↓+8NaCl+O2↑18、次氯酸钠溶液与氯化亚铁溶液反应2FeCl2+5NaClO+5H2O2Fe(OH)3↓+5NaCl+4HClO八、氯化铁1、少量的锌和氯化铁溶液反应:Zn+2FeCl32FeCl2+ZnCl22、过量的锌与氯化铁溶液反应:3Zn+2FeCl33ZnCl2+2Fe3、铁与氯化铁溶液反应:Fe+2FeCl33FeCl24、铜和氯化铁溶液反应:Cu+2FeCl32FeCl2+CuCl25、向氯化铁溶液中通入二氧化硫:2FeCl3+SO2+2H2O2FeCl2+H2SO4+2HCl6、氯化铁溶液呈酸性:FeCl3+3H2O Fe(OH)3+3HCl7、氯化铁溶液中加入氢氧化钠溶液:FeCl3+3NaOH Fe(OH)3↓+3NaCl8、向氯化铁溶液中加入氨水:FeCl3+3NH3·H2O Fe(OH)3↓+3NH4Cl9、向氯化铁溶液中加入碳酸钠溶液:2FeCl3+3Na2CO3+3H2O2Fe(OH)3↓+6NaCl+3CO2↑10、向氯化铁溶液中加入碳酸氢钠溶液:FeCl3+3NaHCO3Fe(OH)3↓+3NaCl+3CO2↑11、向氯化铁溶液中加入偏铝酸钠溶液:FeCl3+3NaAlO2+6H2O Fe(OH)3↓+3Al(OH)3↓+3NaCl12、向氯化铁溶液中加入次氯酸钠溶液:FeCl3+3NaClO+3H2O Fe(OH)3↓+3NaCl+3HClO13、向氯化铁溶液中通入硫化氢:2FeCl3+H2S2FeCl2+S↓+2HCl14、向氯化铁溶液中加入氢碘酸:2FeCl3+2HI2FeCl2+I2+2HCl15、向氯化铁溶液中加入少量的硫化钠溶液:2FeCl3+Na2S2FeCl2+S↓+2NaCl16、向氯化铁溶液中加入过量的硫化钠溶液:2FeCl3+3Na2S2FeS↓+S↓+6NaCl17、氯化铁溶液与碘化钾溶液混合:2FeCl3+2KI2FeCl2+I2+2KCl18、氯化铁溶液与硝酸银溶液混合:FeCl3+3AgNO33AgCl↓+Fe(NO3)319、氯化铁溶液中加入硫氰化钾溶液:FeCl3+3KSCN Fe(SCN)3+3KCl20、氧化镁投入到氯化铁溶液中: 3MgO+2FeCl3+3H2O3MgCl2+2Fe(OH)321、氢氧化镁投入到氯化铁溶液中:3Mg(OH)2+2FeCl33MgCl2+2Fe(OH)3。
钠镁铝所有方程式总结【最全】

钠及其化合物的方程式总结一、Na 单质1、钠在空气中燃烧(黄色的火焰):2Na + O 2 Na 2O 22、钠块在空气中变暗 :4Na + O 2=2Na 2O3、Na 2O 在空气中加热(变黄):2Na 2O + O 2 2Na 2O 24、金属锂在空气中燃烧 :4Li + O 2 2Li 2O5、钠与水反应(浮、熔、游、响、红) 2Na + 2H 2O = 2NaOH + H 2 ↑ 2Na + 2H 2O = 2Na + + 2OH - + H 2 ↑ 二、Na 2O 、Na 2O 2的相关反应:1、碱性氧化物Na 2O 与水的反应 :Na 2O +H 2O =2NaOH2、过氧化钠与水的反应(放热反应、Na 2O 2是强氧化剂,可用于漂白) 2Na 2O 2 + 2H 2O = 4NaOH + O 2 ↑ 2Na 2O 2 + 2H 2O = 4Na ++ 4OH -+O 2↑3、碱性氧化物Na 2O 与CO 2的反应Na 2O + CO 2 = Na 2CO 34、过氧化钠可用在呼吸面具和潜水艇中作为氧气来源(供氧剂),原因是: 2Na 2O 2 + 2CO 2 = 2Na 2CO 3 + O 25、Na 2O + SO 2 = Na 2SO 3 Na 2O 2 + SO 2 = Na 2SO 46、Na 2O + 2HCl = 2NaCl + H 2O7、2Na 2O 2 +4HCl = 4NaCl + 2H 2O + O 2 ↑ 三、NaHCO 3与Na 2CO 31、小苏打受热分解: 2NaHCO 3Na 2CO 3 + H 2O +CO 2 ↑2、固体氢氧化钠和碳酸氢钠混合物在密闭容器中加热 NaHCO 3 + NaOHNa 2CO 3 + H 2O3、若是氢氧化钠和碳酸氢钠溶液中反应有离子方程式:NaHCO 3+NaOH = Na 2CO 3+H 2O HCO 3-+OH - = H 2O +CO 32- 4、向NaOH 溶液中通入少量CO 2 :2NaOH + CO 2 = Na 2CO 3 + H 2O△△△△5、继续通入过量CO2 :Na2CO3 + CO2 + H2O = 2 NaHCO3总反应方程式:NaOH + CO2 = NaHCO36、苏打(纯碱)与盐酸反应:①盐酸中滴加纯碱溶液Na2CO3+2HCl =2NaCl+H2O+CO2↑CO32-+2H+=H2O+CO2↑②纯碱溶液中滴加盐酸,至过量Na2CO3+HCl =NaHCO3+NaCl CO32-+H+=HCO3-NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+=H2O+CO2↑7、Na2CO3溶液、NaHCO3溶液与Ca(OH)2反应:Na2CO3+Ca(OH)2 =CaCO3↓+2NaOHNaHCO3+Ca(OH)2(多)=CaCO3↓+NaOH +H2O2NaHCO3+Ca(OH)2(少)=CaCO3↓+Na2CO3+2H2O8、Na2CO3溶液、NaHCO3溶液与CaCl2反应:Na2CO3+CaCl2 =CaCO3↓+2 Na ClNaHCO3溶液与CaCl2 不反应铝及其化合物的化学方程式和离子方程式一、铝1、铝在氧气中燃烧:4Al+3O22Al2O32、铝在氯气中燃烧:2Al+3Cl22AlCl33、铝和硫共热:2Al+3S Al2S34、铝与稀硫酸反应:2Al+3H2SO4Al2(SO4)3+3H2↑2Al+6H+2Al3++3H2↑5、铝和浓硫酸共热:2Al+6H2SO4Al2(SO4)3+3SO2↑+6H2O6、铝和氢氧化钠溶液反应:2Al+2NaOH+2H2O 2NaAlO2+3H2↑2Al+2OH-+2H2O 2AlO2-+3H2↑7、铝和浓硝酸共热:Al+6HNO3 Al(NO3)3+3NO2↑+3H2O Al+6H++3NO3-Al3++3NO2↑+3H2O8、铝和稀硝酸反应:Al+4HNO3Al(NO3)3+NO ↑+2H2O Al+4H++NO3-Al3++NO ↑+2H2O9、铝与硫酸铜溶液反应:2Al+3CuSO4Al2(SO4)3+3Cu 2Al+3Cu2+2Al3++3Cu10、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe11、铝和四氧化三铁高温共热:8Al+3Fe3O44Al2O3+9Fe12、铝和氧化铜高温共热:2Al+3CuO Al2O3+3Cu13、铝和二氧化锰高温共热:4Al+3MnO22Al2O3+3Mn二、氧化铝1、氧化铝与稀硫酸反应:Al2O3+3H2SO4 Al2(SO4)3+3H2O Al2O3+6H+2Al3++3H2O2、氧化铝与氢氧化钠溶液反应:Al2O3+2NaOH2NaAlO2+H2O Al2O3+2OH-2AlO2-+H2O3、电解氧化铝的熔融液:2Al 2O 3 4Al +3O 2↑三、氢氧化铝1、氢氧化铝与稀硫酸反应: 2Al(OH)3 +3H 2SO 4Al 2(SO 4)3 +6H 2O Al(OH)3 +3H +Al 3++3H 2O2、氢氧化铝与氢氧化钠溶液反应: Al(OH)3 +NaOHNaAlO 2+2H 2O Al(OH)3 +OH -AlO 2-+2H 2O3、加热氢氧化铝:2Al(OH)3 Al 2O 3+3H 2O四、硫酸铝1、硫酸铝溶液与氯化钡溶液混合: Al 2(SO 4)3 +3BaCl 22AlCl 3+3BaSO 4 ↓ SO 42-+Ba 2+BaSO 4 ↓2、硫酸铝的水溶液呈酸性: Al 2(SO 4)3+6H 2O2Al(OH)3 +3H 2SO 4 Al 3++3H 2OAl(OH)3 +3H +3、硫酸铝溶液中加入少量的氢氧化钠溶液: Al 2(SO 4)3 +6NaOH3Na 2SO 4+2Al(OH)3 ↓ Al 3++3OH-Al(OH)3 ↓4、向硫酸铝溶液中加足量的氢氧化钠溶液: Al 2(SO 4)3 +8NaOH2NaAlO 2+3Na 2SO 4+4H 2O Al 3++4OH -AlO 2-+2H 2O5、向硫酸铝溶液中加入少量的氢氧化钡溶液: Al 2(SO 4)3 +3Ba(OH)22Al(OH)3 ↓+3BaSO 4 ↓2Al 3++3SO 42-+3Ba 2++6OH -2Al(OH)3 ↓+3BaSO 4 ↓6、向硫酸铝溶液中加入足量的氢氧化钡溶液: Al 2(SO 4)3 +4Ba(OH)2Ba(AlO 2)2 +3BaSO 4 ↓+4H 2O2Al 3++3SO 42-+3Ba 2++8OH -2AlO 2-+3BaSO 4 ↓+4H 2O7、向明矾溶液中加入少量的氢氧化钡溶液: 3Ba(OH)2 +2KAl(SO 4)22Al(OH)3 ↓+3BaSO 4 ↓+K 2SO 43Ba 2++6OH -+2Al 3++3SO 42-3BaSO 4 ↓+2Al(OH)3 ↓冰晶石电解8、向明矾溶液中加入足量的氢氧化钡溶液:KAl(SO4)2+2Ba(OH)2KAlO2+2BaSO4↓+2H2OAl3++2SO42-+2Ba2++4OH-AlO2-+2BaSO4↓+2H2O9、向硫酸铝溶液中加入氨水:Al2(SO4)3+6NH3·H2O2Al(OH)3↓+3(NH4)2SO4Al3++3NH3·H2O Al(OH)3↓+3NH4+10、向硫酸铝溶液中加入碳酸钠溶液:Al2(SO4)3+3Na2CO3+3H2O2Al(OH)3↓+3Na2SO4+3CO2↑2Al3++3CO32-+3H2O2Al(OH)3↓+3CO2↑11、向硫酸铝溶液中加入碳酸氢钠溶液:Al2(SO4)3+6NaHCO32Al(OH)3↓+3Na2SO4+6CO2↑Al3++3HCO3-Al(OH)3↓+3CO2↑12、向硫酸铝溶液中加入硫化钠溶液:Al2(SO4)3+3Na2S+6H2O2Al(OH)3↓+3Na2SO4+3H2S ↑2Al3++3S2-+6H2O2Al(OH)3↓+3H2S ↑13、向硫酸铝溶液中加入硫氢化钠溶液:Al2(SO4)3+6NaHS+6H2O2Al(OH)3↓+3Na2SO4+6H2S ↑Al3++3HS-+3H2O Al(OH)3↓+3H2S ↑14、向硫酸铝溶液中加入硅酸钠溶液:Al2(SO4)3+3Na2SiO3+6H2O2Al(OH)3↓+3Na2SO4+3H2SiO3↓2Al3++3SiO32-+6H2O2Al(OH)3↓+3H2SiO3↓15、向硫酸铝溶液中加入偏铝酸钠溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O Al(OH)3+NaOH AlO2-+2H2O Al(OH)3+OH-2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O Al(OH)3↓+NaCl AlO2-+H++H2O Al(OH)3↓3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl NaCl+AlCl3+2H2O AlO2-+4H+Al3++2H2O4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O2Al(OH)3↓+Na2CO32AlO2-+CO2+3H2O2Al(OH)3↓+CO32-5、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O Al(OH)3+NaHCO3AlO2-+CO2+2H2O Al(OH)3+HCO3-6、向偏铝酸钠溶液中加入硫酸铝溶液:Al2(SO4)3+6NaAlO2+12H2O3Na2SO4+8Al(OH)3↓Al3++AlO2-+6H2O4Al(OH)3↓7、向偏铝酸钠溶液中加入氯化铵溶液:NaAlO2+NH4Cl+H2O Al(OH)3↓+NaCl+NH3↑AlO2-+NH4++H2O Al(OH)3↓+NH3↑8、向偏铝酸钠溶液中加入氯化铁溶液:3NaAlO2+FeCl3+6H2O3Al(OH)3↓+Fe(OH)3↓+3NaCl3AlO2-+Fe3++6H2O3Al(OH)3↓+Fe(OH)3↓铁及其化合物的化学方程式和离子方程式一、Fe单质1、铁在氧气中燃烧:3Fe+2O2Fe3O42、铁在氯气中燃烧:2Fe+3Cl22FeCl33、常温条件下铁锈的形成:4Fe+3O2+2H2O2[Fe2O3 ·H2O]4、高温条件铁与氧气(Fe过量)反应:2Fe+O22FeO5、铁和硫共热:Fe+S FeS6、铁与水蒸气在高温条件下反应:3Fe+4H2O Fe3O4+4H27、铁与稀硫酸反应:Fe+H2SO4FeSO4+H2 ↑ Fe+2H+Fe2++H2 ↑8、少量的铁与浓硫酸共热:2Fe+6H2SO4(浓) Fe2(SO4)3+3SO2 ↑+6H2O9、少量的铁与浓硝酸共热:Fe+6HNO3(浓) Fe(NO3)3+3NO2 ↑+3H2O Fe+6H++3NO3-Fe3++3NO2 ↑+3H2O10、少量的铁与稀硝酸反应:Fe+4HNO3Fe(NO3)3+NO↑ +2H2O Fe+4H++NO3-Fe3++NO ↑+2H2O11、过量的铁与稀硝酸反应:3Fe+8HNO33Fe(NO3)2+2NO ↑+4H2O 3Fe+8H++2NO3-3Fe2++2NO +4H2O12、铁与硫酸铜溶液反应:Fe+CuSO4FeSO4+Cu Fe+Cu2+Fe2++Cu13、铁与硝酸银溶液反应:Fe+2AgNO3Fe(NO3)2+2Ag Fe+2Ag+Fe2++2Ag14、铁与氯化铁溶液反应:Fe+2FeCl33FeCl2 Fe+2Fe3+3Fe2+二、氧化亚铁1、氧化亚铁在空气中加热:6FeO+O2 2Fe3O42、氧化亚铁与一氧化碳高温反应:FeO+CO Fe+CO23、氧化亚铁与铝粉在高温下反应:3FeO+2Al Al2O3+3Fe4、氧化亚铁与稀硫酸反应:FeO+H2SO4FeSO4+H2O FeO+2H+Fe2++H2O5、氧化亚铁与浓硫酸反应:2FeO+4H2SO4(浓)Fe2(SO4)3+SO2 ↑+4H2O6、氧化亚铁与浓硝酸反应:FeO+4HNO3(浓)Fe(NO3)3+NO2 ↑+2H2O FeO+4H++NO3-Fe3++NO2 ↑+2H2O7、氧化亚铁与稀硝酸反应:3FeO+10HNO33Fe(NO3)3+NO ↑+5H2O 3FeO+10H++NO3-3Fe3++NO ↑+5H2O三、四氧化三铁1、四氧化三铁与铝粉高温下反应:8Al+3Fe3O44Al2O3+9Fe2、四氧化三铁与一氧化碳高温下反应:Fe3O4+4CO3Fe+4CO23、四氧化三铁溶于稀盐酸:Fe3O4+8HCl FeCl2+2FeCl3+4H2O Fe3O4+8H+Fe2++2Fe3++4H2O4、四氧化三铁溶于浓硫酸:2Fe3O4+10H2SO4(浓)3Fe2(SO4)3+SO2 ↑+10H2O5、四氧化三铁溶于浓硝酸:Fe3O4+10HNO3(浓)3Fe(NO3)3+NO2 ↑+5H2OFe3O4+10H++NO3-3Fe3++NO↑ +5H2O6、四氧化三铁溶于稀硝酸:3Fe3O4+28HNO39Fe(NO3)3+NO ↑+14H2O3Fe3O4+28H++NO3-9Fe3++NO ↑+14H2O7、四氧化三铁溶于氢碘酸:Fe3O4+8HI3FeI2+I2+4H2O Fe3O4+8H+3Fe2++I2+4H2O四、氧化铁1、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe2、一氧化碳和氧化铁高温下反应:Fe2O3+3CO2Fe+3CO23、氧化铁溶液稀盐酸:Fe2O3+6HCl2FeCl3+3H2O Fe2O3+6H+2Fe3++3H2O4、氧化铁与氢碘酸反应:Fe2O3+6HI2FeI2+I2+3H2O Fe2O3+6H++2I-2Fe2++I2+3H2O五、氢氧化亚铁1、氢氧化亚铁与稀硫酸反应:Fe(OH)2+H2SO4FeSO4+2H2O Fe(OH)2+2H+Fe2++2H2O2、氢氧化亚铁与浓硫酸反应:2Fe(OH)2+4H2SO4(浓)Fe2(SO4)3+SO2 ↑+6H2O3、氢氧化亚铁与浓硝酸反应:Fe(OH)2+4HNO3(浓)Fe(NO3)3+NO2 ↑+3H2OFe(OH)2+4H++NO3-Fe3++NO2 ↑+3H2O4、氢氧化亚铁与稀硝酸反应:3Fe(OH)2+10HNO33Fe(NO3)3+NO↑ +8H2O3Fe(OH)2+10H++NO3-3Fe3++NO↑ +8H2O5、氢氧化亚铁在空气中被氧化:4Fe(OH)2+O2+2H2O4Fe(OH)36、氢氧化亚铁隔绝空气加热:Fe(OH)2FeO+H2O7、氢氧化亚铁在空气中加热:4Fe(OH)2+O22Fe2O3+4H2O六、氯化亚铁1、铝与氯化亚铁溶液反应:2Al+3FeCl22AlCl3+3Fe 2Al+3Fe2+2Al3++3Fe2、锌与氯化亚铁溶液反应:Zn+FeCl2ZnCl2+Fe Zn+Fe2+Zn2++Fe3、氯化亚铁暴露在空气中变质:12FeCl2+3O2+6H2O8FeCl3+4Fe(OH)3 ↓ 12Fe2++3O2+6H2O8Fe3++4Fe(OH)3 ↓4、酸化的氯化亚铁溶液中通入氧气:4FeCl2+O2+4HCl4FeCl3+2H2O 4Fe2++O2+4H+4Fe3++2H2O5、氯化亚铁溶液中通入氯气:2FeCl2+Cl22FeCl32Fe2++Cl22Fe3++2Cl-6、氯化亚铁溶液中加入溴水:6FeCl2+3Br24FeCl3+2FeBr32Fe2++Br22Fe3++2Br-7、氯化亚铁溶液呈酸性:FeCl2+2H2O Fe(OH)2+2HCl Fe2++2H2O Fe(OH)2+2H+8、氯化亚铁溶液中加入氢氧化钠溶液:FeCl2+2NaOH Fe(OH)2 ↓+2NaCl Fe2++2OH-Fe(OH)2 ↓9、氯化亚铁溶液中加入氨水:FeCl2+2NH3·H2O Fe(OH)2↓+2NH4Cl Fe2++2NH3·H2O Fe(OH)2↓+2NH4+10、氯化亚铁溶液中加入四羟基铝酸钠溶液:FeCl2+2Na[Al(OH)4] Fe(OH)2 ↓+2Al(OH)3 ↓+2NaClFe2++2[Al(OH)4]-+4H2O2Al(OH)3 ↓+Fe(OH)2 ↓11、氯化亚铁溶液中加入硝酸银溶液:FeCl2+2AgNO3Fe(NO3)2+2AgCl↓Ag++Cl-AgCl↓12、氯化亚铁溶液中加入硫化钠溶液:FeCl2+Na2S FeS↓+2NaCl Fe2++S2-FeS↓13、硫酸亚铁溶液与浓硫酸反应:2FeSO4+2H2SO4(浓)Fe2(SO4)3+SO2↑+2H2O14、硝酸亚铁溶液与浓硝酸反应:Fe(NO3)2+2HNO3(浓)Fe(NO3)3+NO2↑+H2OFe2++2H++NO3-Fe3++H2O+NO2↑15、硝酸亚铁溶液与稀硝酸反应:3Fe(NO3)2+10HNO33Fe(NO3)3+NO ↑+5H2O3Fe2++10H++NO3-3Fe3++NO↑ +5H2O16、酸化的氯化亚铁被过氧化氢所氧化:2FeCl2+H2O2+2HCl2FeCl3+2H2O 2Fe2++H2O2+2H+2Fe3++2H2O17、过氧化钠与氯化亚铁溶液反应:4Na2O2+4FeCl2+6H2O4Fe(OH)3 ↓+8NaCl+O2 ↑4Na2O2+4Fe2++6H2O4Fe(OH)3↓+8Na++O218、次氯酸钠溶液与氯化亚铁溶液反应2FeCl2+5NaClO+5H2O2Fe(OH)3↓+5NaCl+4HClO2Fe2++5ClO-+5H2O2Fe(OH)3↓+Cl-+4HClO19、硫酸酸化的酸性高锰酸钾与氯化亚铁溶液反应5FeCl2+KMnO4+4H2SO4=3FeCl3+Fe2(SO4)3+MnSO4 +KCl+4H2O5Fe2+ + MnO4- + 8H+ = 5Fe3+ + Mn2+ + 4H2O七、氯化铁1、少量的锌和氯化铁溶液反应:Zn+2FeCl32FeCl2+ZnCl2Zn+2Fe3+2Fe2++Zn2+2、过量的锌与氯化铁溶液反应:3Zn+2FeCl33ZnCl2+2Fe 3Zn+2Fe 3+3Zn 2++2Fe3、铁与氯化铁溶液反应:Fe +2FeCl 33FeCl2Fe+2Fe3+3Fe2+4、铜和氯化铁溶液反应:Cu+2FeCl32FeCl2+CuCl2Cu+2Fe3+2Fe2++Cu2+5、向氯化铁溶液中通入二氧化硫:2FeCl3+SO2+2H2O2FeCl2+H2SO4+2HCl2Fe3++SO2+2H2O2Fe2++4H++SO42-6、氯化铁溶液呈酸性:FeCl3+3H2O Fe(OH)3+3HCl Fe3++3H2O Fe(OH)3+3H+7、氯化铁溶液中加入氢氧化钠溶液:FeCl3+3NaOH Fe(OH)3↓+3NaCl Fe3++3OH-Fe(OH)3↓8、向氯化铁溶液中加入氨水:FeCl3+3NH3·H2O Fe(OH)3↓+3NH4Cl Fe3++3NH3·H2O Fe(OH)3↓+3NH4+9、向氯化铁溶液中加入碳酸钠溶液:2FeCl3+3Na2CO3+3H2O2Fe(OH)3↓+6NaCl+3CO2↑2Fe3++3CO32-+3H2O2Fe(OH)3↓+3CO2↑10、向氯化铁溶液中加入碳酸氢钠溶液:FeCl3+3NaHCO3Fe(OH)3↓+3NaCl+3CO2↑Fe3++3HCO3-2Fe(OH)3↓+3CO2↑11、向氯化铁溶液中加入四羟基合氯酸钠溶液:FeCl3+3Na[Al(OH)4] Fe(OH)3↓+3Al(OH)3↓+3NaClFe3++3[Al(OH)4]-Fe(OH)3↓+3Al(OH)3↓12、向氯化铁溶液中加入次氯酸钠溶液:FeCl3+3NaClO+3H2O Fe(OH)3↓+3NaCl+3HClOFe3++3ClO-+3H2O Fe(OH)3↓+3HClO13、向氯化铁溶液中通入硫化氢:2FeCl3+H2S2FeCl2+S↓ +2HCl 2Fe 3++H 2S 2Fe 2++S ↓+2H +14、向氯化铁溶液中加入氢碘酸:2FeCl3+2HI2FeCl2+I2+2HCl 2Fe3++2I-2Fe2++I215、向氯化铁溶液中加入少量的硫化钠溶液:2FeCl3+Na2S2FeCl2+S↓ +2NaCl 2Fe3++S2-2Fe2++S ↓16、向氯化铁溶液中加入过量的硫化钠溶液:2FeCl3+3Na2S2FeS↓+S↓ +6NaCl 2Fe3++3S2-2FeS+S ↓17、氯化铁溶液与碘化钾溶液混合:2FeCl3+2KI2FeCl2+I2+2KCl 2Fe3++2I-2Fe2++I218、氯化铁溶液与硝酸银溶液混合:FeCl3+3AgNO33AgCl↓ +Fe(NO3)3Ag++Cl-AgCl↓19、氯化铁溶液中加入硫氰化钾溶液:FeCl3+3KSCN Fe(SCN)3+3KCl Fe3++3SCN-Fe(SCN) 320、氧化镁投入到氯化铁溶液中:3MgO+2FeCl3+3H2O3MgCl2+2Fe(OH)33MgO+2Fe3++3H2O3Mg2++2Fe(OH)3。
高中化学必修1金属部分化学方程式和离子方程式总结

金属及其化合物的相关化学方程式和离子方程式1、钠及其化合物的转化关系①Na 2O +2HCl=2NaCl +H 2O ; Na 2O +2H +=2Na ++H 2O ;②2Na +2HCl=2NaCl +H 2↑; 2Na +2H +=2Na ++H 2↑;或2Na +Cl 2 === 2NaCl ③2Na 2O 2+4HCl=4NaCl +O 2↑+2H 2O ;2Na 2O 2+4H +=4Na ++O 2↑+2H 2O ④ 4Na +O 2=2Na 2O ; ⑤2Na +O 22O 2; ⑥2Na +2H 2O=2NaOH +H 2↑;2Na +2H 2O=2Na ++2OH -+H 2↑ ⑦Na 2O +H 2O=2NaOH ; Na 2O +H 2O=2Na ++2OH -⑧2Na 2O 2+2H 2O=4NaOH +O 2↑; 2Na 2O 2+2H 2O=4Na ++4OH -+O 2↑ ⑨Na 2O +CO 2=Na 2CO 3 ⑩2Na 2O 2+2CO 2=2Na 2CO 3+O 2 ⑾2NaOH +CO 2=Na 2CO 3+H 2O ; 2OH -+CO 2=CO 32-+H 2O ⑿Na 2CO 3+Ca(OH)2=CaCO 3↓+2NaOH ; CO 32-+Ca 2+=CaCO 3↓ ⒀NaOH +CO 2=NaHCO 3 ; OH -+CO 2=HCO 3- ⒁Na 2CO 3+H 2O +CO 2=2NaHCO 3;CO 32-+H 2O +CO 2=2HCO 3-;或 Na 2CO 3+HCl=NaCl+NaHCO 3; CO 32-+H +=HCO 3-(15)2NaHCO 3△Na 2CO 3+H 2O+CO 2↑或NaHCO 3+NaOH=Na 2CO 3+H 2O ;HCO 3-+OH -=CO 32-+H 2O或Ca(OH)2+2NaHCO 3=CaCO 3↓+Na 2CO 3+2H 2O; Ca 2++2OH -+2HCO 3-=CaCO 3↓+CO 32-+2H 2O ⒃Na 2CO 3+2HCl=2NaCl +H 2O +CO 2↑; CO 32-+2H +=H 2O +CO 2↑ ⒄NaHCO 3+HCl=NaCl +H 2O +CO 2↑; HCO 3-+H +=H 2O +CO 2↑(18) Ca(OH)2+NaHCO 3=CaCO 3↓+NaOH +H 2O; Ca 2++OH -+HCO 3-=CaCO 3↓+H 2O 2、铝及其化合物的转化关系①2Al +6HCl=2AlCl 3+3H 2↑; 2Al +6H +=2Al 3++3H 2↑或2Al +3Cl 2 === 2AlCl 3②4Al+3O 2 △═2Al 2O 3; ③2Al+2NaOH+2H 2O=2NaAlO 2+3H 2↑;2Al+2OH -+2H 2O=2AlO 2-+3H 2↑NaCl Na NaOH Na 2Na 2① ② ③ ⑤⑾ ⑿ ⒁ ⒂④点燃△2O 3 A l (O H )3 KAl(SO 4)22AlCl 3④ ⑤⑥⑦⑧ ⑨⑩⑾点燃④Al 2O 3+6HCl=2AlCl 3+3H 2O ; Al 2O 3+6H +=2Al 3++3H 2O ⑤Al 2O 3+2NaOH=2NaAlO 2+H 2O ; Al 2O 3+2OH -=2AlO 2-+H 2O⑥AlCl 3+3NH 3·H 2O=Al(OH)3↓+3NH 4Cl ; Al 3++3NH 3·H 2O = Al(OH)3↓+3NH 4+或AlCl 3 + 3 NaOH(适量) = Al(OH)3↓ + 3NaCl ; Al 3++3OH -= Al(OH)3↓⑦Al(OH)3+3HCl=AlCl 3+3H 2O ; Al(OH)3+3H +=Al 3++3H 2O ⑧Al(OH)3 △═ Al 2O 3 + 3H 2O ⑨NaAlO 2+HCl (少)+H 2O =Al(OH)3↓+NaCl ;AlO 2-+H ++H 2O=Al(OH)3↓或NaAlO 2+2H 2O +CO 2(足)=Al(OH)3↓+NaHCO 3; AlO 2-+2H 2O +CO 2=Al(OH)3↓+HCO 3-或2NaAlO 2+3H 2O+CO 2(少)=2Al(OH)3↓+Na 2CO 3; 2AlO 2-+3H 2O+CO 2=2Al(OH)3↓+CO 32-⑩Al(OH)3+NaOH = NaAlO 2+2H 2O ; Al(OH)3+OH -= AlO 2-+2H 2O ⑾明矾净水:Al 3++3H 2OAl(OH)3胶体+3H +⑿AlCl 3+4NaOH = NaAlO 2+3NaCl +2H 2O ; Al 3++4OH -= AlO 2-+2H 2O (13) NaAlO 2+4HCl(足)= NaCl+ AlCl 3+2H 2O ; AlO 2-+4H += Al 3++2H 2O 3、铁及其化合物的转化关系①Fe 3O 4+4CO===3Fe +4CO 2 (C 、H 2、Al 都可反应)②Fe 3O 4+8HCl=2FeCl 3+FeCl 2+4H 2O; Fe 3O 4+8H +=2Fe 3++Fe 2++4H 2O③ 3Fe +4H 2O(g) △═ Fe 3O 4+4H 2;或3Fe +2O 2===Fe 3O 4④Fe +2HCl=FeCl 2+H 2↑; Fe +2H +=Fe 2++H 2↑或Fe +2FeCl 3 = 3FeCl 2;Fe +2Fe 3+= 3Fe 2+⑤2Fe +3Cl 2 == =2FeCl 3; ⑥2FeCl 2+Cl 2 = 2FeCl 3 ;2Fe 2++Cl 2=2Fe 3++2Cl—⑦Fe +2FeCl 3 = 3FeCl 2;Fe +2Fe 3+= 3Fe 2+或Cu +2FeCl 3 = 2FeCl 2+CuCl 2; Cu +2Fe 3+= 2Fe 2++Cu 2+或2KI +2FeCl 3 = 2FeCl 2+I 2+2KCl; 2I —+2Fe 3+= 2Fe 2++I 2 ⑧FeCl 2+2NaOH = Fe(OH)2↓+2NaCl ;Fe 2++2OH -= Fe(OH)2↓ ⑨Fe(OH)2+2HCl = FeCl 2+2H 2O ; Fe(OH)2+2H += Fe 2++2H 2O⑩4Fe(OH)2+O 2+2H 2O = 4Fe(OH)3 ;白色沉淀迅速变成灰绿色,最后变成红褐色 ⑾FeCl 3+3NaOH=Fe(OH)3↓+3NaCl; Fe 3++3OH -=Fe(OH)3↓;Fe 3++3H 2O Fe(OH)3胶体+3H +(净水)(12)Fe(OH)3+3HCl = FeCl 3+3H 2O; Fe(OH)3+3H += Fe 3++3H 2O(13)2Fe(OH)3 △═Fe 2O 3+3H 2O (14)Fe 2O 3+6HCl=2FeCl 3+3H 2O; Fe 2O 3+6H +=2Fe 3++3H 2O (15) Fe 2O 3+ 3CO == 2Fe +3CO 2(高炉炼铁);(还可与C 、H 2、Al 反应) (16)FeCl 3+3KSCN = Fe(SCN)3+3KCl; Fe 3++3SCN -= Fe(SCN)3FeCl 2 3 2O 3 ①③ ⑧ ⑨ ⑿点燃 点燃高温4、硅及其化合物的转化关系①Si +O 2 △SiO 2②SiO 2+2C 高温 Si +2CO ↑ ※③SiO 2+4HF = SiF 4↑+2H 2O (刻蚀玻璃)④Si +4HF = SiF 4↑+2H 2↑ ⑤SiO 2+CaO 高温CaSiO 3 ※⑥SiO 2+2NaOH = Na 2SiO 3+H 2O SiO 2+CaCO 3高温CaSiO 3+CO 2↑SiO 2+2OH -= SiO 32-+H 2O ※⑦Na 2SiO 3+2HCl = H 2SiO 3↓+2NaCl SiO 2+Na 2CO 3高温Na 2SiO 3+CO 2↑ SiO 32-+2H += H 2SiO 3↓※⑦Na 2SiO 3+H 2O +CO 2=H 2SiO 3↓+Na 2CO 3或Na 2SiO 3+2H 2O +2CO 2=H 2SiO 3↓+2NaHCO 3 SiO 32-+H 2O +CO 2=H 2SiO 3↓+CO 32-或SiO 32-+2H 2O +2CO 2=H 2SiO 3↓+2HCO 3-⑧H 2SiO 3+2NaOH = Na 2SiO 3+2H 2O ⑨H 2SiO 3 △H 2O +SiO 2H 2SiO 3+2OH -= SiO 32-+2H 2O 5、氯及其化合物的转化关系①2Fe +3Cl 2 点燃2FeCl 3②Cu +Cl 2 点燃CuCl 2 ③2FeCl 3+Cu = 2FeCl 2+CuCl 2 2Fe 3++Cu = 2Fe 2++Cu 2+④H 2+Cl 2 2HCl ※⑤MnO 2+4HCl(浓) △MnCl 2+Cl 2↑+2H 2OMnO 2+4H ++2Cl- △2++Cl 2↑+2H 2ONa 2SiO 3 SiF 4Si SiO 2 H 2SiO 3 CaSiO 3① ②③ ④ ⑤ ⑥ ⑦ ⑧ ⑨ CuCl 2 HClO HCl Cl 2 FeCl 3 NaClOCa(ClO)2① ② ③ ④⑤ ⑥ ⑦ ⑧⑨ ⑩ 点燃 或光照 光照※⑥Cl2+H2O = HCl+HClO ※⑦2HClO 2HCl+O2↑光照Cl2+H2O = H++Cl-+HClO 2HClO 2H++2Cl-+O2↑※⑧Cl2+2NaOH = NaCl+NaClO+H2O ※⑨2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O Cl2+2OH-= Cl-+ClO-+H2O 工业制漂白粉※⑩Ca(ClO)2+H2O+CO2 = CaCO3↓+2HClO或Ca(ClO)2+2HCl = CaCl2+2HClOCa2++2ClO-+H2O+CO2= CaCO3↓+2HClO或ClO-+H+= HClO漂白粉的漂白原理向漂白粉溶液中通入过量的CO2:Ca(ClO)2+2H2O+2CO2 = Ca(HCO3)2+2HClOClO-+H2O+CO2 = HCO3-+HClO注:带“※”的反应为重要反应,必须熟记;带“☆”的反应只需了解。
高三化学金属及其化合物化学方程式大全

高三化学金属及其化合物化学方程式大全在高三化学的学习中,金属及其化合物的化学方程式是非常重要的知识点。
熟练掌握这些方程式,对于理解化学反应的本质、解决化学问题以及在考试中取得好成绩都具有关键作用。
下面我们就来一起梳理一下常见的金属及其化合物的化学方程式。
一、钠及其化合物1、钠与氧气反应常温下:4Na + O₂= 2Na₂O加热时:2Na + O₂= Na₂O₂2、钠与水反应2Na + 2H₂O = 2NaOH + H₂↑3、钠与盐酸反应2Na + 2HCl = 2NaCl + H₂↑4、钠在空气中燃烧2Na + Cl₂= 2NaCl5、氧化钠与水反应Na₂O + H₂O = 2NaOH6、过氧化钠与水反应2Na₂O₂+ 2H₂O = 4NaOH + O₂↑7、过氧化钠与二氧化碳反应2Na₂O₂+ 2CO₂= 2Na₂CO₃+ O₂8、碳酸钠与盐酸反应Na₂CO₃+ 2HCl = 2NaCl + H₂O + CO₂↑9、碳酸氢钠与盐酸反应NaHCO₃+ HCl = NaCl + H₂O + CO₂↑10、碳酸氢钠受热分解2NaHCO₃= Na₂CO₃+ H₂O + CO₂↑11、碳酸钠溶液中通入二氧化碳Na₂CO₃+ H₂O + CO₂= 2NaHCO₃二、铝及其化合物1、铝与氧气反应4Al + 3O₂= 2Al₂O₃2、铝与盐酸反应2Al + 6HCl = 2AlCl₃+ 3H₂↑3、铝与氢氧化钠溶液反应2Al + 2NaOH + 2H₂O = 2NaAlO₂+ 3H₂↑4、氧化铝与盐酸反应Al₂O₃+ 6HCl = 2AlCl₃+ 3H₂O5、氧化铝与氢氧化钠溶液反应Al₂O₃+ 2NaOH = 2NaAlO₂+ H₂O6、氢氧化铝与盐酸反应Al(OH)₃+ 3HCl = AlCl₃+ 3H₂O7、氢氧化铝与氢氧化钠溶液反应Al(OH)₃+ NaOH = NaAlO₂+ 2H₂O8、实验室制取氢氧化铝AlCl₃+ 3NH₃·H₂O = Al(OH)₃↓ + 3NH₄Cl9、偏铝酸钠溶液中通入二氧化碳(少量)2NaAlO₂+ CO₂+ 3H₂O = 2Al(OH)₃↓ + Na₂CO₃偏铝酸钠溶液中通入二氧化碳(过量)NaAlO₂+ CO₂+ 2H₂O = Al(OH)₃↓ + NaHCO₃三、铁及其化合物1、铁与氧气反应3Fe + 2O₂= Fe₃O₄2、铁与盐酸反应Fe + 2HCl = FeCl₂+ H₂↑3、铁与硫酸铜溶液反应Fe + CuSO₄= FeSO₄+ Cu4、氧化亚铁与盐酸反应FeO + 2HCl = FeCl₂+ H₂O5、氧化铁与盐酸反应Fe₂O₃+ 6HCl = 2FeCl₃+ 3H₂O6、四氧化三铁与盐酸反应Fe₃O₄+ 8HCl = FeCl₂+ 2FeCl₃+ 4H₂O 7、氯化亚铁溶液中通入氯气2FeCl₂+ Cl₂= 2FeCl₃8、氯化铁溶液中加入铁粉2FeCl₃+ Fe = 3FeCl₂9、氯化铁溶液中加入铜粉2FeCl₃+ Cu = 2FeCl₂+ CuCl₂10、氢氧化亚铁在空气中被氧化4Fe(OH)₂+ O₂+ 2H₂O = 4Fe(OH)₃11、氢氧化铁受热分解2Fe(OH)₃= Fe₂O₃+ 3H₂O四、铜及其化合物1、铜在空气中加热2Cu + O₂= 2CuO2、铜与硝酸反应(浓硝酸)Cu + 4HNO₃(浓) = Cu(NO₃)₂+ 2NO₂↑ + 2H₂O (稀硝酸)3Cu + 8HNO₃(稀) = 3Cu(NO₃)₂+2NO↑ + 4H₂O 3、氧化铜与盐酸反应CuO + 2HCl = CuCl₂+ H₂O4、氢氧化铜受热分解Cu(OH)₂= CuO + H₂O5、硫酸铜溶液与氢氧化钠溶液反应CuSO₄+ 2NaOH = Cu(OH)₂↓ + Na₂SO₄掌握这些金属及其化合物的化学方程式,不仅需要死记硬背,更要理解反应的本质和规律。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
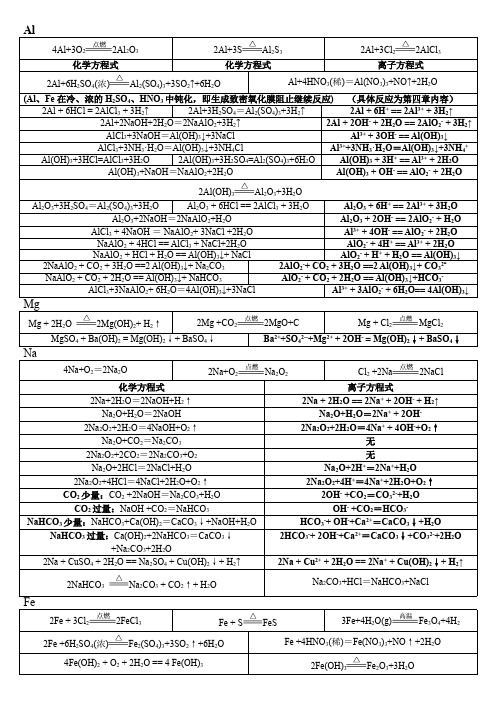
Na 、Mg 、Al 、Fe 及其化合物的化学方程式和离子方程式一、Na 及其化合物的化学方程式和离子方程式 (1)Na 的反应 1、钠和水反应:方程式: 2Na+2H 2O=2NaOH+H 2↑ 离子方程式: 2Na+2H 2O=2Na +2OH -+H 2↑ 2.钠分别和氧气、硫、氯气: 2Na+O 2点燃Na 2O 2 (或加热) 4Na+O 2 = 2Na 2O2Na+S =Na 2S 2Na+Cl 2 点燃2NaCl3.钠分别和盐酸(或硫酸)、醋酸方程式: 2Na+2HCl=2NaCl+H 2↑ 离子方程式: 2Na+2H +=2Na ++H 2↑ 方程式: 2Na+H 2SO 4=Na 2SO 4+H 2↑ 离子方程式: 2Na+2H +=2Na ++H 2↑方程式:2Na+2CH 3COOH=2CH 3COONa+H 2↑ 离子方程式: 2Na+2CH 3COOH=2CH 3COO -+2Na ++H 2↑ 4.钠分别和硫酸铜溶液、氯化铁溶液方程式: 2Na +2H 2O+CuSO 4=Cu(OH)2↓+Na 2SO 4+H 2↑ 离子方程式: 2Na +2H 2O+Cu 2+=Cu(OH)2↓+2Na ++H 2↑ 方程式: 6Na +6H 2O+2FeCl 3=2Fe(OH)3↓+6NaCl+3H 2↑ 离子方程式: 6Na +6H 2O+2Fe 3+=2Fe(OH)3↓+6Na ++3H 2↑(2)Na 的氧化物反应 1.氧化钠分别与水、盐酸方程式: Na 2O+H 2O=2NaOH 离子方程式: Na 2O+H 2O=2Na ++2OH -方程式: Na 2O+2HCl=2NaCl+H 2O 离子方程式: Na 2O+2H +=2Na ++H 2O 2.过氧化钠分别与盐酸、水方程式: 2Na 2O 2+4HCl=4NaCl+2H 2O+O 2↑ 离子方程式: 2Na 2O 2+4H + =4Na ++2H 2O+O 2↑ 方程式: 2Na 2O 2+2H 2O=4NaOH+O 2↑ 离子方程式: 2Na 2O 2+2H 2O=4Na ++4OH -+O 2↑ 3.过氧化钠分别与二氧化碳:2Na 2O 2+2CO 2=2Na 2CO 3+O 2 (3)Na 2CO 3、NaHCO 3盐的反应1.分别加热碳酸钠和碳酸氢钠固体(鉴别固体Na 2CO 3、NaHCO 3的方法)碳酸钠受热不分解 2NaHCO 3△Na 2CO 3+H 2O+CO 2↑2.碳酸钠和碳酸氢钠溶液分别与少量(或过量)的盐酸反应少量的盐酸时:Na2CO3+HCl=NaHCO3+NaCl CO32-+H+=HCO3-NaHCO3+HCl=NaCl+CO2↑+H2O HCO3-+H+=CO2↑+H2O过量的盐酸时:Na2CO3+2HCl=2NaCl+CO2↑+H2O CO32-+2H+=CO2↑+H2ONaHCO3+HCl=NaCl+CO2↑+H2O HCO3-+H+=CO2↑+H2O3.碳酸钠和碳酸氢钠溶液分别与少量(或过量)的醋酸反应少量的醋酸时:Na2CO3+CH3COOH=NaHCO3+CH3COONaCO32-+ CH3COOH=HCO3-+ CH3COO-NaHCO3+CH3COOH=CH3COONa+CO2↑+H2OHCO3-+ CH3COOH=CO2↑+H2O+ CH3COO-过量的醋酸时:Na2CO3+2CH3COOH=2CH3COONa+ CO2↑+H2OCO32-+ 2CH3COOH=2CH3COO-+CO2↑+H2ONaHCO3+CH3COOH=CH3COONa+CO2↑+H2OHCO3-+ CH3COOH=CO2↑+H2O+ CH3COO-4.二氧化碳通入到碳酸钠溶液中(或通入到饱和的碳酸钠溶液中)CO2+ Na2CO3+H2O=2 NaHCO3CO2+CO32-+H2O=2 HCO3-或 CO2+ Na2CO3+H2O=2 NaHCO3↓ CO2+2Na++CO32-+H2O=2 NaHCO3↓5.碳酸钠溶液与澄清石灰水(或氢氧化钠溶液)混合方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH离子方程式: CO32-+ Ca2+=CaCO3↓碳酸钠溶液与氢氧化钠溶液混合不发生反应6. 碳酸氢钠与少量(或过量)的澄清石灰水混合 (类似:澄清石灰水可以改为氢氧化钡溶液)少量澄清石灰水:2NaHCO3+Ca(OH)2=2H2O+CaCO3↓+ Na2CO32 HCO3-+Ca2++2OH-=2H2O+CaCO3↓+ CO32-过量澄清石灰水:NaHCO3+Ca(OH)2=H2O+CaCO3↓+ NaOHHCO3-+Ca2++OH-=H2O+CaCO3↓7.碳酸氢钠与氢氧化钠溶液混合方程式: NaHCO3+ NaOH=Na2CO3+ H2O 离子方程式: HCO3-+OH-=H2O+CO32-8.电解熔融状态的氯化钠、电解饱和食盐水(注意电极反应式的书写)2NaCl(熔融)=Na+Cl 2↑ 2NaCl+2H 2O电解Cl 2↑+H 2↑+2NaOH 2Cl -+2H 2O电解Cl 2↑+H 2↑+2OH -9.碳酸钠溶液、碳酸氢钠溶液滴2滴酚酞试液都呈 色,为什么(用方程式或离子方程式表示) 溶液呈红色 CO 32-+H 2O HCO 3-+OH -溶液呈碱性 HCO 3-+H 2O H 2CO 3 + OH - 溶液呈碱性二、Mg 、Al 及其化合物的化学方程式和离子方程式 (1)Mg 的反应1.镁在空气中燃烧2Mg + O 2 2MgO 3Mg +N 2 Mg 3N 2 2Mg + CO 2 2MgO + C 2.镁能溶解在氯化铵溶液中Mg + 2NH 4Cl = MgCl 2 + H 2↑+ NH 3↑ Mg + 2NH 4+= Mg 2++ H 2↑+ NH 3↑ (2) Al 的反应3.铝是活泼金属,为什么可以直接存放在空气中,用简单的文字和方程式说明:4Al+3O 2=2Al 2O 3 在铝的表面形成致密的氧化铝薄膜,将铝和空气隔绝。
4.铝与盐酸反应、铝与氢氧化钠溶液反应2Al+6HCl = 2AlCl 3+3H 2↑ 2Al+6H += 2Al 3++3H 2↑ 2Al+2NaOH+2H 2O = 2NaAlO 2+3H 2↑ 2Al+2OH -+2H 2O =2AlO 2-+3H 2↑ 5.铝在高温条件下与氧化铁(或FeO 、Fe 3O 4、Fe 2O 3、MnO 2、Cr 2O 3)反应2Al +Fe 2O 3 Al 2O 3 + 2Fe (3)Al 2O 3的反应6.氧化铝分别与盐酸、氢氧化钠溶液反应Al 2O 3+6HCl =2AlCl 3+3H 2O Al 2O 3+6H +=2Al 3++3H 2O Al 2O 3+2NaOH =2NaAlO 2+H 2O Al 2O 3+2OH -=2AlO 2-+H 2O (一般金属氧化物都不与碱反应,Al 2O 3特别,应引起注意) (4) Al(OH)3的反应1.氢氧化铝分别与盐酸、氢氧化钠溶液反应Al(OH)3+3HCl=AlCl 3+3H 2O Al(OH)3+3H +=Al ++3H 2O Al(OH)3+NaOH=NaAlO 2+2H 2O Al(OH)3+OH -=AlO 2-+2H 2O 2.加热氢氧化铝:2Al(OH)3 Al 2O 3+3H 2O(4) Al 3+的反应点燃点燃点燃高温1.氯化铝(硫酸铝)溶液中加入少量(或过量)的氢氧化钠溶液少量NaOH :AlCl3+3NaOH =Al(OH)3↓+3NaCl Al3++3OH-=Al(OH)3↓过量NaOH :AlCl3+4NaOH =NaAlO2+3NaCl +2H2O Al3++4OH-=AlO2-+2H2O2.氯化铝(硫酸铝)溶液中加入少量(或过量)的氨水AlCl3+3NH3·H2O=Al(OH)3↓+3NH4Cl Al3++3NH3·H2O=Al(OH)3↓+3NH4+(5) AlO2-的反应1.偏铝酸钠溶液中加入少量(或过量)的盐酸(Al(OH)3制备方法之一)少量盐酸:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl AlO2-+H++H2O=Al(OH)3↓过量盐酸:NaAlO2+4HCl=AlCl3+NaCl+2H2O AlO2-+4H+=Al3++2H2O2.偏铝酸钠溶液中通入少量(或过量)的二氧化碳(Al(OH)3制备方法之一)少量CO2:2NaAlO2+CO2+3H2O=2Al(OH)3↓+Na2CO32AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-过量CO2:NaAlO2+CO2+2H2O=Al(OH)3↓+NaHCO3AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(6) Al3+与AlO2-的反应及双水解6.氯化铝溶液和偏铝酸钠溶液(Al3+与HCO3-、CO32-、S2-、HS-) (Al(OH)3制备方法之一) AlCl3 + 3NaAlO2 + 6H2O = 4 Al(OH)3↓+3NaCl Al3++ 3AlO2-+ 6H2O = 4Al(OH)3↓7.偏铝酸钠溶液和碳酸氢钠溶液混合NaAlO2+NaHCO3+H2O=Al(OH)3↓+Na2CO3 AlO2-+HCO3-+H2O=Al(OH)3↓+CO32-8.用简单的文字说明和离子方程式描述明矾可以净水的理由明矾溶于水后电离出Al3+发生水解生成吸附性很强的Al(OH)3胶体,吸附杂质达到净水目的:Al3++3H 2O Al(OH)3胶体+3H+(6) Al与Mg的制取工业上生产Mg和Al金属MgCl2(熔融)电解Mg+Cl2↑ 2Al2O3(熔融)电解4Al+3O2↑三、Fe及其化合物的化学方程式和离子方程式(1) Fe的反应1.铁分别在氧气、氯气中燃烧、铁和硫混合加热(氧气、氯气和硫的氧化性:)3Fe+2O2点燃Fe3O4 2Fe+3Cl2点燃2FeCl3 Fe+S △FeS 氧化性:Cl2>O2>S2.铁加入盐酸(或硫酸)中Fe+2HCl=FeCl2+H2↑ Fe+2H+=Fe2++H2↑Fe+H2SO4=FeSO4+H2↑ Fe+2H+=Fe2++H2↑3.铁加入过量..的稀(或浓)硝酸中稀:Fe+4HNO3=Fe(NO3)3+NO↑+2H2O Fe+4H++NO3-=Fe3++NO↑+2H2O浓:Fe+6HNO3=Fe(NO3)3+3NO2↑+3H2O Fe+6H++3NO3-=Fe3++3NO2↑+3H2O4.铁加入少量..的稀(或浓)硝酸中稀:3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O 3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O 浓:Fe+4HNO3=Fe(NO3)2+2NO2↑+2H2O Fe+4H++2NO3-=Fe3++2NO2↑+2H2O 5.铁在高温条件下与水蒸气反应3Fe+4H2O(g)高温Fe3O4+4H26.铁粉加入到氯化铜(或氯化铁)溶液中Fe+CuCl2=FeCl2+Cu Fe+Cu2+=Fe2++CuFe+2FeCl3=3FeCl2 Fe+2Fe3+=3Fe2+ (2) Fe的氧化物的反应1.FeO、Fe3O4、Fe2O3分别与盐酸反应FeO+2HCl=FeCl2+H2O FeO+2H+=Fe2++H2OFe3O4+8HCl=FeCl2+2FeCl3+4H2O Fe3O4+8H+=Fe2++ 2Fe3++4H2OFe2O3+6HCl=2FeCl3+3H2O Fe2O3+6H+=2Fe3++3H2O2.FeO、Fe3O4、Fe2O3分别与稀硝酸反应3FeO+10HNO3=3Fe(NO3)3+NO↑+5H2O 3FeO+10H++NO3-=3Fe3++NO↑+5H2O 3Fe3O4+28HNO3=9Fe(NO3)3+NO↑+14H2O 3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O Fe2O3+6HNO3=2Fe(NO3)3+3H2O Fe2O3+6H+=2Fe3++3H2O3.FeO、Fe3O4、Fe2O3分别与氢碘酸反应FeO+2HI=Fel2+H2O FeO+2H+=Fe2++H2OFe3O4+8HI=3Fel2+I2+4H2O Fe3O4+8H++2I-=3Fe2++I2+4H2OFe2O3+6HI=2FeI2+I2+3H2O Fe2O3+6H++2I-=2Fe2++I2+3H2O 4.FeO、Fe3O4、Fe2O3分别与氢气反应FeO+H2高温Fe+H2O Fe3O4+4H2高温3Fe+4H2O Fe2O3+3H2高温2Fe+3H2O5.FeO、Fe3O4、Fe2O3分别与CO反应FeO+CO高温Fe+CO2 Fe3O4+4CO高温3Fe+4CO2 Fe2O3+3CO高温2Fe+3CO26.FeO、Fe3O4、Fe2O3分别与Al反应3FeO+2Al高温3Fe+Al2O3 2Fe3O4+6Al高温6Fe+4Al2O3 Fe2O3+2Al高温2Fe+ Al2O3 (3) Fe的氢氧化物的反应1.Fe(OH)2、Fe(OH)3、C u(O H)2分别与盐酸(稀硫酸)反应Fe(OH)2+2HCl=FeCl2+H2O Fe(OH)2+2H+=Fe2++H2OFe(OH)3+3HCl=FeCl3+3H2O Fe(OH)3+3H+=Fe3++3H2OC u(O H)2+2HCl=CuCl2+2H2O C u(O H)2+2H+=Cu2++2H2O2.Fe(OH)2、Fe(OH)3、C u(O H)2分别与稀硝酸反应3Fe(OH)2+10HNO3=3Fe(NO3)3+NO↑+8H2O 3Fe(OH)2+10H++NO3-=3Fe3++NO↑+H2OFe(OH)3+3HNO3=FeCl3+3H2O Fe(OH)3+3H+=Fe3++3H2OC u(O H)2+2HNO3=CuCl2+2H2O C u(O H)2+2H+=Cu2++2H2O3.Fe(OH)2、Fe(OH)3、C u(O H)2分别与氢碘酸(或氢硫酸)反应Fe(OH)2+2HI=Fel2+H2O Fe(OH)2+2H+=Fe2++H2O2Fe(OH)3+6Hl=2Fel2+I2+6H2O 2Fe(OH)3+6H++2I-=2Fe2++I2+6H2OC u(O H)2+2Hl=Cul2+2H2O C u(O H)2+2H+=Cu2++2H2O4.Fe(OH)2不稳定,在空气中易被氧化,由白色迅速变成灰绿色,最终变成红褐色:4Fe(OH)2+O2+2H2O=4Fe(OH)35.Fe(OH)3、C u(O H)2受热均易分解2Fe(OH)3△Fe2O3+3H2O Cu(OH)2△CuO+H2O(4) Fe的氢氧化物的制备1.F e(O H)2制备(注意防氧化措施)FeSO4+2NaOH=F e(O H)2↓+Na2SO4 Fe2++2OH-=F e(O H)2↓2.F e(O H)3制备、C u(O H)2制备Fe2(SO4)3+6NaOH=2F e(O H)3↓+3Na2SO4 Fe3++3OH-=F e(O H)3↓CuSO4+2NaOH=C u(O H)2↓+Na2SO4 Cu2++2OH-=C u(O H)2↓(5) Fe2+与Fe3+的转化1.Fe2+盐(绿矾:FeSO4·7H2O)溶液与稀硝酸、O3、H2O2、酸性KMnO4、Cl2水、Br2水、Na2S溶液等3Fe2++4H++NO3-=3Fe3++NO↑+2H2O 6Fe2++O3+6H+=6Fe3++3H2O2Fe2++H2O2+2H+=2Fe3++2H2O 5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O2Fe2++Cl2=2Fe3++2Cl- 2Fe2++Br2=2Fe3++2Br- Fe2++S2-=FeS↓2.用FeCl3溶液腐蚀印刷电路铜板2FeCl3+Cu=2FeCl2+ CuCl2 2Fe3++Cu=2Fe2++ Cu2+3.FeCl3溶液中加入Fe粉、通入H2S气体、加入Na2S溶液、加入氢碘酸等2Fe3++Fe=3Fe2+ 2Fe3++H2S=2Fe2++S↓+2H+ 2Fe3++S2-=2Fe2++S↓ 2Fe3++2I-=2Fe2++I2 4.FeCl3溶液与少量(或过量)的Zn粉反应少量Zn粉:2Fe3++Zn=2Fe2++ Zn2+过量Zn粉:先发生2Fe3++Zn=2Fe2++ Zn2+然后发生Zn+Fe2+= Zn2++ Fe所以过量Zn粉时总反应为:2Fe3++3Zn=2Fe+ 3Zn2+(6) Fe3+的检验1.FeCl3溶液与KSCN溶液混合Fe3++nSCN-=Fe(SCN)n(3-n) 经常写成:Fe3++3SCN-=Fe(SCN)3(血红色,不是沉淀,不标“↓”)。
