人教版高中化学选修三3.1 晶体的常识—晶胞
人教版高中化学选修3课件:3.1.1 晶体的常识

晶体的常识
晶胞中粒子个数计算规律:分摊法(切割法)
顶
角
棱 上
晶晶胞 胞 立方体
顶角 1/8
棱上 1/4
面上 1/2
面 上
中心 1
第 23 页子晶体 金属晶体
与非晶体的区别
晶胞
课时小结第 24 页
的
定义
顶点:1/8
棱边:1/4
原子个数计算
分摊法(切割法)
晶体的常识 2、晶胞的结构特征:
归纳新知第 18 页
的
一般来说,晶胞都是平行六面体(边长不一定相等,也不一定垂直) , 通过上、下、左、右、前、后的平移与下一个晶胞完全重合。
3、晶胞和晶体的关系: 晶体可以看作是数量巨大的晶胞“无隙并置”而成
如何理解“无隙并置”?
晶体的常识
平行六面体
无隙并置
观察思考第 19 页
各1/2个
绿色:8× 1/8+6×1/2 = 4 灰色:12× ¼ +1=4 各4个
7. 人生,最宝贵的莫过于光阴。人生,最璀璨的莫过于事业。人生,最快乐的莫过于奋斗。 10. 让人生与事业结伴,让生命与使命同行。 2. 成功并不能用一个人达到什么地位来衡量,而是依据他在迈向成功的过程中,到底克服了多少困难和障碍。 5. 努力向上的开拓,才使弯曲的竹鞭化作了笔直的毛竹。 14. 勇气不是感觉不到恐惧而是感觉到恐惧也继续做下去 15. 宝剑不磨要生锈;人不学习要落后。1. 生活中最基本的技巧是交流,最可依赖的品质是耐心,最糟糕的行为是抱怨,最易见效的努力是从 自己做起。
化学 · 选修 3《物质结构与性质》
晶体的常识
晶体的常识
绿宝石
图片欣赏第 2 页的
紫水晶
人教化学选修3第三章第一节 晶体的常识第2课时(共34张PPT)

晶胞示意图
铜晶胞
金刚石晶胞
CO2晶胞
NaCl晶胞
思考与交流: (1)上述铜晶体、金刚石、CO2晶体、NaCl晶
体的晶胞的空间构形呈什么形状?
(2)在上述晶体中,晶胞是如何排列的?晶胞 之间是否存在空隙?
无隙并置
平行六 面体
记住
2、特点:通过上、下、
左、右、前、后的平移能 与下一个最小单元(即晶 胞)完全重合
顶点:
棱上:
面心:
体心:
晶胞中粒子个数计算规律(切割法)
晶胞
顶点
棱上
面心
体心
立方体
1/8
1/4
1/2
1
顶点 棱上 面心 体心
常见晶胞中微粒数的计算 (列式计算)
(1)面心立方:在立方体顶点的微粒为8 个晶胞共有,在面心的为2个晶胞共有。
微粒数为:8×1/8 + 6×1/2 = 4
(2)体心立方:在立方体顶点的微粒为 8个晶胞共享,处于体心的粒子全部属 于该晶胞。
活动
铜晶体的晶胞结构属于面心立方晶胞,请大家数 一数,算一算:一个铜晶胞中有几个铜原子?
铜晶胞含有4个铜原子,为什么不是14个?
4.晶胞中粒子个数的计算
均摊法:晶胞任意位置上的一个粒子如果是 被x个晶胞所共有,那么,每个晶胞对这个 粒子分得的份额就是1/x
体心:1 面心:1/2 棱边:1/4 顶点:1/8
非平行六面体---非长方体(正方体)晶体中 粒子视具体情况而定。如石墨晶胞每一层内碳原 子排成六边形,其顶点(1个碳原子)被三个六边 形共有,每个六边形占该粒子的1/3。
晶胞中粒子个数的计 算,其重要问题是正确分 析晶胞中任意位置上的一 个粒子被几个晶胞所共有。
高中化学选修3课件-3.1 晶体的常识2-人教版

晶体可以看作是数量巨大的晶胞 “无隙并置”而成.
“无隙”指相邻的晶胞之间没有任何间隙;
一个晶胞与相邻的晶胞完全共顶点、共棱边、共面
“并置”指所有晶胞都是平行排列的,取向相同。
一个晶胞到另一个晶胞只需平移,不需转动
“完全等同” 指所有晶胞的形状、
内部的原子种类、个数及几何排列完全相同
平行六面体
无隙并置
4.三种典型立方晶体结构 简单立方 体心立方 面心立方
P63 图3-7
铜晶体的一个晶胞中含有 多少个铜原子?
A: 14
B: 4
C: 8
D: 6
答案: B 为什么呢?
请看:
84 51
顶点:1/8
棱边:1/4
中心 1
学与问 P64
2
2
8
8
练习1: 下面几种晶胞中分别含有几个原子?
各1/2个
各4个 绿色:8×1/8 + 6×1/2 = 4 灰色:12× ¼ + 1 = 4
练习2: 下面几种晶胞中分别含有几个原子?
看 图 写 化 学 式
A2BC2
挑战自我
1.现有甲、乙、丙、丁四种晶胞,可推
知:甲晶体中A与B的离子个数比为
31
42
73
面心:1/2
62 2
1
1
体心:1
5.晶胞中粒子个数的ຫໍສະໝຸດ 算方法:均摊法(或切割法) 原则:若粒子被n个晶胞共用,
均摊一个晶胞中为1/n
规律:对立方晶胞
体心:1
顶点:1/8
面心:1/2 棱边:1/4
晶胞中粒子个数计算规律(均摊法)
高中化学人教版选修3教案-3.1 晶体的常识
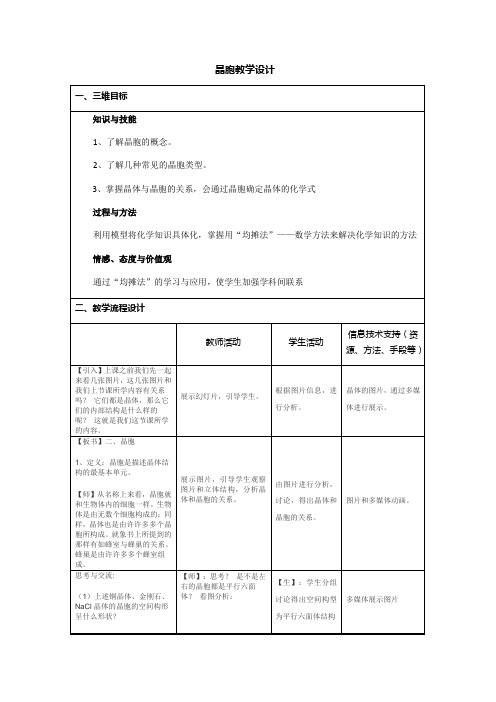
(1)上述铜晶体、金刚石、NaCl晶体的晶胞的空间构形呈什么形状?
(2)在上述晶体中,晶胞是如何排列的?晶胞之间是否存在空隙?
【师】:思考?是不是左右的晶胞都是平行六面体?看图分析:
【生】:学生分组讨论得出空间构型为平行六面体结构
【生】:不是所有的晶胞都是平行六面体,应该是大多数是平行六面体。
多媒体展示图片
【板书】2、晶胞的特点:
(1)大多是平行六面体。
(2)排列方式:“无隙并置”
【板书】3、计算晶体化学式或晶胞中粒子数的一般方法——均摊法
下面我们一起来看一个小视频来分析一下。
【师】:通过视频我们可以明显的看出顶点的原子是被八个晶胞所拥有,所以我们可以得出结论:
【板书】⑴顶点——同时为8个晶胞所共有——每一个晶胞拥有:1/8;
【随堂练习】
练习1:现在我们一起再来回顾一下在一个氯化钠晶胞里是13个钠离子,多少14氯离子?
生:不是
氯离子:8*1/8+6*1/2=4
钠离子:1+12*1/4=4
【学与问】
金属钠:8×1/8+1 =2
金属锌:8×1/8+1 = 2
晶体碘:(8×1/8+6×1/2)×2 = 8
金刚石:8×1/8+6×1/6+4 = 8
【师】:在立方晶胞中,粒子可能出现在到下这几个位置:
【师】:当原子位于顶点时这个原子将被八个晶胞所共用,就像我手中的八个晶胞模型一样,每一个晶胞只拥有该原子的1/8.
【生】:氯离子:8个顶点各有一个,6个面上各有一个,一共是14个铜原子。
钠离子:12在棱的中点1个在体心
共13个
顶点:1/8
棱上:?
面心:?
晶胞教学设计
一、三维目标
人教版化学《晶体的常识》完美课件

I2
金刚石
钠、锌晶胞都是:8×1/8+1=2; 碘:(8×1/8+6×1/2)×2=8; 金刚石:8×1/8+6×1/2+4=8。
高中化学选修3人教版3.1晶体的常识 课件
高中化学选修3人教版3.1晶体的常识 课件
小结
• 1.掌握晶体的特征:自范性、各向异性、固 定的熔沸点、质点排列的高度有序性
• 2.知道晶体和晶胞的关系 • 晶体是由无数晶胞“无隙并置”而成.
No
高中化学选修3人教版3.1晶体的常识 课件
高中化学选修3人教版3.1晶体的常识 课件
3. 下图是氯化钠的一个晶胞。提问:一 个晶胞 占有多少个氯离子?占有多少个钠离子?在NaCl 晶体中,每个Na+周围最近距离的Na+有 个?
ClNa+
高中化学选修3人教版3.1晶体的常识 课件
典例分析 例:2001年报道的硼和镁形成的化合物刷新了 金属化合物超导温度的最高记录。如图所示的是 该化合物的晶体结构单元:镁原子间形成正六棱 柱,且棱柱的上下底面还各有1个镁原子,6个硼 原子位于棱柱内。则该化合物的化学式可表示为
A、MgB B、 MgB2 C、Mg2B D、Mg3B2
典例分析
Mg原子的数目: 12×1/6+2×1/2=3 B原子的数目:6 故化学式可表示为
Mg2B
六、晶体有关计算
利用晶胞参数可计算晶胞体积(V),根据相 对分子质量(M)、晶胞中分子数(X)和阿伏
伽德罗常数NA,可计算晶体的密度 :
7、如图是CsCl晶体的晶胞(晶体中最小的重复单元) 已知晶体中2个最近的Cs+核间距离为acm,氯化铯 的相对分子质量为M,NA为阿佛加德
人教版选修3 化学:3.1 晶体的常识 课件(共25张PPT)

学与问 P64
2
2
8
8
练习: 下面几种晶胞中分别含有几个原子?
各1/2个
各4个 绿色:8× 1/8+6×1/2 = 4 灰色:12× ¼+1=4
小结:
1、晶胞:晶体中的最小重复单元
2、晶胞对质点的占有率 顶点: 1/8
立方晶胞
棱边: 1/4 面心: 1/2 体心: 1
课堂练习
1.钛酸钡的热稳定性好,
选修3 物质结构与性质 第三章 晶体结构与性质
第一节 晶体的常识
教学目标: 知识与技能
1.了解分子晶体和原子晶体的特征。 2.通过NaCl、Cu的晶体结构,学生知道晶体中粒子的 排列规律。 3.通过对晶胞的分析,学生会计算晶胞中粒子的个数。 过程与方法
通过几种典型的晶体(金刚石、石墨、NaCl、金属) 结构的分析,学生能从三维的角度考虑粒子在空间的分 布。 情感态度与价值观
0.39 a3
g. ㎝-3
晶胞 解法3:依ρ= m/v
每个晶胞中所含的Na+和Cl-的个数均为4个,即含4个“NaCl”。
每个晶胞的体积为: (a×10-8)3㎝3
即含4个“NaCl”所占的体积为:(a×10-8)3㎝3
那么1个“NaCl”所占的体积为:(a×10-8)3 /4 ㎝3
则:1molNaCl所占的体积为: 6.02×1023 ·(a×10-8)3 /4 ㎝3
A: 14
B: 4
C: 8
D: 6
答案: B 为什么呢?
请看:
84 51
顶点:1/8
棱边:1/4
31
42
73
面心:1/2
62 2
1
1 体心:1
新人教版高二化学选修3:3.1晶体常识(第2课时)教案 Word版
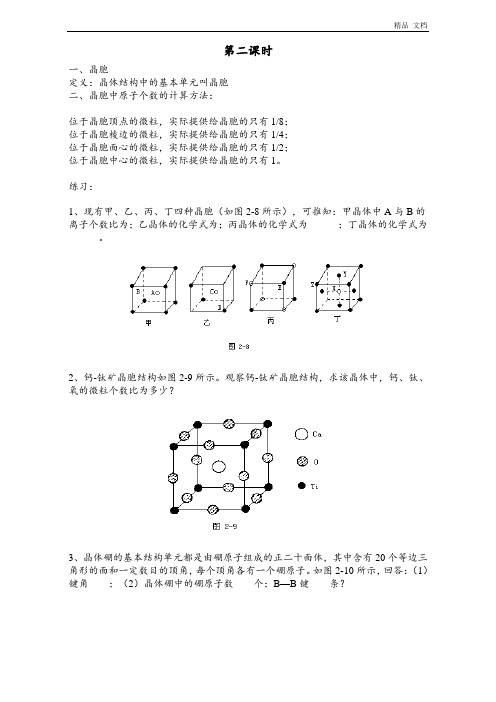
第二课时一、晶胞定义:晶体结构中的基本单元叫晶胞二、晶胞中原子个数的计算方法:位于晶胞顶点的微粒,实际提供给晶胞的只有1/8;位于晶胞棱边的微粒,实际提供给晶胞的只有1/4;位于晶胞面心的微粒,实际提供给晶胞的只有1/2;位于晶胞中心的微粒,实际提供给晶胞的只有1。
练习:1、现有甲、乙、丙、丁四种晶胞(如图2-8所示),可推知:甲晶体中A与B的离子个数比为;乙晶体的化学式为;丙晶体的化学式为______;丁晶体的化学式为______。
2、钙-钛矿晶胞结构如图2-9所示。
观察钙-钛矿晶胞结构,求该晶体中,钙、钛、氧的微粒个数比为多少?3、晶体硼的基本结构单元都是由硼原子组成的正二十面体,其中含有20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子。
如图2-10所示,回答:(1)键角____;(2)晶体硼中的硼原子数____个;B—B键____条?4、在碳单质的成员中还有一种混合型晶体——石墨,如图2-11所示。
它是层状结构,层与层之间依靠作用力相结合。
每层内部碳原子与碳原子之间靠作用力相结合,其键角。
分析图中每个六边形含有个碳原子。
5、C70分子是形如椭球状的多面体,该结构的建立基于以下考虑:(1)C70分子中每个碳原子只跟相邻的3个碳原子形成化学键;(2)C70分子中只含有五边形和六边形;(3)多面体的顶点数、面数和棱边数的关系遵循欧拉定理:顶点数+面数-棱边数=2。
根据以上所述确定:(1)C70分子中所含的单键数和双键数;(2)C70分子中的五边形和六边形各有多少?可以删除编辑的word文档温馨提示:教师授课注意事项:1、立足课本。
2、明确目标。
3、明确重点。
4、把握重难点。
5、注重学习自学和互学。
6、教师少说学生多练习。
7、练习要梯度。
8、当堂训练批改作业。
(由于文档太多,如有错误或侵权,请练习本店马上删除)。
【人教版】高中化学选修3知识点总结:第三章晶体形态与特征

【人教版】高中化学选修3知识点总结:第三章晶体形态与特征
本文档总结了高中化学选修3教材中第三章晶体形态与特征的知识点。
1. 晶体的概念和结构特点
- 晶体是由具有一定空间有序性的原子、离子或分子组成的凝聚态物质。
- 晶体的结构特点包括周期性、长程有序性和层状结构。
2. 晶体的晶体系和晶体面
- 晶体系根据对称性可分为三类:立方晶系、四方晶系和六角晶系。
- 晶体面是晶体表面的平坦部分。
3. 晶体的晶胞和晶格
- 晶胞是最小重复单元,包含了晶体的全部结构信息。
- 晶格是晶胞在空间中无限重复所形成的排列。
4. 晶体的晶体缺陷
- 晶体缺陷是指晶体中存在的结构异常或杂质。
- 晶体缺陷包括点缺陷、线缺陷和面缺陷。
5. 晶体的晶体学性质
- 晶体的晶体学性质包括透明性、折射性和散射性等。
- 不同晶体的晶体学性质有所差异。
以上是第三章晶体形态与特征的知识点总结,希望对您有帮助。
参考资料:
- 《高中化学选修3》人教版。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第二课时 晶胞
二.晶胞
1.定义:描述晶体结构的基本单元 晶体与晶胞的关系正好比蜂巢与蜂室的关系
蜂巢与蜂室
铜晶体
铜晶胞
铜晶体
铜晶胞
晶体结构 晶胞示意图
晶胞形状:
无隙并 置
平行六面 体
说明:
⑴晶胞一般是平行六面体,整块晶体是数量巨大 的晶胞“无隙并置”而成。
⑵晶胞是8个顶角相同的最小正六面体;晶胞的 平行棱相同;晶胞的平行面相同。
Zn: 8× +1=2
I2:
(8×
+
6
×
1 2
)×2
=8
8×1/8+6×1/2+4=8
练习1:
石墨晶体的层状结构,层 内为平面正六边形结构(如 图),试回答下列问题:
图中平均每个正六边形占 有C原子数为____2个、占有的 碳碳键数为____个3 。
碳原子数目与碳碳化学键 数目之比为_____2_:_3.
Cl- 顶点 ( 1/8 ) 8 = 1,
面中心 ( 1/2 ) 6 = 3 , 共 4 个
Na+ 棱上 ( 1/4 ) 12 = 3 ,
体中心
1 共4个
练习6、如图所示晶体中每个阳离子A或阴离子B,均可被 另一种离子以四面体形式包围着,则该晶体对应的化学式 为
A.AB C.AB3
B.A2B D.A2B3
练习2
2001年报道的硼和镁形成的化合物刷新了金属化合物超导温 度的最高记录。如图所示的是该化合物的晶体结构单元:镁 原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子, 6个硼原子位于棱柱内。则该化合物的化学式可表示为( B )
A、MgB C、Mg2B
B、 MCl晶胞中各原子的个数。
(二): 晶胞中粒子个数计算规律
晶胞
顶角 棱上
面上
中心
立方体
1/8
1/4
1/2
1
顶角 棱上 面上
例如
⑴
⑵
⑶
⑴ 微粒数为:8×1/8 + 6×1/2 = 4 ⑵ 微粒数为:8×1/8 + 1 = 2 ⑶ 微粒数为:12×1/6 + 2×1/2 + 3 = 6
学与问:
Na
Zn
I2
C
Na: 8× +1=2
练习8、图是超导化合物一钙钛矿晶体中最小重复单元(晶
胞)的结构.请回答: 该化合物的化学式为____C_a_T_i.O3
三种典型立方晶体结构
简单立方 体心立方 面心立方
NaCl晶体结构示意图:
ClNa+
属于4个小立方体 属 于
8 个 小 立 方 体
2.晶胞中粒子个数的计算:均摊法
体心:1
面心:1/2
顶点:1/8
棱边:1/4
请看: 棱边:1/4 31
84
73
51
62
顶点:1/8
1
体心:1
42
面心:1/2
2 1
