2005年南京工业大学物理化学考研试题
南京工业大学 802+物理化学考试大纲

802《物理化学》考试大纲一、考试的基本要求学生应系统地掌握物理化学的基本概念和基本理论,能熟练运用热力学第一定律、热力学第二定律、多组分热力学、化学平衡原理、相平衡原理、电化学知识、动力学原理和界面化学知识,分析和解决具体问题。
二、考试方式和考试时间闭卷考试(自带计算器),总分150,考试时间为3小时。
三、参考书目1.刘建兰,等.物理化学.第1版. 北京:化学工业出版社,2013.2.傅献彩,等.物理化学.第5版.北京:高等教育出版社,2005.3.胡英,等. 物理化学. 第5版. 北京:高等教育出版社,2007.4.刘俊吉,等.物理化学.第5版.北京:高等教育出版社,2009.四、试题类型:主要包括单项选择题、填空题、简答题、计算题、相图题、证明题等类型,并根据每年的考试要求做相应调整。
五、考试内容及要求第一部分气体的pVT性质掌握:理想气体的概念与微观特征,理想气体状态方程的适用条件;分压定律和分体积定律;范德华方程中常数的影响因素和常数的单位;液体的饱和蒸气压、沸点及相对湿度的概念及其影响因素。
熟悉:实际气体的液化及临界参数,临界状态的特征;压缩因子概念;对比参数的概念。
第二部分热力学第一定律掌握:运用热力学第一定律计算理想气体p V T变化过程、相变过程以及化学反应过程中的热、功、热力学能变和焓变;体积功的计算;化学反应的摩尔恒容热与摩尔恒压热的关系。
熟悉:系统的分类;性质的分类;平衡态具备的条件;热、功和反应进度等概念;热力学第一定律的文字叙述;理想气体的摩尔定容热容和摩尔定压热容;不同系统关于标准状态的规定;物质的 m f H ∆和 m c H ∆概念;基希霍夫公式;可逆过程的概念与特征;节流膨胀后热力学性质的变化、节流膨胀系数。
第三部分 热力学第二定律掌握:理想气体p V T 变化过程、相变过程以及化学反应过程中的熵变、亥姆霍兹函数变化值与吉布斯函数变化值的计算;系统的熵变、环境的熵变和隔离系统的熵变的计算;运用麦克斯韦关系式计算实际气体变化过程中的熵变;克劳修斯-克拉佩龙方程。
2005物理化学与有机化学
S2= [H-G+T1S1]/T2= [-2909.9-15957+300×191.83]/200=193.41 J/K.mol
S= 193.41-191.83=1.58 J/K.mol
∵S= Cpln(T2/T1)+Rln(p1/p2)=3.5Rln(200/300)+Rln(5p /p2)=1.58
Qp=H=(G+TS)=G +TS=-nFE+Qr
Qp=-10270 J
(3)∵Cp= d(H)/dT
J.K-1
(4)对于题给的反应,可以设计为下列电池:
(-)Cu| CuSO4(m)|CuHg(s), Hg(l) (*O=H++OH-在298K时的弛豫时间=37s,试求该反应的正向和逆向反应速率常数kf和kr。
M武汉大学
2005年攻读硕士学位研究生入学考试试题答案
科目名称:物理化学和高分子化学科目代码:
注意:所有的答题内容必须答在答题纸上,凡答在试题或草稿纸上的一律无效。
物理化学部分(75分)
k: 1.381×10-23J·K-1h: 6.626×10-34J·s
1.(15分)一.有一双原子分子理想气体,T1=300K,p1=5p ,Sm (300K,5 p )=191.83 J/K.mol,经历一途径到达末态,已知此始末两态间的G=15957 J/mol,G-F=-831.4 J。试求:此始末两态间的U、H、S、F;以及末态的温度和压力?
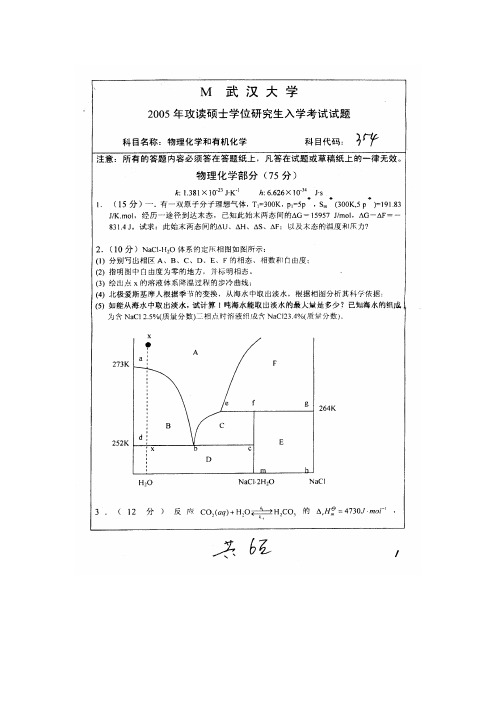
(1)分别写出相区A、B、C、D、E、F的相态、相数和自由度;
(2)指明图中自由度为零的地方,并标明相态。
(3)绘出点x的溶液体系降温过程的步冷曲线;
(4)北极爱斯基摩人根据季节的变换,从海水中取出淡水,根据相图分析其科学依据;
南京工业大学物理化学试题库

第一章热力学第一定律选择题1.热力学第一定律ΔU=Q+W 只适用于()(A) 单纯状态变化 (B) 相变化 (C) 化学变化 (D) 封闭物系的任何变化答案:D2.关于热和功, 下面的说法中, 不正确的是(A) 功和热只出现于系统状态变化的过程中, 只存在于系统和环境间的界面上(B) 只有在封闭系统发生的过程中, 功和热才有明确的意义(C) 功和热不是能量, 而是能量传递的两种形式, 可称之为被交换的能量(D) 在封闭系统中发生的过程中, 如果内能不变, 则功和热对系统的影响必互相抵消答案:B2.关于焓的性质, 下列说法中正确的是()(A) 焓是系统内含的热能, 所以常称它为热焓 (B) 焓是能量, 它遵守热力学第一定律(C) 系统的焓值等于内能加体积功 (D) 焓的增量只与系统的始末态有关答案:D。
因焓是状态函数。
3.涉及焓的下列说法中正确的是()(A) 单质的焓值均等于零 (B) 在等温过程中焓变为零 (C) 在绝热可逆过程中焓变为零(D) 化学反应中系统的焓变不一定大于内能变化答案:D。
因为焓变ΔH=ΔU+Δ(pV),可以看出若Δ(pV)<0则ΔH<ΔU。
4.下列哪个封闭体系的内能和焓仅是温度的函数()(A) 理想溶液(B) 稀溶液(C) 所有气体(D) 理想气体答案:D5.与物质的生成热有关的下列表述中不正确的是()(A) 标准状态下单质的生成热都规定为零 (B) 化合物的生成热一定不为零 (C) 很多物质的生成热都不能用实验直接测量(D) 通常所使用的物质的标准生成热数据实际上都是相对值答案:A。
按规定,标准态下最稳定单质的生成热为零。
6.dU=CvdT及dUm=Cv,mdT适用的条件完整地说应当是()(A) 等容过程 (B)无化学反应和相变的等容过程 (C) 组成不变的均相系统的等容过程(D)无化学反应和相变且不做非体积功的任何等容过程及无反应和相变而且系统内能只与温度有关的非等容过程答案:D7.下列过程中, 系统内能变化不为零的是()(A) 不可逆循环过程 (B) 可逆循环过程 (C) 两种理想气体的混合过程 (D)纯液体的真空蒸发过程答案:D。
考研基础物理化学真题2005年

考研基础物理化学真题2005年(总分:150.01,做题时间:90分钟)一、是非题(总题数:12,分数:24.00)1.一定温度下化学反应的Δr G m一定大于Δr A m。
(分数:2.00)A.正确B.错误√解析:既是物质B的化学势又是物质B的偏摩尔量。
(分数:2.00)A.正确√B.错误解析:3.用ΔG<0判断变化方向,适用于任何系统的任何变化。
(分数:2.00)A.正确B.错误√解析:4.稀溶液的凝固点一定比纯溶剂的凝固点低。
(分数:2.00)A.正确B.错误√解析:5.因为溶胶在一定条件下能存在很长时间,所以它是热力学稳定系统。
(分数:2.00)A.正确B.错误√解析:6.在大气压下,水银在玻璃毛细管中的沸点高于其正常沸点。
(分数:2.00)A.正确B.错误√解析:7.NaCl水溶液在表面层的浓度高于其溶液本体浓度。
(分数:2.00)A.正确B.错误√解析:8.物质B总是从高浓度相自发转移到低浓度相。
(分数:2.00)A.正确B.错误√解析:9.在化学反应中,所有反应物分子实现化学反应都经过反应的最低能量途径。
(分数:2.00)A.正确B.错误√解析:10.超电势的存在,使原电池的输出电压变小。
(分数:2.00)A.正确√B.错误解析:11.NaOH水溶液的摩尔电导率与其浓度有关。
(分数:2.00)A.正确√B.错误解析:12.气体在固体表面的吸附只能是单层的。
(分数:2.00)A.正确B.错误√解析:二、选择题(总题数:8,分数:16.00)13.Na 2 CO 3与H 2 O可以生成如下几种化合物Na 2 CO 3·H 2 O,Na 2 CO 3·7H 2 O,Na 2 CO 3·10H 2 O,在标准压力下与Na 2 CO 3水溶液、冰平衡共存的水合物最多能有几种:______(分数:2.00)A.1种;√B.2种;C.3种。
解析:14.在一密闭恒温容器内,有大小不同的两个微小汞滴,经过足够长时间后,容器内仍有液体汞存在。
南京工业大学2009~2010年第一学期物理化学试题A卷

南京⼯业⼤学2009~2010年第⼀学期物理化学试题A卷南京⼯业⼤学物理化学(B )试题(A )卷(闭)2009--2010学年第⼀学期使⽤班级浦⾼材0706班级学号姓名⼀、选择题:(20分)1、⼀理想⽓体在恒定外压为101.325kPa 下,从10L 膨胀到16L ,同时吸热125.6J 、则此过程的△U 为焦⽿?()A 、-248B 、+842C 、-482D 、+4822、理想⽓体从同⼀始态出发,分别经(1)绝热可逆膨胀,(2)多次恒外压膨胀,达到同⼀压⼒值p 2,则焓变()1S ?和()2S 之间有何关系?()A 、()1S ?>()2S ?B 、()1S ?<()2S ?C 、()1S ? =()2S ?D 、()1S ?和()2S ?⽆法确定3、A 和B 形成理想溶液,已知373 K 时纯A 的蒸⽓压为133.32kPa, 纯B 的蒸⽓压为66.66kPa,与此⼆元溶液成平衡的⽓相中的A 摩尔分数为32时,溶液中A 的摩尔分数为()A 、 1B 、 32C 、 21D 、414、化学反应的平衡状态随下列因素当中的哪⼀个⽽改变()A 、系统组成B 、标准态C 、浓度标度D 、化学反应式中的计量系数γB5、在相同条件下有反应式(1)A+B=2C, ()1Θm r G , Θ1K ,(2)1/2 A+1/2B=C, ()2Θm r G , Θ2K ,则对应于(1)和(2)式的标准摩尔吉布斯函变以及标准平衡常数之间的关系为 ( )A 、()1Θm r G =2()2Θm r G ,Θ1K =Θ2KB 、()1Θm r G =2()2Θm r G ,Θ1K = 22)(ΘKC 、()1Θm r G =()2Θm r G ,Θ1K = 22)(ΘKD 、()1Θm r G =()2Θm r G ,Θ1K =Θ2K6、物质A 与B 的系统在蒸馏时可按⼀定⽐例构成低共沸混合物K 。
已知纯物质时,A 与B 的沸点之间的关系为T b (B)>T b(A)。
最新东南大学物理化学(化)考研部分答案(05至10年)答案

1.实验室中某一大恒温槽(例如油浴)的温度为400K,室温为300K。
因恒温槽绝热不良而有4000J的热传给空气,计算说明这一过程是否为可逆?
解:
该过程为不可逆过程。
2.有一绝热体系如图 2.1所示,中间隔板为导热壁,右边容积为左边容积的2倍,已知气体的,试求:(1)不抽掉隔板达平衡后的S。
(2)抽去隔板达平衡后的S。
解:(1)不抽掉隔板最后达热平衡,平衡后的温度为T,设左边为室1,右边为室2:
解出
(2)抽去隔板后的熵变由两部分组成,一部分为上述热熵变化,另一部分
为等温混合熵变。
3.指出下列各过程中,体系的何者为零?
(1)非理想气体卡诺循环;
(2)实际气体节流膨胀;
(3)理想气体真空膨胀;
(4)H2(g)和O2(g)在绝热刚瓶中发生反应生成水;
(5)液态水在373K及101325Pa压力下蒸发成水蒸气。
解:(1)全部为零
(2)=0
(3)
(4)
(5)
4. 若令膨胀系数,,压缩系数,证明
解: (1)
对定量纯物质。
历年物理化学考研题

物理化学考研题1西安交通大学2001年攻读硕士学位研究生入学考试试题一择瓶(请从每个题用给出的几个答案中选择一个最合适的答案,把正确答案的字母填写在駆号后的括号里.每个题1分,共计18分.选错或多选者不能得分但也不倒扣分J】■()—个休系从状态变化到状态2(门““刃人在此过程中啣个量为定值而与此状态变化的路线无关?A.£ pdV R [炭x C f 7'dS D.『学巳()体枳功的计算公式W nRTln普适用于鼻种筒单雙化过程?A*理想气体的各种状态变化. R理想气休的尊温过程.C理想7体等温叩逆过程。
U任材等温可逆过程*玄()菜个尊温恚变化沿可逆路线宪成时•必然A.环境对系统做最小功. 氏系统对环境做最小功*C.系址的嫡值增大" D-累现的甘布斯属數保持不变.4.某电池在一定温度压力下放电时体枳不变•那么在放电过程中以电池为体系时可以肓定A.AS = Q/T KQ= AHG ^JU= Q —nFE D+ AG = — nFE5.()式AH = pr.dT的使用条件只能是」升A.所有的简单变化’R所有的等抵变温过程・G尊压可逆变化过帳。
D.无非体积功的等压变温过程・6・()反应2H E(g)+O i(g) -*2H:O(g)町在T温贬下茅压完成(路线1),也町在丁温度下等容完成{賂线2)・若反应中的气体均可视为理想气休,那么该反应沿上述两条不同路线完成时必然A.Q,j = Qw = AH ⑵C.反应沿路线(1)进行时H2CXg)的平衡产率较低*O反应沿路线(2)进斤时该反应的平術常散校大"7.()在一定温度压力下*A, AG大于莓的过程一定不能发生*li AG小于零的过程一罡能自发进行.C.肖些小于零的过程也能自发进荷*【丄任何态变化的靖变都可以表示为空=QfT*8-(>下列各式那个代表务组分佯系中组分i的化学踞?9.< )反应3C(s) + 2H2O<g)— CH((g) + 2CO(g)无温度丁下的摩尔反应热效应小于冬•如何控制反应条件才会有利干提高CHJg)的平衡产率?A.温度和压力不变•加入不参与反应的局外气体.K压力不变,提高反应温度.C.温度不变,增加压力.D.T温度下将反应物引入崩性绝热反应器进行反应.10.()电极极化的结果必便A.阳极的电极电势升髙.B.阴极的电极电势升高'C.使原电池的阳极电势升為.便电解池的阴极电炒升為.D.使原电池的阴极电衿升宵,使电解池的阳极电势升囱-11.()当把-根毛细管插人某液体时•可能会发生什么现象?已知>“一A.骨内液面岛于管外液面.K裁内液面上的饱和蕉气压髙于借外液面上的饱和蒸气压.C.骨内液面的曲审半径小于零.D.该毛细管材料能被这种液体润湿"12.< )在一定压力F如果反应A— B的4H.与温度无关•那么A.在一定压力HMA)和H m(B)肯定也与温度无关.B.一建压力下^,S m肖定也与温度无关.C.压力不变•升高温度时不会改变该反应的平衡组成"D.若SHm VO•則该反应不论柱什么温度下都能自发进行。
南京工业大学《801高分子化学与物理》历年考研真题专业课考试试题

目 录
2014年南京工业大学801高分子化学与物理考研真题2013年南京工业大学801高分子化学与物理考研真题2012年南京工业大学801高分子化学与物理考研真题2011年南京工业大学801高分子化学与物理考研真题2010年南京工业大学高分子化学与物理考研真题2009年南京工业大学高分子化学与物理考研真题2008年南京工业大学高分子化学与物理考研真题2007年南京工业大学高分子化学与物理考研真题2006年南京工业大学高分子化学与物理考研真题2005年南京工业大学高分子化学与物理考研真题
2014年南京工业大学801高分子化学与物理
考研真题。
