17 生物化学实验--葡萄糖氧化酶法测定血糖含量
葡萄糖氧化酶法测定血糖

900
900
测定管
12 900
900
2. 比色测定:用空白管溶液调零,测定吸光 度(OD500)。
3. 计算: 葡萄糖浓度(mmol/L) = [样品OD/标准管
OD]×标准品葡萄糖浓度
五、注意事项
1. 必须在线性范围内测定: 0.02-20 mmol/L,浓度超 过20 mmol/L用蒸馏水或生理盐水稀释1:2倍后测量;
量程100-1000ul 加样器 配蓝色枪尖 量程0.5-10ul 加样器配白色小枪尖
1.按照下表加样(桔色标记为试剂的简写)
蒸馏水(μl) ddH2O 标准品(μl) SS 样品(μl) B S 反应工作液(μl)2
900
900
37℃孵育15min
二. 实验原理
葡萄糖氧化酶法测定血糖的原理:
根据Trinder反应原理,葡萄糖在葡萄糖氧化酶 (GOD)作用下生成葡萄糖酸和过氧化氢(H2O2); 然后用过氧化物酶(POD)催化过氧化氢,使色 原物质(4-氨基安替比林)生成醌亚胺,由无色 变成粉红色,颜色的深浅与葡萄糖浓度成正比, 在500-505nm处有最大吸收 值。
三、试剂 1.葡萄糖标准品 SS: 5.55 mmol/L; 2.反应工作液WS : 磷酸盐缓冲液,3,5-二氯-2-羟基苯
磺酸钠(DHBS),葡萄糖氧化酶(GOD),过氧化物酶 (POD),色原物质(4-氨基安替比林); 3.待测血清:B S 4. 蒸馏水。ddH2O 实验仪器:可见光分光光度计,水浴锅,微量加样器
1.学习分光光度计的原理及使用方法 2. 掌握葡萄糖氧化酶(Glucose oxidase, GOD)-过氧化物
酶(peroxidase,POD)测定血糖浓度的原理。
葡萄糖氧化酶法测定血糖的原理_概述及解释说明

葡萄糖氧化酶法测定血糖的原理概述及解释说明1. 引言1.1 概述本文旨在介绍葡萄糖氧化酶法测定血糖的原理,并对其进行详细的解释和说明。
血糖测定是医学和生物科学领域中非常重要的一项实验技术,用于评估人体内的葡萄糖水平以及相关代谢功能的异常情况。
葡萄糖氧化酶法是一种常用的血糖测定方法,其基本原理是利用特定酶对葡萄糖进行氧化反应并与辅助试剂发生显色反应,从而间接地测定血液中的葡萄糖含量。
1.2 文章结构本文将按照以下结构进行展开:首先,介绍葡萄糖氧化酶的简要概况和血糖测定方法的总体概述;其次,详细讲解葡萄糖氧化酶法测定血糖的基本原理;然后,描述实验步骤并给出操作流程;接着,分析实验结果并讨论其中的意义和影响因素;最后,总结实验结论并展望未来该领域的研究意义和发展方向。
1.3 目的本文的目的是全面而清晰地介绍葡萄糖氧化酶法测定血糖的原理,帮助读者了解该方法在实际应用中的作用和意义。
通过本文的阅读,读者可以深入了解葡萄糖氧化酶法的基本理论和操作流程,并对实验结果进行准确而详细的分析与讨论。
同时,本文也旨在提供对该方法局限性和未来发展方向进行探讨,并为相关研究人员提供参考,促进该领域的进一步发展和突破。
2. 葡萄糖氧化酶法测定血糖的原理:2.1 葡萄糖氧化酶简介:葡萄糖氧化酶是一种存在于细胞内的酶类,在生物体中起到将葡萄糖转化为能量的重要作用。
该酶主要参与细胞内氧化还原反应,并催化葡萄糖与辅酶NAD+之间的反应。
在此过程中,葡萄糖被氧化成葡萄糖酸,并产生还原型辅酶NADH。
2.2 血糖测定方法概述:血液中的血糖水平是一个重要的生理指标,可以提供人体能量供给的信息。
因此,血糖水平的测定对于诊断和治疗许多代谢性疾病非常重要。
目前,有多种方法用于测定血液中的血糖浓度,其中最常用且最经典的方法就是使用葡萄糖氧化酶法。
2.3 葡萄糖氧化酶法的基本原理:葡萄糖氧化酶法是一种非常敏感和特异性的测定血糖浓度的方法。
该方法基于葡萄糖氧化酶与葡萄糖的特异性反应,通过检测在该反应中生成的还原型辅酶NADH的产生量来间接测定血液中的血糖浓度。
实验血糖测定(葡萄糖氧化酶法)

4.试管50支,
6.记号笔6支
7.蒸馏水1瓶
此范围仅供参考,各实验室须建立本室的参考值范围。
【参考文献】
1.全国临床检验操作规程(第二版),主编:叶应妩,王敏三,1997,P616.
2.Trinder P. Ann Clin Biochem,1969, 6: 24-27.
血糖测定实验所需器材:
1.紫外分光光度计(比色杯光径1.0cm),
2.恒温水浴箱(能调温度的,37C),
>13000U/L
过氧化物酶(POD
>900U/L
R2
磷酸缓冲液(pH7.0)
100mmol/L
酚
11mmol/L
4-氨基安替吡啉
0.77mmol/L
葡萄糖标准液5.55mmol/L(100mg/dl)
【样本】
新鲜无溶血血清。
【步骤】
将10ml R1与90ml R2混合均匀,即为工作液
空白管
校准管
样品管
工作液
1.50 ml
1.50 ml
1.50 ml
蒸馏水
0.01 ml
校准液
0.01 ml
样品
0.01 ml
分别混合均匀,37C水浴10〜15分钟(避免太阳光直射),用波长505nm比色杯光径1.0cm,用空白管调“零”点测定各管的吸光度(A)值。
【计算】
葡萄糖
葡萄桃
【参考值】
血清/血浆:3.89—6.11 mmol/L(70—110mg/dl)。
实验血糖测定(葡萄糖氧化酶法)
【目的】
体外测定血清或血浆中葡萄糖含量。
【临床意义】
17 生物化学实验--葡萄糖氧化酶法测定血糖含量
葡萄糖氧化酶法测定血糖含量【目的】1 .掌握葡萄糖氧化酶法测定血糖含量的实验方法。
2 .熟悉葡萄糖氧化酶法测定血糖含量的实验原理。
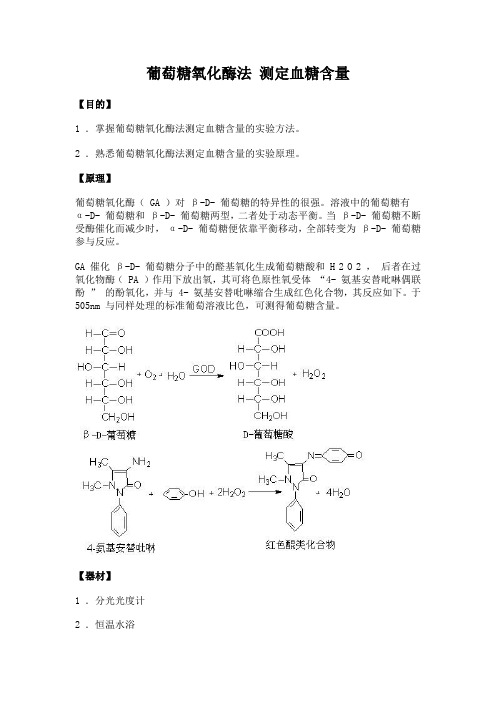
【原理】葡萄糖氧化酶( GA )对β-D- 葡萄糖的特异性的很强。
溶液中的葡萄糖有α-D- 葡萄糖和β-D- 葡萄糖两型,二者处于动态平衡。
当β-D- 葡萄糖不断受酶催化而减少时,α-D- 葡萄糖便依靠平衡移动,全部转变为β-D- 葡萄糖参与反应。
GA 催化β-D- 葡萄糖分子中的醛基氧化生成葡萄糖酸和 H 2 O 2 ,后者在过氧化物酶( PA )作用下放出氧,其可将色原性氧受体“4- 氨基安替吡啉偶联酚” 的酚氧化,并与 4- 氨基安替吡啉缩合生成红色化合物,其反应如下。
于505nm 与同样处理的标准葡萄溶液比色,可测得葡萄糖含量。
【器材】1 .分光光度计2 .恒温水浴3 .微量加样器4 .刻度吸量管5 .中号试管【试剂】1 . 0.01mol/L pH7.0 磷酸盐缓冲液无水 Na 2 HPO 4 18.5g 和 KH 2 PO 4 5.3g 溶于 800ml 蒸馏水中,用少量 1mol/L 的 NaOH 或 HCl 调 pH 至 7.0 ,再加蒸馏水稀释至 1L 。
2 .酶试剂取 GA1200 单位、 PA1200 单位, 4- 氨基安替吡啉 10mg 、叠氮钠 100mg ,加上述磷酸盐缓冲液至 80ml 左右,调 pH 至 7.0 ,再加同上缓冲液至 100ml ,混匀。
冰箱内保存可稳定 3 个月。
3 .酚试剂酚 100mg 溶于 100ml 蒸馏水中。
因酚易在空气中氧化成红色,可先配制成 50g /dl ,贮棕色瓶中,用前稀释。
4 .酶 - 酚混合试剂将试剂 2 、 3 等量混合。
冰箱内保存可稳定 1 个月。
5 .葡萄糖标准贮存液( 20mg/ml )无水 D- 葡萄糖于80 ℃ 烤箱内干燥恒重,冷却后,称取 2.0g 以 0.25% 苯甲酸溶解、稀释定容至 100ml 。
血糖实验报告

一、实验目的1. 了解血糖测定的原理和方法。
2. 掌握葡萄糖氧化酶法测定血糖的步骤和操作技巧。
3. 学会分析实验数据,并得出结论。
二、实验原理血糖是指血液中的葡萄糖含量,是人体重要的能量来源。
血糖浓度的高低直接关系到人体的健康。
葡萄糖氧化酶法是测定血糖的一种常用方法,其原理是葡萄糖氧化酶催化葡萄糖与氧气反应生成葡萄糖酸和过氧化氢,过氧化氢在过氧化物酶的作用下分解产生水和新生态氧,新生态氧与色原性物质反应,产生颜色变化,通过比色法测定葡萄糖浓度。
三、实验器材与试剂1. 器材:葡萄糖氧化酶法血糖测定试剂盒、离心机、移液器、移液管、比色杯、水浴锅、恒温水浴箱、电子天平、白瓷板等。
2. 试剂:葡萄糖标准溶液、葡萄糖氧化酶、过氧化物酶、缓冲液、氧化剂、还原剂等。
四、实验步骤1. 标准曲线的制作(1)取6个比色杯,分别加入0、0.1、0.2、0.3、0.4、0.5毫升的葡萄糖标准溶液,用缓冲液定容至1毫升。
(2)在每个比色杯中加入相应的酶试剂,混匀。
(3)将比色杯放入水浴锅中,恒温反应10分钟。
(4)取出比色杯,用移液器加入还原剂,混匀。
(5)在波长540nm下,用比色杯测定吸光度,以葡萄糖浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
2. 血糖测定(1)取5个比色杯,分别加入0.1毫升待测血清或血浆,用缓冲液定容至1毫升。
(2)在每个比色杯中加入相应的酶试剂,混匀。
(3)将比色杯放入水浴锅中,恒温反应10分钟。
(4)取出比色杯,用移液器加入还原剂,混匀。
(5)在波长540nm下,用比色杯测定吸光度。
(6)根据标准曲线,计算待测血清或血浆中的葡萄糖浓度。
五、实验结果与分析1. 标准曲线的制作根据实验数据,绘制标准曲线,得出线性方程:y = 0.0245x + 0.0043,相关系数R² = 0.9987。
2. 血糖测定根据实验数据,计算待测血清或血浆中的葡萄糖浓度,结果如下:- 血清A:5.2 mmol/L- 血清B:4.8 mmol/L- 血清C:6.0 mmol/L- 血浆D:5.5 mmol/L- 血浆E:4.9 mmol/L六、实验结论通过本次实验,我们成功掌握了葡萄糖氧化酶法测定血糖的原理和步骤。
葡萄糖氧化酶法测空腹血糖(标准管法)

葡萄糖氧化酶法测空腹血糖(标准管法)实验目的:1.了解自动生化分析仪的工作原理2.熟悉糖尿病相关生化的检测项目及检测方法3.掌握糖尿病相关生化检测项目的临床意义。
实验原理:葡萄糖氧化酶法测空腹血糖:葡萄糖可由葡萄糖氧化酶氧化成葡萄糖酸并产生过氧化氢,后者与苯酚及4-氨基安替比林在过氧化物酶作用下产生红色化合物。
在505nm波长测定该红色化合物的吸光度,能计算出葡萄糖含量。
实验操作:1.将准备好的酶工作液(葡萄糖氧化酶和过氧化物酶、苯酚、4-氨基安替比林)加入空白管、浓度标准管、测定管各3ml,再向标准管加20μl葡萄糖标准液(5.55mmol/L),再向测定管加入20μl血清。
2.将三支试管放入水浴锅中,37℃保温20分钟3.调节分光光度计波长505nm,透光度T至100%,将空白管酶工作液对光的吸收调节为0,再用空白管调“零”点测定其他各管的吸光度。
实验结果:分光光度计测得标准管吸光度和测定管吸光度,根据朗伯-比尔定律,得到血清样品血糖值=(测定管吸光度/标准管吸光度)x5.55分析讨论:酶酚混合液变成了红色是否还可以继续使用?不可以。
酶酚混合液应为无色,如酶酚混合液已经变为红色,说明试剂污染,不可使用。
思考题:1.高血糖对机体的影响有哪些?1)引起血管、神经并发症。
糖尿病患者长期高血糖会使血管、神经并发症发生和发展使病情加重。
2)β细胞功能衰竭。
长期高血糖对胰岛β细胞不断刺激,使其功能衰竭,胰岛素分泌更少。
3)电解质紊乱。
高血糖时大量排尿,从尿带走电解质,使电解质紊乱。
4)严重失水。
高血糖引起渗透性利尿,尿量增加,机体失水。
5)渗透压增高。
高血糖时,细胞外液渗透压增高,细胞内液向细胞外流动,导致细胞内失水。
当脑细胞失水时,可引起脑功能紊乱,临床上称高渗性昏迷。
6)全身乏力。
血糖过高,葡萄糖不能很好地被机体吸收利用而从尿中排出。
7)视力减退。
血糖升高时,眼睛视力往往减退。
2.糖尿病患者为何会出现尿糖阳性?糖尿病患者的血糖超过肾糖阈(8.96~10.08mmol/L)时,近端小管对葡萄糖的重吸收达到极限,尿中开始出现葡萄糖。
血糖的定量测定(葡萄糖氧化酶法)

血糖的定量测定(葡萄糖氧化酶法)血糖是指血液中葡萄糖的含量。
葡萄糖是人体主要的能量来源,血糖的测定是检查人体内部能量代谢状态的重要项目之一。
这篇文章将介绍血糖定量测定的实验原理、方法以及实验注意事项。
一、实验原理血糖的定量测定方法主要是利用葡萄糖氧化酶将血液中的葡萄糖在催化反应下转化为过氧化氢和D-酮糖酸,利用过氧化氢的比色法来测定血糖的含量。
具体反应式为:(1)葡萄糖+O2+H2O→葡萄糖氧化酶 D-酮糖酸+H2O2(2)2H2O2+Fe2+→2H2O+Fe3++O2(3)Fe3++TSC(三硝基苯胺)→FeTSC3(红色化合物)其中,TSC(三硝基苯胺)为过氧化氢的比色试剂,用Fe2+作催化剂促进反应进行,所生成的红色化合物FeTSC3与过氧化氢的浓度呈线性关系。
二、实验材料1.血糖标准品:10mmol/L2.葡萄糖氧化酶3.三硝基苯胺(TSC)、醋酸钠、乙二胺四醋酸盐二水合物(EDTA•2H2O)、氢氧化钠(NaOH)4.0.1mol/L磷酸盐缓冲液(pH7.5)5.准确量杯、试管、离心管、吸光度计、恒温水浴器、移液管三、实验步骤1.制备血清样品:将血液放置静置后离心取血清,制成5mmol/L、10mmol/L、15mmol/L、20mmol/L的葡萄糖标准品。
2.实验组织:3个组别,每组3个试管。
A组:加1mL的10mmol/L葡萄糖标准品;B 组:加1mL的血清标本;C组:加入1mL的磷酸盐缓冲液作为对照组。
注意,每组要做三个平行实验。
3.反应体系准备:①将实验组织中的标准品、血清样本和磷酸盐缓冲液分别加入3毫升离心管中。
②分别加入1mL葡萄糖氧化酶。
③分别加入1mL EDTA全部气泡排除。
⑤每组混合后放置在37℃下反应20分钟。
⑥在上述反应过程中,加入2毫升0.1mol/L的NaOH溶液使溶液呈碱性,使催化反应更为稳定。
4.吸光测定:将反应充分混合后,吸取适量的样品,放到吸光度计槽,设定波长为505nm,用对照组值进行比较,计算出各组的吸光度,并根据标准曲线计算出各样本的葡萄糖含量。
生化血糖测定实验报告

生化血糖测定实验报告实验目的,通过实验,掌握生化血糖测定的原理和方法,加深对血糖代谢的理解。
实验仪器与试剂,血糖仪、血糖试剂盒、手套、酒精棉球、生理盐水、实验动物(小鼠)。
实验原理,血糖是人体内最主要的能量来源,其浓度的变化与糖尿病等疾病密切相关。
本实验采用葡萄糖氧化酶法测定血糖浓度,其原理是将血液样品与葡萄糖氧化酶反应,生成过氧化氢,再与对苯二胺反应生成可检测的有色产物,通过检测产物的光密度来计算血糖浓度。
实验步骤:1. 实验前准备,将血糖试剂盒从4°C冰箱取出,放置室温下恢复30分钟。
准备实验动物,取血糖试剂盒中的试剂和标准品。
2. 采血,用手套和酒精棉球进行消毒,取小鼠尾部进行采血。
3. 血糖测定,将采集的血液滴在试剂盒上,按照说明书操作血糖仪进行测定。
4. 数据记录,记录测定结果,包括标准品的测定值和实验动物的测定值。
实验结果,通过实验测定,得到了实验动物血糖浓度的数据。
根据实验结果,可以分析出实验动物的血糖水平,从而对其血糖代谢情况进行评估。
实验结论,本实验通过生化血糖测定,掌握了血糖测定的原理和方法,加深了对血糖代谢的理解。
实验结果对于研究血糖代谢相关疾病具有一定的参考价值。
实验注意事项:1. 实验中需注意动物的福利,遵守动物实验伦理规范。
2. 操作过程中需注意个人安全防护,避免血液接触和溶液飞溅。
3. 实验仪器和试剂的使用应按照说明书进行,避免误操作。
本实验不仅加深了对生化血糖测定原理和方法的理解,也为今后的相关研究提供了重要的实验数据支持。
通过本次实验,对血糖代谢相关疾病的研究有了更深入的了解,也为今后的相关研究工作打下了坚实的基础。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
葡萄糖氧化酶法测定血糖含量
【目的】
1 .掌握葡萄糖氧化酶法测定血糖含量的实验方法。
2 .熟悉葡萄糖氧化酶法测定血糖含量的实验原理。
【原理】
葡萄糖氧化酶( GA )对β-D- 葡萄糖的特异性的很强。
溶液中的葡萄糖有α-D- 葡萄糖和β-D- 葡萄糖两型,二者处于动态平衡。
当β-D- 葡萄糖不断受酶催化而减少时,α-D- 葡萄糖便依靠平衡移动,全部转变为β-D- 葡萄糖参与反应。
GA 催化β-D- 葡萄糖分子中的醛基氧化生成葡萄糖酸和 H 2 O 2 ,后者在过氧化物酶( PA )作用下放出氧,其可将色原性氧受体“4- 氨基安替吡啉偶联酚” 的酚氧化,并与 4- 氨基安替吡啉缩合生成红色化合物,其反应如下。
于505nm 与同样处理的标准葡萄溶液比色,可测得葡萄糖含量。
【器材】
1 .分光光度计
2 .恒温水浴
3 .微量加样器
4 .刻度吸量管
5 .中号试管
【试剂】
1 . 0.01mol/L pH7.0 磷酸盐缓冲液
无水 Na 2 HPO 4 18.5g 和 KH 2 PO 4 5.3g 溶于 800ml 蒸馏水中,用少量 1mol/L 的 NaOH 或 HCl 调 pH 至 7.0 ,再加蒸馏水稀释至 1L 。
2 .酶试剂
取 GA1200 单位、 PA1200 单位, 4- 氨基安替吡啉 10mg 、叠氮钠 100mg ,加上述磷酸盐缓冲液至 80ml 左右,调 pH 至 7.0 ,再加同上缓冲液至 100ml ,混匀。
冰箱内保存可稳定 3 个月。
3 .酚试剂
酚 100mg 溶于 100ml 蒸馏水中。
因酚易在空气中氧化成红色,可先配制成 50g /dl ,贮棕色瓶中,用前稀释。
4 .酶 - 酚混合试剂
将试剂 2 、 3 等量混合。
冰箱内保存可稳定 1 个月。
5 .葡萄糖标准贮存液( 20mg/ml )
无水 D- 葡萄糖于80 ℃ 烤箱内干燥恒重,冷却后,称取 2.0g 以 0.25% 苯甲酸溶解、稀释定容至 100ml 。
6 .葡萄糖应用标准液( 100mg/dl )
取葡萄糖标准液 5ml ,加 0.25% 苯甲酸溶液稀释定容至 100ml 。
7 .蛋白沉淀剂
溶解 Na 2 HPO 4 10g 、 Na 2 WO 4 10g 、 NaCl 19g 于 800ml 蒸馏水中,加入 1mol/LHCl 125ml ,加蒸馏水至 1 000ml 混匀。
【操作】
1 .血浆直接测定
取试管 3 只,标明测定、标准、空白,分别加入血清 20μl ,磷酸盐缓冲液20μl ,然后各管均加酶 - 酚混合剂各 3ml ,混匀后将 3 管同时置37 ℃ 水浴保温 15 min ,到时取出冷却。
用 505nm 波长,以空白管调整零,读取各管吸光度值。
2 .全血去蛋白血滤液测定
取蛋白沉淀剂 1ml 加全血 50μl 混匀,放置 7 分钟后,离心取上清 0.5ml 于测定管内;取蛋白沉淀剂 1ml 加葡萄糖应用标准液 50μl ,混匀后从中取
0.5ml 于标准管内;另取蛋白沉淀剂 0.5ml 于空白管内。
以上三管各加酶 - 酚混合试剂 3ml ,各管分别混匀同时放入37 ℃ 水恒温箱浴保温 15 min 后,取出如前比色测定。
【计算】
血糖浓度( mg/dl )=
血糖浓度 ( mmol/L) =
【注意事项】
1 .葡萄糖氧化酶法测糖,色原性氧受体种类较多,以往曾多用邻联茴香胺等,因其有轻微致癌作用,现已很少应用。
本实验介绍的方法为卫生部临床检验中心所推荐,该法测糖显色灵敏且稳定。
2 .无水葡萄糖结晶属于α-D 型,溶于水中,部分葡萄糖发生变旋光作用,形成β型, 2 小时后α与β比例达成平衡,α型占 36% ,β型占 64% 。
因此葡萄糖标准液需在葡萄糖溶解 2 小时后才能应用。
3 .该酶法测糖特异性高,且干扰测定结果的特质较少。
当溶血标本 Hb 达到 1g /dl ,黄疸标本胆红素浓度达到 20mgr/dl 时,都不大影响测定结果。
样品中加入抗凝剂或糖分解抑制剂如草酸钾浓度达到 20mg/dl 、脚素达 60mg/dl 、 NaF 达 200mg/dl 时,均不干扰测定结果。
标本中尿素达 280mg/dl 、甘油三酯达500mg/dl 时对测定结果无影响。
而维生素 C 及谷胱甘肽等还原性物质可引起结果的负误差。
4 .本法测糖的线性范围宽,至少可达 20mmol/L ( 360mg/dl )。
5 .本法测定血糖正常值为 70 ~ 110 mg/dl 或 3.9 ~ 6.1mmol/L 。
【思考题】
1 .酶试剂为什么要用磷酸盐缓冲液配制,而不用蒸馏水配制?
2 .试分析影响本实验的因素有哪些,为什么?。
