苯环上的取代定位规则
二取代苯的定位规律

二取代苯的定位规律(有机化学基础知识)如果苯环上已经有了两个取代基,当引入第三个取代基时,影响第三个取代基进入的位置的因素较多。
医学教|育网收集整理定性地说,两个取代基对反应活性的影响有加和性。
1.苯环上已有两个邻对位定位取代基或两个间位定位取代基,当这两个定位取代基的定位方向有矛盾时,第三个取代基进入的位置,主要由定位作用较强的一个来决定。
2.苯环上己有一个邻对位定位取代基和一个间位定位取代基,且二者的定位方向相反,这时主要由邻对位定位取代基来决定第三个取代基进入的位置。
3.两个定位取代基在苯环的1位和3位时,由于空间位阻的关系,第三个取代基在2位发生取代反应的比例较小。
苯环的取代定位规律的解释(有机化学基础知识)当苯环上连有定位取代基时,苯环上电子云密度的分布就发生变化。
这种影响可沿着苯环的共轭链传递。
因此共轭链上就出现电子云密度较大和电子云密度较小的交替现象,从而使它表现出定位效应。
①邻对位定位取代基的定位效应:邻对位定位取代基除卤素外,其它的多是斥电子的基团,能使定位取代基的邻对位的碳原子的电子云密度增高,所以亲电试剂容易进攻这两个位置的碳原子。
卤素和苯环相连时,与苯酚羟基相似,也有方向相反的吸电子诱导和共轭两种效应。
医学教|育网收集整理但在此情况下,诱导效应占优势,使苯环上电子云密度降低,苯环钝化,故亲电取代反应比苯难。
但共轭使间位电子云密度降低的程度比邻对位更明显,所以取代反应主要在邻对位进行。
②间位定位基的定位效应:这类定位取代基是吸电子的基团,使苯环上的电子云移向这些基团,因此苯环上的电子云密度降低。
这样,对苯环起了钝化作用,所以较苯难于进行亲电取代反应。
③共振理论对定位效应的解释:邻对位中间体均有一种稳定的共振式(邻对位定位基的影响)。
在间位定位基的影响下,在三个可能的碳正离子中间体中,邻对位共振式中正电荷是在连有吸电子基的碳上,它使碳正离子中间体更不稳定。
所以间位碳正离子中间体是最有利的。
第4.1节 苯及其同系物(2)
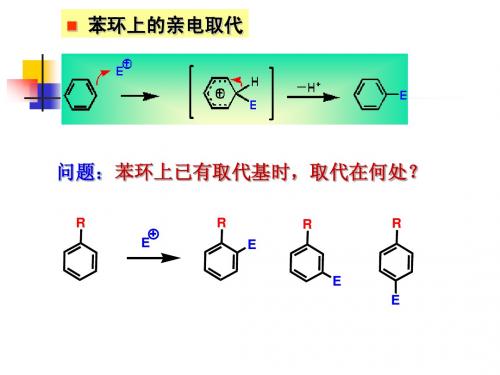
2个邻对位定位基 -OH > -CH3 个邻对位定位基
2个间位定位基 个间位定位基 -NO2> -COOH
若定位效应差别不大时,得混合物。 若定位效应差别不大时,得混合物。 差别不大时
OH
OCH3
NH2 Cl
COOH
Cl
CH3 CH3O- > -CH3 -NH2 > -Cl
NO2 -NO2 > -COOH
取代基对亲电取代的影响
R HNO3 / H2SO4 R NO2 + NO2 + NO2 R R
一些实验结果
R H CH3 Cl NO2 反应温度 55~60oC 30oC 60~70oC 95oC 58% 30% 6% 38% 70% 1% 4% 微量 93% 邻位取代 对位取代 间位取代 反应速度 1 25 0.03 10-4
注意: 属于邻 对位定位基, 使苯环略微钝化, 属于邻、 注意:-X属于邻、对位定位基,但使苯环略微钝化,
取代反应比苯难进行。 取代反应比苯难进行。
间位定位基( ★ 间位定位基( meta direction orienting group) ——第2类定位基 使新引入的第2 使新引入的第2个取代基主要进 入原基团间位( 入原基团间位(间位产物大于 50%),且钝化苯环,使亲电取代 ),且钝化苯环 ),且钝化苯环, 反应比苯难进行。 反应比苯难进行。 例如: 例如: -N+(CH3)3
其它的邻对位定位基
O-N(CH3)2 -NH2 -OH -OCH3 -NH-COCH3 -X
氨基 羟基 甲氧基 乙酰氨基 卤素
氧负离子 二甲氨基
与苯环也有p-π共轭效应(+C),且 +C>-I。 与苯环也有 π共轭效应 + , > 。
二取代苯的定位规律

二取代苯的定位规律(有机化学基础知识)如果苯环上已经有了两个取代基,当引入第三个取代基时,影响第三个取代基进入的位置的因素较多。
医学教|育网收集整理定性地说,两个取代基对反应活性的影响有加和性。
1.苯环上已有两个邻对位定位取代基或两个间位定位取代基,当这两个定位取代基的定位方向有矛盾时,第三个取代基进入的位置,主要由定位作用较强的一个来决定。
2.苯环上己有一个邻对位定位取代基和一个间位定位取代基,且二者的定位方向相反,这时主要由邻对位定位取代基来决定第三个取代基进入的位置。
3.两个定位取代基在苯环的1位和3位时,由于空间位阻的关系,第三个取代基在2位发生取代反应的比例较小。
苯环的取代定位规律的解释(有机化学基础知识)当苯环上连有定位取代基时,苯环上电子云密度的分布就发生变化。
这种影响可沿着苯环的共轭链传递。
因此共轭链上就出现电子云密度较大和电子云密度较小的交替现象,从而使它表现出定位效应。
①邻对位定位取代基的定位效应:邻对位定位取代基除卤素外,其它的多是斥电子的基团,能使定位取代基的邻对位的碳原子的电子云密度增高,所以亲电试剂容易进攻这两个位置的碳原子。
卤素和苯环相连时,与苯酚羟基相似,也有方向相反的吸电子诱导和共轭两种效应。
医学教|育网收集整理但在此情况下,诱导效应占优势,使苯环上电子云密度降低,苯环钝化,故亲电取代反应比苯难。
但共轭使间位电子云密度降低的程度比邻对位更明显,所以取代反应主要在邻对位进行。
②间位定位基的定位效应:这类定位取代基是吸电子的基团,使苯环上的电子云移向这些基团,因此苯环上的电子云密度降低。
这样,对苯环起了钝化作用,所以较苯难于进行亲电取代反应。
③共振理论对定位效应的解释:邻对位中间体均有一种稳定的共振式(邻对位定位基的影响)。
在间位定位基的影响下,在三个可能的碳正离子中间体中,邻对位共振式中正电荷是在连有吸电子基的碳上,它使碳正离子中间体更不稳定。
所以间位碳正离子中间体是最有利的。
苯环定位规则

苯环上原有的取代基对新导入取代基有影响,这种影响包括反应活性和进入位置两个方面。
通常,苯环上原有的第一取代基称为定位基,从大量实验事实的分析总结中发现,定位基的定位作用遵循一定的规律,这一规律称为苯环上亲电取代反应定位规律(又称定位规则)。
下面分别讨论定位基的类型;定位规则的理论解释;二元取代苯的定位规律;定位规律的应用。
(一)定位基的类型1.邻、对位定位基。
这类定位基的结构特征是定位基中与苯环直接相连的原子不含不饱和键(芳烃基例外),不带正电荷,且多数具有未共用电子对。
常见的邻、对位定位基及其反应活性(相对苯而言)如下:强致活基团:―NH2(―NHR,―NR2),―OH中致活基团:―OCH3(―OR),―NHCOCH3(-NHCOR)弱致活基团:―ph(―Ar),―CH3(-R)弱致钝基团:―F,―Cl,―Br,―I这类定位基多数使亲电取代反应较苯容易进行,但卤素例外。
2.间位定位基。
这类定位基的结构特征是定位基中与苯环直接相连的原子一般都含有不饱和键(-CX3例外)或带正电荷。
常见的间位定位基及其定位效应从强到弱顺序如下:―N+H3,―N+R3,―NO2,―CF3,―CCl3,―CN,―SO3H,―COH,―COR,―COOH,―COOR,―CONH2等。
这类定位基属致钝基团,通常使苯环上亲电取代反应较苯难进行,且排在越前面的定位基,定位效应越强,反应也越难进行。
(二)定位规则的理论解释苯环上的取代反应是亲电取代反应。
因此,从反应活性的角度分析,凡有助于提高苯环上电子云密度的基团,就能使苯环活化,反应活性提高;反之,凡是使环上电子云密度降低的基团,就能使苯环钝化,反应活性降低。
从反应位置的角度分析,当苯环上没有取代基时,环上六个碳原子的电子云密度是均等的;但当苯环上有取代基时,由于取代基的电子效应沿着苯环共轭体系传递。
在环上出现了出现了电子云密度的疏密交替分布现象。
第二个取代基总是进入苯环上电子云密度相对较大的部位,从而使这些碳原子上的取代物占了多数。
二取代苯的定位规律

二取代苯的定位规律(有机化学基础知识)如果苯环上已经有了两个取代基,当引入第三个取代基时,影响第三个取代基进入的位置的因素较多。
医学教|育网收集整理定性地说,两个取代基对反应活性的影响有加和性。
1.苯环上已有两个邻对位定位取代基或两个间位定位取代基,当这两个定位取代基的定位方向有矛盾时,第三个取代基进入的位置,主要由定位作用较强的一个来决定。
2.苯环上己有一个邻对位定位取代基和一个间位定位取代基,且二者的定位方向相反,这时主要由邻对位定位取代基来决定第三个取代基进入的位置。
3.两个定位取代基在苯环的1位和3位时,由于空间位阻的关系,第三个取代基在2位发生取代反应的比例较小。
苯环的取代定位规律的解释(有机化学基础知识)当苯环上连有定位取代基时,苯环上电子云密度的分布就发生变化。
这种影响可沿着苯环的共轭链传递。
因此共轭链上就出现电子云密度较大和电子云密度较小的交替现象,从而使它表现出定位效应。
①邻对位定位取代基的定位效应:邻对位定位取代基除卤素外,其它的多是斥电子的基团,能使定位取代基的邻对位的碳原子的电子云密度增高,所以亲电试剂容易进攻这两个位置的碳原子。
卤素和苯环相连时,与苯酚羟基相似,也有方向相反的吸电子诱导和共轭两种效应。
医学教|育网收集整理但在此情况下,诱导效应占优势,使苯环上电子云密度降低,苯环钝化,故亲电取代反应比苯难。
但共轭使间位电子云密度降低的程度比邻对位更明显,所以取代反应主要在邻对位进行。
②间位定位基的定位效应:这类定位取代基是吸电子的基团,使苯环上的电子云移向这些基团,因此苯环上的电子云密度降低。
这样,对苯环起了钝化作用,所以较苯难于进行亲电取代反应。
③共振理论对定位效应的解释:邻对位中间体均有一种稳定的共振式(邻对位定位基的影响)。
在间位定位基的影响下,在三个可能的碳正离子中间体中,邻对位共振式中正电荷是在连有吸电子基的碳上,它使碳正离子中间体更不稳定。
所以间位碳正离子中间体是最有利的。
苯及苯环上的亲电取代反应
五、定位规则在有机合成上的应用
CH3 NO2
例一:由
合成
CH3 CH3Cl AlCl3 con H2SO4 100 。 C
CH3 混酸 SO3H
CH3 NO2
SO3H
CH3 dil H2SO4 NO2
例二: 由 O2N
路线一:
O2N CH3 混酸 O2N
CH3 合成 O2N
COOH NO2
CH3 NO2
Cl2 h
CH2CH3
Br2 h
CHCH3 + Cl 56%
CH2CH2Cl 44%
CHCH3 (用NBS / CCl4亦可) Br 100%
溴代比氯代的选择性更高
注意α-H的卤代反应条件与苯环上的卤代反应条件 是不相同的,不可混淆。
四、取代苯的亲电取代反应的活性和定位规律
1、取代基定位及活化、钝化作用 *** 第一类定位基
HOOC NO2 COOH O2N
三、非苯系芳香烃
C H3 C H2C H2C C H 3 C l C HC H 3 C H3
AlCl 3
C H3 C H3
分子内烷基化
C H2C H2C H2 C C l
=
O
AlCl 3
分子内酰基化
=
O
不同点
a. 烷基化反应难停留在一取代阶段,而 酰基化反应却可以停留在一取代阶段。
C H3
CH3Cl AlCl 3 CH3Cl AlCl 3
在极性溶剂中,萘的酰基化产物以β-异构体为主;在非 极性溶剂中以α-异构体为主。
CH2COOH + ClCH2COOH FeCl3 KBr 。C 200-218
工业上用于制备α-萘乙酸(一种植物生长激素)
苯环上的取代定位规则

苯环上的【2 】代替定位规矩大量试验事实表明,当一些基团处于苯环上时,苯环的亲电代替反响会变得轻易进行,同时指使再进入的基团将衔接在它的邻位或对位.例如,当苯环上已消失一个甲基时(即甲苯),它的卤化.硝化和磺化等反响,反响温度均远低于苯,且新基团的导入均进入苯环上甲基的邻或对位:甲基的这种感化称为定位效应.在这里甲基是一个邻.对位指向基,具有活化苯环的感化,称为活化基.相似的活化基团还有很多,它们也被称为第一类代替基,并按活化才能由大到小的次序分列如下:-NH2,-NHR,-NR2,-OH>-NHCOR,-OR,>-R,-Ph>-X处于这一次序最末的卤素是个特例.它一方面是邻.对位指向基,另一方面又是使苯环致钝的基团,这是因为卤素的电负性弘远于碳,是以其吸电子效应已超过了本身的供电子才能,这就使环上的电子云密度比卤素进入前有所下降,因而使亲电试剂的进攻显得不力.此称为钝化感化.还有很多比卤素致钝力更强,并且使再进基团进入间位的代替基,它们被称为间位指导基或第二类代替基,按其致钝才能由大到小的次序分列如下:-NR3+,-NO2,-CF3,-CCl3>-CN,-SO3H,-CH=O,-COR,-COOH,-COOR 常见的代替基的定位感化见表邻对位定位基间位定位基活化苯环钝化苯环-NR2 -NR2 -NHR-NH2-OH-OCH3 -NHCOR-CH3-C2H5 -CH(CH3)2 -C(CH3)2-Ar(-H)(-H)(-H)-CH2Cl-CH2Cl-F-Cl-Br-I-NO2-CN-SO3H-CHO-COCH3-COOH-COOR-CONH2因为代替基的指向和活化或钝化感化,在合成一个指定化合物时,采取哪种路线就必须事先作周全斟酌.如:欲合成下列化合物时,显然b-路线是合理的.假如以苯为原料,欲合成对-硝基苯甲酸(此物资在后面章节将学到)时,则应当先对苯进行甲基化后再进行硝化,最后将甲基氧化:。
苯环上亲电取代反应的定位规律

HNO3 , H2SO4 30℃ ~60℃
NO2
•磺化 低温(80℃)与浓硫酸生成﹣萘磺酸;高温(165℃)
生成﹣萘磺酸。 ﹣萘磺酸与硫酸共热,也转变为﹣萘磺酸。
+ H 2SO4
80℃ 165℃
SO3H (>95 %)
SO3H (>85 %)
原因:磺酸基体积大,与8位氢原子间距小于其范德华半径之和
•分子式:C10H8;由两个苯环共用两个碳原子并联而成。
•结构:
0.142 0.136
0.1390.140
( 单 位n:m)
8α 7β
6β 5α
1α 2β
3β 4α
——两个苯环共平面;C—C键长介于C—C单键和C = C双键之间 (碳碳单键154pm长,双键134pm长);C—C键键长并不完全相同;
,故﹣萘磺酸稳定性小于﹣萘磺酸。
空间作用大(不稳定) H SO3H
空间作用小(稳定) H
SO3H
H
﹣萘磺酸动力学,﹣萘磺酸热力学控制。﹣萘磺酸是重要的
有机合成中间体,可转化为﹣萘酚、 2020/3/11
﹣萘胺等(合成偶氮染料13的
中间体)。
•酰基化(傅﹣克反应)
——概况 萘的酰基化反应产物与温度和溶剂的极性有关。低温和
NO2 还原
氧化
NO2 COOH COOH
2020/3/11
17
(c)还原反应
用金属钠在液氨和乙醇的混合液中还原生成1,4﹣二氢萘。产物中 的一个孤立双键不被还原。
Na , C2H5OH NH3 (液 )
催 化 加 氢 时 , 可 生 成 1,2,3,4 四 氢 化 萘 ( 又 称 萘 满 ) 或 十 氢 化 萘 (又称萘烷)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
苯环上的取代定位规则
大量实验事实表明,当一些基团处于苯环上时,苯环的亲电取代反应会变得容易进行,同时指使再进入的基团将连接在它的邻位或对位。
例如,当苯环上已存在一个甲基时(即甲苯),它的卤化、硝化和磺化等反应,反应温度均远低于苯,且新基团的导入均进入苯环上甲基的邻或对位:
甲基的这种作用称为定位效应。
在这里甲基是一个邻、对位指向基,具有活化苯环的作用,称为活化基。
类似的活化基团还有许多,它们也被称为第一类取代基,并按活化能力由大到小的顺序排列如下:
-NH2,-NHR,-NR2,-OH>-NHCOR,-OR,>-R,-Ph>-X
处于这一顺序最末的卤素是个特例。
它一方面是邻、对位指向基,另一方面又是使苯环致钝的基团,这是由于卤素的电负性远大于碳,因此其吸电子效应已超过了本身的供电子能力,这就使环上的电子云
密度比卤素进入前有所降低,因而使亲电试剂的进攻显得不力。
此称为钝化作用。
还有许多比卤素致钝力更强,而且使再进基团进入间位的取代基,它们被称为间位指示基或第二类取代基,按其致钝能力由大到小的顺序排列如下:
-NR3+,-NO2,-CF3,-CCl3>-CN,-SO3H,-CH=O,-COR,-COOH,-COOR
常见的取代基的定位作用见表
-OCH3
-NHCOR
-CH3
-C2H5
-CH(CH3)2 -C(CH3)2 -Ar
(-H)-Cl
-Br
-I
?
?
?
?
?
-COCH3
-COOH
-COOR
-CONH2
?
?
?
?
由于取代基的指向和活化或钝化作用,在合成一个指定化合物时,采取哪种路线就必须事先作全面考虑。
如:欲合成下列化合物时,显然b-路线是合理的。
如果以苯为原料,欲合成对-硝基苯甲酸(此物质在后面章节将学到)时,则应该先对苯进行甲基化后再进行硝化,最后将甲基氧化:。
