化工热力学 第3章例题
化工热力学 第三章(魏顺安课后习题)

实际态 T、p
真实气体 H、S
1
理想气体 H 、S 基准态 T0、p 0
* 0
3
* 0
2
理想气体 H*、S* 实际态 T、p
1 2 3 因 p 0 1atm, 所 1 0 为 以 2 3
• 气体在基准态下的 H0和S0 是相对值:
e 0.78785 f P 1.5962 MPa
0.23845
普遍化方程
BPc P r Z 1 RTc Tr BPc B 0 B1 RTc
成于勤,毁于惰, 荒于嬉,败于奢
pr 0 1 ln i B B Tr
铁可磨,石可穿, 攻必克,胜必谦
H0 0
S0 0
id R
• 从设计过程可知:
H H0 H H2 H3 nH nH
id
S S0 S S2 S3 nS nS
1cal( 热力学 ) 4.184J
R
• 为方便后面求解,现将摩尔等压热容进行单位换算。
Cp (0.886 5.602 102 T 2.771 105 T 2 5.266 109 T 3 ) 4.184 3.707 0.2344 1.159 10 4 T 2 2.203 10 8 T 3 ( J .mol1 . K 1 ) T
ZRT 0.65500 8.314 410 Vm 0.40806 10 3 m 3 .mol1 p 5471.55 103
V nVm 1 0.40806 103 4.0806 104 m 3
• (2) 求H、S
设计如下热力学过程:
化工热力学
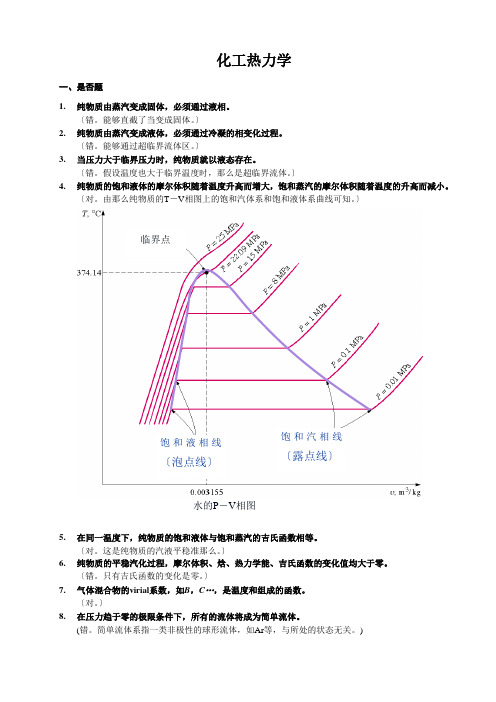
化工热力学一、是否题1. 纯物质由蒸汽变成固体,必须通过液相。
〔错。
能够直截了当变成固体。
〕2. 纯物质由蒸汽变成液体,必须通过冷凝的相变化过程。
〔错。
能够通过超临界流体区。
〕3. 当压力大于临界压力时,纯物质就以液态存在。
〔错。
假设温度也大于临界温度时,那么是超临界流体。
〕4. 纯物质的饱和液体的摩尔体积随着温度升高而增大,饱和蒸汽的摩尔体积随着温度的升高而减小。
〔对。
由那么纯物质的T -V 相图上的饱和汽体系和饱和液体系曲线可知。
〕5. 在同一温度下,纯物质的饱和液体与饱和蒸汽的吉氏函数相等。
〔对。
这是纯物质的汽液平稳准那么。
〕6. 纯物质的平稳汽化过程,摩尔体积、焓、热力学能、吉氏函数的变化值均大于零。
〔错。
只有吉氏函数的变化是零。
〕 7. 气体混合物的virial 系数,如B ,C …,是温度和组成的函数。
〔对。
〕8. 在压力趋于零的极限条件下,所有的流体将成为简单流体。
(错。
简单流体系指一类非极性的球形流体,如Ar 等,与所处的状态无关。
)饱和液相线〔泡点线〕饱和汽相线〔露点线〕水的P -V 相图 临界点二、选择题1. 指定温度下的纯物质,当压力低于该温度下的饱和蒸汽压时,那么气体的状态为〔 〕(C 。
参考P -V 图上的亚临界等温线。
)A. 饱和蒸汽B. 超临界流体C. 过热蒸汽2. T 温度下的过冷纯液体的压力P〔A 。
参考P -V 图上的亚临界等温线。
〕 3. T 温度下的过热纯蒸汽的压力P〔B 。
参考P -V 图上的亚临界等温线。
〕 4. 纯物质的第二virial 系数B〔A 。
virial 系数表示了分子间的相互作用,仅是温度的函数。
〕5. 能表达流体在临界点的P-V 等温线的正确趋势的virial 方程,必须至少用到〔A 。
要表示出等温线在临界点的拐点特点,要求关于V 的立方型方程〕 6. 关于纯物质,一定温度下的泡点压力与露点压力是 (A) A 相同的 B 不同的7. 关于纯物质,一定温度下泡点与露点,在P -T 图上是 (A) A 重叠的 B 分开的8. 关于纯物质,一定温度下泡点与露点,在P-V 图上是 (B) A 重叠的 B 分开的 9. 泡点的轨迹称为 (A) A 饱和液相线 B 饱和汽相线 10. 露点的轨迹称为 (B) A 饱和液相线 B 饱和汽相线 11. 关于混合物,PR 方程常数a 的表达式∑∑==-=3131)1(i j ij jj ii jik a a yy a 中的相互作用参数k ij ,i =j 时,其值 (A)A 为1B 为0C 从实验数据拟合得到,在没有实验数据时,近似作零处理A. >()T P sB. <()T P sC. =()T P sA. >()T P sB. <()T P sC. =()T P sA 仅是T 的函数B 是T 和P 的函数C 是T 和V 的函数D 是任何两强度性质的函数A. 第三virial 系数B. 第二virial 系数C. 无穷项D. 只需要理想气体方程纯物质的P -V 相图P C V C12. 关于混合物,PR 方程常数a 的表达式∑∑==-=3131)1(i j ij jj ii jik a a yy a 中的相互作用参数k ij ,i ≠j 时,其值 ( C )A 为1B 为0C 从实验数据拟合得到,在没有实验数据时,近似作零处理 三、运算题1. 由饱和蒸汽压方程,在合适的假设下估算水在25℃时的汽化焓。
化工热力学课后答案

化工热力学课后答案(填空、判断、画图)第1章 绪言一、是否题1. 封闭体系的体积为一常数。
(错)2. 封闭体系中有两个相βα,。
在尚未达到平衡时,βα,两个相都是均相敞开体系;达到平衡时,则βα,两个相都等价于均相封闭体系。
(对) 3. 理想气体的焓和热容仅是温度的函数。
(对)4. 理想气体的熵和吉氏函数仅是温度的函数。
(错。
还与压力或摩尔体积有关。
)5. 封闭体系的1mol 气体进行了某一过程,其体积总是变化着的,但是初态和终态的体积相等,初态和终态的温度分别为T 1和T 2,则该过程的⎰=21T T V dT C U ∆;同样,对于初、终态压力相等的过程有⎰=21T T P dT C H ∆。
(对。
状态函数的变化仅决定于初、终态与途径无关。
)二、填空题1. 状态函数的特点是:状态函数的变化与途径无关,仅决定于初、终态 。
2. 封闭体系中,温度是T 的1mol 理想气体从(P i ,V i )等温可逆地膨胀到(P f ,V f ),则所做的功为()f i rev V V RT W ln =(以V 表示)或()i f rev P P RT W ln = (以P 表示)。
3. 封闭体系中的1mol 理想气体(已知igP C ),按下列途径由T 1、P 1和V 1可逆地变化至P 2,则A 等容过程的 W = 0 ,Q =()1121T P P R C igP⎪⎪⎭⎫ ⎝⎛--,U =()1121T PP R C igP⎪⎪⎭⎫⎝⎛--,H =1121T P P C ig P ⎪⎪⎭⎫ ⎝⎛-。
B 等温过程的 W =21lnP P RT -,Q =21ln P PRT ,U = 0 ,H = 0 。
第2章P-V-T关系和状态方程一、是否题1. 纯物质由蒸汽变成液体,必须经过冷凝的相变化过程。
(错。
可以通过超临界流体区。
)2. 当压力大于临界压力时,纯物质就以液态存在。
(错。
若温度也大于临界温度时,则是超临界流体。
化工热力学第三版(完全版)课后习题答案解析

化工热力学课后答案第1章 绪言一、是否题1. 封闭体系的体积为一常数。
(错)2. 封闭体系中有两个相βα,。
在尚未达到平衡时,βα,两个相都是均相敞开体系;达到平衡时,则βα,两个相都等价于均相封闭体系。
(对)3. 理想气体的焓和热容仅是温度的函数。
(对)4. 理想气体的熵和吉氏函数仅是温度的函数。
(错。
还与压力或摩尔体积有关。
)5. 封闭体系的1mol 气体进行了某一过程,其体积总是变化着的,但是初态和终态的体积相等,初态和终态的温度分别为T 1和T 2,则该过程的⎰=21T T V dT C U ∆;同样,对于初、终态压力相等的过程有⎰=21T T P dT C H ∆。
(对。
状态函数的变化仅决定于初、终态与途径无关。
)二、填空题1. 状态函数的特点是:状态函数的变化与途径无关,仅决定于初、终态 。
2. 封闭体系中,温度是T 的1mol 理想气体从(P i ,V i )等温可逆地膨胀到(P f ,V f ),则所做的功为()f i rev V V RT W ln =(以V 表示)或()i f rev P P RT W ln = (以P 表示)。
3. 封闭体系中的1mol 理想气体(已知igP C ),按下列途径由T 1、P 1和V 1可逆地变化至P 2,则A 等容过程的 W = 0 ,Q =()1121T P P R C igP⎪⎪⎭⎫ ⎝⎛--,错误!未找到引用源。
U =()1121T PP R C igP⎪⎪⎭⎫⎝⎛--,错误!未找到引用源。
H = 1121T P P C ig P ⎪⎪⎭⎫ ⎝⎛-。
B 等温过程的 W =21lnP P RT -,Q =21ln P PRT ,错误!未找到引用源。
U = 0 ,错误!未找到引用源。
H = 0 。
C 绝热过程的 W =()⎥⎥⎥⎦⎤⎢⎢⎢⎣⎡-⎪⎪⎭⎫ ⎝⎛--11211igPC RigPP P R V P R C ,Q = 0 ,错误!未找到引用源。
化工热力学第三版课后习题答案(1)

化工热力学课后答案第1章绪言—、是否题1. 封闭体系的体积为一常数。
(错)2. 封闭体系中有两个相, 。
在尚未达到平衡时,, 两个相都是均相敞开体系;达到平衡时,则,两个相都等价于均相封闭体系。
(对)3. 理想气体的焓和热容仅是温度的函数。
(对)4. 理想气体的熵和吉氏函数仅是温度的函数。
(错。
还与压力或摩尔体积有关。
)5. 封闭体系的1mol 气体进行了某一过程, 其体积总是变化着的, 但是初态和终态的体积相T 2等,初态和终态的温度分别为 T [和丁2,则该过程的 UC V dT ;同样,对于初、终态T iT 2压力相等的过程有 HC p dT 。
(对。
状态函数的变化仅决定于初、 终态与途径无关。
)T 1二、填空题状态函数的特点是: ________ 。
封闭体系中,温度是 T 的1mol 理想气体从(P , V )等温可逆地膨胀到(P ,V f ),则所做的 功为 W revRTl nV i V f (以 V 表示)或 W rev RT l nP f P (以 P 表示)。
C PP T1T 1。
1.3. 封闭体系中的imol 理想气体(已知C pg ),按下列途径由T 、P i 和V 可逆地变化至P 2,则A 等容过程的 W = _,Q= Cp 1RP 2 P 2P i/C Pg RP 1 1 T 1 , H=B等温过程的RTln l,^RTln t,U= 0 ,H=_0 ___ 。
解:EOSW revV 2 b RTl n丄 V 1 bRTln 纟V 1999In 2 1.0007222. 对于c P为常数的理想气体经过一绝热可逆过程,状态变化符合下列方程解: 3. 解: T 1 P 1(1),其式又是如何?以上a 、b 、 理想气体的绝热可逆过程,C ;gRdTT 22a Rb TT 1aln 旦 b T 2T1RT dV V cT dTCigC !,试问,对于C P a bTcT 2的理想气体,上述关系c 为常数。
化工热力学第三章习题答案

2013年3月28日
§第二题
2013年3月28日
§第二题
始态水为液体,V1 =Vf·m =1.0435× 10-3× 10=0.010435m3 终态水为蒸汽,V2 =Vg·m =1673.0× 10-3× 10=16.730m3 故△V= V2-V1=16.720m3 将△V代入△U=T△S-P△V,得 △U=373.15× 60.485 × 103-0.10113× 106 × 16.720 =20879084J≈20879kJ
2013年3月28日
§第二题
解法二 思路:查出水的汽化潜热Hfg,根据热力学基 本关系式依次求出△H,△S, △A,△U,△G
• 热力学基本关系式:
dH=TdS+Vdp dA=-SdT-pdV dU=TdS-pdV dG=-SdT+Vdp
T,p不变,V变 dH=TdS+Vdp=TdS dA=-SdT-pdV=-pdV dU=TdS-pdV dG=-SdT+Vdp=0
2013年3月28日
§第二题
由dA=-SdT-pdV,且dT=0,得 △A= -p△V= -0.10113× 106 × 16.720J =-1690.9kJ 由dG=-SdT+Vdp,且dT=0,dp=0,得 △G=0
《化工热力学章节习题及解答》第三章 例题

另外,还需要理想气体等压热容的数据,查附录A-4得到,得到异丁烷的理想气体等压热容是
(J mol-1K-1)
初态是T0=300K,P0=0.1MPa的理想气体;终态是T=360K的饱和蒸汽,饱和蒸汽压可以从Antoine方程计算,查附录A-2,得
性质
沸点或蒸汽压
U/Jg-1
H/Jg-1
S/Jg-1K-1
饱和蒸汽
340℃或14.59MPa
2464.5
2622.0
5.3359
总性质
2464500(J)
2622000(J)
5335.9(JK-1)
所以, J; J; JK-1。
又因为,是一个等容过程,故需要吸收的热为 J
7. 压力是3MPa的饱和蒸汽置于1000cm3的容器中,需要导出多少热量方可使一半的蒸汽冷凝?(可忽视液体水的体积)
解:以1g为基准来计算。
(1)对于绝热可逆膨胀,Q=0,W=-1000ΔU,S2=S1,
从 Pa,查附录C-1,得到 , 940.87Jg-1, ,
则 和
由于可确定膨胀后仍处于汽液两相区内,终态压力就是饱和蒸汽压,从 Pa查 , ; ,
从
则W=-1000(U2-U1)=278.45(kJ)
(2)再恒容加热成饱和蒸汽,W=0,
解:由Maxwell关系式
左边= ;
又因为 ,右边= ,由此可以得到
(这种体积关系一般能成立,故方程有一定的可靠性)。
5.试证明 ,并说明 。
解:由定义 ;
右边= =左边。
代入理想气体状态方程, 可以得到
6.证明(a)在汽液两相区的湿蒸汽有 。(b)在临界点有 。
化工热力学 例题 与解答(9).

第 3章均相封闭体系热力学原理及其应用一、是否题1. 体系经过一绝热可逆过程,其熵没有变化。
2. 吸热过程一定使体系熵增,反之,熵增过程也是吸热的。
3. 热力学基本关系式 dH=TdS+VdP只适用于可逆过程。
4. 象 dU=TdS-PdV等热力学基本方程只能用于气体,而不能用于液体或固相。
5. 当压力趋于零时, ((0, , ≡-P T M P T M ig (M 是摩尔性质。
6.[](0ln , P PR P T S S ig+-与参考态的压力 P 0无关。
纯物质逸度的完整定义是,在等温条件下, f RTd dG ln =。
7. 理想气体的状态方程是 PV=RT, 若其中的压力 P 用逸度 f 代替后就成为了真实流体状态方程。
8. 当0→P 时, ∞→P f 。
9. 因为⎰⎪⎭⎫⎝⎛-=PdP P RT V RT 01ln ϕ,当0→P 时, 1=ϕ,所以, 0=-P RT V 。
10. 逸度与压力的单位是相同的。
11. 吉氏函数与逸度系数的关系是 ((ϕln 1, , RT P T G P T G ig ==-。
12. 由于偏离函数是两个等温状态的性质之差, 故不可能用偏离函数来计算性质随着温度的变化。
13. 由于偏离函数是在均相体系中引出的概念, 故我们不能用偏离函数来计算汽化过程的热力学性质的变化。
14. 由一个优秀的状态方程,就可以计算所有的均相热力学性质随着状态的变化。
二、选择题1. 对于一均匀的物质,其 H 和 U 的关系为(B 。
因 H =U +PVA. H ≤UB. H>UC. H=UD. 不能确定2. 一气体符合 P=RT/(V-b 的状态方程从 V 1等温可逆膨胀至 V 2,则体系的∆S 为(C 。
b V b V R b V R dV T P dV V S S V V V V V V V T --=-=⎪⎭⎫⎝⎛∂∂=⎪⎭⎫⎝⎛∂∂=⎰⎰⎰12ln 212121∆ A. bV bV RT --12lnB. 0C. bV bV R --12lnD. 12lnV V R 3. 对于一均相体系, VP T S T T S T ⎪⎭⎫⎝⎛-⎪⎭⎫⎝⎛∂∂∂∂等于(D 。
