南京工业大学-化学反应工程-2005-2006试题B答案
南京工业大学-化学反应工程-2005-2006试题B

南京工业大学 化学反应工程 试题B (开)卷2005—2006学年第一学期 使用班级1.反应器中等温进行着A →P(1)和A →R(2)两个反应,当降低A 的浓度后,发现反应生成P 的量显著降低,而R 的生成量略降低,表明( )A .反应(1)对A 的反应级数大于反应(2)B .反应(1)对A 的反应级数小于反应(2)C .反应(1)的活化能小于反应(2)D .反应(1)的反应速率常数大于反应(2)2.四只相同体积的全混釜串联操作,其无因次停留时间分布的方差值2θσ为( ) A . 1.0 B. 0.25 C .0.50 D .03.对一平行—连串反应R A Q P A −→−−→−−→−)3()2()1(,P 为目的产物,若活化能次序为:E 2<E 1<E 3,为了目的产物的收率最大,则最佳操作温度序列为( )。
A .先高后低 B.先低后高 C .高温操作 D .低温操作4.两个等体积的全混流反应器进行串联操作,反应为一级不可逆,则第一釜的反应速率-r A1与第二釜的反应速率-r A2之间的关系为( )。
两釜反应温度相同。
A .-r A1 > -r A2B .-r A1 = -r A2C .-r A1 < -r A2 D.不能确定何者为大5. 已知一闭式反应器的1.0=r auL D ,该反应器若用多釜串联模型来描述,则模型参数N 为( )。
A . 4.5 B. 5.6 C .3.5 D .4.06.固体催化剂之所以能起催化作用,是由于催化剂的活性中心与反应组分的气体分子主要发生( )。
A .物理吸附B .化学反应C .化学吸附D .质量传递7.包括粒内微孔体积在内的全颗粒密度称之为( )A .堆(积)密度B .颗粒密度C .真密度D .平均密度8.在气固催化反应动力学研究中,内循环式无梯度反应器是一种( )。
A .平推流反应器 B. 轴向流反应器 C. 全混流反应器 D. 多釜串联反应器9.某液相反应,其反应式可写成A+C R+C 这种反应称为( )A .均相催化反应B .自催化反应C .链锁反应 D.可逆反应10.高径比不大的气液连续鼓泡搅拌釜,对于其中的气相和液相的流动常可近似看成( )A .气、液均为平推流B .气、液均为全混流C .气相平推流、液相全混流D .气相全混流、液相平推流二、填空题(每题5分,共30分)1.一不可逆反应,当反应温度从25℃升高到35℃时,反应速率增加一倍,则该反应的活化能为 。
(完整版)反应工程总复习题(答案)

59、可逆放热反应的x-T曲线如图所示,在图中A-H各点中:反应速率为零的点为:
(A)
(A)A和B和C(B)D和E和F(C)G和H
60、如上图,在D、E、F三点中,反应速率由大到小的顺序为:(A)
(A)D>E>F(B)D<E<F(C)无法确定
二、多选题(共20小题,每题1分)
1、一个反应器的特性一般从如下哪几个方面进行描述?(BCE)
A、体积大小B、物质传递C、热量传递D、形状E、动量传递
2、稳态连续操作的反应器特点包括:(BC)
A、参数随时间变化B、参数随空间变化C、累积量为零D、累积量不为零
32、理想平推流反应器达到稳定的定常态操作时,下列哪些说法是正确的:(BC)
C、增大反应器直径D、提高反应器长度
9、固定催化反应床层的空隙率 是影响床层流体流动特性的重要参数,一般情况下当 过大或床层填充不匀时,会导致流体产生:(ABC)
A、沟流现象B、短路流C、壁效应D、床层热点
10、若气固多相催化反应器内存在沟流现象,可以通过下述哪种措施加以改良:(AB)
A、减小催化剂粒径B、改善床层空隙率均一C、增大反应器直径
A、瞬间理想混合B、返混程度为零
C、出口物料参数与器内相同D、独立变量为空间
7、其一级不可逆反应在CSTR中进行时可能有1至3个定常态操作点,则稳定的操作点可能有几个?(ABC)
A、没有B、1个C、2个D、3个
8、可以通过下述何种方式来有效消除固定床反应器的壁效应现象:(BC)
A、增大催化剂颗粒粒径B、减少催化剂颗粒粒径
a、C-Fb、A-Bc、D-Ed、Ge、C
16、对于多段绝热固定床反应器,采用段间换热装置的目的主要是为了:(AB)
《化学反应工程》课后习题答案

(2)放热反应吸热反应
(3)M点速率最大,A点速率最小M点速率最大,A点速率最小
(4)O点速率最大,B点速率最小H点速率最大,B点速率最小
(5)R点速率大于C点速率C点速率大于R点速率
(6)M点速率最大根据等速线的走向来判断H,M点的速率大小。
2.7在进行一氧化碳变换反应动力学研究中,采用B106催化剂进行试验,测得正反应活化能为 ,如果不考虑逆反应,试问反应温度是550℃时的速率比反应温度是400℃时的速率大多少倍?
(1)(1)以反应体积为基准的速率常数kV。
(2)(2)以反应相界面积为基准的速率常数kg。
(3)(3)以分压表示反应物系组成时的速率常数kg。
(4)(4)以摩尔浓度表示反应物系组成时的速率常数kC。
解:利用(2.10)式及(2.28)式可求得问题的解。注意题中所给比表面的单位换算成m2/m3。
2.4在等温下进行液相反应A+B→C+D,在该条件下的反应速率方程为:
原料气和冷凝分离后的气体组成如下:(mol)
组分
原料气
冷凝分离后的气体
CO
26.82
15.49
H2
68.25
69.78
CO2
1.46
0.82
CH4
0.55
3.62
N2
2.92
10.29
粗甲醇的组成为CH3OH 89.15%,(CH3)2O 3.55%,C3H9OH 1.10%,H2O 6.20%,均为重量百分率。在操作压力及温度下,其余组分均为不凝组分,但在冷凝冷却过程中可部分溶解于粗甲醇中,对1kg粗甲醇而言,其溶解量为CO29.82g,CO 9.38g,H21.76g,CH42.14g,N25.38g。若循环气与原料气之比为7.2(摩尔比),试计算:
(整理)化学反应工程第二版课后答案.

第一章习题1化学反应式与化学计量方程有何异同?化学反应式中计量系数与化学计量方程中的计量系数有何关系?答:化学反应式中计量系数恒为正值,化学计量方程中反应物的计量系数与化学反应式中数值相同,符号相反,对于产物二者相同。
2 何谓基元反应?基元反应的动力学方程中活化能与反应级数的含义是什么?何谓非基元反应?非基元反应的动力学方程中活化能与反应级数含义是什么?答:如果反应物严格按照化学反应式一步直接转化生成产物,该反应是基元反应。
基元反应符合质量作用定律。
基元反应的活化能指1摩尔活化分子的平均能量比普通分子的平均能量的高出值。
基元反应的反应级数是该反应的反应分子数。
一切不符合质量作用定律的反应都是非基元反应。
非基元反应的活化能没有明确的物理意义,仅决定了反应速率对温度的敏感程度。
非基元反应的反应级数是经验数值,决定了反应速率对反应物浓度的敏感程度。
3若将反应速率写成tc rd d AA -=-,有什么条件? 答:化学反应的进行不引起物系体积的变化,即恒容。
4 为什么均相液相反应过程的动力学方程实验测定采用间歇反应器?答:在间歇反应器中可以直接得到反应时间和反应程度的关系,而这种关系仅是动力学方程的直接积分,与反应器大小和投料量无关。
5 现有如下基元反应过程,请写出各组分生成速率与浓度之间关系。
(1)A+2B ↔C A+C ↔ D (2)A+2B ↔C B+C ↔D C+D →E(3)2A+2B ↔C A+C ↔D 解(1)D4C A 3D D 4C A 3C 22BA 1C C22B A 1B D 4C A 3C 22B A 1A 22c k c c k r c k c c k c k c c k r c k c c k r c k c c k c k c c k r -=+--=+-=+-+-=(2)E6D C 5D 4C B 3D E 6D C 5D 4C B 3C 22BA 1C D4C B 3C 22B A 1B C22B A 1A 22c k c c k c k c c k r c k c c k c k c c k c k c c k r c k c c k c k c c k r c k c c k r +--=+-+--=+-+-=+-=(3)D4C A 3D D 4C A 3C 22B2A 1C C22B 2A 1B D 4C A 3C 22B 2A 1A 2222c k c c k r c k c c k c k c c k r c k c c k r c k c c k c k c c k r -=+--=+-=+-+-=6 气相基元反应A+2B →2P 在30℃和常压下的反应速率常数k c =2.65×104m 6kmol -2s -1。
南京工业大学有机化学试卷整理集(吐血整理必做)
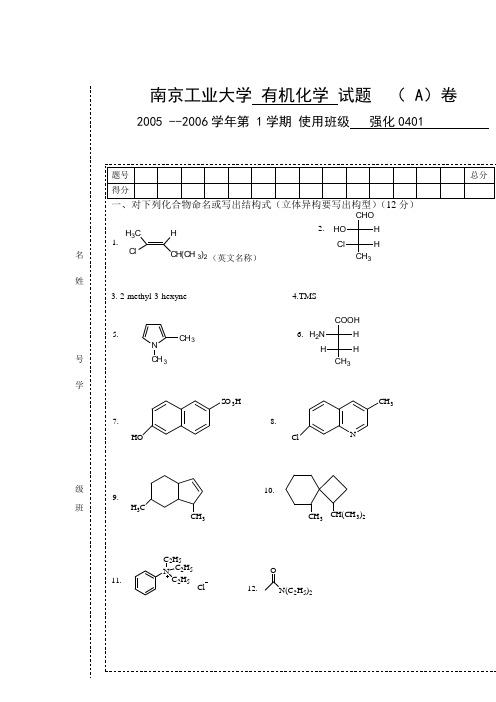
名姓号学级班11混酸混酸NHOKOHCH 3CH 2OHCH 3CH 2Br12N13.24+NaOH+Br 2N H 2O14NaNO , HClNH 20-5℃OH15.三:排序(6 )1.将下列化合物对亲电取代反应的容易程度排列成序BrNO2.比较下列羧酸的酸性COOHCH 3COOHNO 2COOHNO 2COOH3.比较下列化合物的碱性甲胺 二甲胺 氨 苯胺四、区别下列各组化合物:(4)1 甲酸 乙酸 乙醇CH 3OCH 3OOCH 3OCH 3OO CH 3C H 32.五 用化学方法分离下列各组化合物(6)1.邻甲苯酚 水杨酸 N-甲基苯胺 对甲基苯胺 甲苯2CH 3NO 2CH 3CN六 用指定的原料合成下列各化合物(小分子及无机试剂任选) (25)C H 2COOH1.BrC H 32.3.从苯出发合成多巴胺O HO HN H 24从丙二酸脂出发合成OCOOCH 3CH 3CH 3OOOC H 3CH 3CH 3COOH5.七、简要回答问题(19分)1 写出下述反应的机理H 5C 6H 2CCH 2C 6H 5O+C H 2C H 3ONaO CH CH 3OHOH 5C 6C 6H 5C H 3H 3H 3H3H 32.(1) 哪个化合物是手性分子? (2) 写出手性分子的稳定构象式。
3.化合物A (C 9H 10O )不能起碘仿反应,其红外光谱表明在1690cm -1处有一强吸收峰,其核磁共振数据如下:δ1.2(3H,t),δ3.0(2H,q),δ7.2(5H,m)。
写出A的结构并标注对应的化学位移。
南京工业大学有机化学B 试题(A)卷试题标准答案2008--2009 学年第二学期使用班级化学0701-2一:命名1.甲基丁二酸酐2.N,N-二甲基环戊甲酰胺3.3-吡啶磺酸4.溴化二甲基苄基十二烷基铵5.α-环己酮甲酸甲酯6.4-甲基-4’-乙氧基偶氮苯7.3-甲基-丁腈8.(2S,3S)-2-乙基-2,3-二羟基丁二酸9.3-呋喃甲酸10.-甲基葡萄糖二:完成反应C O O HC O O HN H OO1.2CH2NH2ONC H3C H3O H3CH3OC H34.ClON HO H5CH 3CH 3OC H 3OO C H 36NO 27.NH28.H 339.CH 3CNO HCH 3COOH O H10.N H 2NO 211.O 2NO 2NNO 2+NO 2NO 212.OONC H 3OONKNSO 3H13.N H 214.N 2ClNNOH15.三:排序BrNO>>>1.C O O HNO 2COOHNO 2COOHCOOHCH 3>>>2苯胺>>3.二甲胺甲胺>氨四:区别化合物1. 银镜反应,碳酸钠溶液 2. FeCl 3溶液 3. 五:分离1. 兴斯堡反应,蒸馏。
化学反应工程试题库和答案(精心整理)

化学反应工程考试题库(分三个部分)(一)(综合章节)复习题一、填空题:1.所谓“三传一反”是化学反应工程学的基础,其中“三传”是指质量传递、热量传递和动量传递,“一反”是指反应动力学。
2.各种操作因素对于复杂反应的影响虽然各不相同,但通常温度升高有利于活化能高的反应的选择性,反应物浓度升高有利于反应级数大的反应的选择性。
3.测定非理想流动的停留时间分布函数时,两种最常见的示踪物输入方法为脉冲示踪法和阶跃示踪法。
4.在均相反应动力学中,利用实验数据求取化学反应速度方程式的两种最主要的方法为积分法和微分法。
5.多级混合模型的唯一模型参数为串联的全混区的个数N ,轴向扩散模型的唯一模型参数为Pe(或Ez / uL)。
6.工业催化剂性能优劣的三种最主要的性质是活性、选择性和稳定性。
7.平推流反应器的E函数表达式为,()0,t tE tt t⎧∞=⎪=⎨≠⎪⎩,其无因次方差2θσ=0 ,而全混流反应器的无因次方差2θσ= 1 。
8.某反应速率常数的单位为m3 / (mol⋅ hr ),该反应为 2 级反应。
9.对于反应22A B R+→,各物质反应速率之间的关系为 (-r A):(-r B):r R= 1:2:2 。
10.平推流反应器和全混流反应器中平推流更适合于目的产物是中间产物的串联反应。
11.某反应的计量方程为A R S→+,则其反应速率表达式不能确定。
12.物质A按一级不可逆反应在一间歇反应器中分解,在67℃时转化50%需要30 min, 而在80 ℃时达到同样的转化率仅需20秒,该反应的活化能为 3.46×105 (J / mol ) 。
13.反应级数不可能(可能/不可能)大于3。
14. 对于单一反应,在相同的处理量和最终转化率条件下,选择反应器时主要考虑 反应器的大小 ;而对于复合反应,选择反应器时主要考虑的则是 目的产物的收率 ; 15. 完全混合反应器(全混流反应器)内物料的温度和浓度 均一 ,并且 等于(大于/小于/等于)反应器出口物料的温度和浓度。
《化学反应工程》复习题及答案.doc

单选题1.对于反应级数n>0的不可逆气相等温反应,为降低反应器体积,应选用______ 。
(A)(A)平推流反应器(B)全混流反应器(C)平推流串接全混流反应器(D)全混流串接平推流反应器2.分批式操作的完全混合反应器非生产性时间不包括下列哪一项____________ 。
(P22)(A)加料时间(B)反应时间(C)物料冷却时间(D)清洗釜所用时间3.下列单位不属于反应速率的是_______ o(P13)(A)mol/(g • s)(B) m3/s (C) mol/(m2• s)(D) mol/(m3• s)4.反应A T B+C, Z: = 2.50 5_1,则反应级数为 ____________ o (P13)A・ 0 (B) 1 (C) 2 (D) 35.反应NaOH + HCl — NaCl + H2O ,已知k=QAbs!mol ,则反应级数n= ______ o (P13)(A)0 (B) 1 (C) 2 (D) 36.气相基元反应24 T〃,进料时反应物A和稀释剂C以等摩尔比加入,则膨胀率为 ______ o (P58)(A)(B) -0.25 (C) 0.25 (D) 0.57.下面反应器屮不属于理想反应器的是_______ o (P21)(A)间歇反应器(B)全混流反应器(C)平推流反应器(D)膜反应器&下面哪种反应器组合形式可以最大程度降低反应器体积 _________ o (B)(A)平推流反应器串联(B)全混流反应器串联(C)平推流反应器并联(D)全混流反应器并联9.在间歇反应器中进行等温一级反应A -> B, -r4=0.01C4mol/L-s,当C AO=1mol/Lri寸,求反应至C A o=O.Ol mol/L所需时间= ____ 秒。
(P43)(A)400 (B) 460 (C) 500 (D) 560(A) * Vdt r二du (B)而dC R(D)心匚10.在间歇反应器中进行等温二级反应A T B, -r A=0.01C42mol/L-s,当C AO=1mol/L时,求反应至C A o=O.Ol mol/L所需时间1= ___ 秒。
南京工业大学反应工程题集-完全答案解析版

注:红色底色为需注意的题目;黄色为无答案的题目1.对于热效应不大,反应温度的允许变化范围又比较宽的情况,用单级反应器最方便。
2.气固催化平行反应,若主、副反应均为一级不可逆反应,且粒子等温,则内扩散不影响其选择性,在粒子内任意位置,反应速率之比均为速率常数之比。
选择题1.在V=100L/min流量下对三只反应器分别进行示踪实验,测得如下数据:反应器 A B C体积(L)1000 2000 3000σt2 (min)50 100 250则三只釜的反混大小顺序(B)A. A>B>CB. A>C>BC. C>B>AD. C>A>B2. 乙苯在催化剂上脱氢反应生成苯乙烯,经过一段时间反应后,苯乙烯生成量不再增加,但乙苯仍大量存在,表明这是一个(B)反应。
A.慢速B.可逆C.自催化D.不可逆3.反应器中等温进行着A→P(1)和A→R(2)两个反应,当降低A的浓度后,发现反应生成P 的量显著降低,而R 的生成量略降低,表明( A )A .反应(1)对A 的反应级数大于反应(2)B .反应(1)对A 的反应级数小于反应(2)C .反应(1)的活化能小于反应(2)D .反应(1)的反应速率常数大于反应(2)4.在间歇反应器中等温进行一级不可逆反应A →R ,当转化率达90%时,所需反应时间为2h 若反应改在管式反应器中进行,空时为2h ,其它条件同间歇反应器,则转化率为( B )A . 60% B. 90% C .45% D .75%☆两个等体积的全混流反应器进行串联操作,反应为一级不可逆,则第一釜的反应速率-rA1与第二釜的反应速率-rA2之间的关系为(A )。
两釜反应温度相同。
A .-rA1 > -rA2B .-rA1 = -rA2C .-rA1 < -rA2 D.不能确定何者为大5.四只相同体积的全混釜串联操作,其无因次停留时间分布的方差值2θσ为( B )A . 1.0 B. 0.25 C .0.50 D .06.对一平行—连串反应RA QP A −→−−→−−→−)3()2()1( ,P 为目的产物,若活化能次序为:E 2<E 1<E 3,为了目的产物的收率最大,则最佳操作温度序列为( B )。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
南京工业大学 化学反应工程 试题B (开)卷(答
案)
2005—2006学年第一学期 使用班级
1.反应器中等温进行着A →P(1)和A →R(2)两个反应,当降低A 的浓度后,发现反应生成P 的量显著降低,而R 的生成量略降低,表明( )
A .反应(1)对A 的反应级数大于反应(2)
B .反应(1) 对A 的反应级数小于反应(2)
C .反应(1)的活化能小于反应(2)
D .反应(1)的反应速率常数大于反应(2)
2.四只相同体积的全混釜串联操作,其无因次停留时间分布的方差值2
θ
σ为( )
A . 1.0 B. 0.25 C .0.50 D .0
3.对一平行—连串反应R A Q
P A −→−−→−−→−)
3()
2()
1(,P 为目的产物,若活化能次序为:E 2<E 1<E 3,为了目的产物的收率最大,则最佳操作温度序列为( )。
A .先高后低 B.先低后高 C .高温操作 D .低温操作
4.两个等体积的全混流反应器进行串联操作,反应为一级不可逆,则第一釜的反应速率-r A1与第二釜的反应速率-r A2之间的关系为( )。
两釜反应温度相同。
A .-r A1 > -r A2
B .-r A1 = -r A2
C .-r A1 < -r A2 D.不能确定何者为大
5. 已知一闭式反应器的1
.0=r
a uL D ,该反应器若用多釜串联模型来描述,则模型参数N 为( )。
A . 4.5 B. 5.6 C .3.5 D .4.0
6.固体催化剂之所以能起催化作用,是由于催化剂的活性中心与反应组分的气体分子主要发生( )。
A .物理吸附
B .化学反应
C .化学吸附
D .质量传递 7.包括粒内微孔体积在内的全颗粒密度称之为( )
A .堆(积)密度
B .颗粒密度
C .真密度
D .平均密度
8.在气固催化反应动力学研究中,内循环式无梯度反应器是一种( )。
A .平推流反应器 B. 轴向流反应器 C. 全混流反应器 D. 多釜串联反应器
9.某液相反应,其反应式可写成A+C R+C 这种反应称为( )
A .均相催化反应
B .自催化反应
C .链锁反应 D.可逆反应
10.高径比不大的气液连续鼓泡搅拌釜,对于其中的气相和液相的流动常可近似看成( )
A .气、液均为平推流
B .气、液均为全混流
C .气相平推流、液相全混流
D .气相全混流、液相平推流
二、填空题(每题5分,共30分)
1.一不可逆反应,当反应温度从25℃升高到35℃时,反应速率增加一倍,则该反应的活化能为 52894 J /mol 。
解:mol J E E T T R E k k /528942
ln )308
12981(
314
.82ln )11(ln 21
12=∴=-
==-=,
2.一气固催化反应R B A →+,若本征反应速率方程为:
2
)
1(R R B B A A B
B A
A S P K P K P K P K P K k r ++
+=
则该反应可能的反应机理为
σ
R R σσR σB σA σB σ
σB A σσA S
k
+⇔+−→−+⇔+⇔+)
此步为速率控制步骤
( 222
3.间歇釜反应器中进行如下反应:
P A → (1) -r A1=k 1C A a1 S A → (2) -r A2=k 2C A a2
在C A0和反应时间保持不变下,降低反应温度,釜液中C P /C S 增大,表明活化能E1
与E2的相对大小为 E1<E2 ;在温度和反应时间保持不变下,增
高反应浓度,釜液中C P /C S 增大,表明反应级数al 、a2的相对大小为 al>a2 。
A .al>a2
B .al<a2
C .活化能El<E2
D .活化能El>E2
4.从反应器停留时间分布测定中,求得无因次方差98
.02
=θσ,反应器可视为 全混
流反应器 ,
又若求得无因次方差02
.02
=θσ,则反应器可视为 活塞流反应器 。
5.有两个有效容积不等的全混流反应器串联操作,反应为二级不可逆反应A →P ,若大釜在先,小釜在后,出口转化率为x A1,小釜在先、大釜在后,则出口转化率为x A2,两种情况下,进料流速、进料浓度和反应温度均相同,比较x A1和x A2的相对大小为 x A1<x A2 。
6. 在固定床反应器中,分别进行一级和二级不可逆气固催化反应,试比较a 、b 两处的η值大小(a 处靠近反应器的进口,b 处靠近反应器的出口),并说明理由。
(1)一级放热反应,绝热操作;ηa >ηb (2)二级反应,等温操作。
ηa <ηb
三、问答题(每题6分,共12分)
1.液相复合反应
Q B A P
B A k k
−→−+−→−+2122, 若2
5
.025.021B A Q B
A P C C k r C C k r == 为使目的产物P 的选择性高,应选择:
(1) 若采用间歇反应釜,其加料方式为? (2) 若采用管式反应器,其进料方式为?
(3) 若E 1>E 2,则反应温度应尽可能采用高温或低温?
答:为使目的产物P 的选择性高,应选择: (1)若采用间歇反应釜,其加料方式为 A 一次性加入,B 连续滴加 ; (2)若采用管式反应器,其进料方式为 A 从反应器进口处加入,B 沿管长多处加入 ;
(3)若E 1>E 2,则反应温度应采用 高
温 。
2. 在四段绝热式固定床反应器中进行n 级不可逆反应,各段的催化剂量相同,且控制进入各段的反应物料温度相等.若n>0,试问
(1) 哪一段的净转化率最大?哪一段最小?
(2) 若段间采用冷激方法进行降温,试问第一段与第二段之间和第二段与第三段之间 哪处需加入的冷激剂量多?为什么?
解:(1)虽然各段进口温度相等,在催化剂量相同的情况下,净转化率也按1至4段的顺 序递减,第一段最大,第二段次之, 第三段再次之,第四段最小.
(2)因第一段反应量大于第二段反应量,所以1-2段间要取出的热量比2-3段间要取出 的热量大,因而1-2段间需要的冷激量也大于2-3段间需要的冷激剂量.
四、计算题:(第1,2题均为12分,第3题为14分,共38分)
1.在反应体积为1 m 3的釜式反应器中,环氧丙烷的甲醇溶液与水反应生产丙二醇-1,2:
23223+→H C O C H C H H O H C O H C H O H C H
该反应对环氧丙烷为一级,对水为零级,反应温度下反应速率常数等于0.98h -1,原料液中环氧丙烷的浓度为2.1kmol/m 3,环氧丙烷的最终转化率为90%。
(1)若采用间歇操作,辅助时间为0.65h ,则丙二醇-1,2的日产量是多少? (2)有人建议改在定态下连续操作,其余条件不变,则丙二醇-1,2的日产量又是多少?
(3)为什么这两种操作方式的产量会有不同?
解:3
1
01,,0.98, 2.1/,0.9-=====r A A A A V m r kC k h C km ol l X (1) 一级不可逆反应:
h
m
Q Q t t Q V h
x k
t r Af /3/11)65.035.2()(35.2)9.01ln(98
.01)1ln(13
0000==+=+==--
=--
=
丙二醇的浓度=3
0 2.10.9 1.89/=⨯=A A C X km ol m
丙二醇的产量=Af A00x C Q =1.891/30.63/15.15/⨯==日km ol h km ol
(2) 采用定态下连续操作
000.91
(1)
0.98(10.9)
⨯=
=
=--A f r A f Q X Q V k X
所以Q 0=0.109m 3/h
丙二醇的产量=0.109 1.890.2058/ 4.939/⨯==日km ol h km ol (3)因连续釜在低的反应物浓度下操作,反应速率慢,故产量低。
2.对一闭式反应器进行停留时间分布实验测定,在Q =300L/min 下,得到E(t)~t 关系如下图所示。
由于该图放置已久,纵坐标模糊不清。
试根据E(t)函数性质确定并计算:
(1)E(t)
(2)F(t) (3)该反应器体积为多少?
(4)多级串联模型参数N 为多少?
(5)无因次方差2
θσ
为多少? (6)轴向扩散模型参数Pe 为多少?
t/min 答:
(1)E(t)= -1/200(t-20)
(2)F(t)= -t 2
/400+0.1t
(3)V = 2 m 3
(4)多级串联模型参数N = 2
(5)无因次方差
2112
=
=σθN
(6) 2.56Pe 5
.0)e -(1Pe
2
-
Pe
2Pe
-2
2
=∴==
σθ
3.某一级不可逆气固催化反应,在反应温度150℃下,测得k P =5s -1,有效扩散系数D eA =0.2cm 2/s 。
求:
(1) 当颗粒直径为0.1mm 时,内扩散影响是否已消除?
(2) 欲保持催化剂内扩散有效因子为0.8,则颗粒直径应不大于多少?
解:。
