大学物理热学总结I:基本假设及理论
大学物理热学部分小结

大学物理热学部分小结通信工程4班胡素奎0706020415个人学习总结:大学物理的热学部分还是相对不是太难的,因为与高中的物理关联很大,很多概念都是以前接触过的,但是没有深入研究,这已经给这部分的学习带来了极大的便利。
如果说要有什么不同,主要那有如下几个方面:1、研究方法的不一样:虽然很多内容是接触过的,但是重新学习的时候明显感觉到不一样的是研究方法,随着其他知识的累积,尤其是高数的引入,给物理的学习带来的极大的便利,特别是一些公式的推理过程让我们更好的了解公式的来由,更好的便于记忆和理解。
2、准确度的不同:在学习过程中,总有些以前的东西对推翻,因为要考虑的东西越来越多,微观的宏观的等压的等温的……这些都告诉我们要全面细致地学习,应用的知识越来越多,要把知识串成串。
3、学习方法的不同:大学阶段的物理学习和中学阶段的物理学习存在着很大的不同,课少了,作业也少了,但是仍然不能放松,毕竟在中学几乎每天都在学物理,所以现在的物理学习更需要自己的主动和认真。
以下是热学的一些知识点的总结1.温度的概念与有关定义1)温度是表征系统热平衡时的宏观状态的物理量。
2)温标是温度的数值表示法。
常用的一种温标是摄氏温标,用t表示,其单位为摄氏度(℃)。
另一种是热力学温标,也叫开尔文温标,用T表示。
它的国际单位制中的名称为开尔文,简称K。
热力学温标与摄氏温标之间的换算关系为:T/K=273.15℃ + t温度没有上限,却有下限。
温度的下限是热力学温标的绝对零度。
温度可以无限接近于0 K,但永远不能到达0 K。
2.理想气体的微观模型与大量气体的统计模型。
速度分布的特征。
1)为了从气体动理论的观点出发,探讨理想气体的宏观现象,需要建立理想气体的微观结构模型。
可假设:a气体分子的大小与气体分子之间的平均距离相比要小得多,因此可以忽略不计。
可将理想气体分子看成质点。
b分子之间的相互作用力可以忽略。
c分子键的相互碰撞以及与器壁的碰撞可以看作完全弹性碰撞。
大学热学知识点总结图

大学热学知识点总结图一、热力学基础知识1. 温度、热量和热平衡温度是物质内部微观运动的表现,热量是能量的一种形式,热平衡是指两个系统之间不再有能量的净传递。
2. 热力学第一定律能量守恒定律,在自然界中能量不会自行减少或增加。
3. 热力学第二定律热量不会自发地由低温物体传递给高温物体,熵增加原理。
4. 热力学第三定律当温度趋近于绝对零度时,任何实体的熵均趋于零,即系统的熵在温度趋近绝对零度时趋于一个常数。
5. 理想气体理想气体状态方程和理想气体内能的表达式。
6. 凝固和融化物质由固态转变为液态称为融化,由液态转变为固态称为凝固。
凝固和融化温度是由物质特性决定的。
二、热力学循环1. 卡诺循环卡诺循环是热机的理想循环,包括等温膨胀、绝热膨胀、等温压缩和绝热压缩四个过程。
2. 斯特林循环斯特林循环是一种热机的实际循环,包括等温膨胀、绝热膨胀、等温压缩和绝热压缩四个过程。
3. 高尔辛循环高尔辛循环是一种蒸汽轮机工作的热力循环过程,包括等压加热、等容膨胀、等压冷凝和等容压缩四个过程。
三、热力学系统1. 开放系统与闭合系统开放系统和闭合系统能够与外界进行物质、能量交换。
2. 热力学过程等容过程、等压过程、等温过程、绝热过程。
3. 热力学函数内能、焓、吉布斯自由能、哈密顿函数等热力学函数的定义和性质。
四、热传导1. 热传导的基本定律傅里叶热传导定律、傅里叶热传导方程、热导率概念。
2. 热传导的应用导热系数、传热表面积、传热温度差、传热距离等参数。
3. 热传导的热阻和导热系数热阻的概念和计算、导热系数的概念和计算。
五、热辐射1. 热辐射的基本定律斯特藩—玻尔兹曼定律、维恩位移定律、铂居—史恩定律。
2. 黑体辐射和表面发射系数黑体的定义、黑体的吸收、发射和反射的关系。
3. 热辐射的热平衡和热不平衡热辐射的观测和应用。
六、热功学1. 热功学的基本定律各态函数、热力学基本关系和亥姆霍兹自由能、君体—吉布斯函数的性质。
2. 熵增加原理和热功学过程热功学过程的熵增加原理,等熵过程、绝热过程等。
热学物理总结报告范文(3篇)

第1篇一、引言热学是物理学的一个重要分支,研究物体内部的热运动和能量转换规律。
随着科学技术的不断发展,热学在工业、农业、医学、能源等领域都发挥着至关重要的作用。
本报告将对热学物理的基本概念、主要理论、实验方法和应用领域进行总结和分析。
二、热学基本概念1. 热量:热量是物体内部微观粒子运动能量的总和,通常用符号Q表示。
热量的单位是焦耳(J)。
2. 温度:温度是物体内部微观粒子平均动能的度量,通常用符号T表示。
温度的单位是开尔文(K)。
3. 热容:热容是物体吸收或放出热量时温度变化的度量,通常用符号C表示。
热容的单位是焦耳每开尔文(J/K)。
4. 热传导:热传导是热量在物体内部由高温区域向低温区域传递的过程。
5. 热辐射:热辐射是物体由于自身温度而向外发射热量的过程。
6. 热对流:热对流是流体内部热量传递的一种形式,即流体中高温区域的分子向低温区域传递热量的过程。
三、热学主要理论1. 热力学第一定律:热力学第一定律指出,热量、功和内能之间的关系是Q = W+ ΔU,其中Q为吸收的热量,W为外界对系统所做的功,ΔU为系统内能的变化。
2. 热力学第二定律:热力学第二定律表明,热量不能自发地从低温物体传递到高温物体,而且在一个封闭系统中,熵(S)总是增加的。
3. 热力学第三定律:热力学第三定律指出,在绝对零度时,任何物体的熵都为零。
4. 热平衡定律:当两个系统接触时,如果它们之间没有热量交换,那么它们的温度将趋于相同。
5. 热传导定律:傅里叶定律描述了热传导过程中的热量传递速率,即Q = -kAΔT/Δx,其中Q为热量,k为热传导系数,A为传热面积,ΔT为温度差,Δx为距离。
6. 热辐射定律:斯蒂芬-玻尔兹曼定律描述了物体热辐射的能量,即E = σT^4,其中E为辐射能量,σ为斯蒂芬-玻尔兹曼常数,T为物体温度。
四、热学实验方法1. 热平衡实验:通过测量两个物体接触后的温度变化,验证热平衡定律。
2. 热传导实验:通过测量不同材料的热传导系数,研究热传导规律。
大学物理热学总结I:基本假设与理论
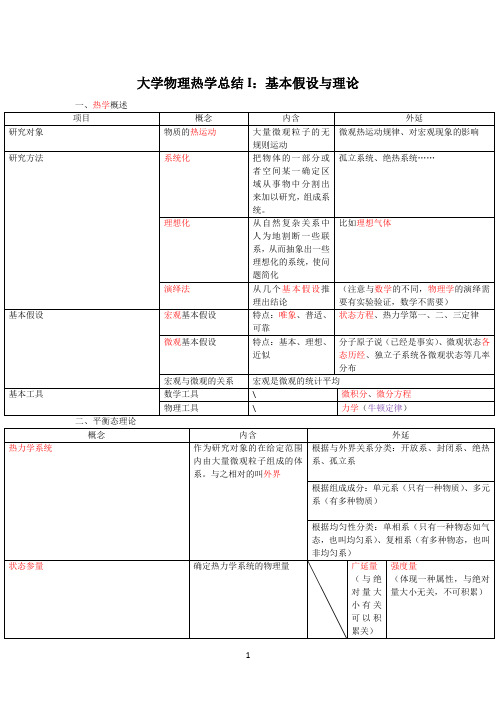
大学物理热学总结I:基本假设与理论二、平衡态理论⑤利用细致平衡原理进一步阐释:就得到用力学算出故两物体如果都和第三物体温度一样,则它们平均动能都和第三个物体一样,由等式传递性它们平均动能一样,从而温度一样。
分子多次碰撞平均动能互相交换,最终平衡。
爱因斯坦扩散方程①布朗运动:大颗粒在液体中受液体分子无序碰撞产生的运动。
是在无序驱动力下的运动。
②流体中斯托克斯公式:f=-6πaηvf:阻力a:物体半径η:粘滞系数v:运动速度③布朗粒子平均能量无序却动力长时间平均值为0 :粒子运动距离平方的平均值。
D:爱因斯坦扩散系数ηT:温度较复杂,略。
无。
麦克斯韦分布律(重点)①数学概率论基础知识,重点是概率密度函数的概念、高斯分布(即正态分布)以及泊松分布(略)。
②数学上多重积分、广义积分知识(略)。
①气体分子通过碰撞达到并维持平衡态②平衡态时分子的位置与速度的概率密度函数不随时间变化③分子位置均匀分布,速度分量为高斯分布①速度分布(y、z方向完全相同):综合公式:②速率分布①确定函数:(1)由于平衡态各向同性,这个函数有旋转不变性,也就是速度分布只和速率有关:(2)方向独立:设每个方向分布函①无量纲速率:定义任意速率值,系数u是无量纲速率。
这样得到无量纲速率分布②麦克斯韦速率分布的实验检验:两个同心圆筒,外层转动,内层分子泰勒展开,得故几率其中为偏移率波尔兹曼分布能量按自由度均分原理准理想气体:分子只有动能,没有势能,分子可以有大小与结构。
理想气体、准理想气体。
①波尔兹曼分布:有势能的系统,势能影响粒子的空间分布。
设坐标(x,y,z)=r则有其中由积分确定,对r的范围积分,结果应该为1。
进一步结论:麦克斯韦分布表现动能影响粒子在动量空间的分布:波尔兹曼分布表现势能影响粒子在几何空间的分布,二者可以综合:②能量按自由度均分原理。
在平衡态下,非相对论粒子的每一个自由度有平均能量。
对于t个平动自由度、r个转动自由度、s个振动自由度的分子,其能量为:注单原子分子t=3 r=s=0刚性双原子分子t=3 r=2 s=0非刚性双原子分子t=3 r=2 s=11、以地球表面附近重力势能为例。
大一热学知识点总结

大一热学知识点总结热学是物理学的重要分支,研究热量的传递、转化和守恒的规律。
在大一学习中,我们对热学有了初步的了解,下面是对大一热学知识点的总结。
一、热力学基本概念1. 热力学系统:指所研究的物体或物质的范围,包括研究对象和周围环境。
2. 热平衡:指热力学系统内部各部分热量的传递达到平衡状态。
3. 热力学第一定律:能量守恒定律,能量可从一种形式转化为另一种形式,但总能量不变。
二、热力学过程与循环1. 等压过程:系统在恒定的压强下进行,体积发生变化。
2. 等容过程:系统的体积保持不变,在容器中发生的过程。
3. 等温过程:系统与周围环境保持温度不变。
4. 绝热过程:系统与外界不进行热量的交换。
5. 热力学循环:系统经历一系列过程后回到初始状态的过程。
三、热力学定律和公式1. 热力学第二定律:热量不会自发地从低温物体传递到高温物体,热量的自发流动方向是从高温到低温。
2. 卡诺循环效率:决定于两个温度之比,既高温与低温的比值。
3. 热力学温标:绝对温度,以绝对零度为零点的温标。
4. 热容量:表示物体吸收或释放热量的能力,单位是焦耳/摄氏度。
5. 等温线和绝热线:在PV图上代表不同过程的曲线。
四、热力学方程1. 理想气体状态方程:PV = nRT,关系压强、体积、物质的摩尔数和温度。
2. 等温变化的理想气体方程:P₁V₁ = P₂V₂,表示等温变化时的物态方程。
3. 等压变化的理想气体方程:V₁/T₁ = V₂/T₂,表示等压变化时的物态方程。
4. 等容变化的理想气体方程:P₁/T₁ = P₂/T₂,表示等容变化时的物态方程。
五、热力学热传导和传热1. 热传导:热量通过物体内部颗粒之间的碰撞传递的过程。
2. 导热系数:衡量物质传热能力的物理量。
3. 热传导的计算:热传导率 = 导热系数 ×断面积 ×温度差 / 材料的厚度。
4. 对流传热:液体或气体中由于温度差而产生的流体运动传递热量。
大学热学知识点总结

热学复习大纲热力学第零定律:在不受外界影响的情况下,只要A 和B 同时与C 处于热平衡,即使A 和B 没有接触,它们仍然处于热平衡状态,这种规律被称为热力学第零定律。
1)选择某种测温物质,确定它的测温属性; 经验温标三要素: 2)选定固定点;3)进行分度,即对测温属性随温度的变化关系作出规定。
经验温标:理想气体温标、华氏温标、兰氏温标、摄氏温标 (热力学温标是国际实用温标不是经验温标) 理想气体微观模型1、分子本身线度比起分子间距小得多而可忽略不计2、除碰撞一瞬间外,分子间互作用力可忽略不计。
分子在两次碰撞之间作自由的匀速直线运动;3、处于平衡态的理想气体,分子之间及分子与器壁间的碰撞是完全弹性碰撞;4、分子的运动遵从经典力学的规律:在常温下,压强在数个大气压以下的气体,一般都能很好地满足理想气体方程。
处于平衡态的气体均具有分子混沌性单位时间内碰在单位面积器壁上的平均分子数 压强的物理意义分子平均平动动能2k 21v m =ε 温度的微观意义 kT v m t 23212==ε 绝对温度是分子热运动剧烈程度的度量是分子杂乱无章热运动的平均平动动能,它不包括整体定向运动动能。
粒子的平均热运动动能与粒子质量无关,而仅与温度有关 气体分子的均方根速率mrms M RTmkTv v 332=== 范德瓦耳斯方程1、分子固有体积修正2、分子吸引力修正k 32εn p =统计关系式宏观可测量量 微观量的统计平均值RT M m b M m V V a M m p V m mol RT b V V ap mm m m m=-⋅+=-+])()][()([:,,)1(,))((:222则范氏方程为体积为若气体质量为范氏气体范德瓦耳斯方程平均值运算法则设)(u f 是随机变量u 的函数, 则)()()()(u g u f u g u f +=+ 若c 为常数,则 )()(u f c u cf =若随机变量u 和随机变量v 相互统计独立。
大学热学物理知识点总结

大学热学物理知识点总结1.热力学基本定律热力学基本定律是热学物理的基础,它包括三个基本定律,分别是热力学第一定律、热力学第二定律和热力学第三定律。
(1)热力学第一定律热力学第一定律是能量守恒定律的热学表述,它规定了热力学系统能量的守恒性质。
简单地说,热力学第一定律表明了热力学系统能量的增减只与系统对外界做功和与外界热交换有关。
热力学第一定律的数学表达式为ΔU=Q-W,其中ΔU表示系统内能的增量,Q表示系统吸热的大小,W表示系统对外界所作的功。
由此可以看出,系统的内能变化量等于吸收热量减去做的功。
(2)热力学第二定律热力学第二定律是热力学系统不可逆性的表述,它规定了热力学系统内部的熵增原理,即系统的熵不会减小,而只会增加或保持不变。
简单地说,热力学第二定律表明了热力学系统内部的任何一种热力学过程都是不可逆的。
这意味着热力学系统永远无法使热量全部转化为功,总会有一部分热量被转化为无效热。
热力学第二定律还表明了热力学过程的方向性,即热量只能从高温物体传递到低温物体,而不能反向传递。
(3)热力学第三定律热力学第三定律规定了当温度趋于绝对零度时,任何物质的熵都将趋于一个有限值,这个有限值通常被定义为零。
简单地说,热力学第三定律表明了在绝对零度时,任何系统的熵都将趋于零。
热力学第三定律的提出对于热学物理的研究具有非常重要的意义,它为我们理解热学系统的性质提供了重要的基础。
2.热力学过程热力学过程是指热力学系统内部发生的一系列变化,包括各种状态参数的变化和热力学系统对外界的能量交换。
常见的热力学过程有等温过程、绝热过程、等容过程和等压过程等。
这些过程在日常生活以及工业生产中都有着广泛的应用。
(1)等温过程等温过程是指在恒定温度下进行的热力学过程。
在等温过程中,系统对外界做的功和吸收的热量之比是一个常数。
这意味着等温过程的压强和体积成反比,在P-V图上表现为一条双曲线。
常见的等温过程有等温膨胀和等温压缩等。
(2)绝热过程绝热过程是指在无热交换的情况下进行的热力学过程。
大学物理(热学知识点总结)

热力发电
利用高温热源和低温热源 之间的温差,通过热力循 环将热能转化为机械能, 再转化为电能。
04
热传递原理
导热、对流和辐射的原理
01 02
导热原理
导热是物质内部微观粒子(如分子、原子等)相互碰撞,将能量从高温 处传到低温处的现象。导热速率与物质的导热系数、温度梯度以及热流 路径的长度有关。
对流原理
热学的发展历程
古代对热现象的认识
01
人类很早就开始对热现象进行观察和利用,如火的使用、烧制
陶器等。
近代热学的形成
02
随着工业革命和科学技术的发展,热学逐渐形成一门独立的学
科,开始有越来越多的学者对热现象进行研究。
现代热学的应用
03
热学在能源利用、环境保护、航天航空等领域得到广泛应用,
成为推动人类社会发展的重要力量。
大学物理(热学知识点总 结)
• 热学概述 • 热力学第一定律 • 热力学第二定律 • 热传递原理 • 热力学与日常生活
01
热学概述
热学的定义与重要性
定义
热学是一门研究热现象的学科,主要 探讨热量传递、热力学过程和热力学 定律等方面的内容。
重要性
热学是物理学的重要分支之一,与日 常生活、工程技术和科学研究密切相 关,对于理解物质的基本性质和变化 规律具有重要意义。
证明
热力学第一定律也可以通过实验来证明。例如,通过测量封闭系统中热量转移和相应体积变化等实验数据,可以 验证热力学第一定律。
定律的应用实例
实例1
在汽车发动机中,燃料燃烧产生的热量转化为机械能,驱动汽车行驶。这正是 热力学第一定律的应用,即能量从一种形式(化学能)转化为另一种形式(机 械能)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大学物理热学总结I:基本假设与理论
二、平衡态理论
(注:只有在平衡态条件下状态参量才有意义。
)
三、各基本假设与基本理论
撞产生的运动。
是在无序驱动力下的运动。
②流体中斯托克斯公式:
f=-6πaηv
f:阻力
a:物体半径η:粘滞系数v:运动速度
③布朗粒子平均能量
ηT:温度
麦克斯韦分布律(重点)①数学概率论基
础知识,重点是
概率密度函数的
概念、高斯分布
(即正态分布)
以及泊松分布
(略)。
②数学上多重积
分、广义积分知
识(略)。
①气体分子通过
碰撞达到并维持
平衡态
②平衡态时分子
的位置与速度的
概率密度函数不
随时间变化
③分子位置均匀
分布,速度分量为
高斯分布
①速度分布(y、z方向完全相同):
综合公式:
②速率分布
③速率分布的特征:
最概然速率(概率密度最大的速
率):
平均速率:
方均根速率(速率平方求平均数再
开根号):
①确定函数:
(1)由于平衡态
各向同性,这个
函数有旋转不变
性,也就是速度
分布只和速率有
关:
(2)方向独立:设
每个方向分布函
数是g
(3)对上式两边
取ln,再对各自
求偏导数,由
三个方向独立
性,这个偏导数
值应该为一个负
的常量:
①无量纲速率:
定义任意速率值
,系数u
是无量纲速率。
这样得到无量纲速
率分布
②麦克斯韦速率分
布的实验检验:
两个同心圆筒,外
层转动,内层分子
飞出来打到外层,
根据飞行途中外层
转过角度来判断飞
行了多少时间,再
用半径差除以时间
算出速率,发现速
率分布非常符合麦
克斯韦分布率。
③逃逸速度。
用方
均根速率比较一个
星球的第二宇宙速
度,算出一种气体
全部逃出某星球大
气层所需时间。
其中为偏移率
波尔兹曼分布
能量按自由度均分原理准理想气体:分
子只有动能,没
有势能,分子可
以有大小与结
构。
理想气体、准理想
气体。
①波尔兹曼分布:有势能的系统,
势能影响粒子的空间分布。
设坐标
(x,y,z)=r则有
其中由积分确定,对r的范围积
分,结果应该为1。
进一步结论:麦克斯韦分布表现动
能影响粒子在动量空间的分布:
波尔兹曼分布表现势能影响粒子在
几何空间的分布,二者可以综合:
②能量按自由度均分原理。
在平衡态下,非相对论粒子的每一
个自由度有平均能量。
对于t个平动自由度、r个转动自由
度、s个振动自由度的分子,其能量
为:
注
单原子分子t=3 r=s=0
刚性双原子分子t=3 r=2 s=0
非刚性双原子分子t=3 r=2 s=1
注:温度不太高的情况下看成刚性
分子。
1、以地球表面附
近重力势能为
例。
①推导等温压强
公式:取截面
dS,高度dz的空
气柱,上、下方
压强差dp,粒子
数密度是n。
压
强与重力平衡:
dpdS=-nmgdzds(
1)
状态方程
P=n
得dp=
代入(1)得
积分得
其中是地面
z=0的粒子数密
度。
再由理想气体状
态方程得到:
等温气压公式。
②推导粒子分
布:
粒子总数
得到
从而
①离心机原理:波
尔兹曼分布(离心
势能)。
②准理想气体内
能。
③非相对论理想气
体定体热容:理想
气体体积一定升高
单位温度所增加的
内能。
摩尔定体热容
每摩尔气体的定体
热容:。
