常用干燥剂的性能和适用范围
高中常用干燥剂及其适用范围

高中常用干燥剂及其适用范围高中常用干燥剂及其适用范围干燥剂是一种能够吸收空气中的水分的物质,常用于保护物品免受潮湿和腐蚀。
在高中化学实验中,干燥剂也是必不可少的实验用品。
下面介绍几种常用的干燥剂及其适用范围。
1. 硅胶干燥剂硅胶干燥剂是一种无毒、无味、无污染的干燥剂,具有良好的吸湿性能。
它通常呈现为白色或淡黄色的颗粒状物质,可以在空气中吸收水分,使其变成透明或淡蓝色。
硅胶干燥剂适用于各种物品的干燥,如衣物、鞋子、书籍、电子产品等。
2. 氯化钙干燥剂氯化钙干燥剂是一种常用的干燥剂,具有很强的吸湿性能。
它通常呈现为白色或淡黄色的颗粒状物质,可以在空气中吸收水分,使其变成水。
氯化钙干燥剂适用于各种物品的干燥,如衣物、鞋子、书籍、电子产品等。
3. 活性炭干燥剂活性炭干燥剂是一种具有良好吸附性能的干燥剂,可以吸附空气中的水分和有害气体。
它通常呈现为黑色或深灰色的颗粒状物质,可以在空气中吸收水分和有害气体,使其变得更加清新。
活性炭干燥剂适用于各种物品的干燥和除臭,如衣物、鞋子、书籍、电子产品等。
4. 碳酸钙干燥剂碳酸钙干燥剂是一种无毒、无味、无污染的干燥剂,具有良好的吸湿性能。
它通常呈现为白色或淡黄色的颗粒状物质,可以在空气中吸收水分,使其变成透明或淡蓝色。
碳酸钙干燥剂适用于各种物品的干燥,如衣物、鞋子、书籍、电子产品等。
总之,干燥剂是一种非常实用的物品,可以保护物品免受潮湿和腐蚀。
在高中化学实验中,干燥剂也是必不可少的实验用品。
以上介绍的几种干燥剂都具有良好的吸湿性能,适用于各种物品的干燥和除臭。
在使用干燥剂时,需要注意选择适合的干燥剂,并按照说明书的要求使用,以达到最佳的干燥效果。
高中化学常用干燥剂

高中化学常用干燥剂有哪些1、浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分;例如常作为H2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂;2、无水氯化钙:因其价廉、干燥能力强而被广泛应用;干燥速度快,能再生,脱水温度473K;一般用以填充干燥器和干燥塔,干燥药品和多种气体;不能用来干燥氨、酒精、胺、酰、酮、醛、酯等;3、无水硫酸镁:有很强的干燥能力,吸水后生成;吸水作用迅速,效率高,价廉,为一良好干燥剂;常用来干燥有机试剂;4、固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质;常用来干燥氢气、氧气和甲烷等气体;5、变色硅胶:常用来保持仪器、天平的干燥;吸水后变红;失效的硅胶可以经烘干再生后继续使用;可干燥胺、NH3、 O2、 N2等6、活性氧化铝Al2O3:吸水量大、干燥速度快,能再生400 -500K烘烤;7、无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差;8、硫酸钙:可以干燥H2 ;O2 ;CO2 ;CO 、N2 ;Cl2、HCl 、H2S、 NH3、 CH4等1 实验室中常用的干燥剂及其特性实验室中常用的干燥剂及其特性①无水氯化钙CaCl2:无定形颗粒状或块状,价格便宜,吸水能力强,干燥速度较快;吸水后形成含不同结晶水的水合物CaCl2·nH2On= 1,2,4,6;最终吸水产物为CaCl2·6H2O 30℃以下,是实验室中常用的干燥剂之一;但是氯化钙能水解成CaOH2 或CaOHCl ,因此不宜作为酸性物质或酸类的干燥剂;同时氯化钙易与醇类,胺类及某些醛、酮、酯形成分子络合物;如与乙醇生成CaCl2·4C2H5OH、与甲胺生成CaCl2·2CH3NH2,与丙酮生成CaCl2·2CH32CO 等, 因此不能作为上述各类有机物的干燥剂;②无水硫酸钠Na2SO4:白色粉末状,吸水后形成带10个结晶水的硫酸钠Na2SO4·10H2O;因其吸水容量大,且为中性盐,对酸性或碱性有机物都可适用,价格便宜,因此应用范围较广;但它与水作用较慢,干燥程度不高;当有机物中夹杂有大量水分时,常先用它来作初步干燥,除去大量水分,然后再用干燥效率高的干燥剂干燥;使用前最好先放在蒸发皿中小心烘炒,除去水分,然后再用;③无水硫酸镁MgSO4:白色粉末状,吸水容量大,吸水后形成带不同数目结晶水的硫酸镁MgSO4·nH2O n=1,2,4,5,6,7;最终吸水产物为MgSO4·7H2O48℃以下;由于其吸水较快,且为中性化合物,对各种有机物均不起化学反应,故为常用干燥剂;特别是那些不能用无水氯化钙干燥的有机物常用它来干燥;④无水硫酸钙CaSO4:白色粉末,吸水容量小,吸水后形成2CaSO4·H2O100℃以下;虽然硫酸钙为中性盐,不与有机化合物起反应,但因其吸水容量小,没有前述几种干燥剂应用广泛;由于硫酸钙吸水速度快,而且形成的结晶水合物在100℃以下较稳定,所以凡沸点在100℃以下的液体有机物,经无水硫酸钙干燥后,不必过滤就可以直接蒸馏;如甲醇、乙醇、乙醚、丙酮、乙醛、苯等,用无水硫酸钙脱水处理效果良好;⑤无水碳酸钾K2CO3:白色粉末,是一种碱性干燥剂;其吸水能力中等,能形成带两个结晶水的碳酸钾K2CO3·2H2O,但是与水作用较慢;适用于干燥醇、酯等中性有机物以及一般的碱性有机物如胺、生物碱等;但不能作为酸类、酚类或其他酸性物质的干燥剂;⑥固体氢氧化钠NaOH和氢氧化钾KOH:白色颗粒状,是强碱性化合物;只适用于干燥碱性有机物如胺类等;因其碱性强,对某些有机物起催化反应,而且易潮解,故应用范围受到限制;不能用于干燥酸类、酚类、酯、酰胺类以及醛酮;⑦五氧化二磷P2O5:是所有干燥剂中干燥效力最高的干燥剂;与水的作用过程是:P2O5与水作用非常快,但吸水后表面呈粘浆状,操作不便;且价格较贵;一般是先用其他干燥剂如无水硫酸镁或无水硫酸钠除去大部分水,残留的微量水分再用P2O5干燥;它可用于干燥烷烃、卤代烷、卤代芳烃、醚等,但不能用于干燥醇类、酮类、有机酸和有机碱;⑧金属钠Na:常常用作醚类、苯等惰性溶剂的最后干燥;一般先用无水氯化钙或无水硫酸镁干燥除去溶剂中较多量的水分,剩下的微量水分可用金属钠丝或钠片除去;但金属钠不适用于能与碱起反应的或易被还原的有机物的干燥;如不能用于干燥醇制无水甲醇、无水乙醇等除外、酸、酯、有机卤代物、酮、醛及某些胺;⑨氧化钙CaO: 是碱性干燥剂;与水作用后生成不溶性的CaOH2,对热稳定,故在蒸馏前不必滤除;氧化钙价格便宜,来源方便,实验室常用它来处理95%的乙醇,以制备99%的乙醇;但不能用于干燥酸性物质或酯类;第四点就是你要求的乙醛的干燥说明,希望这些对你会有所帮助注意:1、固体干燥剂颗粒大小要适当,颗粒太大气体和干燥剂接触面小,不利于干燥效果不好;颗粒太小,气体不易通过,容易堵塞,一般以黄豆粒大小为宜;2、液体干燥剂用量要适当,并控制好通入气体的速度,为了防止发生倒吸,在洗气瓶与反应容器之间应连接安全瓶;二、气体的分类1、根据酸碱性,酸性气体:CO2、SO2、NO2、HCl、Cl2、H2S、HBr、HI等碱性气体:只有NH3中性气体:H2、O2、CH4、CO、CH2=CH2、C2H2、N2等2、根据常温氧化还原性强弱,强还原性气体:H2S、HBr、HI、SO2等一般性气体:H2、O2、CH4等三、气体干燥剂的类型及选择1、常用气体干燥剂按酸碱性可分为三类:①酸性干燥剂,如浓硫酸、五氧化二磷、硅胶;酸性干燥剂能够干燥酸性或中性的气体,如CO2、SO2、NO2、HCl、H2、Cl2、O2、CH4等气体;②碱性干燥剂,如生石灰、碱石灰、固体NaOH;碱性干燥剂可以用来干燥碱性或中性的气体,如NH3、H2、O2、CH4等气体;③中性干燥剂,如无水氯化钙、无水硫酸铜等,可以干燥中性、酸性、碱性气体,如O2、H2、CH4等;2、根据干燥剂的氧化性分两类①强氧化性干燥剂:浓硫酸②一般干燥剂:五氧化二磷、硅胶、生石灰、碱石灰、固体NaOH、CaCl2、CuSO4等3、干燥剂选择的基本原则:根据干燥剂和气体的性质选择,其基本原则是干燥剂只吸收气体中的水分,不吸收被干燥的气体,具体表现在:1在选用干燥剂时,显碱性的气体不能选用酸性干燥剂,如不能用碱石灰、CaO和NaOH干燥CO2、SO2、HCl、H2S、Cl2、NO2等;2显酸性的气体不能选用碱性干燥剂,如不能用P2O5、浓H2SO4干燥NH3;3还原性的气体不能选用有强氧化性的干燥剂,如不能用浓H2SO4干燥H2S、HBr、HI等;虽然H2、SO2、CO、CH4也有还原性,但是浓硫酸在常温下不能氧化它们,可以用浓硫酸干燥;4能与气体反应的物质不能选作干燥剂,如不能用无水氯化钙干燥NH3因生成CaCl2·8NH3;浓硫酸可以和烯、炔、NO2发生反应,浓硫酸不能干燥烯烃、炔烃和NO2;四、气体净化中干燥装置的位置顺序气体的干燥是气体净化的环节之一,在干燥装置和其它净化或反应装置连接时注意:一般情况下,若采用溶液作除杂试剂,则是先除杂后干燥;若采用加热除去杂质,则是先干燥后加热;为了防止大气中的水气侵入,有特殊干燥要求的开口反应装置可加干燥管,进行空气的干燥;。
有机常用干燥剂介绍.jsp

各类有机物常用干燥剂介绍1,CaCL2,中性,与水作用产物:CaCL2.nH2O,n=1,2,4,6。
适用范围:烃类,卤代烃,烯酮,醚,硝基化合物,中性气体,氯化氢。
非适用范围:醇,胺,氨,酚,酯,酸,酰胺和某些醛酮。
特点:吸水量大,作用快,效力不高,是良好的初步干燥剂。
廉价,含有碱性杂质氢氧化钙。
2,硫酸钠中性,与水作用产物:七水和十水硫酸钠。
适用范围:醇,酯,醛,酮,酸,酰胺,卤代烃,硝基化合物等不能用氯化钙干燥的物质。
吸水特点:吸水量大,作用慢,效力低,是良好的初步干燥剂。
3,硫酸镁中性,与水作用产物:一水和七水硫酸镁。
适用范围:醇,酯,醛,酮,酸,酰胺,卤代烃,硝基化合物等不能用氯化钙干燥的物质。
特点:较硫酸钠作用快,效力高。
4,硫酸钙中性,与水作用产物:CaSO4.1/2H2O,适用范围:烷,芳香烃,醚,醇,醛,酮。
特点:吸水量小,作用快,效力高,可先用吸水量大的干燥剂初步干燥后再用。
5,碳酸钾碱性,与水作用产物:1.5水和2水合物。
适用范围:醇,酮,脂,胺和杂环等碱性化合物,非适用范围:酸,酚及其他酸性化合物。
6,硫酸强酸性。
与水作用产物:H3OSO4。
适用范围:脂肪烃,烷基卤代物。
非适用范围:烯,醚,醇及弱碱性化合物。
特点:脱水效力高。
7,氢氧化钾,氢氧化钠强碱性。
适用于胺,杂环等碱性化合物干燥。
非适用于醇,酯,醛酮,酸,酚和酸性化合物干燥。
其特点是干燥快速有效。
8,金属钠强碱性。
适用于醚,三级胺,烃中的痕量水干燥。
对碱土金属或对碱敏感物,醇等不适用。
其特点是效力高,作用慢,需经初步干燥后才可再用,干燥后需蒸馏。
9,P2O5,酸性,适用于醚,烃,卤代烃,腈中痕量水分,酸溶液,二硫化碳。
不适用于醇,酸,酮,胺,,碱性化合物,氯化氢,氟化氢等的干燥。
其特点是吸水效力高,干燥后需蒸馏。
10,CaH2,碱性,适用于碱性,中性,弱酸性化合物干燥,不适用于对碱敏感的化合物干燥。
其特点是效力高,作用慢,先经初步干燥再用,干燥后需蒸馏。
各种常用干燥剂的性能和用途介绍.doc

各种常用干燥剂的性能和用途介绍1、浓H2SO4具有强烈的吸水性,常用来除去不与H2S0衣应的气体中的水分。
例如常作为H2、02 CO S02 N2、HCI、CH4 C02 CI2等气体的干燥剂。
2、无水氯化钙:因其价廉、干燥能力强而被广泛应用。
干燥速度快,能再生,脱水温度473K。
一般用以填充干燥器和干燥塔,干燥药品和多种气体。
不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。
3、无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4.7H2Q吸水作用迅速,效率高,价廉,为一良好干燥剂。
常用来干燥有机试剂。
4、固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质。
党用来干燥氢气、氧气、氨和甲烷等气体。
5、变色硅胶:常用来保持仪器、天平的干燥。
吸水后变红。
失效的硅胶可以经烘干再生后继续使用。
可干燥胺、NH3 02、N2等6活性氧化铝(AI203):吸水量大、干燥速度快,能再生(400 -500K烘烤)。
7、无水硫酸钠:干燥温度必须控制在30C以内,干燥性比无水硫酸镁差。
8、硫酸钙:可以干燥H2。
02。
C02。
C0、N2。
CI2、HCI、H2S NH3、CH4等由上述可知、对一些气体的干燥剂可作如下选择。
气体名称常用干燥剂气体名称常用干燥剂CO 浓H2SO4 CaCI2、P2O5 H2S CaCI2C02 CaCI2、浓H2SO4 P2O5 N2 浓H2SO4 C aCI2、P2O5CI2 CaCI2、浓H2SO4 NH3 CaO KOH或碱石灰H2 CaCI2、P2O5 NO Ca(NO3)2HBr CaBr2、ZnBr2、03 CaCI2HCI CaCI2、浓H2SO4 S02浓H2SO4 CaCI2、P2O5Cal2HI液体适用干燥剂Applicable Con diti on of Drying Age nts常用干燥剂注:使用高氯酸盐时务必小心,碳、硫、磷及一切有机物都不能与之接触,否则会发生猛烈爆炸,造成危险。
高中化学常见干燥剂归纳整理39563知识分享

高中化学常见干燥剂归纳整理1.高中化学常见的干燥剂有哪些浓硫酸、五氧化二磷固体烧碱、石灰和碱石灰(氢氧化钠和氧化钙的混合物)无水氯化钙、无水硫酸镁无水硫酸铜2.分类及使用常用的干燥剂有三类第一类为酸性干燥剂。
有浓硫酸、五氧化二磷、硅胶等;第二类为碱性干燥剂,有固体烧碱、石灰和碱石灰(氢氧化钠和氧化钙的混合物)等;第三类是中性干燥剂,如无水氯化钙、无水硫酸镁等。
常用干燥剂的性能和用途如下:1.浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分。
例如常作为H2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂。
2.无水氯化钙:因其价廉、干燥能力强而被广泛应用。
干燥速度快,能再生,脱水温度473K。
一般用以填充干燥器和干燥塔,干燥药品和多种气体。
不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。
3.无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4·7H2O。
吸水作用迅速,效率高,价廉,为一良好干燥剂。
常用来干燥有机试剂。
4.固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质。
常用来干燥氢气、氧气和甲烷等气体。
5.变色硅胶:常用来保持仪器、天平的干燥。
吸水后变红。
失效的硅胶可以经烘干再生后继续使用。
可干燥胺、NH3、O2、N2等。
6.活性氧化铝(Al2O3):吸水量大、干燥速度快,能再生(400 -500K烘烤)。
7.无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差。
8.硫酸钙:可以干燥H2、O2、CO2、CO 、N2、Cl2、HCl 、H2S、NH3、CH4等。
注:无水硫酸铜(CuSO4)(无水硫酸铜成白色)也具有一定的干燥性,并且吸水后变成蓝色的五水硫酸铜(CuSO4·5H2O),但一般不用来做干燥剂。
3.干燥剂的选择由上述可知、对一些气体的干燥剂可作如下选择。
一般的说,酸性干燥剂不能干燥碱性气体,可以干燥酸性气体及中性气体;碱性干燥剂不能干燥酸性气体,可以干燥碱性气体及中性气体;中性干燥剂可以干燥各种气体。
常用干燥剂及其使用

实验室常用干燥剂及其使用除去固体、液体或气体内少量水分的方法称干燥。
有机实验中几乎所做的每一步反应都会遇到试剂、溶剂和产品的干燥问题,所以干燥是实验室中最普通但最重要的一项操作。
如果试剂和产品不进行干燥或干燥不完全,将直接影响有机反应、定性分析、定量分析、波谱鉴定和物理常数测定的结果。
干燥方法可分为物理方法与化学方法两种。
物理方法有吸附(包括离子交换树脂法和分子筛吸附法)、共沸蒸馏、分馏、冷冻、加热和真空干燥等,化学方法按去水作用的方式又可分为两类:一类与水能可逆地结合生成水合物,如氯化钙、硫酸钠等;一类与水会发生剧烈的化学反应,如金属钠、五氧化二磷等。
下面按有机物的物理状态介绍各种干燥的方法和实验操作。
1.固体的干燥(1)晾干:将待干燥的固体放在表面皿上或培养皿中,尽量平铺成一薄层、再用滤纸或培养皿覆盖上,以免灰尘沾污,然后在室温下放置直到干燥为止,这对于低沸点溶剂的除去是既经济又方便的方法。
(2)红外灯干燥:固体中如含有不易挥发的溶剂时,为了加速干燥,常用红外灯干燥。
干燥的温度应低于晶体的熔点,干燥时旁边可放一支温度计,以便控制温度。
要随时翻动固体,防止结块。
但对于常压下易升华或热稳定性差的结晶不能用红外灯干燥。
红外灯可用可调变压器来调节温度,使用时温度不要调得过高,严防水滴溅在灯泡上而发生炸裂。
(3)烘箱烘干:实验室内常用带有自动温度控制系统的电热鼓风干燥箱,其使用温度一般为50~300℃,通常使用温度应控制在100~200℃的范围内。
烘箱用来干燥无腐蚀、无挥发性、加热不分解的物品。
切忌将挥发、易燃、易爆物放在烘箱内烘烤,以免发生危险。
(4)干燥器干燥:普通干燥器一般适用于保存易潮解或升华的样品。
但干燥效率不高,所费时间较长。
干燥剂通常放在多孔瓷板下面,待干燥的样品用表面皿或培养皿装盛,置于瓷板上面,所用干燥剂由被除去溶剂的性质而定。
1. 变色硅胶是使用较普遍的干燥剂,其制备方法是:将无色硅胶平铺在盘中,在大气中放置几天,任其吸收水分,以减少应力,如果部分干燥的硅胶有内应力,浸入溶液中即会发生炸裂,变成更小的颗粒状,当吸收的水分使它质量增了原质量的1/5时,浸入20%氯化钴的乙醇溶液中,15~30分钟后取出晾干,再置于250~300℃的烘箱中活化至恒重,即得变色硅胶。
常用干燥剂

高中常用干燥剂1、浓H2SO4:具有强烈的吸水性,常用来除去不与H2SO4反应的气体中的水分。
例如常作为H2、O2、CO、SO2、N2、HCl、CH4、CO2、Cl2等气体的干燥剂。
2、无水氯化钙:因其价廉、干燥能力强而被广泛应用。
干燥速度快,能再生,脱水温度473K。
一般用以填充干燥器和干燥塔,干燥药品和多种气体。
不能用来干燥氨、酒精、胺、酰、酮、醛、酯等。
3、无水硫酸镁:有很强的干燥能力,吸水后生成MgSO4.7H2O。
吸水作用迅速,效率高,价廉,为一良好干燥剂。
常用来干燥有机试剂。
4、固体氢氧化钠和碱石灰:吸水快、效率高、价格便宜,是极佳的干燥剂,但不能用以干燥酸性物质。
常用来干燥氢气、氧气和甲烷等气体。
5、变色硅胶:常用来保持仪器、天平的干燥。
吸水后变红。
失效的硅胶可以经烘干再生后继续使用。
可干燥胺、NH3、 O2、 N2等6、活性氧化铝(Al2O3):吸水量大、干燥速度快,能再生(400 -500K烘烤)。
7、无水硫酸钠:干燥温度必须控制在30℃以内,干燥性比无水硫酸镁差。
8、硫酸钙:可以干燥H2。
O2。
CO2。
CO 、N2。
Cl2、HCl 、H2S、 NH3、 CH4等①无水氯化钙(CaCl2):无定形颗粒状(或块状),价格便宜,吸水能力强,干燥速度较快。
吸水后形成含不同结晶水的水合物CaCl2·nH2O(n= 1,2,4,6)。
最终吸水产物为CaCl2·6H2O (30℃以下),是实验室中常用的干燥剂之一。
但是氯化钙能水解成Ca(OH)2或Ca(OH)Cl ,因此不宜作为酸性物质或酸类的干燥剂。
同时氯化钙易与醇类,胺类及某些醛、酮、酯形成分子络合物。
如与乙醇生成CaCl2·4C2H5OH、与甲胺生成 CaCl2·2CH3NH2,与丙酮生成CaCl2·2(CH3)2CO 等,因此不能作为上述各类有机物的干燥剂。
②无水硫酸钠(Na2SO4):白色粉末状,吸水后形成带10个结晶水的硫酸钠(Na2SO4·10H2O)。
常用干燥剂的性能及应用范围
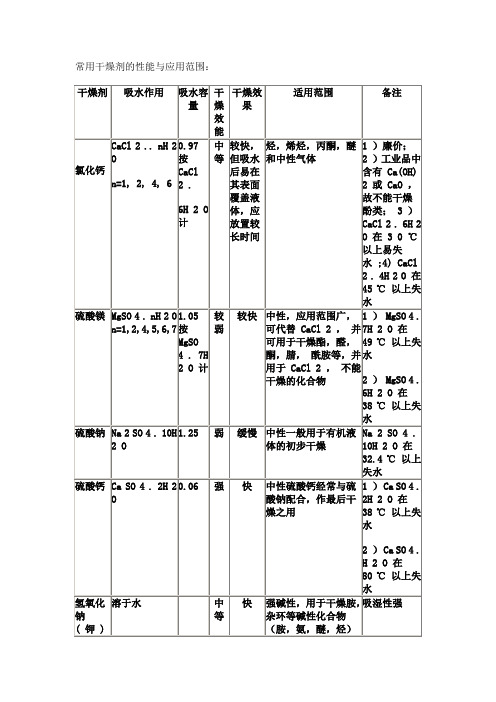
MgSO 4 . nH 2 O n=1,2,4,5,6,7
1.05按MgSO 4 . 7H 2 O计
较弱
较快
中性,应用范围广,可代替CaCl 2,并可用于干燥酯,醛,酮,腈,酰胺等,并用于CaCl 2,不能干燥的化合物
1)MgSO 4 . 7H 2 O在49℃以上失水
2)MgSO 4 . 6H 2 O在38℃以上失水
2较弱慢弱碱性用于干燥醇酮酯胺杂环等碱性化合物可代替koh干燥胺类可用于酸酚快限于干燥醚烃叔胺中痕量水分有吸湿性金属钠nah2o12h2naohcaoh2o强忌水氧化钙碱石灰bao类caoh2强较快中性及碱性气体胺醇乙醚对热很稳定不挥发干燥后可直接蒸馏吸湿性很强用于干燥气体时需与载体相混五氧化二磷p2o53h2o2h3po4强快但吸水后表面被粘浆覆盖操作不便适于干燥烃卤代烃腈等中的痕量水分
硫酸钠
Na 2 SO 4 . 10H 2 O
1.25
弱
缓慢
中性一般用于有机液体的初步干燥
Na 2 SO 4 . 10H 2 O在32.4℃以上失水
硫酸钙
Ca SO 4 . 2H 2 O
0.06
强
快
中性硫酸钙经常与硫酸钠配合,作最后干燥之用
1)Ca SO 4 . 2H 2 O在38℃以上失水
2)Ca SO 4 . H 2 O在80℃以上失水
氢氧化钠(钾)
溶于水
中等
快
强碱性,用于干燥胺,杂环等碱性化合物(胺,氨,醚,烃)
吸湿性强
碳酸钾
K 2 CO 3 . 1/2 H 2 O
0.2
较弱
慢
弱碱性,用于干燥醇,酮,酯,胺,杂环等碱性化合物,可代替KOH干燥胺类,可用于酸,酚
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
备注
CaO
2×10-1
白色固体,碱性氧化物。可干燥O2、N2、NH3等气体,也可干燥低级醇和胺等液态有机物。常在干燥器中使用。不可用来干燥酸性气体,如CO2、HCl、H2S等。
与水结合形成Ca(OH)2加热到450℃再生。
CaCl2
(1.4~2.5)×10-1
白色多孔固体,有较强的吸湿性。可以干燥H2、O2、N2、CO2、CO、SO2、HCl、CH4、C2H4等多种气体。可以干燥烃、卤代物、醚、酮、硝基化合物等液态有机物。不能用来干燥NH3以及含有—OH和—NH2的有机物
与水结合成水合物,不能再生。
CaSБайду номын сангаас4
4×10-3
白色粉末。可干燥H2、O2、N2、CO2、CO、SO2、Cl2、HCl、H2S等气体,也可干燥烷烃、醚、醛、酮、羧酸等液态有机物。不适用于干燥HF、胺、乙醇等。
与水结合形成CaSO4·2H2O,加热到230℃~240℃下脱水再生。
干燥剂
1L空气中残留水的质量/mg
和水形成水化物,不能再生。
Mg(ClO4)2
5×10-4
白色固体,具有极强氧化性,易潮解,有强烈吸水作用。适用于干燥中性或酸性气体,不可以用于能被氧化的物质。严禁与有机物、碳、硫、磷等可燃物接触,以免引起爆炸。
吸水后形成含2、3、4、6个结晶水合物,在190℃以上可烘干再生,温度不可过高,Mg(ClO4)2在251℃时分解。
吸水后形成结晶水合物,加热到260℃再生。
碱石灰
白色固体,呈碱性。可以干燥NH3等气体,不能干燥酸性气体及醇、醛、酮、酸、酯、酚等液态有机物。常用于避免水或CO2进入反应系统装置中。
碱石灰由CaO粉碎后加入NaOH溶液,经充分混合后,置铁皿中于200℃~250℃干燥而成。它的大致成分是:83%Ca(OH)2、5%NaOH、12%H2O。
吸附水后的硅胶可于120℃下烘干再生。
Al2O3
3×10-3
白色粉末,中心,是吸附性较强的多孔性吸附剂,适用于多数气体。
吸附水的氧化铝,可以在175℃下烘干再生。
(100%)H2SO4
95%
3×10-2
3×10-1
氧化性酸。可以干燥H2、O2、N2、CO、SO2、Cl2、HCl、CH4等多种气体,不可以用来干燥NH3、H2S、HBr、HI等碱性或易被氧化的气体。常在干燥器中使用。
BaO
6.5×10-4
白色固体,碱性氧化物,有毒!吸水性强,也能吸收酸性气体。用于干燥O2、N2、NH3等。不可以干燥HCl、H2S、CO2、SO2等酸性气体。
跟水化合成Ba(OH)2,不能再生。
硅胶
(0.5~3)×10-3
是半透明、内表面积很大的多孔固体,属良好的吸附剂,对水有强烈的吸附作用。可干燥O2、N2、NH3等气体。常用于干燥器中。含有钴盐的硅胶,称为变色硅胶,干燥时呈蓝色,吸水后呈粉红色。
MgSO4
白色粉末。常用于干燥卤代物、醇、醛、酮、羧酸、酯、酚、硝基化合物等液态有机物
与水结合成结晶水合物MgSO4·7H2O。
Na2SO4
白色粉末。使用范围同MgSO4
与水结合形成结晶水合物Na2SO4·10H2O
K2CO3
白色粉末,碱性。常用于干燥酮、酯、胺等液态有机物。
与水结合才水合物。
常用干燥剂的性能和适用范围
干燥剂
1L空气中残留水的质量/mg
性质和适用范围
备注
P2O5
2×10-5
白色粉末,酸性,有强烈和水结合的能力,不仅能结合游离水,还能夺取化合物中的水。可以干燥H2、O2、N2、CO2、CO、SO2、CH4、C2H4等气体,不可以干燥氨、胺、卤化氢和硝酸等,也不可用来干燥醇、羧酸和酮等有机物。
