2020-02-21工业流程题 删减版答案解析
2020届高三化学高考考前复习——工业流程图专题训练(有答案)
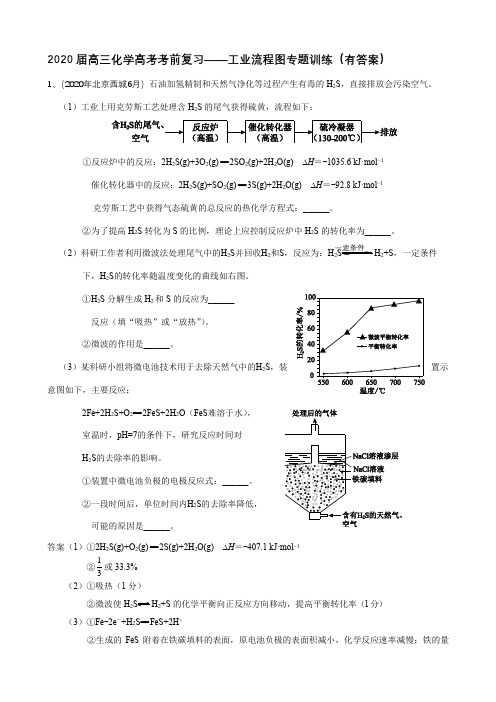
2020届高三化学高考考前复习——工业流程图专题训练(有答案)1、(2020年北京西城6月)石油加氢精制和天然气净化等过程产生有毒的H 2S ,直接排放会污染空气。
(1)工业上用克劳斯工艺处理含H 2S 的尾气获得硫黄,流程如下:①反应炉中的反应:2H 2S(g)+3O 2(g) == 2SO 2(g)+2H 2O(g) ∆H =-1035.6 kJ·mol −1催化转化器中的反应:2H 2S(g)+SO 2(g) == 3S(g)+2H 2O(g) ∆H =-92.8 kJ·mol −1克劳斯工艺中获得气态硫黄的总反应的热化学方程式:______。
②为了提高H 2S 转化为S 的比例,理论上应控制反应炉中H 2S 的转化率为______。
(2)科研工作者利用微波法处理尾气中的H 2S 并回收H 2和S ,反应为:H 2SH 2+S ,一定条件下,H 2S 的转化率随温度变化的曲线如右图。
①H 2S 分解生成H 2和S 的反应为______反应(填“吸热”或“放热”)。
②微波的作用是______。
(3)某科研小组将微电池技术用于去除天然气中的H 2S ,装置示意图如下,主要反应:2Fe+2H 2S+O 2== 2FeS+2H 2O (FeS 难溶于水),室温时,pH=7的条件下,研究反应时间对H 2S 的去除率的影响。
①装置中微电池负极的电极反应式:______。
②一段时间后,单位时间内H 2S 的去除率降低,可能的原因是______。
答案(1)①2H 2S(g)+O 2(g) == 2S(g)+2H 2O(g) ∆H =-407.1 kJ·mol −1② 或33.3% (2)①吸热(1分)②微波使H 2S H 2+S 的化学平衡向正反应方向移动,提高平衡转化率(1分)(3)①Fe -2e -+H 2S == FeS+2H +②生成的FeS 附着在铁碳填料的表面,原电池负极的表面积减小,化学反应速率减慢;铁的量一定条件13因消耗而减少,形成微电池的数量减少,化学反应速率减慢2、资源的高效利用对保护环境、促进经济持续健康发展具有重要作用。
工业流程教案包含答案

(1)贝壳重要成分的化学式是。
(2)操作a的名称是 , 在实验室中进行此项操作, 需要的玻璃仪器有烧杯、玻璃棒、。
(3)工业冶炼镁常用电解MgCl2的方法, 反映为:MgCl2 电解 Mg+ 。
(4)写出第②、③两步反映的化学方程式:② , ③。
解析本题以海水的开发和运用为背景, 结合海水制备金属镁的工艺流程, 综合考察了化学方程式的书写、过滤操作及物质间的反映规律。
石灰乳的成分是氢氧化钙, 与海水中的氯化镁作用可生成Mg(OH)2与氯化钠, 通过过滤操作便可得将两者分离。
答案: (1)CaCO3 (2)过滤漏斗(3)Cl2 (4)②CaO+H2O=Ca(OH)2 ③Mg(OH)2+2HCl=MgCl2+2H2O五、生产牙膏摩擦剂的工艺流程例5. (2023年·苏州中考题)用作牙膏摩擦剂的轻质碳酸钙可以用矿石A来制备, 某化学爱好小组设计了2种转化流程, 如图所示。
已知: a. 二氧化碳连续通入氢氧化钙溶液发生如下反映:CO2+Ca(OH)2==CaCO3↓+H2O, CaCO3+H2O+CO2==Ca(HCO3)2;b.碳酸氢钙微溶于水, 微热易分解:Ca(HCO3)2微热CaCO3↓+H2O+ CO2↑;c. 生石灰与水充足反映后可得到颗粒非常细小的熟石灰浆。
试填空。
(1)小王主张用流程①、②、④和操作Ⅱ的设计, 认为其工艺简朴。
请写出反映①和④的化学方程式:①;④;操作Ⅱ涉及等工序。
(2)制轻质碳酸钙时, D为 (选填“悬浊液”或“溶液”或“乳浊液”),理由是: .(3)小李认为流程①、②、③和操作I比小王的主张更好, 其理由是: ______ ______ ;操作I涉及搅拌和微热等工序。
解析本题为联系生活实际的应用性问题, 它是以碳及其化合物的性质为载体, 考察了学生分析流程图, 解决实际问题的能力。
通过解题, 要使学生更进一步结识化学与社会、生活的密切联系, 增强学习的自觉性和积极性。
化学工业流程高考题汇编(有标准答案)[1]
![化学工业流程高考题汇编(有标准答案)[1]](https://img.taocdn.com/s3/m/41e225fb6bd97f192379e9c9.png)
化学工业流程高考题汇编(有标准答案)(word版可编辑修改)编辑整理:尊敬的读者朋友们:这里是精品文档编辑中心,本文档内容是由我和我的同事精心编辑整理后发布的,发布之前我们对文中内容进行仔细校对,但是难免会有疏漏的地方,但是任然希望(化学工业流程高考题汇编(有标准答案)(word版可编辑修改))的内容能够给您的工作和学习带来便利。
同时也真诚的希望收到您的建议和反馈,这将是我们进步的源泉,前进的动力。
本文可编辑可修改,如果觉得对您有帮助请收藏以便随时查阅,最后祝您生活愉快业绩进步,以下为化学工业流程高考题汇编(有标准答案)(word版可编辑修改)的全部内容。
化工生产真题训练1、(2014山东高考)工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾(K2Cr2O7)。
工艺流程及相关物质溶解度曲线如图:(1)由Na2Cr2O7生产K2Cr2O7的化学方程式为____________________________,通过冷却结晶析出大量K2Cr2O7的原因是____________________________。
(2)向Na2Cr2O7母液中加碱液调PH的目的是____________________________。
(3)固体A主要为__________________(填化学式),固体B主要为________(填化学式)。
(4)用热水洗涤固体A,回收的洗涤液转移到母液______(填“I”“II”或“III”)中,既能提高产率又可使能耗最低。
2、(2014年江苏高考)烟气脱硫能有效减少二氧化硫的排放。
实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6—2x]溶液,并用于烟气脱硫研究。
(1)酸浸时反应的化学方程式为;滤渣Ⅰ的主要成分为.(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)。
工业流程(含答案)

1、MnO2是一种重要的无机功能材料,粗MnO2的提纯是工业生产的重要环节。
某研究性学习小组设计了将粗MnO2(含有较多的MnO2和MnCO3)样品转化为纯MnO2实验,其流程如下:(1)第①步加稀H2SO4时,粗MnO2样品中的___________(写化学式)转化为可溶性物质。
(2)第②步反应的离子方程式(3)第③步蒸发操作必需的仪器有铁架台(含铁圈)、_____________、____________、___________,已知蒸发得到的固体中有NaClO3和NaOH,则一定还有含有_______________________(写化学式)。
(4)若粗MnO2样品的质量为12.69g,第①步反应后,经过滤得到8.7gMnO2,并收集到0.224 L CO2(标准状况下),则在第②步反应中至少需要______mol NaClO3。
(1)MnO2、MnCO3(2)5Mn2+,2,4H2O,5,8H+(3)蒸发皿;酒精灯;玻璃棒;NaCl(4)0.022、高温条件下,辉铜矿(主要成分为Cu2S)通适量的空气可冶炼金属铜,经过一系列反应可得到B和D、E。
G为砖红色沉淀。
请回答下列问题:S)通适量的空气冶炼金属铜的化学方程式为,其中氧化(1)辉铜矿(Cu2剂为。
(2)E的浓溶液与Cu发生反应②的化学方程式是。
(3)利用电解可提纯铜,在该电解反应中阳极物质是,电解质溶液是。
)相遇时会缓慢发生下列反应产生(4)自然界中当胆矾矿与黄铁矿(主要成分为FeS2辉铜矿。
对反应:14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,被氧化的硫和被还原的硫的质量比为。
(1)Cu 2S +O 2(适量)2Cu +SO 2 O 2和Cu 2S (2)Cu +2H 2SO 4(浓)CuSO 4+SO 2↑+2H 2O (3)粗铜 硫酸铜或含Cu 2+的盐溶液(4)3∶7 3、高铁酸盐在能源、环保等方面有着广泛的用途。
工业流程(含答案)
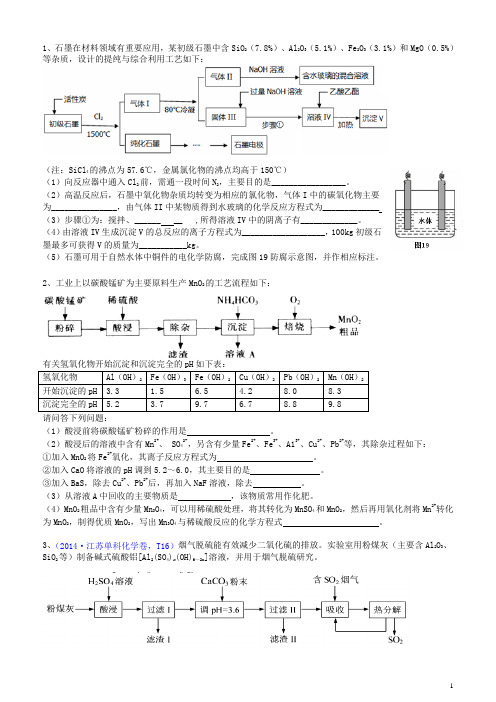
1、石墨在材料领域有重要应用,某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质,设计的提纯与综合利用工艺如下:(注:SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃)(1)向反应器中通入Cl2前,需通一段时间N2,主要目的是_________________。
(2)高温反应后,石墨中氧化物杂质均转变为相应的氯化物,气体I中的碳氧化物主要为_______________,由气体II中某物质得到水玻璃的化学反应方程式为_____________(3)步骤①为:搅拌、______ __ ,所得溶液IV中的阴离子有_____________。
(4)由溶液IV生成沉淀V的总反应的离子方程式为___________________,100kg初级石墨最多可获得V的质量为___________kg。
(5)石墨可用于自然水体中铜件的电化学防腐,完成图19防腐示意图,并作相应标注。
2、工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下:有关氢氧化物开始沉淀和沉淀完全的pH如下表:氢氧化物Al(OH)2Fe(OH)3Fe(OH)2Cu(OH)2Pb(OH)2Mn(OH)2开始沉淀的pH 3.3 1.5 6.5 4.28.08.3沉淀完全的pH 5.2 3.79.7 6.78.89.8请问答下列问题:(1)酸浸前将碳酸锰矿粉碎的作用是。
(2)酸浸后的溶液中含有Mn2+、 SO42-,另含有少量Fe2+、Fe3+、A13+、Cu2+、Pb2+等,其除杂过程如下:①加入MnO2将Fe2+氧化,其离子反应方程式为。
②加入CaO将溶液的pH调到5.2~6.0,其主要目的是。
③加入BaS,除去Cu2+、Pb2+后,再加入NaF溶液,除去。
(3)从溶液A中回收的主要物质是,该物质常用作化肥。
(4)MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2,写出Mn3O4与稀硫酸反应的化学方程式。
2020届高三化学工业流程专题训练试题及答案

2020届高三化学工业流程专题训练试题及答案1、(2020年北京西城4月模拟)我国化学家侯德榜发明的“侯氏制碱法”联合合成氨工业生产纯碱和氮肥,工艺流程图如下。
碳酸化塔中的反应:NaCl+NH3+CO2+H2O== NaHCO3↓+NH4Cl。
下列说法不正确...的是A.以海水为原料,经分离、提纯和浓缩后得到饱和氯化钠溶液进入吸氨塔B.碱母液储罐“吸氨”后的溶质是NH4Cl和NaHCO3C.经“冷析”和“盐析”后的体系中存在平衡NH4Cl(s)NH4+(aq) + Cl-(aq)D.该工艺的碳原子利用率理论上为100%答案:B2、(2019·四川省教考联盟高三第三次诊断性考试)处理锂离子二次电池正极废料铝钴膜(含有LiCoO2、Al等)的一种工艺如下:下列有关说法不正确的是()A.碱浸的目的是溶解铝B.酸溶时H2O2被还原C.H2SO4/H2O2可改用浓盐酸D.铝、钴产物可再利用答案 B3、(2019·佛山市南海区七校联合体模拟)以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下,下列叙述不正确的是()A.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4B.向滤液中通入过量CO2、过滤、洗涤、灼烧沉淀可制得Al2O3C.隔绝空气焙烧时理论上反应消耗的n(FeS2)∶n(Fe2O3)=1∶5D.烧渣分离可以选择用磁铁将烧渣中的Fe3O4分离出来答案 C4、磷酸亚铁锂(LiFePO4)电池是新能源汽车的动力电池之一。
采用湿法冶金工艺回收废旧磷酸亚铁锂电池正极片中的金属,其流程如下:下列叙述错误的是()A.合理处理废旧电池有利于保护环境和资源再利用B.从“正极片”中可回收的金属元素有Al、Fe、LiC.“沉淀”反应的金属离子为Fe3+D.上述流程中可用硫酸钠代替碳酸钠答案 D5、碱式氯化铜[Cu a Cl b(OH)c·x H2O]是一种重要的无机杀虫剂,它可以通过以下步骤制备。
工业流程试题分析与解答讲解34页PPT

15、机会是不守纪律的。——雨果
16、业余生活要有意义,不要越轨。——华盛顿 17、一个人即使已登上顶峰,也仍要自强不息。——罗素·贝克 18、最大的挑战和突破在于用人,而用人最大的锋 20、要掌握书,莫被书掌握;要为生而读,莫为读而生。——布尔沃
END
工业流程试题分析与解答讲解
11、战争满足了,或曾经满足过人的 好斗的 本能, 但它同 时还满 足了人 对掠夺 ,破坏 以及残 酷的纪 律和专 制力的 欲望。 ——查·埃利奥 特 12、不应把纪律仅仅看成教育的手段 。纪律 是教育 过程的 结果, 首先是 学生集 体表现 在一切 生活领 域—— 生产、 日常生 活、学 校、文 化等领 域中努 力的结 果。— —马卡 连柯(名 言网)
高三寒假作业:第十一章 工业流程(含答案解析)

有机化合物1、利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。
某工厂对制革工业污泥中Cr(Ⅲ)的处理工艺流程如下:水含铬污泥预处理后--------滤液I ---------→Cr(OH)(H 2O)5SO 42mol/L H 2SO 4 H 2O 2 NaOH SO 2 已知:①硫酸浸取液中的金属离子主要是Cr 3+,其次是Fe 3+、Al 3+、Ca 2+和Mg 2+。
②常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH 如下:(1)实验室用18.4 mol·L -1的浓硫酸配制480 mL 2 mol·L -1的硫酸,需量取浓硫酸___________________________mL ;配制时所用玻璃仪器除量筒、烧杯和玻璃棒外,还需__________________________________________。
(2)H 2O 2的作用是____________________________________________(用离子方程式表示)。
(3)加入NaOH 溶液使溶液呈碱性,既可以除去某些杂质离子,同时又可以将Cr 2O 72-转化为___________________(填微粒的化学式)(4)钠离子交换树脂的反应原理为:M n+ + nNaR = MR n + nNa +,则利用钠离子交换树脂可除去滤液Ⅱ中的金属阳离子有__________________。
(5)写出上述流程中用SO 2进行还原时发生反应的离子方程式:______________________________________________________________________。
【答案】(1)54.3mL;胶头滴管、500mL容量瓶(2)2Cr3++H2O+3H2O2=Cr2O72-+8H+(3)CrO42-(4)Ca2+和Mg2+(5)2CrO42-+H2O+3SO2=2Cr(OH)(H2O)5 SO4+SO42-+2OH-【详解】(1)根据“大而近”的原则,配制480mL溶液应选用500mL容量瓶。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2020-02-21工业流程题删减版答案解析1.高铁酸钾(K2FeO4)为暗紫色固体,可溶于水,是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染。
工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
结合所学知识回答相关问题:(1)K2FeO4中铁元素的化合价是+6价。
(2)制备高铁酸钠的主要反应为:2FeSO4+6 Na2O2═2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是FeSO4、Na2O2(填化学式),若有1molO2生成,转移电子的物质的量为10 mol。
(3)某反应体系中有六种数粒:Fe(OH)3、ClO—、OH—、FeO42—,Cl—、H2O,写出在碱性条件下,制高铁酸钾的离子反应方程式2Fe(OH)3+3ClO—+4OH—=2FeO42—+3Cl—+5H2O。
(4)在水处理过程中,K2FeO4中的铁元素转化为Fe(OH)3胶体,使水中悬浮物聚沉。
胶体区别于其他分散系的本质特征是分散质粒子直径介于1~100nm。
【解答】解:(1)K2FeO4中铁元素的化合价是0﹣(﹣2)×4﹣(+1)×2=+6 。
(2)Fe元素的化合价由+2价升高为+6价,过氧化钠中O元素的化合价既升高也降低,则还原剂为FeSO4、Na2O2,若有1molO2生成,5molNa2O2作氧化剂,转移电子的物质的量为5mol×2×1=10mol,(3)在碱性条件下,制高铁酸钾的离子反应方程式为2Fe(OH)3+3ClO—+4OH—=2FeO42—+3Cl—+5H2O,(4)胶体区别于其他分散系的本质特征是分散质粒子直径介于1~100nm,2.以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下:(1)焙烧过程均会产生SO2,用NaOH溶液吸收过量SO2的离子方程式为SO2+OH—==HSO3—。
(2)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如题图所示。
已知:多数金属硫酸盐的分解温度都高于600℃硫去除率=(1﹣)×100%①不添加CaO的矿粉在低于500℃焙烧时,去除的硫元素主要来源于FeS2。
②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是硫元素转化为CaSO4而留在矿粉中。
(3)向“过滤”得到的滤液中通入过量CO2,铝元素存在的形式由NaAlO2(填化学式)转化为Al(OH)3(填化学式)。
(4)“过滤”得到的滤渣中含大量的Fe2O3.Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,理论上完全反应消耗的n(FeS2):n(Fe2O3)=1:16。
【解答】解:(1)用NaOH溶液吸收过量SO2生成HSO3—,则发生反应的离子方程式为:SO2+OH—═HSO3—,故答案为:SO2+OH—═HSO3—;(2)①不添加CaO的矿粉中S元素来源是FeS2和金属硫酸盐,金属硫酸盐的分解温度较高,所以可判断焙烧过程中S元素主要来源是FeS2,②700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,考虑加入CaO可能使S转化为CaSO4,形成的硫酸盐分解温度较高,所以会导致S的脱除率降低,故答案为:硫元素转化为CaSO4而留在矿粉中;(3)过滤前使用NaOH溶液进行碱浸,Al2O3转化为NaAlO2,“过滤”得到的滤液中主要含有AlO2—,向“过滤”得到的滤液中通入过量CO2,可以将AlO2—转化为Al(OH)3,故答案为:NaAlO2;Al(OH)3;(4)过滤”得到的滤渣中含大量的Fe2O3,Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,设有x mol Fe2O3和y mol FeS2完全参加反应,根据电子得失守恒:2x×(3﹣)=2y×5+y×﹣2),解得,所以理论上完全反应消耗的n(FeS2):n(Fe2O3)=1:16,故答案为:1:16。
3.铝是应用广泛的金属。
以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时生成偏铝酸钠的离子方程式为Al2O3+2OH—═2AlO2—+H2O。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH减小(填“增大”、“不变”或“减小”)。
(5)铝粉在1000℃时可与N2反应制备AlN.在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN的制备,其主要原因NH4Cl分解产生的HCl能够破坏Al表面的Al2O3薄膜。
【解答】解:(1)“碱溶”时生成偏铝酸钠的离子方程式为Al2O3+2OH—═2AlO2—+H2O;(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,与NaAlO2反应生成氢氧化铝沉淀和碳酸钠,碱性为OH—>AlO2—>CO32—,可知溶液的pH减小,故答案为:减小;(5)铝粉在1000℃时可与N2反应制备AlN.在铝粉中添加少量NH4Cl固体并充分混合,有利于AlN 的制备,其主要原因是NH4Cl分解产生的HCl能够破坏Al表面的Al2O3薄膜,故答案为:NH4Cl分解产生的HCl能够破坏Al表面的Al2O3薄膜。
4.七铝十二钙(12CaO•7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:(1)锻粉主要含MgO和CaO,用适量NH4NO3溶液浸取煅粉后,镁化合物几乎不溶,若滤液Ⅰ中c(Mg2+)小于5×10—6mol•L—1,则溶液pH大于11(Mg(OH)2的K sp=5×10—12);该工艺中不能用(NH4)2SO4代替NH4NO3,原因是CaSO4微溶于水,用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀引起Ca2+的损失。
(2)滤液Ⅰ中阴离子有NO3—,OH—(忽略杂质成分的影响);若滤液Ⅰ中仅通入CO2,会生成Ca(HCO3)2,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为Al2O3+2OH—═2AlO2—+H2O。
【解答】解:(1)锻粉是由白云石高温煅烧而来,在煅烧白云石时,发生反应:CaCO3CaO+CO2↑,MgCO3MgO+CO2↑,故所得锻粉主要含MgO和CaO;用适量NH4NO3溶液浸取煅粉后,镁化合物几乎不溶,即得Mg(OH)2的饱和溶液,根据Mg(OH)2的K sp可知:K sp=c(Mg2+)•c2(OH—)=5×10—12,而c(Mg2+)小于5×10—6mol•L﹣1,故c(OH—)大于10—3mol/L,则溶液中的c(H+)小于10—11mol/L,溶液的pH大于11;CaSO4微溶于水,如果用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀引起Ca2+的损失,故答案为:CaO;11;CaSO4微溶于水,用(NH4)2SO4代替NH4NO3,会生成CaSO4沉淀引起Ca2+的损失;(2)在锻粉中加入适量的NH4NO3溶液后,镁化合物几乎不溶,由于NH4NO3溶液水解显酸性,与CaO反应生成Ca(NO3)2和NH3•H2O,故过滤后溶液中含Ca(NO3)2和NH3•H2O,将CO2和NH3通入滤液I中后发生反应:Ca(NO3)2+2NH3+CO2+H2O=CaCO3↓+2NH4NO3,故滤液中的阴离子主要为NO3—,还含有OH—;若滤液Ⅰ中仅通入CO2,会造成CO2过量,则会生成Ca(HCO3)2,从而导致CaCO3产率降低,故答案为:NO3—,OH—;Ca(HCO3)2;(3)氧化铝和氢氧化钠反应生成偏铝酸钠和水,离子反应为Al2O3+2OH—═2AlO2—+H2O;5.废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍,湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜产品。
某化学小组模拟该方法回收铜和制取胆矾,流程简图如图1:回答下列问题:(1)反应Ⅰ是将Cu转化为Cu(NH3)42+,反应中H2O2的作用是氧化剂,写出操作①的名称:过滤;(2)反应Ⅱ是铜氨溶液中的Cu(NH3)42+与有机物RH反应,写出该反应的离子方程式:Cu(NH3)42++2RH=CuR2+2NH4++2NH3↑,操作②用到的主要仪器名称为分液漏斗,其目的是(填序号)ab。
a.富集铜元素b.使铜元素与水溶液中的物质分离c.增加Cu2+在水中的溶解度(3)反应Ⅲ是有机溶液中的CuR2与稀硫酸反应生成CuSO4和RH,若操作③使用如图2装置,图中存在的错误是分液漏斗尖端未紧靠烧杯内壁;液体过多;【解答】解:废电路板中加入双氧水、氨气、氯化铵溶液,得到铜氨溶液和残渣,分离难溶性固体和溶液采用过滤方法,所以操作①是过滤,反应Ⅰ是将Cu转化为Cu(NH3)42+,Cu元素化合价由0价变为+2价,所以Cu是还原剂,则双氧水是氧化剂,将Cu氧化;反应Ⅱ是铜氨溶液中的Cu(NH3)42+与有机物RH反应,生成CuR2,同时生成NH4+和NH3;互不相溶的液体采用分液方法分离,所以操作②是分液;向有机层中加入稀硫酸,根据流程图知,生成CuSO4和HR,然后采用分液方法分离得到HR,以石墨为电极电解硫酸铜溶液时,阳极上氢氧根离子放电、阴极上铜离子放电;从硫酸铜溶液中获取胆矾,采用加热浓缩、冷却结晶、过滤的方法得到晶体;(1)双氧水具有氧化性,能氧化还原性物质Cu,所以双氧水作氧化剂;分离难溶性固体和溶液采用过滤方法,该混合溶液中贵重金属是难溶物、铜氨溶液是液体,所以操作①是过滤,故答案为:氧化剂;过滤;(2)反应Ⅱ是铜氨溶液中的Cu(NH3)42+与有机物RH反应生成CuR2,同时生成NH4+和NH3,根据反应物和生成物书写该反应的离子方程式Cu(NH3)42++2RH=CuR2+2NH4++2NH3↑;分离互不相溶的液体采用分液方法,分液时常用分液漏斗,分液的目的是富集铜元素、使铜元素与水溶液中的物质分离,所以ab正确,故答案为:Cu(NH3)42++2RH=CuR2+2NH4++2NH3↑;分液漏斗;ab;(3)反应Ⅲ是有机溶液中的CuR2与稀硫酸反应相当于复分解反应,所以生成CuSO4和RH,分液时分液漏斗下端要紧靠烧杯内壁,且分液漏斗内不能盛放太多溶液,故答案为:RH;分液漏斗尖端未紧靠烧杯内壁;液体过多;6.锂离子电池的应用很广,其正极材料可再生利用。
