血管加压素受体拮抗剂(VRAs)
血管紧张素受体拮抗剂的临床应用

血管紧张素受体拮抗剂的临床应用
薛桥
【期刊名称】《临床荟萃》
【年(卷),期】1998(013)015
【摘要】肾素-血管紧张素-醛固酮系统(Renin-Angiotensh,RAAS)在维持正常人体内环境的平衡和在高血压、充血性心衰的病理生理过程中所起的作用早已为人们认识.多年来,人们以药物干预该系统达到某种治疗目的的尝试始终未曾停过.RAAS 的限速酶为肾素,效应分子为血管紧张素Ⅱ(Angiotensin Ⅱ,AT Ⅱ),因此药物研究的重点放在对这两种物质的干预上.针对肾素的非肽类口服制剂已用于临床,因其生物利用度低和作用时间短,限制了它的发展.由于肾素作用底物的专一性,
【总页数】3页(P697-699)
【作者】薛桥
【作者单位】解放军第四六四医院
【正文语种】中文
【中图分类】R972
【相关文献】
1.血管紧张素Ⅱ受体拮抗剂在冠心病患者中的临床应用建议(2018) [J], 李建平;魏盟;严晓伟;霍勇;陈韵岱;高传玉;李勇;苏国海;孙宁玲;唐熠达;王继光
2.血管紧张素转换酶抑制剂与血管紧张素Ⅱ受体拮抗剂在原发性高血压治疗中的临床应用 [J], 赵秀丽
3.血管紧张素Ⅱ受体拮抗剂的药理作用和临床应用 [J], 姚丽艳
4.血管紧张素转换酶抑制剂及血管紧张素Ⅱ受体拮抗剂的临床应用 [J], 吴可光;刘鸿琴
5.血管紧张素Ⅱ受体拮抗剂的临床应用及进展 [J], 罗正良
因版权原因,仅展示原文概要,查看原文内容请购买。
血管紧张素Ⅱ受体拮抗剂在心脑血管病的临床应用

血管紧张素Ⅱ受体拮抗剂在心脑血管病的临床应用
丁小蓉;常晓琪
【期刊名称】《中国医药导刊》
【年(卷),期】2012(14)10
【摘要】目的:探讨血管紧张素Ⅱ受体拮抗剂在心脑血管病的应用效果.方法:选择我院2006年1~12月心脑血管科就诊的患者100例,随机分为实验组与对照组,对实验组病例全部运用氯沙坦钾片治疗,而且对照组患者则运用其它非血管紧张素Ⅱ受体拮抗剂治疗.结果:实验组患者的治疗效果明显高于对照组,P<0.05.结论:血管紧张素Ⅱ受体拮抗剂具有缓解血管平滑肌收缩、降低血管升压素分泌、抑制心肌细胞的生长,减轻心肌负荷、降低周围血管阻力、增加肾脏血流量的作用.
【总页数】2页(P1764-1764,1766)
【作者】丁小蓉;常晓琪
【作者单位】第四军医大学第三附属医院老年病科,西安710032;第四军医大学第三附属医院老年病科,西安710032
【正文语种】中文
【中图分类】R540.5
【相关文献】
1.血管紧张素转换酶及血管紧张素Ⅱ受体拮抗剂在心力衰竭治疗中的地位 [J], 周颖玲
2.心力衰竭的进展(8)血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体拮抗剂在心力
衰竭治疗中的作用 [J], 马虹
3.血管紧张素转换酶抑制剂和血管紧张素受体拮抗剂在心房颤动一级预防中的可能作用 [J], 周力;王翠英;陈晖;李敏
4.血管紧张素Ⅱ受体拮抗剂在心血管疾病的临床应用 [J], 王静;郑刚;刘兆昶
5.血管紧张素Ⅱ受体拮抗剂在心血管疾病中的临床应用 [J], 于力;裴兆辉
因版权原因,仅展示原文概要,查看原文内容请购买。
血管紧张素受体拮抗剂临床应用
血管紧张素II受体拮抗剂的临床应用青岛大学医学院附属心血管病医院(青岛266071)吕晓冰,,曹广智血管紧张素II受体拮抗剂(ARB ),是继血管紧张素转换酶抑制剂(ACEI )之后的对高血压、动脉硬化、心肌肥厚、心力衰竭、糖尿病肾病等具有良好作用的新一类作用于肾素-血管紧张素系统(RAS)的重要药物。
与ACEI比较,它作用于RAS的末端受体水平,更充分、更直接、更具选择性地阻断ARS,且不具有干咳、血管神经性水肿等副作用。
随着循证医学证据的不断更新,ARB的临床应用日趋广泛。
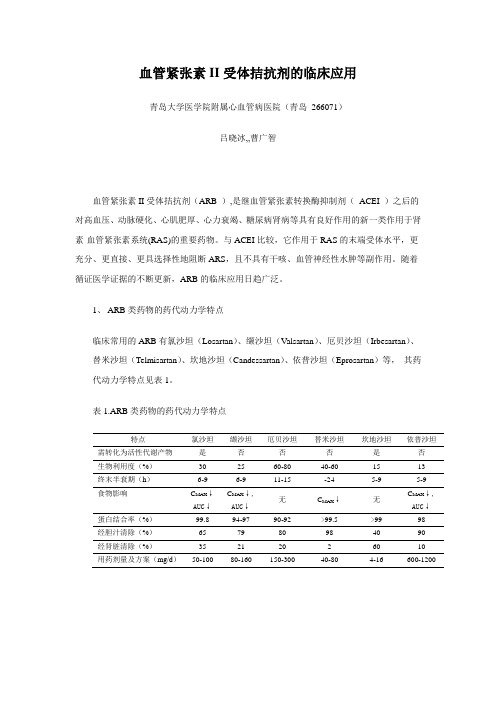
1、ARB类药物的药代动力学特点临床常用的ARB有氯沙坦(Losartan)、缬沙坦(Valsartan)、厄贝沙坦(Irbesartan)、替米沙坦(Telmisartan)、坎地沙坦(Candessartan)、依普沙坦(Eprosartan)等,其药代动力学特点见表1。
表1.ARB类药物的药代动力学特点特点氯沙坦缬沙坦厄贝沙坦替米沙坦坎地沙坦依普沙坦需转化为活性代谢产物是否否否是否生物利用度(%)30 25 60-80 40-60 15 13 终末半衰期(h)6-9 6-9 11-15 -24 5-9 5-9食物影响C MAX↓AUC↓C MAX↓,AUC↓无C MAX↓无C MAX↓,AUC↓蛋白结合率(%)99.8 94-97 90-92 >99.5 >99 98经胆汁清除(%)65 79 80 98 40 90经肾脏清除(%)35 21 20 2 60 10用药剂量及方案(mg/d)50-100 80-160 150-300 40-80 4-16 600-12001 ARB的基础特征几乎所有AngII 的生理作用均是通过细胞表面膜受体介导完成的。
目前已知的AngII 受体亚型有AT1 、AT2、AT3、AT4 4 种,后两种的研究较少。
AT1受体主要分布在人体血管、心脏、肾脏、脑、肺及肾上腺皮质,其主要生理效应是介导血管和心肌收缩、垂体激素和醛固酮分泌、水钠重吸收及细胞增殖肥大等。
血管紧张素受体拮抗剂在高血压治疗中的作用及地位

知识篇19 继续医学教育 第21卷第1期过去的5~10年中,血管紧张素受体拮抗剂(ARB)已经确立了其作为有效抗高血压药物的地位。
ARB具有较好的降压疗效,耐受性与安慰剂相同。
在降压的同时对2型糖尿病患者及糖尿病肾病患者有较好的器官保护作用,对于有心力衰竭的高血压患者及血压正常的患者长期治疗也可获益,因此,这类药物在国际上得到认可,并广泛应用于临床的高血压治疗及糖尿病肾病的治疗。
但由于ARB还是一类新的降压药物,我国的临床使用经验还不足,特别是近期公布的Value研究[1]的结果,使临床医生对ARB在高血压患者的治疗产生了一些疑虑,到底ARB在临床高血压治疗中的地位如何?1 ARB是否为血管紧张素转换酶抑制剂(ACEI)的替代物在高血压的治疗中,ARB用于不能耐受ACEI的高血压患者。
回答应当是否定的。
目前ARB完全可以作为一线或初始的降压药物。
在ARB上市后国际上做过一项大型的ARB与其他降压药物降压疗效及耐受性的临床试验,这项被称为ICE的研究[2],比较ARB、ACEI、钙离子拮抗剂、β-受体阻滞剂、利尿剂之间的降压疗效及耐受性和安全性。
研究结果发现,在1年的治疗中ARB降压幅度与其他药物相比进一步使收缩压下降4.8 mm Hg,舒张压降3.2 mmHg,1年中需要换药的ARB组为8.5%、其他降压药为13.6%,需要联合用药的在1年的治疗中ARB(厄贝沙坦)组中的为16.1%,而其他降压药为25.3%。
研究证实ARB降压疗效肯定,副作用少,安全耐受性高,用于高血压治疗有其作用及地位。
ACEI与ARB在降压机制和器官保护上有许多相似的地方,虽然有不同的抑制肾素-血管紧张素系统(RAS)激活的途径但确有共同的抑制RAS激活的作用,同时ACEI又有许多循血管紧张素受体拮抗剂在高血压治疗中的作用及地位孙宁玲(北京大学人民医院心内科 100044)证医学的证据,加上医生们有长期临床应用的经验,所以许多人将ARB作为ACEI的替代药物,而没有作为主动应用的初始药物。
血管加压素受体拮抗剂(VRAs)

血管加压素受体拮抗剂(VRAs)传统治疗等容性或高容量性低钠血症的方法包括限水、应用高渗盐水及去甲金霉素等,但均有明显的副作用,导致其临床应用受限。
血管加压素受体拮抗剂(VRAs)主要通过阻断过度产生的(精氨酸加压素)AVP,使净水(非溶质水)排出增加,达到升高血浆渗透压的作用已被美国食品药品管理局(FDA)批准用于治疗等容性低钠血症。
对此类药物的进一步研究发现VRAs还可用于治疗由于AVP受体变异导致的肾源性糖尿病(NDI),甚至可能延缓多囊肾的进展。
本文对于目前国内外非肽类VRAs药物的研究情况进行综述,并进一步探讨其潜在的临床使用价值。
1 AVP及其受体AVP又被称为抗利尿激素(ADH),是下丘脑垂体分泌的一种肽类激素,还有文献报道外周组织如心脏也可分泌AVP〔1〕。
AVP在体内主要负责调节水的重吸收,维持体液渗透压、血容量、血压等,还在细胞收缩、增殖和肾上腺皮质激素的分泌等方面扮演重要角色,这些生理作用都是通过与其受体结合而产生的〔1〕。
AVP受体属于G蛋白耦联受体,有3种亚型:V1a受体(V1aR)、V1b受体(V1bR)和V2受体(V2R),它们在体内的分布和信号传导的机制均不同。
V1aR位于血管平滑肌、血小板、肝细胞和子宫肌层,通过激活磷脂酶C 增加细胞内钙离子浓度,分别介导血管收缩、血小板聚集、肝糖原分解及子宫收缩;V1bR 位于垂体前叶,介导促肾上腺皮质激素(ACTH)释放;V2受体(V2R)位于肾脏集合管细胞的基底侧膜,通过激活蛋白激酶A使位于细胞内囊泡中已形成的水孔蛋白2(AQP2)磷酸化并使其插入集合管细胞顶膜,从而调节集合管对水的通透性。
V2R还在血管内皮及血管平滑肌细胞表达,可诱导血管性血友病因子第8因子(vWF)及Ⅷ因子释放及介导血管扩张效应。
正常情况下,当体液渗透压降低至一定水平,血浆AVP水平也相应下调,同时产生利尿效应。
在抗利尿激素分泌异常综合征(SIADH)患者,虽然存在低渗,但AVP释放却不完全受抑制。
首个血管加压素受体拮抗剂

首个血管加压素受体拮抗剂获SFDA批准国家食品药品监督管理局(SFDA)近日正式批准选择性血管加压素(AVP)Ⅱ型受体(简称V2受体)拮抗剂托伐普坦(商品名为苏麦卡)在中国生产并销售。
托伐普坦是世界上首个口服普坦类药物,也将是中国市场第一个V2受体拮抗剂,可用于治疗因肝硬化、心衰、抗利尿激素分泌异常综合征(SIADH)所导致的高容量性和等容量性低钠血症。
AVP又称抗利尿激素,在下丘脑合成,储存在垂体后叶,是调节人体水平衡最主要的激素。
当人体血容量降低或血浆渗透压增高时,AVP从垂体后叶中释放进入血循环。
AVP受体有V1A、V1B和V2,其中V2受体主要分布于肾脏集合管,负责调节水在原尿和血液间的转运,以维持人体体液平衡。
正常人血中几乎测不出AVP的存在。
没有AVP时,肾脏集合管内膜是不透水的,多余水份从尿液中排出。
心衰、肝硬化、SIADH等疾病可导致体内AVP水平增高,增高的AVP 与V2受体结合并激活V2受体,刺激水通道蛋白2合成,在内膜上形成孔道,使自由水经由集合管内腔进入细胞,继之入血,从而增加水的重吸收,导致血容量不成比例增加及稀释性低钠血症。
患者可表现出恶心、意识障碍、昏睡、注意力缺失、步态不稳和意外摔倒等症状,低钠严重时可出现惊厥、昏迷,甚至死亡。
目前对高容量性和等容量性低钠血症尚无有效的治疗方法。
在临床上,限制液体摄入常被作为首选方法,但患者很难做到,即便患者严格遵守了限液医嘱,其提高血钠的幅度也不超过3~4 mEq/L。
对肝腹水和心衰患者,因可能加重高容量状况从而使病情进展,故不建议采用滴注高渗盐水来纠正低钠血症。
而现有利尿剂均通过抑制钠的重吸收来增加尿量,故在低钠血症时不推荐使用。
托伐普坦的诞生给这些患者带来了新希望。
其与V2受体的亲和力是天然AVP的1.8倍,可拮抗AVP的作用,抑制水的重吸收,增加不含电解质的自由水排出,有效纠正高容量性和等容量性低钠血症,并可纠正高容量患者的水肿症状。
血管紧张素_受体拮抗剂的作用和用途_林新中

血管紧张素Ⅱ受体拮抗剂的作用和用途林新中(福建省妇幼保健院福州350001)摘要:血管紧张素Ⅱ是肾素-血管紧张素-醛固酮系统的活性激素,对血压和肾功能等都有作用。
其通过与各种组织细胞膜上的特异性受体(AT 1受体)结合而发挥作用。
血管紧张素Ⅱ受体拮抗剂,现在已有6种沙坦类药物上市。
本文综述它们的药动学、药理作用、临床应用以及安全性与耐受性。
总之,它们作用确切,副作用少,是一类很有发展前途的抗高血压药物,还可治疗心力衰竭等疾病。
关键词:血管紧张素Ⅱ受体拮抗剂;沙坦类;抗高血压中图分类号:R 972 文献标识码:A 文章编号:1006-3765-(2001)03-0006-04 心血管疾病的发病机制与机体内许多系统有密切关系,其中肾素-血管紧张素-醛同酮系统(R A AS)参与调控。
血管紧张素Ⅱ(Ang Ⅱ)是RA AS 的活性激素,它可在血管紧张素转换酶(A CE)的作用下由Ang Ⅰ转化生成。
Ang Ⅱ对周身每个系统及每个器官均有作用,但主要作用是对血压和肾功能,它可使血管收缩(是去甲肾上腺素的40倍)、醛固酮分泌、缓激肽分解加快、血压升高等。
1 血管紧张素Ⅱ受体Ang Ⅱ通过与各种组织细胞膜上的特异性受体结合发挥其作用。
Ang Ⅱ受体有A T 1和A T 2等亚型。
A T 1受体集中在肾脏、心脏、血管、平滑肌细胞、脑、肾上腺、血小板、脂肪细胞和胎盘。
A T 2受体在胎儿形成期是重要的,但产后期数量减少。
在成人组织中,仅以低水平存在。
Ang Ⅱ的临床作用是由A T 1受体介导。
A T 1受体兴奋时表现:①血管收缩(优先冠状的、肾的、大脑的血管);②尿潴留(血管紧张素、醛固酮产生);③水潴留(血管加压素释放);④肾素抑制(负性反馈);⑤肌细胞和平滑肌细胞肥大;⑥刺激血管和心肌纤维化;⑦变力的/收缩的(心肌细胞);⑧变时的/致心律不齐的(心肌细胞);⑨刺激纤维蛋白溶酶原活化剂抑制剂-1;10刺激高度缺氧化物形成;1活化交感神经系统;12增加内皮素分泌[1]。
血管紧张素受体拮抗剂治疗高血压

血管紧张素受体拮抗剂治疗高血压马骏;王延玲;王荣;贾正平【期刊名称】《中华老年多器官疾病杂志》【年(卷),期】2014(000)004【摘要】肾素-血管紧张素-醛固酮系统(RAAS)是调节血压的主要机制,也是治疗高血压病的重要靶点。
血管紧张素受体拮抗剂(ARBs),通过阻滞特异性血管紧张素受体,干扰RAAS的活性,成为治疗高血压的一线药物。
临床结果显示ARBs作为单用药或联合其他降压药物治疗高血压有其特殊的优势。
在降压方面,与血管紧张素转换酶抑制剂和其他类型的降压药物相比,ARBs具有良好的耐受性而适合用于治疗更广泛的患者。
最近研究结果显示在12个月期间使用ARBs治疗高血压依从性明显高于其他降压药物,而且副作用少。
具备临床有效性和良好耐受性的ARBs药物,可以作为治疗高血压的主要药物。
%The renin-angiotensin-aldosterone system (RAAS) plays a major role in blood pressure regulation, and is thus an important therapeutic target in the management of hypertension. Angiotensin receptor blockers (ARBs), which interrupt RAAS overactivity by blocking a specific receptor of angiotensin Ⅱ, act for the management of hypertension. Clinical evidence demonstrates that ARBs are effective in the management of hypertension as monotherapy or in combination with other agents. Although comparable to angiotensin-converting enzyme inhibitors and other major classes of antihypertensive agents in the treatment of hypertension, ARBs are attractive alternatives for many patients due to its favorable tolerability profile. Recent evidencesuggests that treatment persistence with ARBs therapy during a 12-month period be typically higher than that with other antihypertensive classes, and fewer side effects are observed. The advantages of clinical efficacy and tolerability qualify the ARBs as major treatment alternatives for hypertension.【总页数】5页(P313-317)【作者】马骏;王延玲;王荣;贾正平【作者单位】兰州军区兰州总医院药剂科,兰州 730050;兰州军区兰州总医院药剂科,兰州 730050;兰州军区兰州总医院药剂科,兰州 730050;兰州军区兰州总医院药剂科,兰州 730050【正文语种】中文【中图分类】R544.1【相关文献】1.血管紧张素转换酶抑制剂与血管紧张素Ⅱ受体拮抗剂在原发性高血压治疗中的临床应用 [J], 赵秀丽2.血管紧张素转换酶抑制剂和血管紧张素Ⅱ受体拮抗剂联合治疗肾性高血压的疗效观察 [J], 祁昊3.血管紧张素转化酶抑制剂和血管紧张素Ⅱ受体拮抗剂联合应用治疗高血压病的研究进展 [J], 赵德生;佘强4.血管紧张素转换酶抑制剂与血管紧张素Ⅱ受体拮抗剂治疗高血压疗效比较 [J],5.短期血管紧张素Ⅱ受体拮抗剂治疗不能延缓有高血压危险病人的高血压发展 [J],因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
血管加压素受体拮抗剂(VRAs)传统治疗等容性或高容量性低钠血症的方法包括限水、应用高渗盐水及去甲金霉素等,但均有明显的副作用,导致其临床应用受限。
血管加压素受体拮抗剂(VRAs )主要通过阻断过度产生的(精氨酸加压素)AVP,使净水(非溶质水)排出增加,达到升高血浆渗透压的作用已被美国食品药品管理局(FDA )批准用于治疗等容性低钠血症。
对此类药物的进一步研究发现VRAs还可用于治疗由于AVP受体变异导致的肾源性糖尿病(NDI ),甚至可能延缓多囊肾的进展。
本文对于目前国内外非肽类VRAs药物的研究情况进行综述,并进一步探讨其潜在的临床使用价值。
1 AVP及其受体AVP又被称为抗利尿激素(ADH),是下丘脑垂体分泌的一种肽类激素,还有文献报道外周组织如心脏也可分泌AVP〔1〕。
AVP在体内主要负责调节水的重吸收,维持体液渗透压、血容量、血压等,还在细胞收缩、增殖和肾上腺皮质激素的分泌等方面扮演重要角色,这些生理作用都是通过与其受体结合而产生的〔1〕。
AVP受体属于G蛋白耦联受体,有3种亚型:V1a受体(V1aR )、V1b受体(V1bR )和V2受体(V2R),它们在体内的分布和信号传导的机制均不同。
V1aR位于血管平滑肌、血小板、肝细胞和子宫肌层,通过激活磷脂酶C增加细胞内钙离子浓度,分别介导血管收缩、血小板聚集、肝糖原分解及子宫收缩;V1bR位于垂体前叶,介导促肾上腺皮质激素(ACTH )释放;V2受体(V2R )位于肾脏集合管细胞的基底侧膜,通过激活蛋白激酶A使位于细胞内囊泡中已形成的水孔蛋白LJ2_(AQP2 )磷酸化并使其插入集合管细胞顶膜,从而调节集合管对水的通透性。
V2R还在血管内皮及血管平滑肌细胞表达,可诱导血管性血友病因子第8因子(vWF)及忸因子释放及介导血管扩张效应。
正常情况下,当体液渗透压降低至一定水平,血浆AVP水平也相应下调,同时产生利尿效应。
在抗利尿激素分泌异常综合征(SIADH)患者,虽然存在低渗,但AVP释放却不完全受抑制。
而在肝硬化及慢性充血性心力衰竭(CHF)患者,由于肾小球滤过率降低导致水排泄受限,同时非渗透压刺激下的AVP释放或与受体结合也可能参与了体液潴留的发生机制。
正常生理环境下,心室、颈动脉窦和主动脉弓的压力感受器通过输出的迷走神经张力抑制AVP、肾素、儿茶酚胺释放。
CHF时动脉扩张异常和压力感受器受抑制导致迷走神经张力下降,上述激素分泌增加〔2, 3〕。
而在肝硬化时,脾血管的持续扩张导致了动脉充盈不足,AVP释放增加。
肝硬化伴有腹水及浮肿的患者,其AVP、肾素及醛固酮水平较水排泄正常的肝硬化患者明显升高。
给予肝硬化动物模型行垂体切除或应用去甲金霉素发现体液潴留减轻,提示SIADH、CHF及肝硬化导致的低钠血症均是由AVP介导的。
2非肽类VRAs20世纪70年代,第一个肽类V2R拮抗剂在动物实验中被证实有效,而在人体却产生弱的V2R激动作用〔4〕,且口服生物利用度差,限制了其应用。
1993年,Ohnishi等〔5〕首先报道了口服非肽类选择性V2R拮抗剂,并在健康人体内产生了水排泄作用。
目前的研究集中于 4种非肽类药物,它们均是 benzazepine 或2_羟基吲哚(oxindole )的衍生物,其中考尼伐坦(conivaptan ) (丫皿087)是联合的V1aR/V2R 拮抗剂,利希普 坦(lixivaptan)(许闵9壮)、托伐普坦(tolvaptan)及SRF121463是选择性V2R 拮抗剂。
这些药物均是细胞色素 P450 3A4 (CYP3A4 )系统的抑制剂,其中 conivaptan 作用最强。
2005年12月,conivaptan 被FDA 批准用于治疗等容性低钠血症,虽然它口服有效,但为 了避免产生严重的药物相互作用, FDA 规定将其制成注射剂型,并仅限于院内短期使用。
其他三种VRAs 对CYP3A4活性抑制有限,目前正在研究将其作为长期口服用药。
而有关5R~121463的报道极少,而国内尚无此类药物相关的应用经验,故本文未对其进行相关阐 述。
目前Lixivaptan 的研究报道较多,n 期临床实验发现在 SIADH 患者,用药48 h 后血清 钠浓度和尿流率明显增加,伴有体重、尿渗透压、尿钠下降,而血浆肾素、醛固酮、 和肌酐清除率无变化。
而在肝硬化的患者,用药 72 h 后血清钠明显上升,但尿钠、尿钾及血浆AVP 均升高,同时肾素和血管紧张素水平无变化〔 6〕。
提示SIADH 患者纠正容量负荷过度时伴随有体内钠潴留,而治疗肝硬化时则是作用于远端肾小管使钠转运增加。
在大规 模、长时间的临床研究中发现, Lixivaptan 升高血钠有剂量依赖效应,使用高剂量提升血钠更快。
在这些实验中,不良反应报道较少,唯一的明显副作用便是出现了烦渴的症状,且在 高剂量组中更为明显〔7〕。
2.2 Tolvaptan (托伐普坦)Tolvaptan 在正常人、肝硬化及 SIADH 患者中使用均达到了预期的尿钠增加和水排泄 效应〔8,9〕。
该药物还在CHF 患者中进行了一些研究,一项在纽约心脏病协会( NYHA ) 分级为心功能n 〜川级的患者中进行的研究证实治疗组患者产生了明显的体重下降、尿渗透 压下降及血钠上升的效应,且不会轻易发生明显的高钠血症〔10〕。
而在另一项以射血分 数<40%的CHF 患者为对象进行的研究发现使用Tolvaptan 可降低患者死亡率,而在合并有 肾功能异常或严重循环充血的患者更为明显〔11〕。
关于Tolvaptan 是否可降低心血管疾病 死亡率还需要更多的临床研究进一步证实。
最近的一项临床实验发现 Tolvaptan 可产生明显 的血钠增加效应,但该实验中有 37%的肝硬化患者、17%的CHF 患者和11%的SIADH 患者出现药物抵抗(定义为用药后血钠水平升高不超过2.3 Conivaptan (考尼伐坦)Conivaptan 是联合的V1aR/V2R 拮抗剂,理论上可减轻单独使用选择性 V2R 拮抗剂产 生的V1aR 激动效应,尤其是在 CHF 患者中。
在NYHA 分级川〜W 级的患者中,治疗组肺 毛细血管锲压及右心房压均明显降低,同时尿渗透压下降,尿量增加, 但心脏指数,平均动脉压,系统血管阻力,肺血管阻力及心率没有显著变化。
同时发现血钠升高,伴有AVP 水 平轻微上升〔13〕。
但肺毛细血管锲压的下降是由于V2R 介导的水排泄效应还是部分由于 V1aR 拮抗剂的作用目前尚不明确。
在 SIADH 、CHF 及低钠血症患者中的研究证实静脉应2.1 Lixiva ptan (利昔伐坦)AVP 5 mmol/L )〔 12〕。
用Conivaptan 可使血钠明显升高,这一效应有剂量依赖性,且高剂量组发生作用更快,唯 一副作用是注射部位局部的刺激症状〔 14〕。
Conivaptan 口服也同样有效,20 mg 2次/d , 同时限水1.5 L/d ,已在2例SIADH 导致的慢性低钠血症患者中成功地维持血钠水平正常〔15〕。
但由于其可能与其他通过 CYP3A4通路代谢的药物产生相互作用,因此口服给药并不推荐作为长期临床使用方案。
2.4安全性评估虽然如此,血钠水平上升速 度大于8〜12 mmol/24 h 应慎用此类药物〔16〕。
由于它们的半衰期小于12 h ,可通过停 止给药或降低剂量限制血钠水平的进一步升高, 还可以使用低渗性液体来纠正过快的血钠升 高。
临床医生还应该仔细辨别导致低钠血症的原因,避免在低容量性低钠血症情况下使用VRAs ,因为水排泄可导致容量进一步下降, 产生低血压。
而使用选择性 V2R 拮抗剂是否会 导致出凝血功能异常、内皮功能紊乱尚不清楚,需要更多的研究进一步证实。
而在肝硬化患 者阻断了 AVP 的血管加压效应是否会导致潜在的血管扩张、脏器出血及低血压效应也无类似的研究报道。
此外在长期治疗过程中还需考虑这些药物对 其他药物产生相互作用。
3潜在的临床价值FDA 已批准将Conivaptan 用于治疗住院期间发生的等容性低钠血症,但根据 用推测此类药物还可能有以下潜在的临床治疗价值:3.1 CHFV2R 拮抗剂tolvaptan 可降低心血管疾病死亡率〔11〕。
由于V1aR 介导AVP 的加压和促有丝分裂效应,已有部分报道在 V2R 被阻 断的情况下血浆 AVP 水平可能升高〔18〕,因此,CHF 患者长期应用选择性 V2R 阻断剂 也可能导致病情的进一步恶化。
有关 CHF 患者使用V2R 的长期疗效以及使用选择性 V2R拮抗剂或联合性V1aR/V2R 的选择有待更多临床研究证实。
3.2肝硬化虽然肝硬化患者发生低钠血症的机制与CHF 在某些方面类似,但这些患者常存在体位 性低血压,因此需要考虑:阻断 V1aR 可能产生低血压,阻断脏器血管床的是否会导致脏器出血等问题。
因此,目前在这些患者中仅能使用选择性 V2R 拮抗剂。
但目前在肝硬化患者中使用 Lixivaptan 和Tolvaptan 的临床实验取得了相反的结果,因此尚不明 确在这类患者中使用该类药物是否有效。
3.3多囊肾至今尚没有使用该类药物出现高渗透性脱髓鞘改变的报道。
CYP3A4活性的抑制可能会与 AVP 的作 目前发现CHF 患者体内AVP 、肾素、血管紧张素、醛固酮及儿茶酚胺水平均升高 0」肾上腺 亚组分析提示在更高危患者如伴有 〔17〕。
多项临床实验也已证实使用血管紧张素转换酶抑制剂、血管紧张素受体阻断剂、素受体阻断剂和醛固酮拮抗剂可降低心血管疾病死亡率。
肾功能异常或严重循环充血表现人群使用选择性 步恶化。
有关AVP 加压效应环3', 5'单磷酸腺苷依赖基因促进了液体分泌形成肾囊肿,同时使细胞增生〔 囊素口E 能直接抑制腺苷环化酶,而多囊素U2可增加细胞内钙,从而抑制腺苷环化酶、增加集合管磷酸二脂酶的活性。
因此,多囊素缺失可能通过增加细胞内环 3', 5'单磷酸腺苷 而促进肾囊肿发展。
AVP 作用于V2R 的第二信号即是环 3', 5'单磷酸腺苷。
在多囊肾动物模型中进行的研究证实了使用 V2R 拮抗剂|OPCn31250可降低肾脏大小和囊肿体积 〔20〕。
在常染色体显性遗传的多囊肾患者中使用Tolvaptan 的临床实验正在进行中。
3.4 NDI先天性NDI 可能是由于 V2R 或AQP2变异。
V2R 变异包括2型变异(导致异常折叠和干扰受体从内质网向细胞膜的转移)及 的不稳定转录)。
外源性给予 V2R 拮抗剂可与细胞内异常折叠的 细胞膜转运〔21〕。
在性联NDI 患者中进行的临床研究证实使用选择性 伐普坦(relcovaptan )可显著增加尿渗透压,降低 24 h 尿流量〔22〕,从而改善多尿症状。
