氨基酸的常见化学反应教程文件
氨基酸的重要反应演示文稿

2022/2/17
13
第13页,共20页。
茚三酮
还原茚三酮
O OH OH
O
O
CH
O
+
R
NH2 CH COOH
OH
+
H
H N
H
OH
C
C
C
O
O
C
NC
C
O
还原茚三酮
O
CH OH
O
O + HO
HO O
茚三酮
蓝紫色复合物 (λmax=570nm)
+ NH3
CO2 RCHO
H+
Pro、Hy-Pro与直接形成黄色化合物( λmax=440nm)
第20页,共20页。
R1
HC + H2N
O
COOH H
R
- H2O
+H2O
转氨基反应中间产物
R1
COOH
C N CH
H
R
西佛碱(Schiff’s base)
第8页,共20页。
(二)α-羧基参加的反应
1、成盐、成酯反应
可以屏蔽羧基活化氨基
NH2 R CH COOH
+
C2H5OH
成酯反应
干燥, HCl 回流
+
NH3ClR CH COOC2O5
侧链基团可与特异试剂发生特定反应,用于氨基酸的鉴定,氨 基酸的修饰。
蛋白质化学修饰:在较温和的条件下,以可控制的方式使蛋白 质某些试剂起特异反应,以引起蛋白质中个别氨基酸侧链或功能基 团发生共价化学改变。
第16页,共20页。
1、酪氨酸的酚羟基:
在3和5位上容易发生亲电取代反应,例如发生碘 化或硝化,分别生成一碘酪氨酸和二碘酪氨酸或一硝
有机化学基础知识氨基酸的合成和反应

有机化学基础知识氨基酸的合成和反应有机化学基础知识——氨基酸的合成和反应氨基酸是构成蛋白质的基本单元,对于理解生命活动的基础过程和分子结构具有重要意义。
本文将介绍氨基酸的合成和反应,帮助读者进一步了解有机化学中的氨基酸相关知识。
一、氨基酸的合成氨基酸可以通过多种途径合成,其中最主要的方法有以下几种:1. 斯特莱克合成法斯特莱克合成法是合成α-氨基酸的一种常用方法。
这种方法以碳酸和胺为原料,在存在催化剂的条件下,发生酰胺的羰基活化,得到氨基酸。
2. 格布斯合成法格布斯合成法是一种通过氨基酸的脱水缩合反应合成新的氨基酸的方法。
该方法通过两个不同的氨基酸分子间的羧基和氨基的反应,生成新的氨基酸,反应需要在酸性条件下进行。
3. 氨基化合物的合成此外,还可以通过合成氨基化合物,再将其转化为氨基酸。
例如,通过胺与酸酐反应生成酰化胺,再通过水解反应将酰化胺转化为相应的氨基酸。
二、氨基酸的反应氨基酸在有机化学中具有丰富的反应性,主要表现在以下几个方面:1. 缩合反应氨基酸的缩合反应是指多个氨基酸在酸性或碱性条件下,通过酯键或酰胺键的形成缩合为多肽。
这种反应在生物体内形成蛋白质的过程中尤为重要。
2. 氨化反应氨基酸可以与氨基化合物反应,发生氨化反应生成新的氨基酸衍生物。
这种反应可通过调整反应条件和反应物的选择,实现氨基酸结构的改变和扩展。
3. 酸碱性反应氨基酸中的氨基和羧基具有酸碱特性,可发生与酸或碱的反应,形成相应的盐类。
当氨基酸在碱性溶液中时,氨基接受H+生成氨离子,氨离子极易溶解于水中。
4. 氧化还原反应氨基酸中的羧基和氨基都可以参与氧化还原反应。
例如,氨基酸的羧基可以被氧化生成相应的羧酸,而氨基则可以被还原生成相应的胺。
三、氨基酸的应用氨基酸作为生物体内重要的生物分子,在医药、食品、化妆品等领域具有广泛的应用价值。
1. 医药领域氨基酸作为药物的原料,可以合成多种药物,如抗生素、抗肿瘤药物等。
此外,氨基酸还可以作为体外代谢工程和靶向药物传递的载体。
化学反应中的氨基酸的酸碱中和反应

化学反应中的氨基酸的酸碱中和反应化学反应是化学领域中不可或缺的研究内容,其中氨基酸的酸碱中和反应更是广泛应用于生物化学、医学等领域。
本文将着重介绍氨基酸的酸碱中和反应过程以及其在生物化学中的应用。
一、氨基酸的结构与性质在化学领域中,氨基酸是指含有羧基(COOH)和胺基(NH2)的有机化合物。
根据侧链不同,氨基酸可以分为20种,其中人体中常见的氨基酸有丝氨酸、半胱氨酸、甘氨酸、赖氨酸等。
与一般有机化合物不同,氨基酸具有明显的酸碱性质。
当氨基酸在溶液中时,可根据其的羧基和胺基上的游离质子(即H+)含量分为三类:酸性氨基酸、碱性氨基酸和中性氨基酸。
二、氨基酸的酸碱中和反应过程当氨基酸分子中的游离质子数等于负离子数时,氨基酸表现出中性性质。
例如,丝氨酸(Ser)分子式为HO2CCH(NH2)CH2OH,当其处于中性状态时,其游离质子数等于负离子数,即:HO2CCH(NH2)CH2OH ⇌ H+ + O2CCH(NH2)CH2OH-当氨基酸处于酸性条件下,即游离质子(H+)的浓度高于胺基(NH2)的浓度时,氨基酸表现出酸性性质。
此时,质子(H+)会与胺基(NH2)中的自由电子形成NH3+,羧基(COO-)中的电子会往外挤,形成COOH。
例如,在酸性环境下,丝氨酸会发生如下的反应:HO2CCH(NH2)CH2OH ⇌ H+ + HO2CCH(NH3+)CH2OHHO2CCH(NH3+)CH2OH ⇌ HO2CCH(NH2)CH2OH + H+当氨基酸处于碱性条件下,即游离质子(H+)的浓度小于或等于胺基(NH2)的浓度时,氨基酸表现出碱性性质。
此时,胺基(NH2)会接受水分子中的质子(H+),形成NH3+。
例如,在碱性环境下,丝氨酸会发生如下的反应:HO2CCH(NH2)CH2OH ⇌ HO2CCH(NH)CH2OH- + H+HO2CCH(NH)CH2OH- + H2O ⇌ HO2CCH(NH3+)CH2OH三、氨基酸的酸碱中和反应在生物化学中的应用人体内有许多重要的物质,例如各种酶、激素和细胞膜等都是由氨基酸组成的。
氨基酸脱水缩合化学反应式

氨基酸脱水缩合化学反应式
氨基酸脱水缩合反应是生物体内构建蛋白质的重要过程。
在这个过程中,两个氨基酸分子通过脱水反应结合成肽键,形成多肽链。
这个化学反应式可以用以下方式表示:
氨基酸1 + 氨基酸2 → 肽键 + H2O
在这个反应中,两个氨基酸分子之间的羧基和氨基发生反应,生成一个肽键,并释放出一个水分子。
这一反应在生物体内发生的同时,也可以通过实验室合成。
合成多肽链的方法有多种,例如固相合成和液相合成等。
无论是在生物体内还是实验室中,氨基酸脱水缩合反应都是蛋白质合成的基础。
氨基酸脱水缩合反应具有重要的生物学意义。
生物体内的蛋白质合成依赖于这个反应,通过不同的氨基酸组合,可以合成出各种不同功能的蛋白质。
蛋白质作为生物体内最基本的大分子,参与了许多重要的生命活动,如酶的催化作用、结构的维持和信号传导等。
因此,氨基酸脱水缩合反应对于生物体的正常功能发挥至关重要。
除了在生物体内合成蛋白质,氨基酸脱水缩合反应还可以用于合成药物和高分子材料。
通过合成不同的氨基酸序列,可以获得具有特定功能的多肽药物,如抗菌肽和抗肿瘤肽等。
此外,氨基酸脱水缩合反应还可以用于制备具有特定功能的高分子材料,如聚酰胺和聚酯等。
氨基酸脱水缩合反应是生物体内合成蛋白质的基础过程,也是合成药物和高分子材料的重要手段。
通过这个化学反应,我们可以合成出具有特定功能的蛋白质、药物和材料,推动生物科学和化学科学的发展。
氨基酸脱水缩合反应的研究将为我们深入了解生命的奥秘和开发新型功能材料提供重要的理论和实践基础。
氨基酸的化学反应
4
、
氨基酸的化学反应
与
苯
异 硫
AA
弱碱
AA
氰 PITC+ 多肽
酸 酯
蛋白
反
PTC—多肽 无水甲酸 蛋白
或HF
应
PTH-AA + 少一个AA的多肽或蛋白
(乙酸乙酯)
用途:可以用来鉴定多肽或蛋白质NH2末端氨
基酸.亦称Edman反应
Edman反应
— —
-N=C=S +H 2NCHCO-NHCHCO
—
=O
C
C
C N= C
C
C
③产物颜色过久易退。
R-CHO
=O
蓝紫色
用途:常用于 氨基酸的定性或定量分析。
=O
• 反应要点
A.该反应由-NH2与-COOH共同参与 B.茚三酮是强氧化剂 C.该反应非常灵敏,可在570nm测定吸光值 D. 测定范围:0.5~50µ g/ml E.脯氨酸与茚三酮直接生成黄色物质(不释放NH3) • 应用: A.氨基酸定量分析(先用层析法分离) B.氨基酸自动分析仪:
HO-Hg+
COO-
对羟汞苯甲酸
团 的 化
-OOC CHCH2 S Hg+ NH3+
COO-
学
性 质
作用:与金属离子的螯合性质可用于体内解毒
也是蛋白质结晶学中制备重原子衍生物最常用的方法
(1) 巯基(-SH)的性质
6
.
侧 链 基
-OOC CHCH2 SH NH3+
团
-OOC CHCH2 SH
的
NH3+
化
学
性
质
-OOC -OOC
氨基酸的重要化学反应
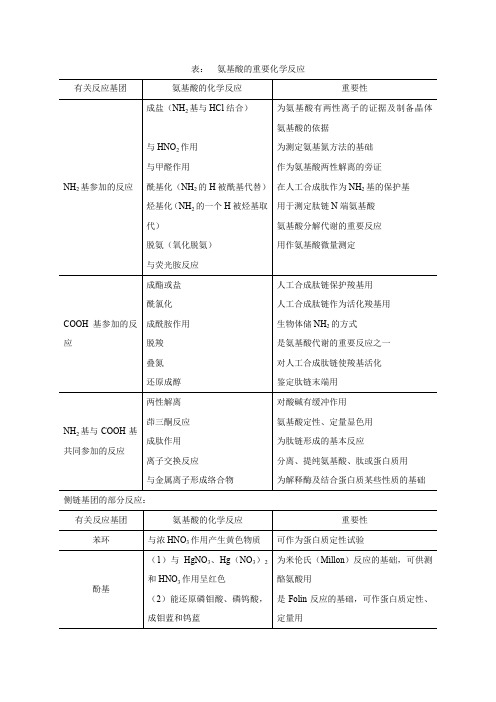
COOH 基参加的反 应
成酰胺作用 脱羧 叠氮 还原成醇 两性解离 茚三酮反应
NH2 基与 COOH 基 共同参加的反应
成肽作用 离子交换反应 与金属离子形成络合物
侧链基团的部分反应: 有关反应基团 苯环 氨基酸的化学反应 与浓 HNO3 作用产生黄色物质 ( 1 )与 HgNO3 、 Hg (NO3 ) 2 酚基 和 HNO3 作用呈红色 (2)能还原磷钼酸、磷钨酸, 成钼蓝和钨蓝 重要性 可作为蛋白质定性试验 为米伦氏(Millon)反应的基础,可供测 酪氨酸用 是 Folin 反应的基础,可作蛋白质定性、 定量用
(3)与重氮化合物(如对氨基 苯磺酸的重氮盐) 结合生成橘黄 色 (1)与乙醛酸及浓 H2SO4 作用 呈紫红色 吲哚基 (2)能还原磷钼酸、磷钨酸, 成钼蓝、钨蓝 与 α-萘酚和次溴酸盐作用生成 胍基 红色物质(在碱性液中) (1) 亚胺—NH 部位可同三苯甲 基或磷酸结合 咪唑基 (2)与重氮苯磺酸作用生成棕 红色 (1) -SH 基可与 (C6H5) 3—C— 基结合成—S—C(C6H5)3 基 硫氢基 (—SH与 Ellman 试剂作 用 OH 基(丝氨酸、酪 氨酸)
表: 氨基酸的重要化学反应 有关反应基团 氨基酸的化学反应 成盐(NH2 基与 HCl 结合) 重要性 为氨基酸有两性离子的证据及制备晶体 氨基酸的依据 与 HNO2 作用 与甲醛作用 NH2 基参加的反应 为测定氨基氮方法的基础 作为氨基酸两性解离的旁证
酰基化(NH2 的 H 被酰基代替) 在人工合成肽作为 NH2 基的保护基 烃基化 (NH2 的一个 H 被烃基取 代) 脱氨(氧化脱氨) 与荧光胺反应 成酯或盐 酰氯化 人工合成肽链保护羧基用 人工合成肽链作为活化羧基用 生物体储 NH2 的方式 是氨基酸代谢的重要反应之一 对人工合成肽链使羧基活化 鉴定肽链末端用 对酸碱有缓冲作用 氨基酸定性、定量显色用 为肽链形成的基本反应 分离、提纯氨基酸、肽或蛋白质用 为解释酶及结合蛋白质某些性质的基础 用于测定肽链 N 端氨基酸 氨基酸分解代谢的重要反应 用作氨基酸微量测定
《生物化学》氨基酸

氨基酸的两性解离:
阳离子
两性离子
阴离子
以甘氨酸为例: pK1= 2.34 pK2 = 9.60
+
H3N-CH2-COOH
[Gly+]
K’1
+H3N-CH2-COO- +[ H+] [ Gly±]
pI = 5.97
[Gly±][H+]
K1’=
[Gly+]
+H3N-CH2-COO- K’2 [Gly±]
苯丙氨酸
Phenylalanine Phe F
— CH 2— CH— COO-
NHN3H+ 3+
酪氨酸
Tyrosine Tyr Y
HO —
— CH 2— CH— COO-
NH3+ NH3+
组氨酸
Histidine His H
HC C — CH 2— CH— COO-
+HN
NH
C H
咪唑基
NH3+
如图所示
H3N+
COOH CH2
(Gly+)
COO-
H3N+ CH (G2 ly±)
COO-
H2N
CH2
(Gly-)
pH 14 12 10 8
[Gly+ ] = [Gly±]
6 4 2 0
0.1
pK1=2.34
0.05
加入的H+ mol数甘Βιβλιοθήκη 氨pK2=9.60
酸
的
pI=5.97
滴
[Gly ±] = [Gly-]
[Gly±][H+] K1’
= K2’ [Gly±]
氨基酸的四个重要化学反应原理及应用

氨基酸的四个重要化学反应原理及应用氨基酸是构成蛋白质的基本组成单元,对于生物体的生长和代谢至关重要。
在生物体内,氨基酸参与了许多重要的化学反应,这些反应不仅在生物体内起着关键作用,也在医学和生物化学领域有着广泛的应用。
本文将介绍氨基酸的四个重要化学反应原理及其在生物体内和医学领域中的应用。
一、酸碱中和反应酸碱中和反应是氨基酸在生物体内起着关键作用的一种重要化学反应。
氨基酸分子中的氨基和羧基均可与其他分子中的酸性或碱性基团进行中和反应,形成盐和水。
这种反应对于维持生物体内部的酸碱平衡至关重要。
当氨基酸在胃部被蛋白酶分解而产生的羧基和氨基离子进入肠道时,它们会与肠道中的盐酸进行中和反应,使酸碱平衡得以维持。
酸碱中和反应也在体外试管实验中被广泛应用,例如在酶反应体系中调节pH值,以促进酶的活性。
二、氨基酸脱羧反应氨基酸脱羧反应指的是氨基酸分子中的羧基被氨基所脱去的过程。
这种反应在生物体内参与了许多重要的代谢途径,例如氨基酸的降解和合成。
在氨基酸的降解过程中,氨基酸通过脱羧反应生成相应的醛、酮或其他代谢产物,参与能量产生或其他生物化学途径。
在生物体内的代谢途径研究中,氨基酸脱羧反应也被广泛地应用。
在肝脏中,氨基酸脱羧反应参与了尿素循环的代谢途径,调节体内氮代谢平衡。
三、氧化还原反应氨基酸分子中的氨基和羧基均可参与氧化还原反应,这些反应对于氨基酸的功能和代谢至关重要。
在肝脏中,氨基酸的氨基可被氧化为酮酸,而氨基酸的羧基可被还原为醇,这些反应参与了氨基酸的代谢途径。
氨基酸分子中的硫氢基还可参与氧化还原反应,形成二硫键或参与其他重要的生物化学反应。
在医学领域,氨基酸的氧化还原反应被广泛地应用于氨基酸代谢异常的诊断和治疗。
四、氨基酸的缩合反应氨基酸的缩合反应是指两个或多个氨基酸分子通过缩合作用形成肽键的过程。
这种反应在蛋白质的合成过程中起着关键作用,通过氨基酸的缩合反应,氨基酸分子可以串联成长链状的多肽或蛋白质分子。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
氨基酸的常见化学反应
⏹ -氨基的反应
⏹亚硝酸反应
⏹范围:可用于Aa定量和蛋白质水解程度的测定(Van slyke法)
⏹注意:生成的氮气只有一半来自于Aa,ε氨基酸也可反应,速度较
慢.
⏹与酰化试剂的反应
⏹Aa+酰氯,酸酐-→Aa被酰基化
⏹丹磺酰氯用于多肽链末端Aa的标记和微量Aa的定量测量.
⏹烃基化反应
⏹Aa的氨基的一个氢原子可被羟基(包括环烃及其衍生物)取代.
⏹与2,4-二硝基氟苯(DNFB,FDNB)反应
⏹最早Sanger用来鉴定多肽或蛋白质的氨基末端的Aa
⏹与苯异硫氰酸酯(PITC)的反应
⏹Edman用于鉴定多肽或蛋白质的N末端Aa.在多肽和蛋
白质的Aa顺序分析方面占有重要地位(Edman降解法)
⏹形成西佛碱反应
⏹Aa的α-NH2能与醛类化合物反应生成弱碱,即西佛碱(schiff ‘s
base)
⏹前述甲醛滴定:甲醛与H2N-CH2-COO-结合,有效地减低了后者的
浓度,所以对于加入任何量的碱, [H2N-CH2-COO- ]/
[+H3N-CH2-COO- ]的比值总要比不存在甲醛的情况下小得多。
加入
甲醛的甘氨酸溶液用标准盐酸滴定时,滴定曲线B并不发生改变。
⏹脱氨基反应
⏹Aa在生物体内经Aa氧化酶催化即脱去α-NH2而转变成酮酸
⏹α-COOH参加的反应
⏹成盐和成酯反应
⏹Aa + 碱-→盐
⏹Aa + NaOH -→氨基酸钠盐(重金属盐不溶于水)
⏹Aa-COOH + 醇-→酯
⏹Aa+ EtOH ---→氨基酸乙酯的盐酸盐
⏹当Aa的COOH变成甲酯,乙酯或钠盐后,COOH的化学反
应性能被掩蔽或者说COOH被保护,NH2的化学性能得到
了加强或活化,易与酰基结合。
Aa酯是制备Aa的酰氨or
酰肼的中间物
⏹
⏹成酰氯反应
⏹当氨基酸的氨基用适当的保护基保护以后,其羧基可与二氯亚砜作
用生成酰氯
⏹用于多肽人工合成中的羧基激活
⏹叠氮反应
⏹氨基酸的氨基通过酰化保护后,羧基经酯化转变为甲酯,然后与肼
和亚硝酸变成叠氮化合物
⏹用于多肽人工合成中的羧基激活
⏹脱羧基反应
⏹α-氨基和α-羧基共同参与的反应
⏹与茚三酮反应
⏹茚三酮在弱酸性溶液中与α-氨基酸共热,引起氨基酸氧化脱氨、脱
羧反应,最后茚三酮与反应产物中的氨和还原茚三酮发生作用生成
紫色物质
⏹Pro与hyPro(羟脯氨酸)不释放氨,而直接生成黄色化合物
⏹定性,定量测定各种Aa,蛋白质
⏹测定CO2 的量,从而可计算参加反应的Aa的量
⏹成肽反应
⏹一个Aa的NH2+另一个Aa的COOH可以缩合成肽,形成的键称肽
键
⏹侧链R基参加的反应
⏹R功能基:
⏹羟基,酚基,巯基(二硫键),吲哚基,咪唑基,胍基,甲硫基,非
α-NH2,非α-COOH
⏹酪氨酸的酚基在3和5位上容易发生亲电取代反应
⏹二碘酪氨酸或一硝基酪氨酸和二硝基酪氨酸
⏹酪氨酸的酚基可以与重氮化合物(对氨基苯磺酸的重氮盐)生成桔
黄色的化合物。
——Pauly反应
⏹组氨酸的咪唑基可以发生类似反应但产物颜色为棕红色。
⏹精氨酸的侧链胍基在硼酸钠缓冲液(pH 8-9, 25-35︒C)中,与1.2-环已二酮
反应,生成缩合物。
该缩合物在羟胺缓冲液中,重新生成Arg
⏹色氨酸的侧链吲哚基在温和条件下可被N-溴代琥珀酰亚胺
(N-bromosuccinimide)氧化。
此反应可用于分光光度法测定蛋白质中色氨
酸的含量,并能在色氨酸和酪氨酸残基处选择性化学断裂肽键。
⏹蛋氨酸侧链上的甲硫基是一个很强的亲核基团,与烃化试剂如甲基碘容易形
成锍盐(sulfonium salt)
⏹此反应可被硫基试剂逆转。
在逆转反应中,原有的甲基和新加入的
甲基除去的机会是相等的,因此当用14C标记的甲基碘处理时,获
得的蛋氨酸将有50%是同位素标记的。
⏹半胱氨酸侧链上的巯基(-SH)有很强的反应活性,可参与很多反应
⏹二硫键的形成和打开
⏹2R-SH + 1/2 O2-→R-S-S-R + H2O ;Cu2+,Fe2+ ,
Co2+和Mn2+存在下,巯基的空气氧化将显著提高。
⏹胱氨酸中的二硫键在稳定蛋白质的构象上起很大的作用。
氧
化剂和还原剂都可打开二硫键。
过甲酸可以定量地打开二硫
键,生成磺基丙氨酸(cysteic acid)残基。
还原剂如巯基化
合物(R-SH)也能打开二硫键,生成半胱氨酸残基及相
应的二硫化物
⏹二硫苏糖醇(dithiothreitol,缩写为DTT),与胱氨酸中的二
硫键反应形成一个含分子内二硫键的稳定六元环
⏹巯基能和各种金属离子形成稳定程度不等的络合物e.g. 对氯汞苯甲
酸(p-chloromercuribenzoic acid)
⏹由于许多蛋白质,如SH酶,其活性中心涉及-SH基,当遇
到重金属离子而生成硫醇盐时,将导致酶的失活,因此制备
这类蛋白质时应避免进入重金属离子
⏹半胱氨酸可与二硫硝基苯甲酸(dithionitrobenzoic acid,缩写为
DTNB)或称Ellman氏试剂发生硫醇-二硫化物交换反应
⏹反应中1分子的半胱氨酸引起1分子的硝基苯甲酸的释放。
它在pH8.0时,在412nm波长处有强烈的光吸收,因此可利
用比色法定量测定-SH基。
