大学物理:13-8 热力学第二定律的统计解释
13 热力学第二定律 熵

结论: 宏观态包含的微观状态 数越多(状态几率越大), 系统 的熵就越大, 无序程度越高.
* 熵是系统状态的单值函数.
(熵的增量与过程无关)
* 熵是系统无序性的量度.
* 熵是系统接近平衡态程度的
S 0 等号对应可逆过程
熵增加的条件 1) 统计规律: 熵减小的过程并非 不可能发生, 而是在大量粒子组 成的群体中出现的概率太小. 2) 普遍性: 任何事物如果任其发 展, 其混乱程度一定有增无减. 思考: 1. 结冰的过程和化冰的过程都 是熵增加吗? 2. 人从出生到老年一直是熵增 加吗? 答案: 开放系统的自组织能力使系统 有序.
能量守恒, 为何会有能源危机? 可见: 自然界中遵从能量守恒 的过程并非都可以实现! 结论: 1. 从不平衡到平衡的过程可自 发进行, 且不可逆, 例如热传递 实现热平衡. 2. 从不均匀到均匀的过程可自 发进行, 且不可逆, 例如气体扩 散实现分布均匀. 3. 从有序到无序的过程可自发 进行, 且不可逆, 例如功变热, 花 瓶摔碎实现有序性降低.
结论: 1. 从不平衡到平衡的过程可自 发进行, 且不可逆, 例如热传递 实现热平衡. 2. 从不均匀到均匀的过程可自 发进行, 且不可逆, 例如气体扩 散实现分布均匀. 3. 从有序到无序的过程可自发 进行, 且不可逆, 例如功变热, 花 瓶摔碎实现有序性降低.
总之, 凡是系统从不平衡, 不均 匀, 有序的状态向平衡, 均匀, 无序的状态进行的过程都可以 自发地实现, 且不可逆.
克劳修斯熵公式:
S S 2 S1
2
1
dQ T
思考 1. 就整个热学框架,热力学第二定律对热力学第一定律做了什 么样的补充? 2. 热力学第二定律的定量描述是什么? 3. 熵的计算与系统的热力学过程有关吗?
热力学第二定律详解

热力学第二定律(英文:second law of thermodynamics)是热力学的四条基本定律之一,表述热力学过程的不可逆性——孤立系统自发地朝着热力学平衡方向──最大熵状态──演化,同样地,第二类永动机永不可能实现。
这一定律的历史可追溯至尼古拉·卡诺对于热机效率的研究,及其于1824年提出的卡诺定理。
定律有许多种表述,其中最具代表性的是克劳修斯表述(1850年)和开尔文表述(1851年),这些表述都可被证明是等价的。
定律的数学表述主要借助鲁道夫·克劳修斯所引入的熵的概念,具体表述为克劳修斯定理。
虽然这一定律在热力学范畴内是一条经验定律,无法得到解释,但随着统计力学的发展,这一定律得到了解释。
这一定律本身及所引入的熵的概念对于物理学及其他科学领域有深远意义。
定律本身可作为过程不可逆性[2]:p.262及时间流向的判据。
而路德维希·玻尔兹曼对于熵的微观解释——系统微观粒子无序程度的量度,更使这概念被引用到物理学之外诸多领域,如信息论及生态学等克劳修斯表述克劳修斯克劳修斯表述是以热量传递的不可逆性(即热量总是自发地从高温热源流向低温热源)作为出发点。
虽然可以借助制冷机使热量从低温热源流向高温热源,但这过程是借助外界对制冷机做功实现的,即这过程除了有热量的传递,还有功转化为热的其他影响。
1850年克劳修斯将这一规律总结为:不可能把热量从低温物体传递到高温物体而不产生其他影响。
开尔文表述参见:永动机#第二类永动机开尔文勋爵开尔文表述是以第二类永动机不可能实现这一规律作为出发点。
第二类永动机是指可以将从单一热源吸热全部转化为功,但大量事实证明这个过程是不可能实现的。
功能够自发地、无条件地全部转化为热;但热转化为功是有条件的,而且转化效率有所限制。
也就是说功自发转化为热这一过程只能单向进行而不可逆。
1851年开尔文勋爵把这一普遍规律总结为:不可能从单一热源吸收能量,使之完全变为有用功而不产生其他影响。
热力学第二定律的统计解释
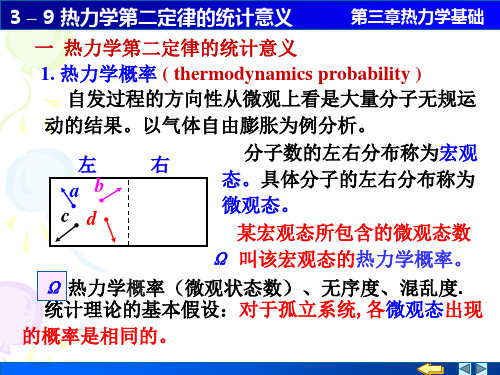
3 – 9 热力学第二定律的统计意义
第三章热力学基础
N1
2
4
N
Ω
(左)
2
22
24
2N
0
N个分子,Ωi
2 N。
若N=100, 则:
Ωi 2100 1030
而左右各半的平衡态及其附近宏观态的热力学概率则
占总微观状态数的绝大比例。 Ω(N左)
一般热力学系统 N的数量级约
N 很大
为1023,上述比例实际上是百分
概率小的状态
概率大的状态
讨论 N 个粒子在空间的分布问题
可分辨的粒子集中在 左空间的概率
N 1, 2
N 2, 4
3 – 9 热力学第二定律的统计意义
第三章热力学基础
b Aa
B
cd
ab
bc
c
a dcd
a bd
a bd
c
1 1264
A
bBa
cd
bd c
a
ab
c d
分子的分布
容器 A
的部
分B
设 S f(),求 f 的函数形式。
由 S 的可加性来分析:
1 S1, 1
1+2
S,
2 S2, 2 1、2彼此独立
∴ 应有: f( ) ln
3 – 9 热力学第二定律的统计意义
第三章热力学基础
S k ln
─ 玻耳兹曼熵公式
1877年玻耳兹曼提出了S ln 。
1900年普朗克引进了比例系数 k 。
ab cd
0
0a
b
c
d
bc ac ab a a d d d bc b
abbc cd d
大学物理热力学第二定律知识点总结

大学物理热力学第二定律知识点总结热力学第二定律是大学物理热学部分的重要内容,它揭示了热现象过程中的方向性和不可逆性。
理解和掌握热力学第二定律对于深入研究热学以及相关领域具有重要意义。
以下是对热力学第二定律相关知识点的详细总结。
一、热力学第二定律的表述1、克劳修斯表述热量不能自发地从低温物体传向高温物体。
这意味着热传递的过程具有方向性,如果没有外界的干预,热量只会从高温物体流向低温物体,而不会反向流动。
2、开尔文表述不可能从单一热源吸取热量,使之完全变为有用功而不产生其他影响。
也就是说,第二类永动机是不可能制成的。
第二类永动机是指一种能够从单一热源吸热,并将其全部转化为功,而不产生其他变化的热机。
二、热力学第二定律的微观解释从微观角度来看,热力学第二定律反映了大量分子热运动的无序性。
在一个孤立系统中,分子的热运动总是从有序趋向无序,这是一个自发的过程。
比如,将不同温度的气体混合在一起,它们会自发地达到温度均匀分布的状态,而不会自动地分离成原来的不同温度区域。
这是因为分子的无规则运动使得它们更容易趋向无序的分布。
三、熵熵是描述系统无序程度的热力学概念。
熵的增加表示系统的无序程度增加。
对于一个绝热过程,系统的熵永不减少。
如果是可逆绝热过程,熵不变;如果是不可逆绝热过程,熵增加。
熵的计算公式为:$dS =\frac{dQ}{T}$,其中$dQ$ 是微元过程中的吸热量,$T$ 是热力学温度。
四、卡诺循环与卡诺定理1、卡诺循环卡诺循环由两个等温过程和两个绝热过程组成,是一种理想的热机循环。
通过卡诺循环,可以计算出热机的效率。
卡诺热机的效率为:$\eta = 1 \frac{T_2}{T_1}$,其中$T_1$ 是高温热源的温度,$T_2$ 是低温热源的温度。
2、卡诺定理(1)在相同的高温热源和低温热源之间工作的一切可逆热机,其效率都相等,与工作物质无关。
(2)在相同的高温热源和低温热源之间工作的一切不可逆热机,其效率都小于可逆热机的效率。
热力学第二定律的微观解释

自然过程总是向着 使系统热力学几率 增大旳方向进行。
注意:微观状态数最 大旳平衡态状态是最 混乱、最无序旳状态。
一切自然过程总是 沿着无序性增大旳 方向进行。
1)合用于宏观过程对微观过程不合用, 如布朗运动。
2)孤立系统有限范围。 对整个宇宙不合用。
4.熵与熵增长原理
“熵”是什么?“熵”是德国物理学家克劳修斯在 1850年发明旳一种术语,他用熵来表达任何一种能量 在空间分布旳均匀程度。能量分布得越均匀,熵就越 大。假如对于我们所考虑旳那个系统来说,能量完全 均匀地分布,那么这个系统旳熵就到达最大值。
1.电冰箱能够不断地把热量从温度较低旳冰箱内部 传给温度较高旳外界空气,这阐明了 BD A.热量能自发地从低温物体传给高温物体 B.在一定条件下,热量能够从低温物体传给高温物 体 C.热量旳传导过程不具有方向性 D.在自发地条件下热量旳传导过程具有方向性
[精与解] 我们懂得,一切自发过程都有方向性,如热传导, 热量总是由高温物体传向低温物体;又如扩散,气体总是由密 度大旳地方向密度小旳地方扩散。假如在外界帮助下气体能够 由密度大旳地方向密度小旳地方扩散,热量能够从低温物体传 向高温物体,电冰箱就是借助外力做功把热量从低温物体─冷 冻食品传向高温物体─周围旳大气。所以,在回答热力学过程 旳方向问题时,要区别是自发过程还是非自发过程,电冰箱内 热量传递旳过程是有外界参加旳。本题答案是A错B对C错D对。
多种宏观态不是等几率旳。那种宏观态包括旳微 观态数多,这种宏观态出现旳可能性就大。
定义热力学几率:与同一宏观态相应旳微观态数称为 热力学几率。记为 。 在上例中,均匀分布这种宏观态,相应旳微观态最多, 热力学几率最大,实际观察到旳可能性或几率最大。
对于1023个分子构成旳宏观系统来说,均匀分布这种 宏观态旳热力学几率与多种可能旳宏观态旳热力学几 率旳总和相比,此比值几乎或实际上为100%。
热力学第二定律的表述及理解

热力学第二定律的表述理解热力学第一定律阐明了能量转换过程中的守恒关系,指出了不消耗能量而能不断输出功的第一类永动机确是一种幻想。
热力学第二定律则更深刻地揭示了能量的品质问题。
熵,或许发明这一物理量的先贤也未始能预料到其对自然科学甚至哲学竟能产生如此巨大的影响。
热力学第二定律有数种表达形式,最闻名于世的有克劳修斯表达和开尔文表达。
1.开尔文表述英国物理学家开尔文(1824~1907),1845年毕业于剑桥大学,1846年受聘为格拉斯哥大学自然哲学教授,长达50余年,1851年被选为英国皇家学会会员,1877年被选为法国科学院院士,1890年至1895年担任皇家学会会长,他对热学和电磁学的发展都作出了重要的贡献。
1851年开尔文在爱丁堡皇家学会会刊上发表了一篇论文,题目是“论热的动力理论”,文章指出:不存在这样一个循环过程,系统从单一热源吸收热量,使之完全变为有用功而不产生其他影响.表述中“单一热源”是指温度均匀且恒定的热源;“其他影响”指除了由单一热源吸热,把吸收的热用来做功以外的任何其他变化.若有其他影响产生时,把由单一热源吸来的热量全部用以对外做功是可能的.自然界任何形式的能都可能转化为热,但热却不能在不产生其他影响的条件下完全转变成其他形式的能.开尔文的论述虽然较克劳修斯晚一年,但他的论述更为明确,使得热力学第二定律的研究更加深入,此外,开尔文还从第二定律断言:能量耗散是普遍趋势.2.克劳修斯表述德国物理学家克劳修斯(1822~1888),曾在柏林大学学习4年,后于1848年毕业于哈雷大学.1850年他任柏林皇家炮工学校物理教授,1855年后他相继任苏黎士维尔茨堡和波恩大学物理教授.他除了建立热力学第二定律,引入态函数——熵,还对气体分子动理论做了较全面的论述,用统计平均的方法导出了理想气体的压强、温度和气体的平均自由程公式。
克劳修斯于1850年在《德国物理学年鉴》上率先发表了《论热的动力及能由此推出的关于热本质的定律》,把卡诺定理作了扬弃而改造成与热力学第一定律并列的热力学第二定律.他提出,热量总是自动地从高温物体传到低温物体,不可能自动地由低温物体向高温物体传递.或者说不可能把热量从低温物体传到高温物体,而不引起其他变化.即在自然条件下,这个转变过程是不可逆的,若想让热传递的方向逆转,则必须消耗功才能实现.以上两种表述是等效的,说明了热量不可能全部转化为机械功以及这一转化过程的方向性.人们一度曾设想一种能从单一热源吸收热量,使之完全转变成有用的机械功而不产生其他影响的第二类永动机,第二类永动机虽不违背热力学第一定律,但违背热力学第二定律,因而是不可能造成的.第二定律除了以上两种表述外,还有其他不同的表述,例如热效率为100%的热机是不可能制成的;不需要由外加功而可操作致冷的机器是不可能造成的等.第二定律无论采用何种表述,其内容实质相同,不外乎主张不可逆变化的存在.各种表述的实质在于说明一切与热现象有关的实际宏观过程都是不可逆的。
热力学第二定律的微观解释

第五节
热力学第二定律 的微观解释
知识回顾
热力学第二定律
两种表述
克劳修斯表述: 热量不能自发地 从低温物体传到 高温物体 等价
开尔文表述:不 可能从单一热库 吸收热量,使之 完全变成功,而 不产生其他影响
热力学第二定律:
反映宏观自然过程具有方向性
A B
A
B
宏观过程的自发定向性 与系统大量微观粒子的无 规则运动有关。 学习用微观的统计方法,从本质上说明热力学第 二定律的统计意义。
4.常规能源的大量消耗带来了环境问题 (1)温室效应:温室效应是由于大气里温室气体(二氧化碳、甲 烷等)含量增大而形成的。石油和煤炭燃烧时产生二氧化碳。 (2)酸雨:大气中酸性污染物质,如二氧化硫、二氧化碳、氢氧 化物等,在降水过程中溶入雨水,使其成为酸雨。煤炭中含有 较多的硫,燃烧时产生二氧化硫等物质。 (3)光化学烟雾:氮氧化合物和碳氢化合物在大气中受到阳光中 强烈的紫外线照射后产生的二次污染物质 —— 光化学烟雾,主 要成分是臭氧。
新知学习
有序
无序
宏观态
微观态
1.有序和无序
有序:一个系统的个体按确定的某种规则,有顺 序地排列,即为有序。
无序:对个体分布没有确定的要求,“怎样分布 都可以”,即为无序。
自然界有怎样的规则?
宏观状态生活中的有序和无序
有序的队伍
散乱的人群
宏观状态生活中的有序和无序
以大小排列为规则
杂乱无章的扑克牌
有序排列的扑克牌
宏观状态生活中的有序和无序 以花色排列为规则
杂乱无章的扑克牌
有序排列的扑克牌
总结:由于规则的变更,有序和无序是相对的
如果以大小排列为规则,判断有序、无序 如果以花色排列为规则,判断有序、无序
热力学第二定律具体内容

热力学第二定律具体内容:热力学第二定律是热力学定律之一,是指热永远都只能由热处转到冷处.热力学第二定律是描述热量的传递方向的分子有规则运动的机械能可以完全转化为分子无规则运动的热能;热能却不能完全转化为机械能.此定律的一种常用的表达方式是,每一个自发的物理或化学过程总是向著熵(entropy)增高的方向发展.熵是一种不能转化为功的热能.熵的改变量等于热量的改变量除以绝对温度.高、低温度各自集中时,熵值很低;温度均匀扩散时,熵值增高.物体有秩序时,熵值低;物体无序时,熵值便增高.现在整个宇宙正在由有序趋于无序,由有规则趋于无规则,宇宙间熵的总量在增加.克劳修斯表述不可能把热量从低温物体传到高温物体而不引起其他变化.开尔文表述不可能从单一热源吸取热量,使之完全变为有用功而不产生其他影响.开尔文表述还可以表述成:第二类永动机不可能造成.若要简捷热能不能完全转化为机械能,只能从高温物体传到低温物体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第五版
讨论 N 个粒子在空间的分布问题
可分辨的粒子集中在左空间的概率
N = 1, W = 1 2
N = 2, W =1 4
第十三章 热力学基础
4
物理学
13-8 热力学第二定律的统计解释
第五版
可分辨粒子总数 N = 4 n1 1
第 i 种分布的可能状态数 ni
n2 4 各种分布的状态总数 ni 16
为了纪念玻耳兹 曼给予熵以统计解释 的卓越贡献 ,他的 墓碑上寓意隽永地刻
着 S k lnW
这表示人们对玻耳兹 曼的深深怀念和尊敬.
第十三章 热力学基础
8
物理学
13-8 热力学第二定律的统计解释
第五版
耗散结构 (1)宇宙真的正在走向死亡吗?
实际宇宙万物,宇宙发展充满了无序 到有序的发展变化 .
(2) 生命过程的自组织现象
n3 6
i
粒子集中在左空间的概率
n3 4
W
1 16
1 24
n5 1 粒子均匀分布的概率
W' 6 3 16 8
第十三章 热力学基础
5
物理学
13-8 热力学第二定律的统计解释
第五版
N1
2
4
N
1
1
1
1
(W左) 2
22
24
2N
0
三 熵与热力学概率 玻耳兹曼关系式
熵
S k lnW
W 热力学概率(微观状态数)、 无序度、混乱度.
第十三章 热力学基础
6
物理学
13-8 热力学第二定律的统计解释
第五版
(1)熵的概念建立,使热力学第二定律 得到统一的定量的表述 .
(2)熵是孤立系统的无序度的量度.(平 衡态熵最大.)(W 愈大,S 愈高,系统无序 度愈高.)
第十三章 热力学基础
7
物理学
13-8 热力学第二定律的统计解释
第五版
玻耳兹曼的墓碑
第十三章 热力学基础
10
物理学
13-8 热力学第二定律的统计解释
第五版
dSe 系统与外界交换能量或物质而引
起的熵流
dSi
系统内部不可逆过程所产生的熵 增加
孤立系统 dSi≥ 0, dS ≥ 0
开放系统
dSi≥ 0, dSe < 0 dSi≤ dSe , dS < 0
第十三章 热力学基础
11
物理学
第五版
选择进入下一节:
本章目录
13-0 教学基本要求
13-1 准静态过程 功 热量
13-2 热力学第一定律 内能
13-3 理想气体的等体过程和等压过程 摩尔热容
13-4 理想气体的等温过程和绝热过程
第十三章 热力学基础
12
物理学
13-8 热力学第二定律的统计解释
第五版
一 熵与无序
热力学第二定律的实质:自然界一
切与热现象有关的实际宏观过程都是不可
逆的 .
热序
无序
第十三章 热力学基础
1
物理学
13-8 热力学第二定律的统计解释
第五版
热传导 高温物体 自发传热 低温物体 非自发传热
非均匀、非平衡
均匀、平衡
生物体的生长和物种进化是从无序到 有序的发展.
第十三章 热力学基础
9
物理学
13-8 热力学第二定律的统计解释
第五版
(3) 无生命世界的自组织现象
云、雪花、太阳系、化学实验、热对 流、激光等.
(4)开放系统的熵变
(和外界有能量交换和物质交换的系 统叫开放系统)
开放系统熵的变化dS dSe dSi
扩散过程
自发
V 外力压缩 V V
第十三章 热力学基础
2
物理学
13-8 热力学第二定律的统计解释
第五版
二 无序度和微观状态数
不可逆过程的本质
系统从热力学概率小的状态向热力学 概率大的状态进行的过程 .
一切自发过程的普遍规律
概率小的状态
概率大的状态
第十三章 热力学基础
3
物理学
13-8 热力学第二定律的统计解释
