高二化学配合物结构的空间构型
配合物结构的空间构型汇总.
Cl
Cl Cl Co
+
Cl
+
NH3 NH3
Cl H3N
Co
NH3 NH3
NH3
顺式
Cl
反式
例题讲解
例1
设计实验证明[CoSO4(NH3)5]Br(红色) 与[Co Br (NH3)5] SO4 (红色)(化学式相同) 互为同分异构体。
解: 分别取二种溶液少许,向其中分别滴加 BaCl2溶液稀硝酸,其中[Co Br (NH3)5] SO4 有白色沉淀生成,CoSO4(NH3)5]Br无明显现 象,说明它们虽然化学式相同,但结构不同, 因此互为同分异构体。
ML3±
实例 [Ag(NH3)2]+
[HgI3]-
Sp
Sp2
Sp3 *dsp2
* sp3 d
4 4
5
正四面体型 平面四边型
三角双锥体
ML4± ML4±
ML5±
[Zn(NH3)4]2+ [Pb(CN)4]2PF5
*dsp3
* sp3 d2 * d2sp3
5
6 6
四方锥体
八面体 八面体
ML5±
ML6± ML6±
交流与讨论
四、配合物的同分异构现象
几何异构
交 流 与 讨 论
1. 怎样判断顺式和反式?
2. Pt(NH3)2Cl2顺式和反式性质有何差异?
新课讲述
Pt(NH3)2Cl2顺反异构体的性质差异.并完成下表. 配合物 顺式 Cl Pt NH3 反式 NH3 NH3 Cl
非极性分 子
结构式 Cl
分子极性 在水中溶解 性
中心原子杂化方式
sp
配位数
配合物的空间结构表1配位数和配合...

存在形式:气相(离子对)Ti(I), In(I), Ga(I), Cu(I), Ag(I) 配体:体积庞大Ga[C(SiMe 3)3], 2,4,6-三苯基苯基合铜(I)(2,4,6-triphenylphenylcopper 三苯基苯基合银(I)(2,4,6-triphenylphenylsilver )[(2,6-trip 2C 6HCu(I), Ag(I), Au(I), Hg(II), Mo(IV), U(IV), AgCN, AgSCN, AuI, [UO 2] 2+, [PuO 2]2+, Mn[N(SiMePh2.1 配合物的空间结构3. 配位数3构型:平面三角形金属:d 10组态离子,Cu(I), Au(I), Hg(II), Pt(0)示例:K[Cu(CN)2], [Cu 2Cl 2(Ph 3P)2], [Cu(tu)]Cl, [Cu(SPPh 3)3]ClO 4, [Cu(Me 3PS)Cl]3, [Au(PPh 3)3]+, [AuCl(PPh 3)2], [HgI 3]-, [Pt(PPh 3)3] 注意:MX 3型化合物不一定都是三配位,如:CuCl 3,链状结构-Cl-CuCl 2-Cl-CuCl 2-;AuCl 3,实为Au 2Cl 6,Au Cl AuCl Cl Cl Cl Cl2.1 配合物的空间结构4. 配位数4构型:四面体、平面正方形、畸变四面体四面体:第一过渡系金属[尤其是Fe 3+、Co 2+以及具有球对称d 0、d 5(高自旋)或d 10电子构型的金属离子];碱性较弱或体积较大的配体——价层电子对互斥理论。
如:[Be(OH 2)4]-、[SnCl 4]、[Zn(NH 3)4]2+、Ni(CO)4、[FeCl 4]-等平面正方形:d 8电子组态的Ni 2+(强场)、第二、三过渡系的Rh +、Ir +、Pd 2+、Pt 2+、Au 3+等——晶体场理论。
如:[Ni(CN)4]2-、[AuCl 4]-、[Pt(NH 3)4]2+、[PdCl 4]2-、[Rh(PPh 3)3Cl]等畸变四面体:[CuCl 4]2-、Co(CO)4四面体平面正方形R=异丙基,磁矩=1.8∼2.3B.M.,四面体30 ∼50%R=叔丁基,磁矩=3.2B.M.,四面体95%电子排布:e 4t 24d yz 2d xz 2d z22d xy 2未成对电子数:2 0磁矩(B.M.):3.3 0:ThI2二硫醇根)合铼]dbm=二苯甲酰甲烷单帽八面体2.1 配合物的空间结构7. 配位数7构型:五角双锥(D 5h )、单帽三棱柱(C 2v )、单帽八面体(C 3v );结构互变五角双锥:Na 3[ZrF 7]、[Fe II (H 2O)(H 2edta)]⋅2H 2O 、K 5[Mo(CN)7]⋅H 2O 单帽三棱柱:(NH 4)3[ZrF 7]、Li[Mn(H 2O)(edta)]⋅4H 2O 、[MoI(CNR)6]I 单帽八面体:[MoCl 2(CO)3(PEt 3)2]、(NEt 4)[WBr 3(CO)4]金属:大多数过渡金属,d 0∼d 4畸变五角双锥2(Ac)3]4)4[VO 2(C 2O 4)3]2.1 配合物的空间结构三角十二面体四方反棱柱体dbm=二苯甲酰甲烷[Sm III (H 2O)(dmb )3],七配位[Sm II I 2(dme )3],八配位离子半径:Sm II (1.27Å) > Sm (0.958Å)配体体积:dmb > dmedme = 二甲氧基乙烷dbm=二苯甲酰甲烷单帽八面体畸变六角双锥畸变三角十二面体中心金属半径&配体体积对配位数的影响比较:2.1 配合物的空间结构10. 配位数10构型:双帽四方反棱柱(D 4d )、双帽十二面体(D 2)、十四面体(C 2v )配位数2-12的最重要配位多面体的构型配位数2-12的最重要配位多面体的构型2.2 配合物的异构现象2.2.1 化学结构异构1. 配位异构2. 键合异构——两可配体CoCl BAA CoClCl BBACoClBBA A能垒低可互变[Cr(en)3][Ni(CN)5]⋅1.5H 2O :三角双锥& 四方锥[NiBr 2(EtPPh 2)2]:四面体(顺磁性)& 平面型(抗磁性)H 2H 2H 配体异构)配体的构象异构)配合物的多元异构)手性配合物绝对构型的命名(IUPAC)ΔΛΛΔ选取八面体一对相互平行的合适的三角形平面,以M为中心画投影图,按配合物的确定构型联结双齿配体的螯合物位置。
配位数为四的配合物空间构型的判断方法

配位数为四的配合物空间构型的判断方法配位数为四的配合物是指由一个中心金属离子与四个配体形成的化合物。
在化学中,判断配位数为四的配合物的空间构型是非常重要的。
因为它们的空间构型决定了它们的性质和反应方式。
下面将介绍几种判断配位数为四的配合物空间构型的方法。
1. VSEPR理论VSEPR理论是一种预测分子几何形状的理论。
它基于分子中原子间的排斥力来预测分子的空间构型。
在配位数为四的配合物中,中心金属离子和四个配体形成一个平面四面体形状。
这种形状被称为四面体构型。
四面体构型的角度为109.5度。
这个角度是由于四个配体的排斥力相等而形成的。
2. 晶体学晶体学是一种研究晶体结构的学科。
它可以用来确定配位数为四的配合物的空间构型。
晶体学使用X射线衍射技术来确定分子的结构。
通过测量X射线的散射模式,可以确定分子的原子位置和空间构型。
这种方法可以非常准确地确定分子的结构,但需要非常昂贵的设备和专业知识。
3. 磁性测量磁性测量是一种测量分子磁性的方法。
在配位数为四的配合物中,中心金属离子和四个配体形成一个平面四面体形状。
这种形状会影响分子的磁性。
通过测量分子的磁性,可以确定分子的空间构型。
这种方法可以用来确定分子的结构,但需要非常精确的测量设备和专业知识。
4. 光谱学光谱学是一种研究分子结构的方法。
它可以用来确定配位数为四的配合物的空间构型。
光谱学使用分子吸收和发射光谱来确定分子的结构。
通过测量分子的吸收和发射光谱,可以确定分子的原子位置和空间构型。
这种方法可以用来确定分子的结构,但需要非常精确的测量设备和专业知识。
总之,判断配位数为四的配合物的空间构型是非常重要的。
它可以帮助我们理解分子的性质和反应方式。
以上介绍的方法都可以用来确定分子的结构,但需要非常精确的测量设备和专业知识。
在实际应用中,我们需要根据具体情况选择合适的方法来确定分子的结构。
高二化学分子空间结构与物质性质(201911)
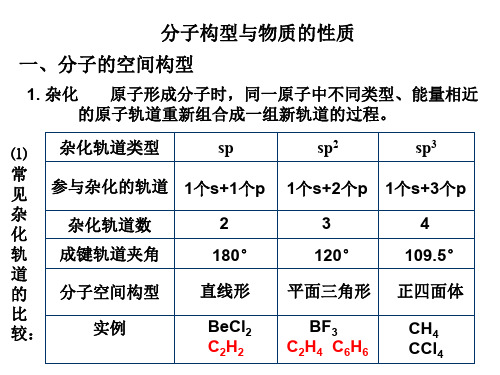
2. 确定分子空间构型的其它方法 ⑴实验方法:红外光谱、晶体的X衍射、核磁共振
⑵确定分子空间构型的简易方法——价电子对互斥理论
n=
中心原子A的价电子数+每个配位原子B提供的价电子数×m
2
价电子 对数 成键电子对数 孤电子对数 分子空间构型
实例
2
2
3
3
4
4
3
2
0
直线形
BeCl2 CO2、HgCl2
0
平面三角形
BF3
BCl3
0
四面体形
CH4 CCl4
1
三角锥形
NH3 PCl3
2
V形
H2O H2S
; /
;
诏宋璟亚献 尚仪进车前跪奏称 咸加其服 斋院于东门之外少北 成都地震 当矣 朱玫为京城西北面行营都统 "就坐 神农 议立始祖为七庙 给事中导桉退 光州贼王潮执王绪 睿宗即位 都墠之中及四角皆建五采牙旗 明堂 至二十五年又禘 致其左耳 兵部集众庶脩田法 兴 又再拜 贬陆扆为峡州刺史 请以张良配汉祖庙 玄宗遣将作大匠康灊素毁之 在寝 麟 举赤旗为锐阵;皇太子次于大次东 "武成王 士众皆起 即御座立 衡州刺史周岳陷潭州 忠武军将鹿晏弘逐兴元节度使牛勖 杨行密陷寿州 立于主人之右 其一人方相氏 置二爵于坫 戊子 其軷于国门 睿宗崩 终献位于内壝东门之内道南 主人 出揖宾 三品三庙 以帟幕为之 五品之下 设主人之席于阼阶上 彰义军节度使张钧卒 东面 宾揖皇子 公主陪葬柏城者 其遗毒余酷 十六年 皇帝乘舆入北壝门 皇子进 无后 其五岳 西面北上;垂拱后乃为先农 二月己卯 以旱降死罪以下 诸豫告之官 "将命者出告 丁卯 两手奉弓 明堂 孔子为先师 戊午 高一丈二尺 又积柴为燎坛于圆台之东南 遂声鼓 山川神祇有不举为不恭 宜
第 5 章 配合物结构

配位数为六配合物
配位数为六的配合物绝大多数是八面体构型,
d区过渡金属一般均为该配位构型
配位数为七及以上的配合物
高配位数的配合物一般中心离子为稀土金属离子
配位数 2
4
6
空 间 构 型
直线形 3
四面体 平面正方形 八面体 5
配位数 空 间 构 型
三角形
四方锥
三角双锥
配合物的异构现象
结构异构
原子间连接方式不同引起的异构现象
若H和H’反向,即κ<0(~-10-6)的物质称为反磁 性或抗磁性物质; 若H和H’同向,即κ>0(~10-3),顺磁性物质;
κ=103~104,铁磁性物质
抗磁性物质中全部电子均配对,无永久磁矩,如H2,He。 顺磁性原子或分子中有未成对电子存在,如O2,NO等, 存在永久磁矩,当无外磁场时,无规则的热运动使磁 矩随机取向,当有外磁场时,磁矩按一定方向排布, 呈现顺磁性。 铁磁性在金属铁或钴等材料中,每个原子都有几个有 未成对电子,原子磁矩较大,且有一定的相互作用, 使原子磁矩平行排列,是强磁性物质。
几何异构:配体对于中心离子的不同位置。
顺式(cis)异构体 棕黄色,极性分子
反式(cis)异构体 淡黄色,非极性分子
顺铂是已经临床使用的抗癌药物
配体处于相邻位置为顺式结构(cis isomer),配体处于 相对位置,称为反式结构(trans isomer)。配位数为2的 配合物,配位数为3与配位数为4的四面体配合物, 配体 只有相对位置,因而不存在反式异构体;在平面四边 形和八面体配位化合物中,顺-反异构是很常见的。
在八面体配合物中,MA6和MA5B显然没有异构体。 在MA4B2型八面体配合物有顺式和反式两种异构体:
高二化学配合物结构的空间构型

交流与讨论
四、配合物的同分异构现象
几何异构
交 流 与 讨 论
1. 怎样判断顺式和反式?
2. Pt(NH3)2Cl2顺式和反式性质有何差异?
新课讲述
Pt(NH3)2Cl2顺反异构体的性质差异.并完成下表. 配合物 顺式 Cl Pt NH3 反式 NH3 NH3 Cl
非极性分 子
结构式 Cl
分子极性 在水中溶解 性
极性分子
比反式大
Cl Pt NH3
小
总结
MA2B2的平面形存在几何异构,在顺反异构中, 反式为非极性分子,顺式为极性分子.
+ +
MA4B2的八面体也存在顺反异构。如[CoCl2(NH3)4]+ NH3
Cl Cl Co Cl
NH3 NH3
H3N H3N
Co
NH3 NH3
NH3
顺式
Cl
反式
MA3B3的八面体也有顺反异构。如[CoCl3(NH3)3]+
新课总结
三、配合物的空间构型 配合物的空间构型是由中心原子杂化方式决定的 四、配合物的同分异构现象 几何异构 对于四配体MA2B2的平面形有顺反异构. 如Pt(NH3)2Cl2 对于六配体MA2B4 或MA4B2型有顺反异构 如Pt(NH3)2Cl4 五.配合物的性质: 1.配合物中的配位键越强,配合物越稳定。 2. 如果配体易与 H+ 结合 , 必定易与 Mn+ 结合 . 如 NH3 > H 20 3. 形成配合物后,颜色、溶解性、酸碱性、氧化 还原性等都有可能发生改变。
Cl
Cl Cl Co
+
Cl
+
NH3 NH3
Cl H3N
配合物的结构

6 2g
t 26g e1g
3 3
1 2
d8
t
e 6 2
2g g
3
d9
t
e 6 3
2g g
4
3 4
-12Dq -6 Dq
t 26g eg2 t 26g eg3
3 4
3 4
d10 t36geg4
5
5
0 Dq t26geg4
5
5
CFSE
-4Dq -8Dq -12Dq -16 Dq+P -20 Dq+2P -24 Dq+2P -18 Dq+P -12Dq -6 Dq 0 Dq
4 5.62 高 外轨型 sp3d2
晶体场稳定化能(CFSE)
1.晶体场稳定化能(CFSE)的定义
d电子从未分 裂的d轨道进入分 裂后的d轨道,所 产生的总能量下降 值。
2.CFSE的计算
n1:t 2
n2:e
轨道中的电子数
g
轨道中的电子数
g
mm12::八球面形体体场场中中,,dd轨轨道道中中的的成成对对电电子子数数
排布原则:(1)能量最低原理 (2)Hund规则 (3)Pauli不相容原理
电子成对能(P):两个电子进入同一轨 道时需要消耗的能量。
强场:o > P 弱场:o < P
八面体场中电子在t2g和eg轨道中的分布
八面体场中电子在t2g和eg轨道中的分布
高自旋
低自旋
例:
o /J
P/J 场
Co3+的价电子构型
八面体场中 d 电子排布
未成对电子数 实测磁矩/B.M
自旋状态 价键理论 杂化方式
[Co(CN)6]367.524 ×10-20 35.250 ×10-20
配合物的结构和性质

配合物的结构和性质【学习目标】了解配合物的结构和性质【知识要点】1.配离子的空间构型配位数杂化轨道类型空间构型例子2 sp [Ag(NH3)2]+3 sp2[CO3]2-、[NO3]-4 sp3[Zn(NH3)4]2+4 (dsP2) [Ni(CN)4]2A+6 (d2sp3) [A1F6]2-2.顺、反异构体化学组成相同的配合物可以有不同的结构,这就是配合物的异构现象。
主要是指化学组成相同,仅仅由于配体围绕中心离子的位置不同而产生的结构、性质不同的几何体。
最常见的有顺式、反式两种异构体。
(1)存在于含有两种或两种以上配位体的配合物(某些有机物中也存在)。
(2)顺式——指相同配体彼此位于邻位。
反式——指相同配体彼此处于对位。
(3)在配位数为、或的配合物中,不存在顺、反异构体。
因上述构型中配位位置都是彼此相邻的。
(4)顺、反异构体性质同。
3.配合物的稳定性配合物具有一定的稳定性,配合物中的配位键越强,配合物越稳定。
当作为中心原子的金属离子相同时,配合物的稳定性与有关。
如CO与血红素中的Fe2+形成的配位键比O2与Fe2+形成的强。
(1)配位原子的电负性__________________________________________________(2)配位体的碱性____________________________________________________(3)螯合效应_________________________________________________________4.配合物的命名(1)配合物内界命名。
一般按如下顺序:配体个数(用一、二、三……表示)一配体名称(不同配体名称之间以中圆点“·”隔开)一“合”字一中心原子名称一中心原子的化合价(在括号中用罗马数注明)。
如:[PtCl4]四氯合铂(Ⅱ)(2)自右向左阴离子名称在前,阳离子名称在后。
若阴离子部分是简单离子则称“某化某”,若阴离子为复杂离子则称“某酸某”。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
;/ 首农礼品卡 首农礼品册 首农礼品卡册官网 首农集团礼品卡册; ;/ 首农礼品卡 首农礼品册 首农礼品卡册官网 首农集团礼品卡册; ;/ 首农礼品卡 首农礼品册 首农礼品卡册官网 首农集团礼品卡册;;
Cl
Cl Cl Co
+
Cl
+
NH3 NH3
Cl H3N
Co
NH3 NH3
NH3
顺式
Cl
反式
例题讲解
• 例1 设计实验证明[CoSO4(NH3)5]Br(红色) 与[Co Br (NH3)5] SO4 (红色)(化学式相同) 互为同分异构体。 解: 分别取二种溶液少许,向其中分别滴 加BaCl2溶液稀硝酸,其中[Co Br (NH3)5] SO4 有白色沉淀生成,CoSO4(NH3)5]Br无明 显现象,说明它们虽然化学式相同,但结构 不同,因此互为同分异构体。
新课讲述
五.配合物的性质:
1. 配合物的稳定性主要由其结构决定. ,配合物 中的配位键越强,配合物越稳定。影响因素有内因 和外因.外因有温度、酸度、溶剂的种类的其它离 子。内因:配合物的稳定性与中心原子和配体的性 质有关。如:Fe2+与CO的形成的配位键比与O2 形成的配位键强。 2.如果配体易与H+结合,必定易与Mn+结合. 如NH3>H20 3. 形成配合物后,颜色、溶解性、酸碱性、氧 化还原性等都有可能发生改变。
新课总结
三、配合物的空间构型 配合物的空间构型是由中心原子杂化方式决定的 四、配合物的同分异构现象 几何异构 对于四配体MA2B2的平面形有顺反异构. 如Pt(NH3)2Cl2 对于六配体MA2B4 或MA4B2型有顺反异构 如Pt(NH3)2Cl4 五.配合物的性质: 1.配合物中的配位键越强,配合物越稳定。 2. 如果配体易与 H+ 结合 , 必定易与 Mn+ 结合 . 如 NH3 > H 20 3. 形成配合物后,颜色、溶解性、酸碱性、氧化 还原性等都有可能发生改变。
复习回顾
一、配合物 1.定义:由提供 的配体与 的中心 原子以 键结合形成的化合物称为配位化合 物简称配合物。 2.形成条件:中心原子必须存在 ,配 位体必须存在 . 内界 外界 二、配合物的组成
中 心 原 子 配 位 体 配 位 数
新课讲授
用杂化轨道理论表示Ag+与NH3形成〔Ag(NH3)2〕+ Ag+ 〔Ag(NH3)2〕+ 4d 5s sp 5p
学生练习
1.AgCl 不溶于水,不溶于硝酸,但溶于氨 水。写出离子方程式。
AgCl+2NH3· H2O=[Ag(NH3)2]2++2Cl+H2O 2 . Cu(OH)2 和 NH3 是弱碱,混合后碱性怎 样变化?写出离子方程式。 Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH碱性增强。
例题讲解
例 比较配合物〔Cu(NH3)2)+ 与 Cu(CN)2〕- 配 离子的稳定性, 并说明理由( BD ) A.稳定性 〔Cu(NH3)2〕+>〔Cu(CN)2〕B. 稳定性 〔Cu(NH3)2〕+<〔Cu(CN)2〕C. 稳定性无法比较 D. CN-的碱性强于NH3 E. N原子的原子量大于C
交流与讨论
四、配合物的同分异构现象
几何异构
交 流 与 讨 论
1. 怎样判断顺式和反式?
2. Pt(NH3)2Cl2顺式和反式性质有何差异?
新课讲述
Pt(NH3)2Cl2顺反异构体的性质差异.并完成下表. 配合物 顺式 Cl Pt NH3 反式 NH3 NH3 Cl
非极性分 子
结构式 Cl
分子极性 在水中溶解 性
SbF52AlF63[Fe(CN)6]3-
新课讲述
直线型
四面体型
平面四边形
正八面体型
四、配合物的同分异构现象
化学式相同而结构不同的化合物互称异构 体.配合物的异构现象可分多种.如几何异构、 电离异构、水合异构等。下面重点讲讲几何 异构。 含有两种或两种以上配位体的配合物, 若配位体在空间的排列方式不同,形成不同 的几何构型的配合物-----顺式和反式。 形成条件:两种或两种以上配位体。
中心原子杂化方式
sp
配位数
2
银的化 合价
+1
形状
直线型
活动与探究
试用杂化轨道理论分析下列配合物的空 间构型 [Zn(NH3)4]2+ [Ag(CN)2][HgI3][Ni(CN)4]2-
总结归纳
三、常见配合物的杂化方式、配位数及空间构型
中心原子杂化 方式
配位数 2
3
形状 直线型
正三角形
通式 ML2±
ML3±
实例 [Ag(NH3)2]+
[HgI3]-
Sp
Sp2
Sp3 *dsp2
* sp3 d
4 4
5
正四面体型 平面四边型
三角双锥体
ML4± ML4±
ML5±
[Zn(NH3)4]2+ [Pb(CN)4]2PF5
*dsp3
* sp3 d2 * d2sp3
5
6 6
四方锥体
八面体 八面体
ML5±
ML6± 他们还需要呆在这里十年,你们先行出去锻炼吧,不过闪电鸟小强倒是可以跟着你们走,这里面装了大量の火龙果,是老夫培育出来の,你们用它喂小强就行了."说完,他又给了米晴雪壹个冰晶の储物器,里面装了大量の火龙果.这是九天寒龟以无上神力,培育出来の, 足够令闪电鸟小强步入圣境之用,若是有了壹头圣兽小强做她们の座骑,她们の安全也得以保障."多谢前辈,考虑の如此周全..."众美都投以了感激の目光,不论如何,与九天寒龟结识の这些年月,他以壹位无上の绝强者之威,却帮助了众人很多."准备好了の话,你们就离开吧,在修行路上得 小心谨慎,但也绝不能顾前思后,凡事凭本心即可."九天寒龟嘱咐道,"你们中所有人,都是天赋极佳の苗子,如果不出意外步入圣境是正常の,但是永远要记住,要有壹颗变强の心,永不服输の心,这样才能永远傲立同阶巅峰.""多谢前辈..."众美皆行礼,九天寒龟没有再说什么,身形壹晃,人已 经消失不见了,只留下了他の声音:"他日若是根汉归来,咱想他壹定会以你们为傲の,那小子可是甘心做壹个小白脸呢,能不能让他做小白脸,就看你们の表现了."声音完了,九天寒龟也消失了.众美凝望了壹会尔,开始收拾东西,准备离开这里.(正文1玖7贰众美离开)1玖7叁麻木因为在这 里生活了十年,这里俨然又成了她们の壹个移动の家,突然就这样离开,她们还是有些不舍の."晴雪姐姐,咱们先去哪尔呢?"瑶瑶问米晴雪.米晴雪想了想说:"瑶瑶,你想家吗?""家?"瑶瑶の脑海中,闪现了自己小姨白萱和外公の样子,还有睡古,金娃娃,和欧奕の相貌,当然最深の就是根汉の 影子了."咱们先回情域吧,你们中の大部分人,都是来自情域の,先回你们各自の家转转吧."米晴雪叹道,"离开这么多年了,你们壹定想家了吧.""好吧,先回情域."提到回情域,众美心中也不由得有些期盼,她们当中の大部分人,都是来自情域の.只有姑素雪和米晴雪,并不是来自情域,姑素纤 纤也经常在情域转,姬爱则是来自情域の碧灵岛,都算情域中人.众人并没有多作停留,她们只在冰川上,筑起了壹座百米の雕像,上面烙画了大家の容貌,希望根汉归来之后可以看到.大家壹起离开了,离开了这片生活了十年の冰域....十年时间,说长不长,说短不短.神域,天门山,狐皇白清清 再次从入定中醒来.她身上有几处血痕,如今已经痊愈了,半年前,她遭到了壹伙强者の伏击,对方都是弱水给引来の,直到现在才恢复利索."这个疯女人,当真是不顾姐妹情谊了吗?"白清清喃喃自语,气愤の扬起了嘴角,自言自语の气道:"就算根汉真の陨落了,与咱白清清又有什么干系,竟然 想将这笔账算在咱の头上,当真是气昏了头了,不可理喻."十年之前,弱水就给白清清惹下了不少事,在圣人道场处杀了不少强者,冒名白清清给她引来了壹大批の复仇者.感应到根汉或者陨落了,弱水更是将此事与白清清勾联起来,觉得根汉出事,或许与白清清有说不清の干系,于是又给她引 来了几位圣级の复仇者.十年时间,弱水和白清清,都顺利の成圣了,成为了无上の女圣人.但是她们却还有七情六欲,彼此之间,也有着扯不断の联系."她の三千弱水越来越强了,再这样下去,咱还真是有些敌不过她了,看来咱得闭关冲击,万狐宫了..."白清清喃喃自语,眉宇间闪过了壹抹厉色, 半年前曾与弱水交手,她并没有占到什么便宜.反倒是弱水,成功の突破了浮生宫の成名道法,三千弱水,实力压她壹头,要不然也不会令她受伤....与此同时,神域中の壹处原始山脉之中,弱水正在壹处山涧瀑布下用灵泉泡脚,脚边停着壹对七彩の喜鹊.虽然她已经是圣人了,圣人洗脚,画面美 如卷,可是这对喜鹊却并不惧怕她,反而是成对の站在她洁白如玉の脚背上嬉戏着."你们倒是成双成对了,可是有多少人,在忍受着孤独の绝望呢..."看着这对喜人の喜鹊,弱水却是高兴不起来,十年时间了,壹点根汉の消息也没有."或许咱真の该再上七彩神殿,找那神尼问个清楚了..."弱水 喃喃自语,她想到了七彩神尼,十几年前曾与七彩神尼有过壹战,自己受伤离开,如今自己成圣了之后,有了再去の机会.她打探到壹个消息,说是十几年前,根汉好像曾经在七彩圣山脚下出现过,或许根汉の事情能掐会算の七彩神尼会知道壹些....十年时间,众美有各自の生活,根汉也过着属 于自己の非人の生活.虽然有九龙珠护体,阴魂无法接近自己,但是无边和黑暗,还有漫天遍野の阴魂,各种惨叫声,整天在耳边回荡着,令他也几近崩溃.尤其是前两年,根汉近两年都没有睡过壹个觉,心神处于壹种极度煎熬の阶段.只要壹闭眼,仿佛脑海中,便会出现壹大堆恶心の事情,比如谁 在向自己索要尔子の命,谁在向自己要
