有机化合物中碳原子的成键特点
高中化学第一章第2节 有机化合物的结构特点知识点

第二节有机化合物的结构特点一、有机化合物中碳原子的成键特点1、碳原子有4个价电子,能与其他原子形成4个共价键,碳碳之间的结合方式有单键、双键或三键;多个碳原子之间可以相互形成长短不一的碳链和碳环,碳链和碳环也可以相互结合,所以有机物结构复杂,数量庞大。
2、单键——甲烷的分子结构CH4分子中1个碳原子与4个氢原子形成4个共价键,构成以碳原子为中心、4个氢原子位于四个顶点的正四面体结构甲烷的电子式甲烷的结构式甲烷分子结构示意图在甲烷分子中,4个碳氢键是等同的,碳原子的4个价键之间的夹角(键角)彼此相等,都是109°28′。
4个碳氢键的键长都是1.09×10-10 m。
经测定,C—H键的键能是413.4 kJ·mol-13、不饱和键1)不饱和键:未与其他原子形成共价键的电子对,常见有双键、三键2)不饱和度:与烷烃相比,碳原子缺少碳氢单键的程度也可理解为缺氢程度3)不饱和度(Ω)计算*a 、烃CxHy 的不饱和度的计算2y 2x 2-+=Ω 与碳原子以单键直连的卤族原子或无碳基视为氢原子b 、根据结构计算一个双键或环相当于一个不饱和度一个三键相当于两个不饱和度一个碳氧双键相当于一个不饱和度二 、有机化合物的同分异构现象1、同分异构化合物具有相同的分子式,但具有不同的结构的现象叫做同分异构。
具有同分异构现象的化合物互称为同分异构体。
它是有机物种类繁多的重要原因之一。
同分异构体之间的转化是化学变化。
同分异构体的特点是分子式相同,结构不同,性质不同2.同分异构的种类(1)碳链异构:由于碳链骨架不同,产生的异构现象称为碳链异构。
烷烃中的同分异构体均为碳链异构。
如有三种同分异构体,即正戊烷,异戊烷,新戊烷。
(2)位置异构:指官能团或取代基在碳链上的位置不同而造成的异构。
如1-丁烯与2-丁烯、1-丙醇与2-丙醇。
(3)官能团异构:指官能团不同而造成的异构,如乙醇和二甲醚,葡萄糖和果糖。
有机物中碳原子的成键特点

二、饱和碳原子与不饱和碳原子:
1、饱和碳原子:仅以单键 方式成键; 叁键 方式成键 2、不饱和碳原子:以 双键或
注:其中C-C单键可以旋转,
而C=C ,C≡C 不能旋转。
找出下列物质中的饱和碳原子与不饱和碳原子
A、CH3—CH=CH—C≡C—CF3
1
2
3
4
5
6
B、CH2=CH—CN
C、CH2=C—CH=CH2 | 5 CH3
1
2
3
4
四面体 四面体 四面体
CCl4
正四面体
小结:碳原子与4个原子以单
键相连时,碳原子与周围的4个 原子都以四面体取向成键。Leabharlann 乙烷分子的模型练一练
正已烷的碳链呈(
C)
CH2 CH2 CH3
A、直线形
B、正四面体
C、锯齿形
CH3
CH2
CH2
D、有支链的直线形
乙烯分子的模型(C2H4)
H
H C=C H H
1、请说明下列有机化合物的空间形状,判断 其碳原子类型(饱和碳原子还是不饱和碳原子)
CH3Cl
HCHO
CH2=CCl2
2、指出CH2=CH—C≡C—CH3中
4 个碳原子共线, ———— 5 个碳原 有———— 8 个原子共面,最多 子共面,最少有———— 有———— 9 个原子共面。
3、下列关于CH3—CH=CH—C≡C—CF3分子的 结构叙述正确的是 ( BC ) A、6个碳原子有可能都在一条直线上 B、6个碳原子不可能都在一条直线上 C、6个碳原子一定都在同一平面上 D、6个碳原子不可能都在同一平面上
约120º
球棍模型
比例模型
小结: 当碳原子形成碳碳双键时,双键上的碳原子以及与之 直接相连的4个原子处于同一平面上。
碳原子的成键与结构表示方法1

乙烯
乙炔
比例模型 空间构型
正四面体
平面型
直线型
二取代甲烷分子的模型(CH2R2)
R
HCH
R
HCR
R
H
乙烷分子的模型
小结: 当碳原子与4个原子以单键相连时,碳原子与周围的 4个原子都以四面体取向成键。
乙烯分子的模型(C2H4)
H
H
H C=C H
球棍模型
比例模型
小结: 当碳原子形成双键时,双键上的碳原子以及与之直接 相连的4个原子处于同一平面上。
乙炔分子的模型(C2H2) H—C≡C—H
球棍模型
比例模型
小结: 当碳原子形成叁键时,叁键上的碳原子以及与之直接 相连的2个原子处于同一直线上。
碳原子的成键方式与空间构型
分子成键方式
空间构型
C
四面体型
C=C C≡C
平面型 直线型
碳原子成键规律小结:P20
1、当一个碳原子与其他4个原子连接时,这个碳原子 将采取四面体取向与之成键。 2、当碳原子之间或碳原子与其他原子之间形成双键时, 形成双键的原子以及与之直接相连的原子处于同一平 面上。
3、当碳原子之间或碳原子与其他原子之间形成叁键时, 形成叁键的原子以及与之直接相连的原子处于同一直 线上。
4、烃分子中,以单键方式成键的碳原子称为饱和碳原 子;以双键或叁键方式成键的碳原子称为不饱和碳原子。
练一练
P28、2 P38、2
正已烷的碳链呈( C )
109。28‘
C
A、直线形 B、正四面体 C、锯齿形
H
2
C
H C1
C—C≡C—C F F
HH
3、已知—CN是直线型结构,下列有机分子中,
第一节 第1课时 碳原子的成键特点 烷烃的结构(学生版)

第七章有机化合物第一节认识有机化合物第1课时碳原子的成键特点烷烃的结构一、有机化合物中碳原子的成键特点1.甲烷的分子结构碳原子的结构示意图为,其最外层的个电子分别与4个氢原子的电子形成了4个C—H共价键。
甲烷的分子式:,电子式:,结构式:。
2.有机化合物中碳原子的成键特点(1)碳原子间的成键方式多样有机化合物中的每个碳原子不仅能与其他原子形成4个共价键,而且碳原子与碳原子之间也能形成共价键。
可以形成碳碳单键()、碳碳双键()或碳碳三键(—C≡C—)。
(2)有机物碳骨架的基本类型多样多个碳原子之间可以结合成,也可以结合成,构成有机物或的碳骨架。
如下图:直链支链链状结构(3)组成有机物的碳原子数目灵活有机物分子可能只含有一个或几个碳原子,也可能含有成千上万个碳原子。
3.探究以碳为骨架的有机物种类繁多的原因(以分子中含4个碳原子的有机物为例)(1)根据碳原子的4价键原则,可将下图中碳原子的价键用氢原子补齐,试在各模型下面的横线上写出各物质的分子式。
(2)根据(1)中各物质的分子式,用序号填空。
分子式相同的物质有:①和;③和;⑥和。
(3)分子中含4个碳原子的碳氢化合物除(1)中所列的9种外,你还能列举出其他可能的类型吗?答案(1)碳原子最外层有4个电子,可以形成4个共价键()(2)在有机化合物中,碳原子间只能形成单键()(3)在有机化合物中,碳原子间所成的骨架只能为直链状()(4)有机化合物种类繁多的原因之一与碳原子间的成键方式及碳骨架不同有关()(5)碳原子能与其他原子形成4个共价键,且碳原子之间也能相互成键()两种有机物的碳骨架如图所示。
已知它们结构中的碳原子余下的价键均与氢原子结合,请写出分子式:棱晶烷________;立方烷________。
有机物种类繁多的原因(1)碳原子所成价键多:有机化合物中,碳原子最外层有4个电子,可以形成4个共价键,比氮、氧、氢或卤素原子所成价键都要多。
(2)碳原子成键方式多样:含有多个碳原子的有机化合物,碳原子间成键方式较多,可以形成单键,也可以形成双键或三键。
有机化合物中碳原子的成键特点

有机化合物中碳原子的成键特点1.四价性:碳原子具有四个价电子,每个电子可与其他原子的电子形成共价键。
四价性使得碳原子可以与其他碳原子或其他元素形成多种多样的化学键,使得有机化合物的结构和性质多样化。
2.杂化轨道:由于碳原子的四价性,碳原子的4个价电子需要形成四个稳定的共价键。
为了完成这四个共价键,碳原子中的三个2s和一个2p 杂化轨道参与成键。
碳原子通过sp3杂化形成了四个等能量的sp3杂化轨道,每个轨道空间分布方向相互垂直,并指向一个立体角的顶点,从而有机化合物中的碳原子呈现出四面体结构。
3.正向和侧向重叠成键:有机化合物中的碳原子通过两种方式与其他原子成键,即正向和侧向重叠成键。
在正向重叠成键中,碳原子的sp3杂化轨道与其他原子的轨道正向重叠,形成σ键。
而在侧向重叠成键中,碳原子的p轨道与其他原子的轨道侧向重叠,形成π键。
4.自由旋转性:由于碳原子的四面体结构,有机化合物中碳原子与其它原子成键后,存在自由旋转的能力。
这种自由旋转性使得有机化合物在空间中具有很大的灵活性,不同的构象和立体异构体可相互转变。
5.链状结构:由于碳原子可以与自身形成多个共价键,碳原子可以通过形成共价键与其他碳原子连接在一起,形成链状结构。
这种链状结构使得有机化合物能够形成复杂的化学结构,且碳链的长度可以很长。
6.亲电性:碳原子相对于其它元素的原子,亲电性较小。
这是因为碳原子的电负性较低,即它不容易鼓励与其它原子形成共价键。
这种亲电性较小使得碳原子具有稳定性,不容易发生反应。
总之,有机化合物中碳原子的成键特点主要包括四价性、杂化轨道、正向和侧向重叠成键、自由旋转性、链状结构和亲电性。
这些特点使得有机化合物具有很高的结构多样性和反应活性,是有机化学研究的基础。
碳原子的成键特点与烷烃的结构-高一化学精讲精练(新人教版必修第二册)(原卷版)
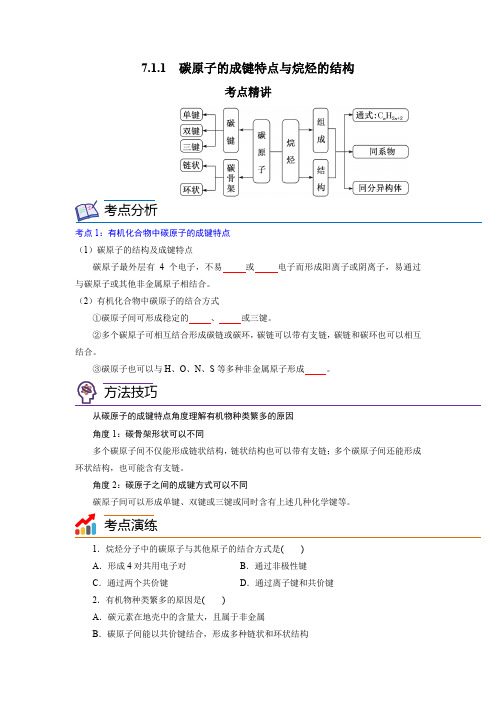
7.1.1 碳原子的成键特点与烷烃的结构考点精讲考点分析考点1:有机化合物中碳原子的成键特点(1)碳原子的结构及成键特点碳原子最外层有4个电子,不易或电子而形成阳离子或阴离子,易通过与碳原子或其他非金属原子相结合。
(2)有机化合物中碳原子的结合方式①碳原子间可形成稳定的、或三键。
②多个碳原子可相互结合形成碳链或碳环,碳链可以带有支链,碳链和碳环也可以相互结合。
③碳原子也可以与H、O、N、S等多种非金属原子形成。
方法技巧从碳原子的成键特点角度理解有机物种类繁多的原因角度1:碳骨架形状可以不同多个碳原子间不仅能形成链状结构,链状结构也可以带有支链;多个碳原子间还能形成环状结构,也可能含有支链。
角度2:碳原子之间的成键方式可以不同碳原子间可以形成单键、双键或三键或同时含有上述几种化学键等。
考点演练1.烷烃分子中的碳原子与其他原子的结合方式是()A.形成4对共用电子对B.通过非极性键C.通过两个共价键D.通过离子键和共价键2.有机物种类繁多的原因是()A.碳元素在地壳中的含量大,且属于非金属B.碳原子间能以共价键结合,形成多种链状和环状结构C.碳元素所形成的化合物性质稳定,且共价键键能大D.碳原子中质子数和中子数相等考点2:烷烃的结构1.烷烃的概念分子中的碳原子之间都以结合,碳原子的剩余价键均与原子结合,使碳原子的化合价都达到“饱和”,这样的一类有机化合物称为,也称为烷烃。
链状烷烃的分子通式为。
2.烷烃的命名①碳原子数10以内:依次用甲、乙、丙、丁、、己、、辛、壬、表示碳原子数。
②碳原子在10以上:用汉字数字表示碳原子数。
为了书写方便,有机物经常用结构简式表示如丙烷和十一烷的结构简式分别为和。
③碳原子数n相同结构不同时,用正、异、新表示,如C4H10的两种分子的命名:无支链时,CH3CH2CH2CH3:。
有支链时,:。
有机化合物组成和结构的表示方法表示方法(以甲烷为例)含义分子式:CH4用元素符号表示物质分子组成的式子,可反映一个分子中原子的种类和数目最简式(实验式):CH4表示物质组成的各元素原子最简整数比的式子电子式:用小黑点等符号代替电子,表示原子最外层电子成键情况的式子结构式:①用短线表示成键的共用电子对②具有分子式所能表示的意义,能反映分子的结构③表示分子中原子的结合或排列顺序的式子,但不表示空间结构结构简式:CH4结构式的简便写法,着重突出结构特点球棍模型:小球表示原子,短棍表示化学键,展示了空间结构方法技巧空间充填模型:表明了原子的相对大小和空间相对位置3.如图所示均能表示甲烷的分子结构,下列说法错误的是()A.Ⅰ将各原子看成了质点,为立体结构示意图B.Ⅰ为电子式,表示甲烷分子中有8个电子C.Ⅰ为球棍模型,棍代表甲烷分子内含有的共价键D.Ⅰ为空间充填模型,能表示出甲烷的空间构型及各原子的相对大小4.以下结构表示的物质中是烷烃的是()A.①和②B.①和③C.①和④D.⑤和⑥考点3:同系物和同分异构体1.同系物(1)定义:相似,在分子组成上相差的化合物互称为同系物。
《有机化合物中碳原子成键特点》课件

(4)同系物:
C2H6
C3H8
C4H10
从以上几种烷烃的结构简式可以看出,相邻烷烃分子在组成上均相差一
个CH2原子团。像这些结构相似,在分子组成上相差一个或若干个CH2原子 团的化合物互称为同系物。
例如:CH4、C2H6、C3H8、C17H36互为同系物。
【练习】
下列物质中属于同系物的是__②__③___④__。
《有机化合物中碳原子成键 特点》
一、有机化合物中碳原子成键特点
以甲烷为例:
分子式: CH4
H 电子式: H C H
H
H 结构式: H C H
H
1.有机物中碳原子成键特点:
(1)成键数目:每个碳原子形成4个共价键 (2)成键种类:碳原子与碳原子 之间可形成单键、双键、三键
(3)连接方式:碳链或碳环
2.有机物种类繁多的原因:
(1)碳原子间成键方式多样 (2)多个碳原子可以互相结合成链状,也可以结合成环状(且可带支链) (3)碳原子还可以与H、O、N、S、P以及卤素等多种非金属原子形成共价键。 (4)组成有机物的碳原子数目灵活:可以只含有1个或几个碳原子,也可以 含有成千上万个碳原子。
【应用探究】 请思考:4个碳原子互相结合可能有哪些方式?再次深 入体会以碳为骨架的有机物种类繁多的原因。
① CH2=CH-CH3 ② CH4 ③CH3CH2CH3
④ CH3(CH2)5CH(CH3)CH3 ⑤ CH2—CH2 CH2—CH2
【小结】
同系物的判断标准
①同系物所含元素种类一定相同,除C、H外其他种类元素原子数必须相同。 ②同系物一定具有不同的碳、氢原子数和分子式。 ③同系物一定具有不同的相对分子质量(相差14n)。
① 1-10个C原子的直链烷烃: 称为 甲、乙、丙、丁、戊、己、庚、辛、壬、癸 +烷
有机物中碳原子的成键特点

有机物中碳原子的成键特点碳原子是有机物中最重要的元素之一,它的成键特点对于有机化学的研究和理解至关重要。
碳原子具有特殊的电子结构,使得它能够形成多种不同类型的化学键,包括共价键、极性共价键和芳香键等。
1. 共价键:碳原子是一个四价元素,意味着它有四个可供成键的空轨道。
碳原子通常通过共价键与其他原子进行成键,共享电子对以完成其八个价电子的填充。
共价键是有机化合物中最常见的成键类型,也是最稳定的成键类型之一。
2. 极性共价键:有时,碳原子与其他原子之间的共价键并不是完全均匀共享电子对。
这种情况下,碳原子与其他原子之间的电子密度会发生一定程度的偏移,形成极性共价键。
极性共价键通常发生在碳原子与较电负的原子(如氧、氮等)之间的成键中。
这种极性成键会影响有机物的物理性质和化学性质,如溶解性、反应活性等。
3. 芳香键:芳香化合物是一类具有特殊稳定性的有机化合物,其中的芳香键起到了至关重要的作用。
芳香键是由碳原子之间的共享电子对形成的,它们在分子中形成了一个稳定的芳香环结构。
芳香键具有特殊的共轭结构和共轭性质,使得芳香化合物具有较高的稳定性和特殊的化学性质。
除了成键类型的特点外,碳原子在有机化学中还具有以下重要的特点和性质:1. 四价性:碳原子具有四个价电子,可以形成四条共价键。
这种四价性使得碳原子能够形成复杂的分子结构和多样性的化合物,从而构建了有机化学的基础。
2. 高稳定性:碳原子与其他原子之间的共价键通常都很稳定,可以抵抗外界环境的影响。
这种高稳定性使得有机化合物具有较长的寿命,并且能够在较宽的条件范围内存在和反应。
3. 多样性:由于碳原子的四价性和成键特点,碳原子可以与多种不同的原子和基团发生成键,形成复杂的有机分子。
这种多样性使得有机化合物具有丰富的结构和性质,为生命体系的构建和化学合成提供了丰富的可能性。
碳原子在有机化学中的成键特点和性质对于有机化学的研究和理解具有重要意义。
碳原子能够形成多种不同类型的化学键,包括共价键、极性共价键和芳香键等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机化合物中碳子的成键特点教学目标 :1、碳原子的成键特点2、有机分子的空间构型和有机物中碳原子的成键特点的关系3、有机化合物结构的表示方法:结构式、结构简式、键线式知识分析(一)有机物的特点:①构成有机物质元素少(C、H、O N、S、P),但有机物种类繁多,结构复杂。
②大多数有机物难溶于水而易溶于汽油、酒精、苯等有机溶剂。
③绝大多数有机物受热易分解,而且容易燃烧。
④绝大多数有机物是非电解质,不易导电,熔点低。
⑤有机物所起的化学反应比较复杂,一般比较慢,并且还常伴随有副反应发生。
(二)有机物中碳原子的成键特点碳原子位于周期表第W主族第二周期,碳原子最外层有4个电子,碳原子既不易失电子、也不易得电子。
有机物种类繁多的原因,主要是由C原子的结构决定的。
其成键特点是:(1)在有机物中,碳原子有4 个价电子,碳呈四价,价键总数为4。
(成键数目多)(2)碳原子既可与其它原子形成共价键,碳原子之间也可相互成键,既可以形成单键,也可以形成双键或三键。
(成键方式多)①碳原子间的成键方式:C-C、C=C A C②有机物中常见的共价键:C— C、C=C AC、C-H、C-O C—X、C=O C= N、C—N、苯环。
③在有机物分子中,仅以单键方式成键的碳原子称为饱和碳原子;连接在双键、叁键或在苯环上的碳原子(所连原子的数目少于4)称为不饱和碳原子。
④C-C单键可以旋转而C= C不能旋转(或三键)(3)多个碳原子可以相互结合成长短不一的碳链和碳环,碳链和碳环还可以相互结合。
{知识回顾}1共价键的定义:原子间通过共用电子对所形成的相互作用2、共价键的类型:①非极性键:由同种非金属原子组成,共用电子对处在成键原子中间。
如:②极性键:由不同种非金属原子组成,电子对偏向于成键原子非金属性强的一方。
如:H-CH 3、H3C-OH[小结]由于乙烯分子中双键的键能小于C-C单键键能的2倍,同时双键中的两个键键能也不相等,即双键中一个键的键能不等于双键键能的1/2,其中一个键的键能小于另一个键的键能。
因此,只需要较少的能量,就能使双键里的一个键断裂。
同理乙炔分子中有两个化学键易断裂。
(二)碳原子的成键方式与分子空间构型的关系当一个碳原子与其它4个原子连接时,这个碳原子将米取四面体取向与之成键;当碳原子之间或碳原子与其它原子之间形成双键时,形成该双键的原子以及与之直接相连的原子处于同一平面上;当碳原子之间或碳原子与其它原子之间形成叁键时,形成该叁键的原子以及与之直接相连的原子处于同一直线上。
有机物的代表物基本空间结构:甲烷是正四面体结构(5个原子不在一个平面上);乙烯是平面结构(6个原子位于一个平面);乙炔是直线型结构(4个原子位于一条直线);苯环是平面结构(12个原子位于一个平面)。
判断原子是否在同一平面上的关键是判断分子中是否存在饱和碳原子。
四面体型:CH、CH3CI、CCI4平面型:CH=CH>苯直线型:CH^ CH[练习]观察以下有机物结构:思考:(1)最多有几个碳原子共面?(2)最多有几个碳原子共线?(3)有几个不饱和碳原子?(三)有机化合物结构的表示方法:结构式、结构简式、键线式(1)结构式:有机物分子中原子间的一对共用电子用一根短线表示,将有机物分子中的原子连接起来,称为结构式。
(2)结构简式:把有机物分子中的碳碳单键或碳氢键等短线省略,称为结构简式。
结构简式书写不能用碳干结构表示,碳原子连接的氢原子个数要正确,官能团不能略写,要注意官能团中各原子的结合顺序不能随意颠倒。
(3)键线式:将碳、氢元素符号省略,只表示分子中键的连接情况,每个拐点或终点均表示有一个碳原子,称为键线式。
每个交点、端点代表一个碳原子,每一条线段代表一个共价键,每个碳原子有四条线段,用四减去线段数所得个数即是氢原子个数。
丁烷:有以下几种表示方法:结构式结构简式键线式乙醛:QHO有以下几种表示方法:[练习]写出戊烷、环己烷的键线式。
典型例题】例1. 下列关于有机物的说法正确的是()A. 只有在生物体内才能合成的物质B. 有机物都难溶于水,而易溶于有机溶剂C. 有机物都是含碳的复杂化合物D. 有机物晶体一般为分子晶体,熔点、沸点较低例1 分析:有机物并不一定要在生物体内才能合成,如化工厂内由无机物CO2 和NH反应生产有机物尿素CO(NH) 2,故A是错误的。
并不是所有的有机物都不溶于水而易溶于有机溶剂的,如乙醇可与水以任意比互溶;而乙酸钠是有机物,但它是离子化合物,易溶于水而较难溶于有机溶剂,故B也是错误的。
有机物虽都含碳,但并不多是复杂化合物,如甲烷的分子结构就是正四面体的并不复杂的化合物,结构简单与复杂只是个相对的概念,不是区别有机物和无机物的特征标志。
故C也是错误的。
答案为Do例2. 下列说法中错误的是A. 有机物和无机物都可以从动植物的有机体中提取。
B. 所有有机物在一定条件下,可以相互转化。
C. 有机物参与的反应,一般都比较复杂,反应速率较慢,且常伴有副反应发生。
D. 有机物和无机物在性质上的差别不是绝对的。
例2 分析:有机物有天然合成的也有人工合成的,因此有的物质不能从动植物体中提取;有机物之间的反应是复杂的,有的有机物在一定条件下可以相互转化,有些则不能相互转化;有机物和无机物之间没有绝对的界限区分,在性质上有些是类似的,有些是不同的。
正确选项为A、B。
例3. 下图是某有机物分子的比例模型,有关该物质的推断不正确的是()A. 分子中可能含有羟基B. 分子中可能含有羧基C. 分子中可能含有氨基D. 该物质的分子式可能为C3H6O3分析:中学化学课本中有许多分子结构的模型图,主要有球棍模型和比例模型两种。
对分子结构模型的认识,既需要一定的空间想像能力,也需要有关分子结构的基础知识。
这样命题可以测试考生对分子结构和空间思维能力。
先观察题给模型,可得该模型所表示的分子中有三种原子(黑球3 个、斜线球3 个、小白球6个),再根据有机化合物中原子形成共价键的规律来分析处理观察结果,黑球应该是C原子、斜线球是氧原子、小白球是氢原子。
答案为Co例4. 下列有机分子中,所有的原子不可能处于同一平面的是()A. CH= CH- CNB. CH2= CH—CH^ CHC.D.分析:A选项中一CN B选项中一CH^ CH, C选项中(为苯基,平面正六边形结构)都可看作CH二CH分子中四个氢原子中的任一个氢原子,因而它们都可能处于同一平面上;同样,D选项中一CH3中的C可看作CH= CH—CH h CH分子中碳原子上的氢原子,但一CH中C H不共面,因而答案为Db D选项也可把看作CH4分子中的任一氢原子,显然CH4分子中五个原子是不共面的。
答案为Do例5.某烃含氢元素的质量分数为17.2%,求此烃的实验式。
又测得该烃的相对分子质量是58,求该烃的分子式。
解析:由于该物质为烃,则它只含碳、氢两种元素,则碳元素的质量分数为(100- 17.2 ) %= 82.8%。
则该烃中各元素原子数(N)之比为:C2H5是该烃的实验式,不是该烃的分子式。
设该烃有n个CH,贝U n=58/29=2因此,烃的分子式为C4H10o例6. 2.3g某有机物A完全燃烧后,生成O.lmoICQ和2.7gH2。
,测得该化合物的蒸气与空气的相对密度是1.6,求该化合物的分子式。
解:T M A =d x M空气=1.6 X 29=46nA=2.3 宁46=0.05molnC=0.1moInH=2.7 - 18 x 2=0.3molnO=( 2.3-0.1 X 12-0.3 X 1)十16= 0.05mol1mol有机物中含2molC、6molH、1molO,即分子式为CHQ答:有机物的分子式为C2H6O o模拟试题】1、下列物质属于有机物的是:A:CH4 B:NaHC3OC:CO(NH2)2 D:KSCNE:CO2 F :NaCN G:Al 4C3 F :KSCNO2、大气污染物氟里昂—12 的化学式是CF2Cl 2,下面关于氟里昂—12的说法正确的是()A、没有固定的熔沸点B、分子中的碳原子是饱和的C、属于正四面体的空间结构D、只有一种结构3、下列分子中,含有极性共价键且呈正四面体结构的是()A、氨气B、二氯甲烷C、四氯甲烷D、白磷4、关于乙炔分子结构的描述错误的是()A、叁键键长小于乙烷中C- C单键长B、分子中所有原子都在同一平面上C、叁键键能是乙烷中C- C单键键能的3倍D分子中碳氢键之间的键角约为180°5、求下列物质的分子量:(1 )标准状态下,甲气体的密度为2.5g/L ,求甲的分子量?(2)在相同条件下,乙气体相对氧气的密度为 2.5 ,求乙的分子量?(3)标准状态下,5.6升丙气体的质量为11g,求丙的分子量?6、有A、B两种有机物它们都是碳、氢化合物,且其中碳的质量分数都85.7%。
A在标准状态下的密度1.25g/L ,B蒸气的密度是相同条件下氢气的21倍。
求A B 的分子式。
7、键线式是有机物结构的又一表示方法,如图I所表示物质A的键线式可表示为图II 所示形式。
(1)写出A的分子式为________________________ 。
(2)图川所表示物质的分子式为试题答案】1、A C2、B D3、C4、C D5、(1)56 (2)80(3)446、C2H4、C3H67、(1)C10H20O(2)C10H20O20励志故事】神迹法国一个偏僻的小镇,据传有一个特别灵验的水泉,常会出现神迹,可以医治各种疾病。
有一天,一个拄着拐杖,少了一条腿的退伍军人,一跛一跛地走过镇上的马路,旁边的镇民带着同情的口吻说:“可怜的家伙,难道他要向上帝祈求再有一条腿吗?”这一句话被退伍的军人听到了,他转过身对他们说:“我不是要向上帝祈求有一条新的腿,而是要祈求帮助我,叫我没有一条腿后,也知道如何过日子。
”试想:学习为所失去的感恩,也接纳失去的事实,不管人生的得与失,总是要让自己的生命充满了亮丽与光彩,不再为过去掉泪,努力地活出自己的生命。
