九年级化学上册第二章 2.3构成物质的微粒Ⅱ__原子和离子第3课时相对原子质量离子作业课件新版粤教版
《构成物质的微粒(Ⅱ)-原子和离子》精品复习课件

注意:原子在化学变化中是否可分? 原子是化学变化中最小粒子,不能再分,但原子本身 还有更复杂的结构,通过其他方法可以再分。在化学 变化中,原子的种类、质量、数量等都不发生变化。
知识回顾
3.原子的性质 (1)质量、体积都很_小___。 (2)在不停地运动且与温度有关;温度越高,运动 速率越_快___。 (3)原子间存在间隔。同一物质气态时原子间间隔 最__大__,固态时原子间间隔最_小___。 物体的热胀冷缩 现象就是原子间的间隔受热时_增__大___,遇冷时__变__小__ 的缘故。
例题解析
►类型二 原子结构中各粒子间的关系 命题角度:考查学生对原子结构的掌握情况。
例2 据报道上海某医院正在研究用放射性碘治疗肿瘤。 这种碘原子的核电荷数为53,相对原子质量为125。下 列关于这种原子的说法中,错误的是( B )
A.中子数为72
B.质子数为72
C.电子数为53
D.质子数和中子数之和为125
知识回顾
8.原子种类与原Байду номын сангаас结构的关系
原子分类
稀有气 体原子
最外层电 子数
原子结构 变化趋势 化学性质
(稳定或不 稳定)
(得失电子)
(稳定或 活泼)
8个(氦 为2个)
相对稳 定结构
不得不失
稳定
金属原子
一般小 于4个
不稳定结构
易失电子
活泼
非金属原子
一般大 于4个
不稳定结构
易得电子
活泼
知识回顾
知识点2 离子
1.定义:__带__电____的原子叫做离子。
2.分类: 离子
阳离子 阴离子
带正电的原子,如Na+ 带负电的原子,如Cl-
科粤版化学-九年级上册-《构成物质的微粒(Ⅱ)-原子和离子》

课堂 小结
❖化学变化中的最小微
粒
❖原子
❖质 子
❖原 ❖原子的结
核
❖中
子
构
❖核外电 子
原 子 和
❖相对原子质
子
量
离 子
❖原子得失电子形成离 ❖离 ❖带电的原子子或原子
子
团❖阳离
❖分 类
❖阴子离
子
Thyoaunk
End
一个氢原子的质量只有1.674×10-27kg,
即
1.674
kg
1 000 000 000 000 000 000 000 000 000
H
如此小的值,
该如何计算
相对原子质量(Ar) =
原子的实际质量 碳原子质量的1/12
新知 学习
C
碳原子
碳原子质量的1/12
氧原子的相对原子质量= O ÷ ≈16
❖原子的构 成
新知 学习
点 击 图 片 播 放 动 画
新知 学习
物理学家玻尔
+++ ++++ +++
电子壳层模型
新知 学习
表示原子核以及 核内的质子数
+8 ❖2❖6
表示电子层 以及电子层 上的电子数
❖氧原子的结构示意 图
最外层电子数不超过8个(只有一层的,电子不超过2个)
新知 学习 非金属原子 稀有气体原子
原子是构成物质世界的最小微粒吗?
新知 学习
英国科学家汤姆森
-
-
--
-
电子
汤姆森原子模型
新知 学习
α粒子束发生偏转
α
粒 子
+
粤教版化学-九年级上册-《2.3 构成物质的微粒(Ⅱ)——原子和离子》参考课件

稀有气 体元素
非金属 元素
金属元 素
1-18号元素的原子结构示意图
氢(H) 氢(H)
氦(He) 氦(He)
锂(Li) 铍(Be) 硼(B) 碳(C) 氮(N) 氧(O) 氟(F) 氖(Ne )
钠(Na) 镁(Mg) 铝(Al) 硅(Si) 磷(P) 硫(S)
稀有气 体元素
最外层 是否达到相 电子数 对稳定结构
-
-
--
-
-
钠原子
-- - +11 - -
--
氯原子
-
---
-
- +17
-
-
--
-- -
-
-
钠原子
---
-
+11
-
-
--
氯原子
-
-- -
-
+17
-
--
-
-
-
--
--
钠离子
--
-
--
+11
--
-
--
+11 2 8 Na+
氯离子
我
-
-
-
--
--
-
-
+17
, !
谢 谢
也 稳 定
了
-
---
-
-
-
-
+17 2 8 8
(填“得到”或“失去”)一个电子, 所形成的离子符号为__C_l_-__。
Cl
(3)钠原子和氯原子相同的是___③___(填序号)。
①质子数 ②电子数 ③电子层数 ④最外层电子数。
达标测试
下图形象地表示了氯化钠的形 成过程.下列相关叙述中不正
2.3_构成物质的微粒(原子)

质量/kg
相对质量
质子
1.6726×10-27
1 1
1 1840
中子
1.6748×10-27
电子
9.1176×10-31
2、相对原子质量= 质子数+中子数
练习: 1、已知P的相对原子质量为31, 求中子数 2、硫的质子数为16,中子数16, 求硫的相对原子质量
相对原子质量
碳原子的质量的1/12约 1.66×10-27千克
得失电子
化学性质 (活泼与 否)
8
2
(He为
不易得失、 结构 稳定 ) 相对稳定
稳定
一般 一般
< >
4个 4个
不稳定结构 易 失去 电子 不稳定 不稳定 得到 电子 不稳定 结构 易
所 以 , 最外层电子数 决定了元素的化学性质 。
练习 指出下列哪几种元素的化学性质相似 B和D, C和E
A
B
C
D
E
原子的特性:(与 分子一样)
1、原子是在不断地运动。 2、原子间存在间隙。 3、原子的质量和体积很小。 4、同种原子性质相同,不同种原子性质 不同。
5、原子在化学变化中不能再分。
分子、原子的区别与联系
分子
相同 点
原子
质量、体积小;彼此间存在间隙;不断运动; 同种分子(原子)性质相同,反之。
3.根据下列的图形给物质分类(混合物、 纯净物)
纯净物
纯净物
混合物
纯净物
离子的形成
原子核的半径约为原子半径的十 万分之一,电子在核外作高速运动。
电子在核外是怎么作高速运动的? 电子多了会不会出现“撞车”现象? 会不会被原子核吸掉?会不会飞到原 子的外面来?
《构成物质的微粒(Ⅱ)——原子和离子》知识总结

2.3构成物质的微粒(Ⅱ)——原子和离子一、原子:1、原子是构成物质的另一种微粒。
原子构成分子,原子也可直接构成物质,如金属汞、稀有气体等。
2、在化学变化中,分子本身发生变化,而原子本身没有变化,只是重新组合成新的分子,构成新的物质,所以,原子是化学变化中的最小粒子。
(注意:原子不是构成物质的最小粒子。
)※、分子与原子的比较化学反应的实质:在化学反应中分子分裂为原子,原子重新组合成新的分子。
二、原子的构成原子的的构成:原子由核外带负电的电子和带正电的原子核构成,原子核由带正电的质子和不带电的中子构成。
在不显电性的粒子里:核电荷数=质子数=核外电子数注意:原子不是构成物质的最小粒子。
原子只是化学变化中的最小粒子;普通氢原子核中只有质子无中子,氢原子的原子核就是一个质子。
(1)原子结构示意图的认识核外电子排布的规律:核外电子按能量由低到高从里往外排,第一层最多容纳2个电子,第二、三层最多容纳8个电子。
按顺序背诵:质子数从1~18的元素符号和名称: 氢氦锂铍硼 碳氮氧氟氖 钠镁铝硅 磷硫氯氩 (1)在原子中核电荷数=质子数=核外电子数 (2)原子的质量主要集中原子核 上决定元素种类 质子数(核电荷数) (3)三决定 决定元素化学性质 最外层电子数 决定原子的质量 原子核(4)相对原子质量≈质子数+中子数说明:最外层电子数相同其化学性质不一定都相同(Mg ,He 最外层电子数为2) 最外层电子数不同其化学性质有可能相似(He ,Ne 均为稳定结构) 稳定结构:最外层电子数是8(只有一层的为2)的结构。
元素的化学性质跟原子的最外层电子数关系最密切,原子的最外层电子数决定元素的化学性质:最外层电子数小于4时,易失去最外层所有电子,成为阳离子;(通常是金属元素)最外层电子数多于4时,易得到电子使最外层电子数变为8,成为阴离子(通常是非金属元素)最外层电子数与化合价的关系:(元素的最高正价等于原子的最外层电子数) 最外层电子数小于4时,最外层电子数就是元素的化合价(正价); 最外层电子数多于4时,最外层电子数-8=元素的化合价三、相对原子质量:以一种碳原子(碳-12)质量的1/12作为标准,其他原子的质量跟它相比较所得的数值,是该种原子的相对原子质量。
3.1 构成物质的基本微粒 背记知识点-2020秋沪教版(全国)九年级化学上册

知识像烛光,能照亮一个人,也能照亮无数的人。--培根 子是由两个氢原子和一个氧原子构成的,一个氧分子是由两个氧原子构成的。
4/8
知识像烛光,能照亮一个人,也能照亮无数的人。--培根
第 3 课时 原子结构 相对原子质量 一、原子的构成 1.α 粒子轰击金箔实验(图示)
(1)卢瑟福的 α 粒子轰击金箔实验推翻了汤姆生在 1903 年提出的原子结构模型, 为建立现代原子理论打下了基础。
3.微粒之间有间隔 实验一:水与酒精的混合实验(提示:水中含有红墨水)
现象:酒精与水混合后体积小于二者体积之和。
1/8
知识像烛光,能照亮一个人,也能照亮无数的人。--培根 结论:实验证明微粒之间有间隔。 实验二:水和空气的压缩实验
(1)水和空气都可以被压缩,因为构成物质的微粒之间有间隔。 (2)比较是一种很好的实验探究方法,通过上图对比发现,空气要比水更易被压
第 2 课时 分子 原子 一、分子 1.分子的基本性质 (1)分子的质量和体积均很小、分子在不停地运动、分子之间有间隔。 (2)同种物质的分子化学性质相同,不同种物质的分子化学性质不同。如:氧气
和液氧均能支持燃烧是因为二者均是由氧分子构成的。 (3)由分子构成的物质,分子是保持该物质化学性质的最小微粒。 (4)分子由原子构成,分子可以分成原子。 2.用分子的观点解释物质的变化及分类 (1)区别物理变化和化学变化
缩,说明:气体微粒间的间隔大于液体微粒间的间隔。 二、构成物质的微粒
构成物质的微粒有:分子、原子、离子。 1.由分子构成的物质:如氧气、水、酒精等。 2.由原子直接构成的物质:如铁、金刚石等。 3.由离子直接构成的物质:如氯化钠由氯离子和钠离子构成。
2/8
知识像烛光,能照亮一个人,也能照亮无数的人。--培根
九年级化学上册2.3构成物质的微粒Ⅱ—原子和离子3
第五页,共三十二页。
氧化汞发生了用下面文字表示(biǎoshì)的变化:
氧化汞 加热(jiā rè) 汞 + 氧气
(HgO) (Hg) (O2)
思考:
1.在化学变化中,反应物氧化汞的分子(fēnzǐ)发 生了怎样变化?
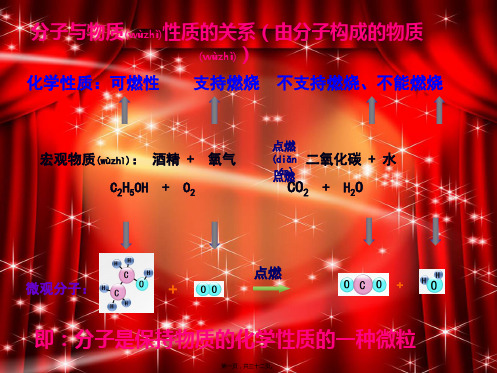
分子与物质(wùzhì)性质的关系(由分子构成的物质 ) (wùzhì)
化学性质:可燃性 支持燃烧 不支持燃烧、不能燃烧
宏观物质(wùzhì): 酒精 + 氧气 C2H5OH + O2
点燃
(diǎn 二氧化碳 + 水
点rán燃C)O2 + H2O
点燃
微观分子:
+
+
即:分子是保持物质的化学性质的一种微粒
(2)有一小部分α粒子改变了原来的运动路径,原因
是
它们途径金原子核附近时,受到斥力而改变
了原来运动方向.说明原子核带正电
(3)极少数α粒子被弹了回来。原因是
它们撞击到金原子核而被弹回.说明(shuōmíng)原子 原子核几乎集中了原子的全部质量
第二十六页,共三十二页。
当堂 检测 (dānɡ tánɡ)
1.1803年,道尔顿原子(yuánzǐ)模型
道尔顿认为
原子是坚硬(jiānyìng)、光滑的实心小球, 无法分割
第十四页,共三十二页。
2.1904年汤姆森原子(yuánzǐ)模型
-
---
英国(yīnɡ
-
汤姆森认为
物理 ɡuó)
原子是带负电荷的
学家汤 姆森
电子镶嵌在里面(lǐmiàn)就象
粤教版化学-九年级上册-科粤版九年级上册2.3构成物质的微粒Ⅱ_原子和离子 离子的形成教案
让学生在黑板上或者在本子上画出钠原子和氯原子的结构图,提问原子在什么情况下是最稳定的?老师讲述原子的稳定结构。
通过在黑板上和PPT上原子到离子的演变图,认识到离子的形成过程。演示离子和原子的区别是什么?它们的联系又是什么?
练习题
既复习了上节课内容又引入了下节课内容。
把上下两节课的内容联结起来了。
锻炼学生的思考能力,同时也复习上节课知识,同时也引入原子的结构。
由已有知识联系新知识
把微观的原子和离子宏观化,降低难度
巩固知识
离子是构成物质的微粒。
2、知道同一元素的原子和离子可以互相转化,初步认识核外电子在化学反应中的作用。
一、教材分析
本课题包括核外电子的排布和离子的形成两部分内容。
离子的形成是本课题的核心,是教学重点。为了说明离子是什么,它是怎样形成的,就必须介绍原子核外电子的排布和金属、非金属、稀有气体元素原子核外电子层结构的特征与其化学性质的关系。
本课题内容不同于宏观物质运动的规律,远离学生的生活经验,如学生对电子层的了解就有一定困难,是教学中的难点,但并不是教学的重点。所以在实际教学过程中,结合本课题内容的特点,从以下几方面突破难点和重点。
1.采用画图和生动的比喻,力求教学直观。
2.充分利用书上的插图,让学生仔细观察,细心体会它的含义。
3.课程标准对本课题的内容要求不高,只要能形成初步观念就可以了,所以要掌握分寸,在教学上不必探究。
四、教学重点难点
教学重点
离子的形成。
教学难点
离子的表示。
五、教法学法
画示意图形象生动的解决,微观世界宏观化,用宏观的大图变化去演示原子变到离子的过程。
