有机化学a2教学课件吉林大学周环反应输出
合集下载
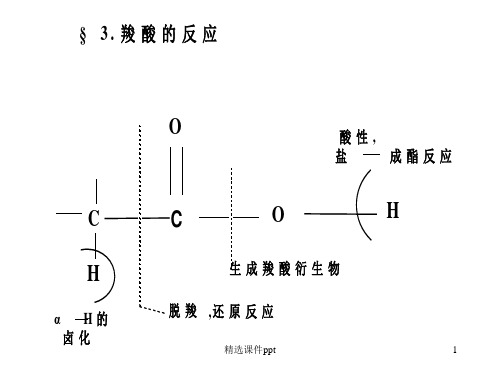
有机化学a2教学课件(吉林大学)羧酸的反应
+NaC
12
3.3.4形 成 酰 胺
羧 酸 与 N 3 R H 2 R N 2 N 反 H 应 H
O
O
RCOH + N3H R C ONH4
O R C OH
+ NH 3
O-
+
R C OH2
NH2 精选课件ppt
O R C NH2
+ H2O
13
3.4 还 原 反 应
常用还原剂: LiAl4H (对烯键\炔键无影响
( C H 3 ) 3 C - O * H H +( C H 3 ) 3 C - O + * H 2 -H2O * (CH3)3C+
O RC OH +(C H 3 )3 C +
- H+
精选课件ppt
OC(CH3)3
RC
+
OH
O
RCOCH (83)C 3
O
浓硫酸
C OH
O
+
C OH2
-H2O
O
C + ROH
但 两 个 羧 基 的 空 间 位 置 不 同 , 脱 去 的 基 团 不 同 .
COOH COOH
HCO +O CH 2O
CO 2 +H2O
COOH
CH 2 COOH
C 3 C HO+ O C H 2O
精选课件ppt
19
O OH OH
O
O OH OH
O
O O + H2O
O
O O+ H 2O
O
精选课件ppt
R- + B C 2r + O H 2 O +H2 g
《周 环 反 应》课件

一个σ键由共轭体系的一端迁移到另一 端,同时发生共轭双键的移动。
A
1
3
2
A
1
3
2
四.周环反应的理论
1. 分子轨道和成键轨道
周环反应的过程,可用轨道来描述,有机化 学中涉及最多的原子轨道为1p轨道和2s轨道。
原子轨道线性组合成分子轨道。当两个等价 原子轨道组合时,总是形成两个新的分子轨道, 一个是能量比原子轨道低的成键轨道,另一个是 能量比原子轨道高的反键轨道。
前者对电子的束缚力较松弛,具电子供体的性质,易给予电 子;后者对电子的亲和力较强,具电子受体的性质,易接受电子。 它们在化学反应中犹如价电子一样起作用,处于反应的最前沿, 所以称为前线轨道,其上的电子称为前线电子。
进行反应时是前线分子轨道,即HOMO和LUMO之间的作用。
发生作用的HOMO和LUMO必须对称性一致。能量水平接近。
电环化反应的立体选择性规律
π电子数
反应条件
立体化学
4n
分子轨道对称守恒原理有三种理论解释: 前线轨道理论; 能量相关理论; 芳香过渡态理论(休克尔-莫比乌斯结构理论)。
现代有机合成之父伍德沃德
伍德沃德1917年4月10日生于美国波士顿。从小喜读书, 善思考。1933年夏,仅16岁的伍德沃德以优异的成绩,考入美 国著名大学麻省理工学院。在全班学生中,他年龄最小,素有
3 H
CH3 H
CH3 LUMO HOMO
hv 对旋
H H3C
CH3
H3C
+
H
H
H CH3
子
H3C
CH3
H
H
轨 道
2 H
CH3 H
CH3 HOMO
+
A
1
3
2
A
1
3
2
四.周环反应的理论
1. 分子轨道和成键轨道
周环反应的过程,可用轨道来描述,有机化 学中涉及最多的原子轨道为1p轨道和2s轨道。
原子轨道线性组合成分子轨道。当两个等价 原子轨道组合时,总是形成两个新的分子轨道, 一个是能量比原子轨道低的成键轨道,另一个是 能量比原子轨道高的反键轨道。
前者对电子的束缚力较松弛,具电子供体的性质,易给予电 子;后者对电子的亲和力较强,具电子受体的性质,易接受电子。 它们在化学反应中犹如价电子一样起作用,处于反应的最前沿, 所以称为前线轨道,其上的电子称为前线电子。
进行反应时是前线分子轨道,即HOMO和LUMO之间的作用。
发生作用的HOMO和LUMO必须对称性一致。能量水平接近。
电环化反应的立体选择性规律
π电子数
反应条件
立体化学
4n
分子轨道对称守恒原理有三种理论解释: 前线轨道理论; 能量相关理论; 芳香过渡态理论(休克尔-莫比乌斯结构理论)。
现代有机合成之父伍德沃德
伍德沃德1917年4月10日生于美国波士顿。从小喜读书, 善思考。1933年夏,仅16岁的伍德沃德以优异的成绩,考入美 国著名大学麻省理工学院。在全班学生中,他年龄最小,素有
3 H
CH3 H
CH3 LUMO HOMO
hv 对旋
H H3C
CH3
H3C
+
H
H
H CH3
子
H3C
CH3
H
H
轨 道
2 H
CH3 H
CH3 HOMO
+
有机化学课件——周环反应

(2E, 4Z, 6E)-2, 4, 6-辛三烯属于有 6 个π电子的共轭体系,其热电环化反应在基态进行, 因 HOMO 的对称性是 S,故对旋关环成键,生成顺-5, 6-二甲基-1, 3-环己二烯,是轨道对称 性允许的,顺旋则是禁阻的;光电环化反应在激发态进行,其 HOMO 的对称性是 A,故顺 旋关环成键,生成反-5, 6-二甲基-1, 3-环己二烯,是轨道对称性允许的,对旋则是禁阻的。
+
环状过渡态
在周环反应中,旧键的断裂与新键的形成是同时进行的,反应不经过自由基或离子等活 性中间体阶段;周环反应一般受反应条件加热或光照的制约,而且加热和光照所产生的结果 也是不同的;此外,周环反应还具有高度的立体专一性的特点。
1965 年 R.B.Woodward 和 R.Hoffmann 在总结了大量反应规律的基础上,把分子轨道理 论引入周环反应的机理研究中,提出了分子轨道对称守恒原理,并推导出一系列选择规律, 用以推测协同反应能否进行及其立体化学过程,这是近代有机化学最大成就之一。
顺旋
H
H
H Me H Me
Me
Me
顺旋 Me
Me
H Me H Me
H
H
顺,反-2, 4-己二烯
顺-3, 4-二甲基环丁烯
如果 C2—C3 和 C4—C5 键是对旋,则 C2 上 p 轨道或 sp3 轨道的一叶能够只能与 C5 上 p 轨道 或 sp3 轨道相位相反的一叶接近,故不能重叠成键而生成反-3, 4-二甲基环丁烯:
分子轨道对称守恒原理把分子轨道理论用于研究化学反应的动态过程,能够很好的解 释和预测周环反应的立体化学过程以及反应进行的条件,其具体表述方法有前线轨道理论、 能级相关理论等,其中前线轨道理论最为简单而且形象,已被普遍接受。下面以共轭二烯和 共轭三烯为例,介绍这一重要原理。
+
环状过渡态
在周环反应中,旧键的断裂与新键的形成是同时进行的,反应不经过自由基或离子等活 性中间体阶段;周环反应一般受反应条件加热或光照的制约,而且加热和光照所产生的结果 也是不同的;此外,周环反应还具有高度的立体专一性的特点。
1965 年 R.B.Woodward 和 R.Hoffmann 在总结了大量反应规律的基础上,把分子轨道理 论引入周环反应的机理研究中,提出了分子轨道对称守恒原理,并推导出一系列选择规律, 用以推测协同反应能否进行及其立体化学过程,这是近代有机化学最大成就之一。
顺旋
H
H
H Me H Me
Me
Me
顺旋 Me
Me
H Me H Me
H
H
顺,反-2, 4-己二烯
顺-3, 4-二甲基环丁烯
如果 C2—C3 和 C4—C5 键是对旋,则 C2 上 p 轨道或 sp3 轨道的一叶能够只能与 C5 上 p 轨道 或 sp3 轨道相位相反的一叶接近,故不能重叠成键而生成反-3, 4-二甲基环丁烯:
分子轨道对称守恒原理把分子轨道理论用于研究化学反应的动态过程,能够很好的解 释和预测周环反应的立体化学过程以及反应进行的条件,其具体表述方法有前线轨道理论、 能级相关理论等,其中前线轨道理论最为简单而且形象,已被普遍接受。下面以共轭二烯和 共轭三烯为例,介绍这一重要原理。
周环反应课件

H OCOCH3 DH
300 ℃
CH3 1
3
2
[1,3 ]σ键烷基迁移 (同面 / 翻转)
H OCOCH3 HD
CH3 1
3
2
C[ 1, 5] 迁移(4n+2 π 电子) :
加热下,同面迁移构型保持,异面迁移构 型翻转;光照下,同面迁移构型翻转,异面 迁移构型保持保持。
CH3 CH3
[1,5]碳移位
H
A BD
R 同 面 迁 移 1 ,3H B D
(4) C[ i, j ] 迁移 [3,3]迁移:
① Cope重排
NC
NC
EtOOC
[3, 3]
EtOOC
1, 5-二烯类化合物在加热条件下发生的 [3,3] 迁移, 生成取代基更多、更稳定的烯烃。
i C 1 C 2 C 3
j
o CC
1' 2' 3'
对
H
Ph Ph
H
H
Ph
Ph
H
H 3 C CH 3 H Ph
Ph
顺
Ph
H Ph
H
CH 3 H H CH 3
HH
HH
练习
CH3
o
(1)
H
175
H
顺旋
CH3
CH3
(2)
顺旋
CH3
CH3
CH3
H
+
H
CH3
CH3
H
CH3 CH3 H
CH3
对旋
(3) hv
CH3
顺旋
CH3
CH3 CH3
CH3
(5) (6)
在化学反应过程中,能形成环状过渡态的协同反 应称为周环反应。所谓协同反应的含义是:在一个 反应中,有两个或两个以上的化学键相互协调地同 时破裂和形成,所以协同反应是一种基元反应。
第二十一章周环反应PPT课件

.
25
但在光的作用下,丁二烯及其衍生物按对旋的方式变为环丁烯及
其衍生物。这一反应大多数是形成关环化和物,而逆向开环反应则 不易发生。这是由于双烯比烯吸收光的力量更强,因此双烯容易被 激化。由于逆向反应是热禁阻的,所以应当预料到,产物非常稳定。 这是合成环系的有效方法。
.
27
环加成反应
两分子烯烃或多烯烃变成环状化合物的反应叫做环加成。 例如:
[4+2]环化加成反应(热反应)允许
.
37
[4+2] 环 化 加 成 反 应 具 有 下 列 特 点 :
(i)是可逆的反应。利用逆反应有时可以得到一些用别
的方法难以合成的化合物。例如:
(ii)加成时是立体专一性的,无例外的都是顺 式加成。
(iii)如亲双烯分子上还有其它的不饱和基团时,加成后不饱 和基团是靠近于新产生的双键一面。它是一个经验规则,称为 阿尔德规则,也称不饱和性最大积累规则。[夏炽中译[美]F.A. 凯里等“高等有机化学“A卷P367]。例如,两个分子的环戊二 烯合成反应时,一个分子供给一个双键,作为亲双烯使用。 加 成时生成二环戊二烯, 理论上应有两种取向: 一种是外型 (Oxo)的, 即原有的双键和新生成的双键处在离的较远的位 置; 另一种是双键处在离的较近的位置, 这叫作内型(Endo) 的,双烯合成主要产生内型产物。(邢其毅主编”基础有机化 学示范教学“P308,胡宏纹讲的”周环反应“解释为次基轨道 的结果)。
Woodward和Hoffman指出:“当反应物与产物的轨道 对称性相合(轨道对称性匹配或者说相位相同)时,反应 易于发生,并不相合时,反应难于发生。”顺旋时反应物 与产物对称性相合。前线轨道理论,只看HOMO的两头 的相位,不管中间。
有机反应中的周环反应PPT共69页

有机反应中的周环反应
31、别人笑我太疯癫,我笑他人看不 穿。(名 言网) 32、我不想听失意者的哭泣,抱怨者 的牢骚 ,这是 羊群中 的瘟疫 ,我不 能被它 传染。 我要尽 量避免 绝望, 辛勤耕 耘,忍 受苦楚 。我一 试再试 ,争取 每天的 成功, 避免以 失败收 常在别 人停滞 不前时 ,我继 续拼搏 。
33、如果惧怕前面跌宕的山岩,生命 就永远 只能是 死水一 潭。 34、当你眼泪忍不住要流出来的时候 ,睁大 眼睛, 千万别 眨眼!你会看到 世界由 清晰变 模糊的 全过程 ,心会 在你泪 水落下 的那一 刻变得 清澈明 晰。盐 。注定 要融化 的,也 许是用 眼泪的 方式的 光荣可 以被永 远肯定 。
谢谢
11、越是没有本领的就越加自命不凡。——邓拓 12、越是无能的人,越喜欢挑剔别人的错儿。——爱尔兰 13、知人者智,自知者明。胜人者有力,自胜者强。——老子 14、意志坚强的人能把世界放在手中像泥块一样任意揉捏。——歌德 15、最具挑战性的挑战莫过于提升自我。——迈克尔·F·斯特利
有机化学a2教学课件(吉林大学)期末总结和综合练习

3.酯的缩合:酰基化、烷基化
4.酮的酰基化、烷基化:注意选择性(热力学产物,动力学产物)
5. 1,3-二羰基化合物的烷基化及酰基化(α-,γ-)
6.安息香缩合反应,二苯乙醇酸重排:机理。
四、胺
1.碱性比较
2. Hofmann 消除:注意Hofmann规则 3.胺的氧化和cope反应:注意立体化学 4.重氮盐的形成:条件 5.三级胺的鉴别
NH3
NH2 + CH2CO ONH4
C H3C HO + BrC H 2C O O Et
OZnBr C H3C HCH2COOEt
H3O+
C H3C HCHCOOH
2.
O O 3 H3C -C -C H 2-C -O Et
O O H3C -C -C H-C -O Et BrC H 2C O O Et CH2COOEt EtO Na O H3C -C -C H 2 CH2COOH
C
)
D. 癸二酸
13、芳香性由大到小的顺序是: A > C > D > B
。
A. 苯
B. 呋喃
C. 噻吩
D. 吡咯
14、亲电取代反应活性由大到小的顺序是:
D>B >C >A
。
A. 苯
B. 呋喃
C. 噻吩
D. 吡咯
15、指出下列协同反应的类型
H A. H
OH C. OH O O
O O B. O O O O
六、杂环化合物
五元杂环化合物:
1.芳香性比较 2.亲电取代反应:(活性比较,完成反应式)
3. 吡咯的特殊反应:发生瑞穆尔-悌曼反应,柯尔伯-施 密特反应,重氮盐的偶合反应 六元杂环体系
1.亲电取代反应:定位β位,注意定位规律,活性比较 2.亲核取代反应:烷基化,芳基化,氨化。定位α,γ位 定位规律
15 - 最新吉林大学林英杰老师有机化学课件

第十五章周环反应概述周环反应:反应过程中无离子或自由基中间体生成,而生成环状过渡态的反应协同反应如: Diels-Alder反应Claisen重排反应§15.1 周环反应的特点和类型一、反应特点1. 不经过中间体:C+、C-、C•、:C等2. 不受溶剂极性、催化剂、自由基引发剂的影响3. 反应条件:加热、光照4. 有明显的立体选择性任何一个单电子可用波函数ϕi表示分子轨道ψ=ΣCi ϕi§15.2 分子轨道对称性守恒及前线分子轨道理论一、分子轨道理论二、分子轨道对称守恒化学反应是分子轨道进行重新组合的过程,在一个协同反应中,分子轨道的对称性是守恒的,即由原料到产物轨道的对称性始终不变。
三、前线轨道理论前线轨道:最高占有轨道:HOMO最低空轨道:LUMO 反应时,电子从一个分子的HOMO 流入另一分子的LUMO,且HOMO 与LUMO的P轨道位相一致§15.3 电环化反应一、定义:在光或热作用下,共轭烯烃转变为环烯烃或它的逆反应1. 取代丁二烯的电环化ψψ6反§15.3 环加成反应一、定义:在光或热作用下,两个或多个烯烃、共轭烯烃或含孤对电子的分子相互作用,形成一个稳定环状化合物的反应。
H CH H H§15.4 σ迁移反应一、定义:在光或热作用下,一个σ键沿共轭体系由一个位置转移到另一个位置,同时伴随π键转移的反应。
A.RCH23DCH-CH=CH-CH=CD221300。
C1 267。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C H3 H
H
H
+
C H3 C H3 H H
C H3 C H3
相同化合物,内消旋体 牛牛文档分享C. 光环化反应顺旋 C H3 H H C H3 C H3 H H C H3 H C H3 C H3 H
C H3 H
H C H3
+
H C H3
C H3 H
外消旋体,一对对映体
在一个协同反应中,分子轨道的对称性是守恒的, 即由原料到----电子最高占有轨道 LUMO----最低未占轨道
处在前线轨道上的电子。 前线电子:
CH2 CH2
节点 1 0
2个π分子轨道,2个π电子
对称性 A(反对称) S(对称)
+
H Ph
H Ph
Ph
H H
Ph
H
H
Ph H
+
Ph H
H Ph
Ph
H H
Ph
Ph
电环化反应有两种立体化学变
R'
R
H
H +
R H
H
R'
R'
逆时针顺旋
顺时针顺旋
对旋:
R H H R'
R
H H
H H
R' R
R'+内向对旋 牛牛文档分享 牛牛文档分享
激发态(h) LUMO
LUMO HOMO
HOMO
1
0
: HOMO
CH3
顺旋
H CH3
H
CH3
HH
CH3
H CH3
CH3 H
外消旋体
h : HOMO
CH3
对旋
H H
CH3
CH3
HH
CH3
H H
内消旋体
CH3 CH3
① 反应过程中没有 自由基, 离子 等活性中间体产生;
② 反应速率极少受到 H
+
, OH 催化剂
及自由基引发剂,抑制剂影响;
③ 反应条件一般只需加热或光照,且在加热或光照下 得到的产物具有不同的立体选择性.
运用前线轨道理论及分子轨道对称守恒原理, 可以总结出周环反应的立体选择性. 牛牛文档分享§ 4. 环加成反应
在光和热的作用下,两个或多个带有双键,共轭双键或 孤电子对的分子相互作用, 形成一个稳定的环状化合物
① 一个反应物的 HOMO 与 另一个反应物的 LUMO 形成新的成键轨道;
如果两分子都给出 HOMO, 则会使电子占据反键轨道, 使分子不稳定:
基态() 激发态(h) 牛牛文档分享 乙烯π分子轨道对称性与能级分布及电子排布
前线轨道理论
分子中存在着前线电子,在分子间或分子内反应中 起关键作用,占有或未占有电子的前线轨道在分子 反应中起着主要的作用。
反应时:电子从一个分子的HOMO,流入另一个分子的 LUMO,且HOMO与LUMO的P轨道位相一致。
CH 3
H
CH 3
H
顺旋
光照
CH3
H
H +
H
H
CH3
CH3CH3 牛牛文档分享A. 1,3,5- 己三烯的分子轨道:对旋 C H3 H H C H3
H C H3
H C环,具有相同的立体选择性.
例如:
Ph
H
Ph
H H H
+
H
Ph
顺旋
Ph P ① 正确书写分子轨道:节面 , 对称性. ② 同相重叠才能成键. ③ 加热时,电子没有跃迁;光照时,电子发生跃迁.
§2. 分子轨道理论及前线轨道理论
任何一个单电子可用波函数 φI 表示 分子轨道用 ψ =∑ ci φI 表示。 分子轨道对称守恒原则: 轨道的波函数有正值和负值之分,只有正值部 分和正值部分重叠,负值部分和负值部分重叠, 才能组成分子轨道,称为对称性符合。即所谓 同相重叠成键。
化学反应是分子轨道进行重新组合的过程,
外向对旋
1. 含有4n个π电子的共轭烯烃的电环化反应
Ph
H
+ Ph
Ph H H Ph
H
顺旋
H
Ph
Ph
H
hγ 对旋
Ph
HPhH 牛牛文档分享1,3 – 丁二烯型的分子轨道:
CH3CH
CH CH CHCH 3 4个π分子轨道,4个π电子
基态() 3 2 A S A S
HOMO
LUMO
稳定
HOMOHOMO 牛牛文档分享不稳定②光照时,一个反应物给出基态,另一个反应物给出激发态; 加热时,两个反应物都给出基态在光或热的作用下,共轭烯烃转变成环烯烃或它的逆反应 共轭烯烃的两个末端碳的π电子环合,形成新的σ键。
共轭烯
CH3 CH3 H H
或 光照
环烯
CH3 CH3 HH 牛牛文档分享电环化反应的立体化学
Ph Ph H
④ 开环和关环的立体选择性H3 H H CH3
CH3 H H CH3 (E,E)
h
CH3
CH3 CH3 H H 牛牛文档享2. 含有4n+2π电子的共轭烯烃的电环化反应
对旋
CH 3 H H CH 3 牛牛文档分享3. 电环化反应规则
牛牛文档分享H H80℃
240℃
H
H
高温加热可导致激发态产生 4n 发生了加热对旋
CH 3 CH 3 CH 3
hv
CH 3 CH 3 CH 3
光照时. 周环反应的类型和特点
在化学反应过程中,能形成环状过度态的协同反应---周环反应. 例如:狄尔斯-阿尔德反应,克莱森重排反应,科普 反应:
环加成反应:
+
