有机化学中国人名反应
有机人名反应策略

有机人名反应策略有机合成是现代化学的重要组成部分,其中人名反应则是有机合成中的关键反应之一。
通过运用人名反应,可以有效实现目标化合物的合成。
本文将介绍有机人名反应策略的四个主要方面:目标化合物的识别与定位、人名反应的筛选与匹配、合成路径的设计与优化、反应条件的探索与选择。
一、目标化合物的识别与定位在有机合成中,首先需要明确目标化合物的结构,并对其进行识别和定位。
这可以通过化学结构分析和官能团识别等方法实现。
在确定目标化合物后,需要进一步了解其性质和用途,以便为其选择合适的人名反应。
二、人名反应的筛选与匹配人名反应是指以科学家姓氏命名的合成反应,这些反应通常具有较高的选择性和效率。
在有机合成中,需要根据目标化合物的结构和性质,筛选出适合的人名反应,并确定最佳的反应条件和催化剂。
通过合理的人名反应筛选与匹配,可以大大提高目标化合物的合成效率。
三、合成路径的设计与优化在确定了人名反应后,需要设计合理的合成路径,并对路径进行优化。
合成路径的设计需要考虑原料的易得性、反应条件的温和程度、产物的纯化和分离等因素。
通过不断优化合成路径,可以提高目标化合物的收率和纯度,降低生产成本。
四、反应条件的探索与选择反应条件是有机合成中的重要因素之一,它直接影响着人名反应的效率和目标化合物的质量。
因此,需要探索和选择最佳的反应条件,如温度、压力、溶剂、催化剂等。
在确定最佳反应条件后,还需要对其进行验证和优化,以确保目标化合物的顺利合成。
总之,有机人名反应策略是有机合成中的重要方法之一。
通过合理运用人名反应,可以有效实现目标化合物的合成,提高合成效率和产物的质量。
在实际应用中,需要根据具体情况进行综合分析和实验验证,以确保有机合成的成功和可靠性。
有机人名反应——机理及合成应用

有机人名反应——机理及合成应用有机化学里,有一个有趣的领域叫做“人名反应”,听到这个名字是不是觉得有点像是某种神秘的仪式?其实,人名反应是指那些以某个人名命名的经典化学反应。
就像有人给你起个外号,化学家们也给这些反应起了名字,以纪念那些对化学有重大贡献的前辈。
今天我们就来聊聊这些反应的机理以及它们在合成中的应用,让大家对这个领域有个直观的了解。
1. 有机人名反应的机理1.1 什么是机理?简单来说,机理就是解释化学反应为什么会这样发生的故事。
就像你在看一部悬疑剧时,想知道凶手怎么作案一样,化学家们也想弄清楚反应的“幕后黑手”是什么。
机理告诉我们每一步反应过程中的分子怎么舞动,反应怎么一步步进行,就像揭开了化学反应的神秘面纱。
1.2 经典人名反应的机理我们先从最著名的几个反应说起吧,比如费林反应(FriedelCrafts反应)和迈克尔加成反应。
费林反应是由化学家费林(Friedel)和克拉夫茨(Crafts)一起开发的,它主要用来生成芳香族化合物的衍生物。
简单来说,就是把一个芳香环(比如苯)跟一个其他的基团结合起来,形成新化合物。
这就好比把你喜欢的几个菜肴混合在一起,变成一道新的美味。
迈克尔加成反应就像是个“组合拳”,它把两个分子合并,形成一个新的结构。
具体来说,它是一种加成反应,其中一个分子上的亲电中心(可以理解成化学反应中的“吸引力中心”)和另一个分子的亲核中心(“发射点”)发生反应。
这个过程有点像一个化学版的“双簧”——需要两个分子之间的默契配合,才能奏效。
2. 有机人名反应的合成应用2.1 药物合成中的应用说到应用,那可真是五花八门。
药物合成中,有机人名反应简直就是神兵利器。
比如说,某些复杂的药物分子可以通过这些反应合成出来,像阿莫西林这样的抗生素就是通过特定的反应步骤制作的。
想象一下,你要制作一款超级复杂的料理,怎么做呢?得有可靠的食谱和技巧对吧?化学家们也是如此,他们用这些反应作为合成的“食谱”,让复杂的药物分子得以顺利生成。
人名反应药物合成反应中主要的人名反应
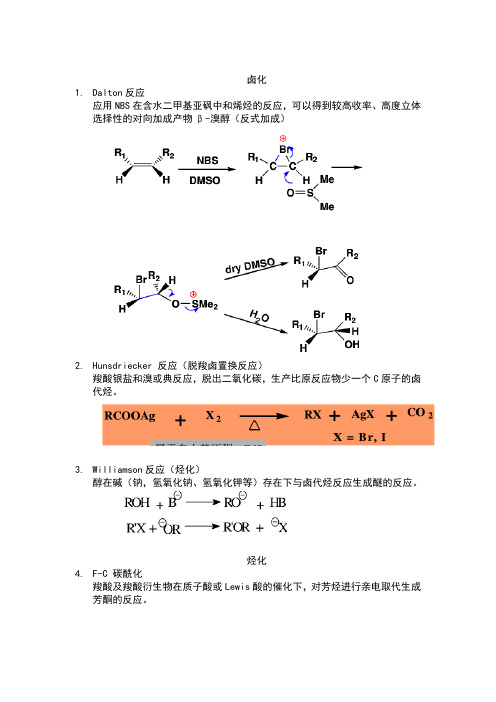
卤化1.Dalton反应应用NBS在含水二甲基亚砜中和烯烃的反应,可以得到较高收率、高度立体选择性的对向加成产物β-溴醇(反式加成)2.Hunsdriecker 反应(脱羧卤置换反应)羧酸银盐和溴或典反应,脱出二氧化碳,生产比原反应物少一个C原子的卤代烃。
3.Williamson反应(烃化)醇在碱(钠,氢氧化钠、氢氧化钾等)存在下与卤代烃反应生成醚的反应。
烃化4.F-C 碳酰化羧酸及羧酸衍生物在质子酸或Lewis酸的催化下,对芳烃进行亲电取代生成芳酮的反应。
酰化1.Gattermann反应羟基或烷氧基取代的芳烃在ZnCl2,AlCl3等Lewis酸的催化下与氰化氢和氯化氢反应,生成亚胺盐酸盐,在经水解生成相应的芳醛的反应。
2.Vilsmeier-Haack反应3.Reimer-tiemann反应4.Claisen和Dieckmann反应缩合1.Claisen-Schmidt反应2.Prins反应3.安息香缩合4.Blanc反应(氯甲基化)5.Mannich反应(氨甲基化)反应机理6.β-羟烷基化反应7. Michael反应8.Wittg反应9.羧基α活性亚甲基反应10.α,β-环氧化烷基化反应(Darens反应)11.D-A反应重排12.13.Pinacol重排14.B-B-Z重排15.Favorskii重排16.Beckmann重排17.Hofmann重排18.Stevens重排19.Sommelet-hauser重排20.Claisen重排还原21.Clemansen还原22.黄明龙反应23.氨基保护剂还有Boc。
有机人名反应、试剂与规则

有机人名反应、试剂与规则
有机化学是研究含碳分子结构、性质和反应的科学,它以有机分子的命名、合成和应用为主要内容。
有机人名反应、试剂与规则是有机化学中的重要内容,它们为有机化学家们提供了一种通用的语言和方法,使得大家可以更好地理解、记忆和应用有机化学知识。
本文将介绍有机人名反应、试剂与规则的基本概念和应用。
一、有机人名反应
有机人名反应是以人名命名的有机反应,通常因为其发现者、发展者、研究者的名字而得名。
有机人名反应是有机化学中的重要内容之一,它们被广泛应用于有机合成和有机反应机理的研究中。
常见的有机人名反应有:Diels-Alder 反应、Wittig 反应、Aldol 反应、Grignard 反应等。
二、有机试剂
有机试剂是指在有机合成中所使用的化学试剂,通常需要具有高纯度、高活性和低毒性等特点。
有机试剂的种类繁多,包括有机金属试剂、有机酸试剂、有机碱试剂、有机卤素试剂等。
有机试剂的选择和使用应遵循安全、经济、环保和高效的原则。
三、有机命名规则
有机命名规则是指有机化合物的命名方法和规则。
有机化合物的命名一般遵循以下步骤:1、确定基团;2、确定主链;3、编号主链;
4、确定取代基和它们的位置;
5、给取代基编号;
6、组合,写出名字。
常见的有机命名规则有:IUPAC 命名法、常用名称命名法等。
总之,有机人名反应、试剂与规则是有机化学中不可或缺的内容,它们为有机化学的研究、应用和发展提供了重要的支撑和指导。
我们应该学好有机人名反应、试剂与规则,掌握有机化学的基本概念和原理,以更好地理解、应用和创造有机化学知识。
有机化学人名反应(人卫版附)

有机化学⼈名反应(⼈卫版附)1、Cannizzaro 反应凡α位碳原⼦上⽆活泼氢的醛类和浓NaOH或KOH⽔或醇溶液作⽤时,不发⽣醇醛缩合或树脂化作⽤⽽起歧化反应⽣成与醛相当的酸(成盐)及醇的混合物。
此反应的特征是醛⾃⾝同时发⽣氧化及还原作⽤,⼀分⼦被氧化成酸的盐,另⼀分⼦被还原成醇:脂肪醛中,只有甲醛和与羰基相连的是⼀个叔碳原⼦的醛类,才会发⽣此反应,其他醛类与强碱液,作⽤发⽣醇醛缩合或进⼀步变成树脂状物质。
醛⾸先和氢氧根负离⼦进⾏亲核加成得到负离⼦,然后碳上的氢带着⼀对电⼦以氢负离⼦的形式转移到另⼀分⼦的羰基不能碳原⼦上。
2、Claisen 酯缩合反应含有α-氢的酯在醇钠等碱性缩合剂作⽤下发⽣缩合作⽤,失去⼀分⼦醇得到β-酮酸酯。
如2分⼦⼄酸⼄酯在⾦属钠和少量⼄醇作⽤下发⽣缩合得到⼄酰⼄酸⼄酯。
⼄酸⼄酯的α-氢酸性很弱(pK a-24.5),⽽⼄醇钠⼜是⼀个相对较弱的碱(⼄醇的pK a~15.9),因此,⼄酸⼄酯与⼄醇钠作⽤所形成的负离⼦在平衡体系是很少的。
但由于最后产物⼄酰⼄酸⼄酯是⼀个⽐较强的酸,能与⼄醇钠作⽤形成稳定的负离⼦,从⽽使平衡朝产物⽅向移动。
所以,尽管反应体系中的⼄酸⼄酯负离⼦浓度很低,但⼀形成后,就不断地反应,结果反应还是可以顺利完成。
3、Claisen 重排烯丙基芳基醚在⾼温(200°C)下可以重排,⽣成烯丙基酚。
当烯丙基芳基醚的两个邻位未被取代基占满时,重排主要得到邻位产物,两个邻位均被取代基占据时,重排得到对位产物。
对位、邻位均被占满时不发⽣此类重排反应。
交叉反应实验证明:Claisen重排是分⼦内的重排。
采⽤ g-碳 14C 标记的烯丙基醚进⾏重排,重排后 g-碳原⼦与苯环相连,碳碳双键发⽣位移。
两个邻位都被取代的芳基烯丙基酚,重排后则仍是a-碳原⼦与苯环相连。
Claisen 重排是个协同反应,中间经过⼀个环状过渡态,所以芳环上取代基的电⼦效应对重排⽆影响。
Wolff-Kishner-黄鸣龙反应

Wolff-Kishner-黄鸣龙还原反应一些对酸不稳定而对碱稳定的醛类或酮类在碱性条件下与肼作用,羰基被还原为亚甲基;原本的Wolff-Kishner的方法是将醛或酮与肼和金属钠或钾在高温(约200 °C)下加热反应,需要在封管或高压釜中进行,操作不方便;黄鸣龙改进不用封管而在高沸点溶剂如一缩二乙二醇(二甘醇,沸点245°C)中,用氢氧化钠或氢氧化钾代替金属钠反应。
对碱敏感的化合物不适合用此还原法,可用Clemmensen还原法。
反应机理:反应实例:进行黄鸣龙还原法还原时, 只要在二甘醇或三甘醇中, 将羰基化合物酮类或醛类与强碱氢氧化钾或氢氧化钠、85%(有时可用50%)水合肼同置于圆底烧瓶内, 回流1 h, 然后除去冷凝管, 继续加热, 使反应液温度上升到190~200 ℃, 此时再加上冷凝管, 保持此温度继续加热2~3 h, 还原反应即可完成. 反应液冷却后可用水稀释, 还原产物如为中性或碱性固体, 则在水中析出,可进行过滤分离. 若还原产物为中性或碱性液体, 则可用乙醚等有机溶剂提取. 还原产物若为酸性, 则产物溶解在碱性反应液中, 需先用稀酸中和至酸性, 产物始能析出.对于某些遇碱敏感的羰基化合物, 如醛类、酮酸类、双酮类以及在羰基邻近有不对称碳原子的化合物, 在还原时可先不加氢氧化钾, 而在二甘醇中将此类羰基化合物先与85%水合肼回流1 h 制成腙, 冷却后再加入氢氧化钾, 然后加热去水至反应液温度上升到190~200 ℃,以后操作同前.在应用上述操作进行还原反应时, 若被还原的羰基化合物或还原产物的沸点低于190~200 ℃, 则在蒸去水分时, 物质亦随水汽蒸发, 故此时不除去冷凝管, 而在烧瓶和冷凝管之间加一分液器, 以便除去水份.在黄鸣龙还原法中使用甘醇或三甘醇作为溶剂, 这有两方面的作用, 其一是作为高沸点溶剂, 提高反应温度, 可使反应液中的水分逸出. 其二是作为宿主溶剂(Host solvent), 使OH-离子几乎处于“祼露”状态, 从而大大提高它的碱性, 有利于腙的分解而生成碳氢化合物, 后一种作用正是其它高沸点溶剂所不具备的. 二甘醇或三甘醇的用量, 随羰基化合物或其腙衍生物的溶解度而定. 只要使反应液在加热过程中成澄清或几乎澄清即可. 如果某些羰基化合物在二甘醇或三甘醇中的溶解度不大, 可先用少量乙醇溶解, 再加入二甘醇或三甘醇及其它试剂.氢氧化钾或氢氧化钠的用量, 一般使碱溶解于溶剂中成10%的浓度即可. 至于85%或50%的水合肼的用量,一般均用过量, 大概用羰基化合物摩尔数的3~4 倍. 在此还原法中, 使用过量的水合肼是非常重要的, 此点必需重视, 否则容易生成嗪而得不到正常还原产物, 如芴酮需用6~7 倍物质的量的水合肼才能得到98%的芴.对某些不稳定的、或难于提纯的羰基化合物, 例如萘醛,可先制成腙或缩氨基脲的衍生物, 再加碱升温分解即可. 由于此还原法在高温下进行, 难免对酯基发生水解和醚基发生裂解.黄鸣龙(1898-1979),有机化学家。
有机化学中的人名反应

O C H + HCHO NaOH
CH2 OH + HCO2
Cannizzaro反应
具有α-活泼氢原子的醛和甲醛首先发生羟醛缩合反应,得到无α-活泼氢 原子的β-羟基醛,然后再与甲醛进行交叉Cannizzaro反应,如乙醛和甲 醛反应得到季戊四醇:
HCHO + CH3CHO NaOH C CH2OH 4 + HCO2
人名反应
Koble-Schmitt 反应
酚钠和二氧化碳在加压下于125-150 ºC反应,生成邻羟基苯甲酸,同时有 少量对羟基苯甲酸生成
Gabriel合成法
邻苯二甲酰亚胺与氢氧化钾的乙醇溶液作用转变为 邻苯二甲酰亚胺盐,此盐和卤代烷反应生成N-烷基 邻苯二甲酰亚胺,然后在酸性或碱性条件下水解得 到一级胺和邻苯二甲酸,这是制备纯净的一级胺的 一种方法
GO
Clemmensen还原法
醛类或酮类分子中的羰基被锌汞齐和浓盐酸还原为亚甲基:
O C
Zn-Hg HCl
CH2
+
H2O
此法只适用于对酸稳定的化合物。对酸不稳定而对碱稳定的化合物可用 Wolff-Kishner-黄鸣龙反应还原。
GO
Wolff-Kishner还原法
醛类或酮类在碱性条件下与肼作用,羰基被还原为亚甲基:
感谢您的聆听
Diels-Alder反应
含有一个活泼的双键或叁键的化合物(亲双烯体)与共轭二烯类化合物(双
烯体)发生1,4-加成,生成六员环状化合物:
R1 R3
R1 R3
+
R4 R2
R4 R2
Diels-Alder 反应
这个反应极易进行并且反应速度快,应用范围极广泛,是合成环状 化合物的一个非常重要的方法。
《有机化学人名反应》课件

人名反应的定义与重要性
定义
人名反应是指以科学家或化学家的名字命名的有机化学反应。这些反应通常具 有独特性、重要性或实用性。
重要性
人名反应是化学领域中的重要知识,掌握这些反应有助于理解有机化学的基本 原理,提高解决实际问题的能力。同时,人名反应也是化学领域中科学研究的 成果,体现了人类对化学反应的深入认识和探索。
一种重要的烷基化反应
详细描述
Friedel-Crafts反应是一种在芳香化合 物中引入烷基的亲电取代反应。通常 在路易斯酸(如AlCl3)催化下进行, 该反应广泛应用于有机合成中。
Wittig 反应
总结词
制备烯烃的经典方法
详细描述
Wittig反应是一种通过磷酸酯和醛之间的反应制备烯烃的方法。该反应涉及一个五元环 过渡态,生成具有特定立体化学特征的烯烃。
ቤተ መጻሕፍቲ ባይዱ
在材料科学中的应用
材料科学是一个跨学科的领域,涉及材料的设计、制备、性 能和应用。人名反应在材料科学中的应用主要涉及新型材料 的合成和改性。
通过人名反应,可以合成出具有优异性能和功能的新型材料 ,如高分子材料、陶瓷材料、复合材料等。这些材料在能源 、环境、信息等领域具有广泛的应用前景,为科技进步和社 会发展提供重要支持。
亲电取代反应
总结词
亲电取代反应是一种有机化学反应,其中亲电试剂进攻并取代反应物分子中的某 个基团。
详细描述
这类反应通常发生在苯环、芳香烃和杂环化合物的反应中,其中亲电试剂具有正 电性,能够进攻富电子的碳原子。常见的亲电取代反应包括:EAS reaction、 Elimination reaction等。
详细描述
这类反应通常发生在烯烃、炔烃和芳香烃的反应中,其中加成试剂能够与不饱和键结合形成新的键。 常见的加成反应包括:Diels-Alder reaction、Addition reaction等。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
有机化学中国人名反应
中国人名反应是指以中国有机化学家的名字命名的有机化学反应。
这些反应通常是由这些化学家发现或发展,并且对有机化学领域的发展做出了重要贡献。
以下将介绍几个著名的中国人名反应。
1. 曾光明反应
曾光明反应是由中国有机化学家曾光明教授于1981年首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将酮类化合物与硅醚反应,形成相应的醇类化合物。
曾光明反应在有机合成中具有广泛的应用,可以高效地构建C-O键,是合成醇类化合物的重要工具。
2. 毛宗回反应
毛宗回反应是由中国有机化学家毛宗回教授于1978年首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将酮类化合物与有机硅化合物反应,生成相应的醇类化合物。
毛宗回反应在有机合成中广泛应用,具有高效、高选择性和环境友好等优点,被广泛用于合成复杂有机分子。
3. 李盛骏反应
李盛骏反应是由中国有机化学家李盛骏教授于20世纪80年代中期首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将炔烃与醛类化合物反应,形成相应的α,β-不饱和醛类
化合物。
李盛骏反应在有机合成中具有重要的应用价值,可以高效地构建C-C键和C=O键,是合成复杂有机分子的重要工具。
4. 王立群反应
王立群反应是由中国有机化学家王立群教授于1992年首次报道的一种重要的合成方法。
该反应以过渡金属催化剂为催化剂,能够将酮类化合物与炔烃反应,形成相应的烯醇类化合物。
王立群反应在有机合成中具有广泛的应用,可以高效地构建C-C键和C-O键,是合成天然产物和药物分子的重要工具。
5. 陈茵反应
陈茵反应是由中国有机化学家陈茵教授于20世纪70年代末首次报道的一种重要的合成方法。
该反应以金属有机化合物为催化剂,能够将酮类化合物与酸类化合物反应,形成相应的酯类化合物。
陈茵反应在有机合成中具有重要的应用价值,可以高效地构建C-C键和C-O键,是合成酯类化合物的重要工具。
以上所介绍的中国人名反应只是其中的一部分,还有许多其他的中国人名反应对有机化学领域的发展做出了重要贡献。
这些反应的发展和应用不仅促进了有机合成的发展,也为新药物的合成和天然产物的结构修饰提供了重要的方法学基础。
随着中国有机化学家的不断努力和创新,相信将会有更多的中国人名反应被发现和应用于有机化学领域,为化学科学的发展做出更大的贡献。
