知识讲解 无机推断专题(基础)
高三化学无机推断题知识点

高三化学无机推断题知识点一、化学无机推断的概念和目的化学无机推断是指通过实验方法,根据各种反应现象和特征性质来确定未知物质的性质和组成。
它在化学分析中起着重要的作用,能够帮助我们准确地确认化合物的成份、结构和性质。
化学无机推断的目的主要有两个方面:一是通过实验结果推断出未知物质的性质,例如判断其是否为盐酸、硫酸等酸性物质;二是通过实验结果推断出未知物质的组成和结构,例如判断其是否为氯化钠、硫酸铜等化合物。
二、无机盐的推断方法1. 阳离子的推断方法(1)利用化学特性:根据阳离子的特性,如化学反应、颜色、气味等,来推断出未知物质中所含的阳离子。
例如,铁离子在NaOH溶液中生成红棕色沉淀,可以推断出未知物质中可能含有Fe3+离子。
(2)利用气体的生成:一些阳离子在特定条件下能够生成气体,通过气体的产生来判断阳离子的存在。
例如,硫酸钾溶液中存在铜离子时,加入氨水会产生蓝色沉淀,同时释放出氨气,可以推断出未知物质中可能含有铜离子。
2. 阴离子的推断方法(1)利用溶液的凝固特性:一些阴离子在特定条件下能够凝固成为固体沉淀,通过凝固的出现来判断阴离子的存在。
例如,硝酸银溶液中存在氯离子时,会产生白色沉淀,可以推断出未知物质中可能含有氯离子。
(2)利用特殊的化学反应:一些阴离子在特定条件下会发生特殊的化学反应,通过反应的出现来判断阴离子的存在。
例如,加入Barfoed试液后,出现红色沉淀,可以推断出未知物质中可能含有还原糖。
三、常见无机化合物的推断1. 硝酸盐的推断(1)加热产生棕色气体:利用加热产生棕色气体的特点,可以推断出未知物质中可能含有硝酸盐。
(2)与亚硝酸银反应:亚硝酸银溶液可以与硝酸盐反应生成红褐色沉淀,从而推断出未知物质中可能含有硝酸盐。
2. 硫酸盐的推断(1)与氯化钡反应:氯化钡溶液可以与硫酸盐反应生成白色沉淀,通过判断是否有白色沉淀的生成来推断出未知物质中可能含有硫酸盐。
(2)加入氯化钠酸化亚硫酸:硫酸盐加入氯化钠酸化亚硫酸后产生气体的反应,可以推断出未知物质中可能存在硫酸盐。
无机推断专题讲座共18页文档

F、G、M四种气体,这四种气体之间的反应如图所
示:
O2 A H2O E
H2O
B H2O F
N
Ni,△
C H2O G
Q
燃烧 H2O
N+ W
H2O
燃烧 N +
W
D H2O M NH3
催化剂, △
H2O
N+ I
NO
I是一种遇空气变红棕色的气体,请填写下列空 白: A是 Na2O2 ,B是 Na ,C是 CaC2 ,D是 Mg3N2 , E是 O2 ,F是 H2 ,G是 C2H2 ,M是 。 NH3
Cl2
Br2
Br2 H2 HBr
H2
练习1 已知A、B、C、D为气体,E、F为固体,G
是氯化钙,它们之间的转化关系如图所示:
D
A
点燃
C
B
NH4Cl
E 加热
F
D H
G CaCI2
(1)D的化学式(分子式)是 NH3 ,E的化学式(分子式)
是 NH4Cl 。 (2)A和B反应生成C的化学方程式:H2
+
电解 2CuSO4+2H2O====2Cu+O2↑+2H2SO4
也可能是活泼金属的无氧酸盐;
电解 2NaCl+2H2O====2NaOH+Cl2↑+H2 ↑
2.需要催化剂:①氨气的催化氧化
②工业合成氨气
③SO2+O2 ④KClO3制氧气 ⑤双氧水分解
3.需要高温条件:
CaCO3分解;铝热反应;水泥和玻璃的工业反应;FeS2 高温 煅烧;
X是固体,Y是液体,Z是无色气体,W为黄绿色气体,B
的溶液显强酸性。则:
无机推断题的必备知识

无机推断题的必备知识无机推断题是指通过化学物质的性质、结构和反应来推断出化学现象的方法,具有广泛的适用性和实用性。
在化学实验、工业生产、环境保护和农业生产等领域中都得到了广泛应用。
以下是无机推断题必备的知识:一、离子反应的基本原理离子反应是指在溶液中发生的离子间相互作用的过程,也是无机推断题中最常用的反应类型之一。
离子反应的基本原理包括:1. 离子反应的本质是离子间的电荷转移过程。
2. 离子反应需要离子在溶液中的存在,即不能在干态中进行。
3. 离子反应可以通过产生沉淀、气体、水和酸碱中和等方式来进行判断和推断。
二、化学计量的基本概念化学计量是指在化学反应中,物质数量之间的关系。
在无机推断题中,常用化学计量的概念包括摩尔质量、摩尔比、反应产物的摩尔数等。
化学计量的基本概念包括:1. 摩尔质量:表示物质中单个分子或原子的质量,单位为g/mol。
2. 摩尔比:表示在化学反应中,反应物之间的物质量比值。
3. 摩尔数:表示在化学反应中,反应物和产物中每种物质所含的摩尔数量。
三、酸碱反应的性质和判断方法酸碱反应是指酸和碱在水溶液中发生的反应,也是无机推断题中常见的反应类型。
酸碱反应的性质和判断方法包括:1. 酸性溶液含有自由游离的H+离子,碱性溶液含有自由游离的OH-离子。
2. 酸碱反应中,酸和碱发生中和反应,产生盐和水。
3. 酸碱指示剂可以用于判断溶液的酸碱性质,其中最常用的指示剂是酚酞、溴甲酚等。
四、氧化还原反应的基本原理和判断方法氧化还原反应是指反应物中的某个原子或分子失去或得到电子的过程。
氧化还原反应在无机推断题中也是常见的反应类型。
氧化还原反应的基本原理和判断方法包括:1. 氧化作用是指物质失去电子,还原作用是指物质得到电子。
2. 氧化还原反应必须涉及电子的移动,其中电子的移动方向可以通过氧化还原半反应求解。
3. 氧化还原反应中,常见的还原剂包括金属、非金属、还原性离子等,氧化剂包括氧化态较高的元素和化合物等。
无机推断
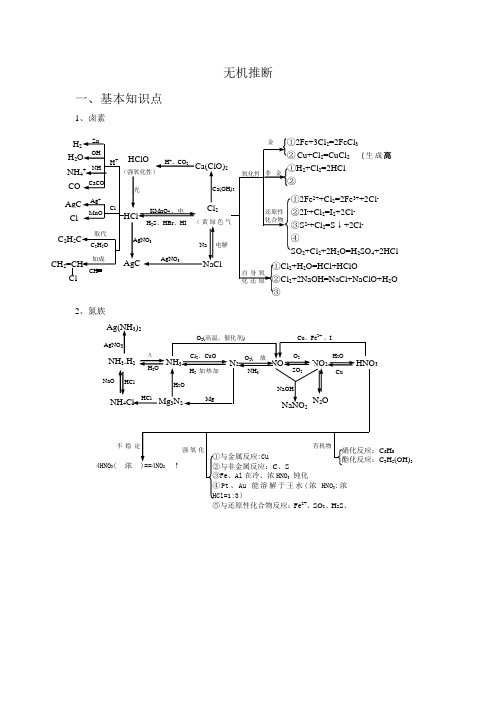
无机推断一、基本知识点1、卤素23、硫和硫的化合物4、碳族5、过渡元素【知识网络】6、镁和铝7、碱金属高考化学无机推断题解题方法及最新试题题典一.金属部分:[题眼归纳] 1.特征现象:(1)焰色反应:Na +(黄色)、K +(紫色) (2)浅黄色固体:S 或Na 2O 2或AgBr(3)有色溶液:Fe 2+(浅绿色)、Fe 3+(黄色)、Cu 2+(蓝色)、MnO 4-(紫色)有色固体:红色(Cu 、Cu 2O 、Fe 2O 3)、红褐色[Fe(OH)3]蓝色[Cu(OH)2] 黑色(CuO 、FeO 、FeS 、CuS 、Ag 2S 、PbS )黄色(AgI 、Ag 3PO 4) 白色[Fe(0H)2、CaCO 3、BaSO 4、AgCl 、BaSO 3]有色气体:Cl 2(黄绿色)、NO 2(红棕色) (4)特征反应现象:])([])([32OH Fe OH Fe 红褐色白色沉淀空气−−→−(5)既产生淡黄色沉淀又产生刺激性气味的气体:S 2O 32-+2H +=S ↓+SO 2↑+H 2O (Na 2S 2O 3 + H 2SO 4) (6)溶液颜色变为浅绿色,并产生淡黄色沉淀: 2FeCl 3+H 2S=2FeCl 2+S ↓+2HCl (7) 通CO 2变白色浑浊:石灰水(过量变清)、Na 2SiO 3、饱和Na 2CO 3、浓苯酚钠、NaAlO 22.基本反应:(1)与水反应产生气体或沉淀: ○1单质⎪⎩⎪⎨⎧↑+=+↑+=+22222422222O HF O H F H NaOH O H Na○2化合物()()()⎪⎪⎩⎪⎪⎨⎧↑+=+↑+↓=+↑+↓=+↑+=+22222232323222322222326233422H C OH Ca O H CaC S H OH Al O H S Al NH OH Mg O H N Mg O NaOH O H O Na ○3双水解: ()()()()()⎪⎩⎪⎨⎧↓−−→−↓+↑−−→−↓+↑−−→−-----+32322323233222OH Al AlO OH Al S H HS S OH Al CO HCO CO Al O H O H O H 与(2) 既能酸反应,又能与碱反应 ①单质:Al 、Si②化合物:Al 2O 3、Al(OH)3、弱酸弱碱盐、弱酸的酸式盐、氨基酸。
化学无机推断题技巧(一)

化学无机推断题技巧(一)化学无机推断题技巧引言在化学课上,无机化学推断题不仅是考试重点,也是学生最为头疼的部分。
本文将聚焦于无机化学推断题技巧,帮助学生更好地应对化学课上的考试。
技巧一:准确描述化学反应在推断题中,正确描述化学反应是获得分数的关键。
建议学生记清楚常见化学反应方程式,简要描述化学物质间的相互作用以及形成的物质。
技巧二:注意化学反应间的量比关系化学反应中,物质的量比关系是影响推断过程的重要因素。
学生需要根据所给物质的量推断不同物质数量和性质。
在推断过程中需要注意比例关系,合理运用化学方程式求出未知物质的量。
技巧三:根据性质排查可能的物质推断过程中,根据化学物质的性质可以推断可能的物质种类。
例如,对某种金属离子进行检测时,根据是否有气体产生和具体产生的气体情况,可以排查出可能含有的金属离子种类。
技巧四:有序推断整个过程在推断过程中,学生需要有序地进行推断,一步步确定未知物质的种类和性质。
需要注重每一步推断过程的准确性和逻辑性,确保每一步推断没有遗漏或错误。
结论以上是化学无机推断题的相关技巧,希望大家在备考时能够重视这些技巧,提高自己的化学无机推断题能力。
只有掌握正确的方法,才能赢得优异的成绩!补充技巧:掌握常见离子的性质在无机化学推断中,掌握常见的离子的性质是非常重要的。
比如,硫化氢气体可以用于检测金属离子,铵盐可以用于检测氨基酸等等。
因此,学习化学无机推断,需要搞清楚各种离子的特性,熟悉它们的化学反应和检测方法。
补充技巧二:练习解析技能想要在化学无机推断题中获得更高的分数,需要掌握解析技能。
平时多做习题,了解各种答题技巧,例如分类讨论、化合物判断等等,可以帮助提高解析和推断的能力。
同时,也可以加强注记与解析的能力,更快更好地推断出未知物质的性质。
结论以上的补充技巧同样对于学习和应对化学无机推断题非常有帮助。
在学习过程中,掌握各种离子的性质和解析技巧是非常重要的。
希望大家能够在这些技巧的帮助下更好地学习和应对化学无机推断的考试。
高考化学无机推断知识点

高考化学无机推断知识点高考化学无机推断是高考化学考试中的一个重要内容,也是考生需要重点关注和掌握的知识点之一。
本文将通过介绍无机推断的基本概念、常见方法、应用和注意事项,来帮助考生全面了解并有效备考化学无机推断。
一、基本概念无机推断是通过一系列实验方法和化学反应,根据物质在反应过程中的特点,推断出物质的组成成分、性质或结构的一种方法。
它是根据指定化合物在特定条件下的物理和化学性质,通过与未知物质的反应,确定未知物质的成分和性质,从而推断出未知物质的特征。
二、常见方法1. 滴定法:滴定法是通过反应物容量的测定来推断未知物质的化学组成。
常见的滴定法包括酸碱滴定法、氧化还原滴定法和络合滴定法等。
2. 沉淀法:沉淀法是通过沉淀形成与溶液中某些离子形成不溶性沉淀物,来推断未知物质中的离子组成。
常见的沉淀法包括硫化沉淀法、氯化沉淀法和碳酸盐沉淀法等。
3. 反应法:反应法是通过观察未知物质与其他物质发生反应的结果,来推断出未知物质的性质和成分。
常见的反应法包括酸碱中和反应、氧化还原反应和络合反应等。
三、应用无机推断在实际应用中具有广泛的用途,主要体现在以下几个方面:1. 化学分析:无机推断可以应用于分析化学领域,通过对样品中各种离子的推断,来判断样品的组成和性质。
这对于环境监测、食品检测和医药分析等具有重要意义。
2. 金属材料检验:无机推断可以帮助检验人员快速准确地判断金属材料的成分和品质。
例如,通过检测金属材料中的杂质元素,可以评估其纯度和可用性。
3. 矿物鉴定:无机推断在地质学和矿物学中有着重要的应用,可以帮助研究人员确定矿物样品的成分和结构,从而进一步探索矿产资源和地质活动。
四、注意事项在进行无机推断的过程中,考生应注意以下几点:1. 实验操作的准确性:化学实验操作的准确性对于推断结果的准确性至关重要,因此考生需要熟练掌握实验操作技巧,并注意实验条件和反应时间等关键因素。
2. 化学反应的基本原理:在进行无机推断时,考生需要了解化学反应的基本原理,掌握不同反应类型的特点和规律,从而能够准确判断未知物质的性质和成分。
无机推断专题知识讲稿 (2)

无机推断的重要性
无机推断在化学工业、新材料研 发、环境保护等领域具有广泛的 应用价值,是解决实际问题的重
要手段之一。
通过无机推断,可以深入了解物 质的性质和反应机理,为新材料
的发现和应用提供理论支持。
无机推断也是化学教育的重要组 成部分,对于培养学生的逻辑思
维和创新能力具有重要意义。
无机推断的基本原则
实例二:反应原理推断题解析
总结词
反应原理推断题是考查学生对化学反应原理的理解和 应用能力的题目,需要学生根据题目给出的信息和化 学反应原理,推断出未知反应的反应物、产物和反应 条件。
详细描述
反应原理推断题一般会给出一些化学反应的信息,如反 应条件、反应现象、产物的性质等,以及它们之间的关 系。学生需要根据这些信息和化学反应原理,逐步推断 出未知反应的反应物、产物和反应条件。在解题过程中 ,学生需要熟练掌握化学反应原理和化学反应规律,能 够根据已知反应的信息和反应原理,推测未知反应的反 应过程和产物。同时,学生还需要注意反应条件的控制 和反应现象的观察,以便更好地推断出未知反应的反应 物和产物。
实例三:结构推断题解析
总结词
结构推断题是考查学生对物质结构和化学键的理解和 应用能力的题目,需要学生根据题目给出的信息和物 质结构,推断出未知分子的结构和组成。
详细描述
结构推断题一般会给出一些分子的性质或结构特征,如 分子式、键长、键角等,以及它们之间的关系。学生需 要根据这些信息和物质结构的规律,逐步推断出未知分 子的结构和组成。在解题过程中,学生需要熟练掌握物 质结构和化学键的知识,能够根据已知分子的结构和组 成,推测未知分子的结构和组成。同时,学生还需要注 意分子中化学键的连接方式和空间构型,以便更好地推 断出未知分子的结构和组成。
无机化学推断题知识汇总

27 无机化学推断题知识汇总(一)化学中物质的颜色种类较多,但分散在各个知识中,比较零碎,而在物质推断题中常常用到颜色进行分析和判断,为了便于查找和记忆,规类总结如下:1.黄色黄色:AgI、Ag3PO4、P4(黄磷)、溴水(黄→橙)、FeS2、Al2S3、甲基橙在弱酸性、中性或碱性环境中、某些蛋白质加浓硝酸。
淡黄色:S、Na2O2、TNT、PCl5、AgBr、浓HNO3(混有NO2)、浓HCl(混有Fe3+)、(混有NO2)。
灰黄色:Mg3N 2棕黄色:FeCl3溶液、碘水(深黄→褐)。
2.黑色:CuS、Ag2S、Cu2S、HgS(黑色或红色)、FeS、FeO、Fe3O4、MnO2、CuO、Ag2O、I2(紫黑色)、Si(灰黑色)、C、Ag(粉末)、KMnO4(固体)、石油。
3.绿色:CuCl2溶液、Cu2(OH)2CO3、FeSO4·7H2O(浅绿色)、F2(淡黄绿色)、Cl2(黄绿色)、氯水(淡黄绿色)。
4.红色:Cu2O、Cu、甲基橙在酸性环境中、紫色石蕊试液在酸性环境中、酚酞在碱性环境中、品红试液、Fe(SCN)2+、Br2(深红棕)、红磷(暗红)、Br2的CCl4溶液(紫红)、苯酚被空气氧化(粉红)。
5.棕色:固体FeCl3、固体CuCl2、NO2(红棕)、Fe2O3(红棕)。
6.紫色:KMnO4溶液、I2的CCl4溶液。
7.灰色:As、Sn、Fe3C。
8.褐色:碘酒、2Fe2O3·3H2O、Fe(OH)3(红褐)。
9.蓝色:CuSO4·5H2O、Cu(OH)2、淀粉遇碘、紫色石蕊试液加碱、Cu2+的稀溶液。
(二)、无机推断知识规律1.同一元素的气态氢化物和气态氧化物反应,生成该元素的单质和水,元素可能是硫或氮。
2.同一元素的气态氢化物和最高价氧化物对应的水化物化合,生成盐的元素一定是氮。
3.两溶液混合生成沉淀和气体,这两种溶液的溶质可能分别是①Ba(OH)2与(NH4)2SO,;②可溶性铝盐与可溶性金属硫化物或可溶性碳酸盐或碳酸氢盐;③可溶性铁盐与可溶性碳酸盐或碳酸氢盐;④硫代硫酸盐与强酸(如盐酸、稀H2S04等)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
知识讲解无机推断专题(基础)文字叙述型推断题、框图型推断题等,从近年高考题来看,无机推断题正朝着综合性方向发展,尤其是理综中的化学推断题,侧重学科内综合能力考查。
【方法点拨】一、无机推断题解题思路读题(了解大意)→审题(寻找明显条件、挖掘隐含条件与所求)→解题(抓突破口)→推断(紧扣特征与特殊)→得出结论→正向求证检验→规范书写读题:读题的主要任务是先了解题目大意,寻找关键词、句,获取表象信息。
切勿看到一点熟悉的背景资料就匆匆答题,轻易下结论,这样很容易落入高考试题中所设的陷阱。
审题:对读题所获信息提炼、加工,寻找明显的或潜在的突破口,更要注意挖掘隐含信息-“题眼”。
“题眼”常是一些特殊的结构、状态、颜色,特殊的反应、反应现象、反应条件和用途等等。
审题最关键的就是找出”题眼”。
解题:找到“题眼”后,就是选择合适的解题方法。
解无机推断题常用的方法有:顺推法、逆推法、综合推理法、假设法、计算法、实验法等。
通常的思维模式是根据信息,大胆猜想,然后通过试探,验证猜想;试探受阻,重新阔整思路,作出新的假设,进行验证。
一般来说,先考虑常见的规律性的知识,再考虑不常见的特殊性的知识,二者缺一不可。
验证:不论用哪种方法推出结论,都应把推出的物质代入验证。
如果与题设完全吻合,则说明我们的结论是正确的。
最后得到正确结论时还要注意按题目要求规范书写,如要求写名称就不要写化学式。
规范书写:物质的名称、化学式、结构简式、电子式、化学方程式、热化学方程式、电极反应式、离子方程式、电离方程式。
二、无机推断题的相关知识储备1、物质的特征现象(1)物质的颜色:有色气体单质:F2(浅绿色气体)、Cl2(黄绿色气体)、O3(淡蓝色气体)其他有色单质:Br2(深红色液体,蒸气为红棕色)、I2(紫黑色固体)、S(淡黄色固体)、Cu(紫红色固体)、Si(灰黑色晶体)、C(黑色粉未)无色气体单质:N2、O2、H2有色气体化合物:NO2(红棕色)黄色固体:AgI、Ag3PO4、AgBr(浅黄)、Na2O2(淡黄)、S(淡黄)黑色固体:FeO、Fe3O4、MnO2、C、CuS、PbS、Ag2S、CuO红色固体:Fe(OH)3(红褐色)、Fe2O3(红棕色)、Cu2O(红色)、Cu(红色)蓝色固体:五水合硫酸铜(俗称胆矾或蓝矾)CuSO4·5H2O、Cu(OH)2;绿色固体:七水合硫酸亚铁(绿矾)FeSO4·7H2O;碱式碳酸铜Cu2(OH)2CO3,俗称铜绿;紫黑色固体:KMnO4、碘单质。
有色离子(溶液)Cu2+(蓝色)、Fe2+(浅绿)、Fe3+(棕黄)、MnO4-(紫红色)、Fe(SCN)2+(血红色)不溶于稀酸的白色沉淀:AgCl、BaSO4、Ag2SO4不溶于稀酸的(浅)黄色沉淀:S、AgBr、AgI焰色反应显黄色的是钠元素,显紫色的钾元素(透过蓝色钴玻璃观察)(2)气体特征:常见的气体有:单质:H2、Cl2、O2、O3、N2、F2氢化物:NH3、H2S、HCl氧化物:CO2、SO2、NO、NO2、CO有机物:CH4、C2H2、C2H4、HCHO、CH3Cl (3)物质的气味:有臭鸡蛋气味的气体:H2S有刺激性气味的气体:Cl2、SO2、NO2、HX、NH3有刺激性气味的液体:浓盐酸、浓硝酸、浓氨水、氯水、溴水(4)物质的毒性:非金属单质有毒的:Cl2、Br2、I2、F2、S、P4常见的有毒气体化合物:CO、NO、NO2、SO2、H2S、能与血红蛋白结合的是CO和NO(5)物质的溶解性特征:CO2(1∶1)、Cl2(1∶2)、SO2(1∶40)、HCl(1∶500)、NH3(1∶700)极易溶于水的气体:HX、NH3常见的难溶于水的气体:H2、N2、NO、CO、CH4、C2H4、C2H2S和P4不溶于水,微溶于酒精,易溶于二硫化碳。
(6)熔沸点特征:H2O HF NH3形成氢键反常;离子化合物MgO、Al2O3熔点高、可以做耐火材料。
2、物质的数据特征(1)组成的数据关系:如短周期元素X和Y元素可形成1:1和2:1的化合物,涉及到的化合物有H2O2和H2O、Na2O和Na2O2。
若按1:2组成化合物时,除了要考虑离子化合物(如MgCl2)外,还要考虑共价化合物(如CO2),还得考虑有机物中的乙烯等,甚至还有不常见的物质如N2H4。
(2)相对分子质量相等的情况:①式量为28:N2、CO、C2H4②式量为30:NO、HCHO;式量为32有S 、O2③式量为44:CO2、CH3CHO、C3H8、N2O④式量为78:Na2O2、Al(OH)3、Na2S、C6H6;式量为84有NaHCO3、MgCO3⑤式量为98:H2SO4、H3PO4⑥式量为100:CaCO3、KHCO3、Mg3N2⑦式量为120:Al2S3、MgSO4、NaHSO4⑧式量为160:Fe2O3、CuSO4。
(3)电子数相等的微粒常见的10电子微粒:①分子:CH4、NH3、H2O、HF、Ne;②离子:NH4+、H3O+、OH-、Na+、Mg2+、Al3+、F-、O2-、N3-③关系:OH-+H3O+=2H2O;NH4++OH-NH3↑+H2O;CH4+H2O3H2+CO;2F2+2H2O=4HF+2O2Al3++3OH-=Al(OH)3↓;Al3++4OH-=AlO2-+H2O ;Mg2++2OH-=Mg(OH)2↓常见的18电子微粒:①分子:Ar、HCl、H2S、PH3、SiH4、F2、H2O2、C2H6、CH3OH、N2H4②离子:K+、Ca2+、P3-、S2-、HS-、Cl-当然还有很多电子数相等的微粒,如:14电子微粒:N2、CO、C22-等。
(4)数据差量关系:如连续氧化前后相差16。
3、归纳和熟记1-18号元素中的一些特点(1)H:原子半径最小;最外层电子数=周期数;电子总数=电子层数;原子序数最小;有一种氢原子没有中子;单质密度最小;单质可由金属与水或酸反应得到;单质是水电解产物之一;与氧可生成两种物质H2O、H2O2。
(2)He:最外层属于饱和结构,但不是8电子;电子总数是电子层数的2倍。
(3)Li:最外层电子数是次外层电子数的一半;单质在空气中燃烧,不能形成过氧化物;密度最小的金属;保存于石蜡油中。
(4)Be:最外层电子数=次外层电子数;最外层电子数=电子层;氧化物为BeO;价态为+2价。
(5)B:原子最外层不满足8电子结构(BF3属非极性分子)。
(6)C:尿素中N质量分数为46%;除稀有气体外,既难得电子,又难失电子,难以形成单核离子;可以和浓硫酸和浓硝酸在加热条件下反应。
(7)N:单质空气中含量中最多;N2具有一定的惰性,通常情况下难与其它物质反应;氢化物NH3;氧化物形式最多(六种);含氧酸有HNO3和HNO2;气态氢化物水溶液呈碱性;(8)O:有H2O2、H2O 、Na2O2、Na2O 等特殊氧化物,存在O2、O3等同素异形体。
(9)F:前18号元素中除氢外原子半径最小;无正价;不能被任何物质氧化;能与水反应置换中水中的氧;没有含氧酸;HF水溶液是弱酸,并且形成氢键。
(10)Ne:化学性质不活泼;用于装饰灯(霓红灯广告牌)。
(11)Na:最外层电子数是最内层的一半,可以形成一些特殊的氧化物,Na2O2可以和水或二氧化碳反应。
(12)Mg:最外层电子数=最内层电子数;次外层电子数是最外层电子数的4倍;Mg可以和N2反应,生成的Mg3N2和水反应生成Mg(OH)2和氨气。
(13)Al:最外层电子数=电子层数;Al、Al2O3、Al(OH)3均能与强酸、强碱反应;是地壳中含量最多的金属元素。
(14)Si:最外层电子数是次外层数的一半;地壳含量中排第二位,是半导体材料;SiO2是硅酸盐水泥、玻璃的主要成分;SiO2是光导制品的基本原料。
(15)P:PH3可自燃(鬼火);有同素异形体白磷和红磷;磷酸为三元中强酸,磷酸可形成三种形式的盐。
(16)S:可形成SO2、SO3两种氧化物,FeS2是黄色物质,其中硫呈-1价。
(17)Cl:单质为黄绿色;电解食盐水制氯气;HClO具有漂白性。
(18)Ar:最外层属于8电子饱和结构,化学性质不活泼。
4、特殊的转换关系(1)与水反应有气体生成的有关方程式:2Na + 2H2O = 2NaOH + H2↑(现象:浮、熔、游、响、红)2Na2O2 + 2H2O = 4NaOH + O2↑Mg3N2 + 6H2O = 3Mg(OH)2↓+ 2NH3↑Al2S3 + 6H2O = 2Al(OH)3↓+ 3H2S↑CaC2 + 2H2O Ca(OH)2 + C2H2↑2NaCl+2H2O 2NaOH +H2↑+Cl2↑4AgNO3+2H2O4Ag+ O2↑+4HNO3(2)与碱反应产生气体NH4+ + OH -NH3↑+ H2O2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑(3)与酸反应产生气体2Al + 6HCl = 2AlCl3 + 3H2↑C+2H2SO4 (浓) CO2↑+2SO2↑+2H2OCa2CO3 + 2HCl = CaCl2 + H2O + CO2↑(4)、既能与强酸反应,又能与强碱反应的物质一般有:①某些金属:Al②两性氧化物:Al2O3③两性氢氧化物:Al(OH)3④弱酸的酸式盐:NaHCO3、NaHS、NaHSO3等⑤弱酸的铵盐:(NH4)2CO3、CH3COONH4、(NH4)2SO3等⑥氨基酸如:H2N-CH2-COOH(5)、置换反应的类型①金属置换非金属的反应:2Na + 2H2O = 2NaOH + H2↑2Al + 6HCl = 2AlCl3 + 3H2↑3Fe + 4H2O(气)Fe3O4 + 4H22Mg+CO22MgO+C②金属置换金属:2Al+Fe2O3Al2O3+2FeFe+Cu2+=Fe2++Cu③非金属置换金属:C+2Cu O CO2+2CuH2+CuO Cu+H2O④非金属置换非金属:C + H2O CO + H22F2 + 2H2O = 4HF + O2Cl2+2Br-=2Cl-+Br2(6)、特征转换:A B C D(酸或碱)①C CO CO2H2CO3②CH4CO CO2H2CO3③N2NO NO2HNO3④NH3NO NO2HNO3⑤S SO2SO3H2SO4⑥H2S SO2SO3H2SO4⑦Na Na2O Na2O2NaOH (7)、三角转换:(8)、重要的反应条件Ⅰ、需催化剂的无机反应:①氯酸钾的分解:②过氧化氢的分解:2H2O22H2O+O2↑;③合成氨反应:④氨的催化氧化:⑤二氧化硫的催化氧化:⑥水煤汽生产的第二步反应:Ⅱ、必须控制170℃才能发生的反应,必是制取乙烯的反应;C2H5OH C H 2=C H 2↑+H2OⅢ、需放电才能进行的反应:N2与O2的反应:N2+O22NO;Ⅳ、需光照的反应:HNO3、HClO的分解;H2与Cl2混合见光爆炸;5、重要的化工生产反应⑴、煅烧石灰石:CaCO3CaO+CO2↑;⑵、水煤汽的生产:C+H2O CO+H2,⑶、盐酸的工业制法:用氢气在氯气中燃烧的方法来生产盐酸H2+Cl22HCl;⑷、漂白粉的生产:工业上将氯气通入石灰乳中反应来制漂白粉2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O漂白粉有效成分是次氯酸钙,真正起漂白作用的则是次氯酸。
