1食品动物用兽用抗菌药物临床应用管理办法 - 中华人民共和国农业部
食品动物用兽用抗菌药物临床应用管理办法

食品动物用兽用抗菌药物临床应用管理办法一、前言随着人口的不断增长和生活水平的提高,食品产业发展迅速。
然而,与此同时,食品安全问题也日益凸显。
其中,动物源性食品中的抗菌药物残留是一个严重的问题。
为了加强对食品动物用兽用抗菌药物的临床应用管理,本文制定了《食品动物用兽用抗菌药物临床应用管理办法》。
二、背景1.食品动物用兽用抗菌药物的定义:指用于预防和治疗食品动物疾病的药物,包括抗生素、化学合成药物和其他抗菌药物。
2.食品动物用兽用抗菌药物的临床应用管理的重要性:通过规范抗菌药物的使用,可以减少抗菌药物在食品中的残留,保障食品安全,减少抗菌药物滥用导致的抗药性问题,提高兽医临床用药水平。
三、管理办法的主要内容1.抗菌药物使用原则–严格按照兽医学和临床实践规范使用抗菌药物。
–禁止在食品动物中使用人用抗菌药物。
–鼓励使用替代抗菌药物,如中草药、生物制品等。
2.抗菌药物使用程序–兽医师在临床使用抗菌药物前,必须对食品动物进行全面的体检和病史调查,确保抗菌药物的使用是合理的。
–使用抗菌药物时,应按照药物说明书中的剂量和疗程进行使用,禁止超量使用和长期使用。
–兽医师必须对使用抗菌药物的食品动物进行记录,包括药物名称、剂量、使用时间等信息,并与兽医师协会进行备案。
3.抗菌药物监测与评估–食品动物用兽用抗菌药物使用情况的监测和评估由相关部门负责。
–监测和评估的内容包括抗菌药物的使用情况、残留水平、抗菌药物耐药性状况等。
–监测结果将定期向社会公布,提高公众对食品动物用兽用抗菌药物临床应用管理的知情度和参与度。
4.处罚与奖励–对违反管理办法的兽医师和食品动物养殖场将进行处罚,包括罚款、吊销执业证书等。
–对遵守管理办法的兽医师和食品动物养殖场将给予奖励,包括表彰、奖金等。
四、管理效果预期1.减少食品动物中抗菌药物的残留,提高食品安全水平。
2.减少抗菌药物滥用和抗菌药物耐药性的发生,保障公众健康。
3.提高兽医师临床用药水平,确保抗菌药物的合理使用。
1食品动物用兽用抗菌药物临床应用管理办法 - 中华人民共和国农业部

附件1食品动物用兽用抗菌药物临床应用管理办法(征求意见稿)第一条为加强食品动物用兽用抗菌药物临床应用管理,控制动物源细菌耐药,保障动物疾病防治效果、动物产品质量安全及公共卫生安全,根据《兽药管理条例》《执业兽医管理办法》和《兽用处方药和非处方药管理办法》等规定,制定本办法。
第二条本办法所称兽用抗菌药物是指防治细菌、支原体、衣原体、立克次体、螺旋体、真菌等病原微生物所致感染性疾病的药物,不包括防治各种病毒所致感染性疾病和寄生虫病的药物。
第三条农业部负责全国食品动物用兽用抗菌药物临床应用的监督管理。
县级以上地方人民政府兽医行政管理部门负责本行政区域内食品动物用兽用抗菌药物临床应用的监督管理。
第四条本办法适用于各级各类食品动物养殖场(户)兽用抗菌药物临床应用管理工作。
第五条兽用抗菌药物临床应用应当遵循保障动物健康,维护公共卫生安全和动物产品质量安全的原则。
第六条国家对兽用抗菌药物实行分级管理。
根据安全性、疗效、对动物感染治疗的重要性及细菌耐药性等因素,将兽用抗菌药物分为非限制使用级、限制使用级、特殊使用级等三级。
具体分级标准如下:(一)非限制使用级抗菌药物。
经长期兽医临床应用证明安全、有效,对动物严重感染治疗重要,细菌耐药性关注比较小的抗菌药物。
(二)限制使用级抗菌药物。
经长期兽医临床应用证明安全、有效,对动物严重感染治疗高度重要,细菌耐药性关注比较大的抗菌药物。
(三)特殊使用级抗菌药物。
具有以下情形之一的:对动物具有明显或者严重不良反应,不宜随意使用的;对动物严重感染治疗极为重要的;细菌耐药性受到高度关注的;上市不足5 年的抗菌药物新品种。
第七条养殖场(户)应依据有关法律、法规、规章的相关规定制定本机构《兽用抗菌药物临床应用管理办法实施细则》、建立兽用抗菌药物临床应用评估与持续改进制度。
第八条养殖场(户)应当严格执行《兽用处方药和非处方药管理办法》,加强对抗菌药物遴选、采购、处方、调剂、兽医临床应用和药物评价的管理。
农业部令(2013年第2号)《兽用处方药和非处方药管理办法》

中华人民共和国农业部令2013年第2号《兽用处方药和非处方药管理办法》已于2013年8月1日经农业部第7次常务会议审议通过,现予发布,自2014年3月1日起施行。
附件:《兽用处方药和非处方药管理办法》部长韩长赋2013年9月11日兽用处方药和非处方药管理办法第一条为加强兽药监督管理,促进兽医临床合理用药,保障动物产品安全,根据《兽药管理条例》,制定本办法。
第二条国家对兽药实行分类管理,根据兽药的安全性和使用风险程度,将兽药分为兽用处方药和非处方药。
兽用处方药是指凭兽医处方笺方可购买和使用的兽药。
兽用非处方药是指不需要兽医处方笺即可自行购买并按照说明书使用的兽药。
兽用处方药目录由农业部制定并公布。
兽用处方药目录以外的兽药为兽用非处方药。
第三条农业部主管全国兽用处方药和非处方药管理工作。
县级以上地方人民政府兽医行政管理部门负责本行政区域内兽用处方药和非处方药的监督管理,具体工作可以委托所属执法机构承担。
第四条兽用处方药的标签和说明书应当标注“兽用处方药”字样,兽用非处方药的标签和说明书应当标注“兽用非处方药”字样。
前款字样应当在标签和说明书的右上角以宋体红色标注,背景应当为白色,字体大小根据实际需要设定,但必须醒目、清晰。
第五条兽药生产企业应当跟踪本企业所生产兽药的安全性和有效性,发现不适合按兽用非处方药管理的,应当及时向农业部报告。
兽药经营者、动物诊疗机构、行业协会或者其他组织和个人发现兽用非处方药有前款规定情形的,应当向当地兽医行政管理部门报告。
第六条兽药经营者应当在经营场所显著位置悬挂或者张贴“兽用处方药必须凭兽医处方购买”的提示语。
兽药经营者对兽用处方药、兽用非处方药应当分区或分柜摆放。
兽用处方药不得采用开架自选方式销售。
第七条兽用处方药凭兽医处方笺方可买卖,但下列情形除外:(一)进出口兽用处方药的;(二)向动物诊疗机构、科研单位、动物疫病预防控制机构和其他兽药生产企业、经营者销售兽用处方药的;(三)向聘有依照《执业兽医管理办法》规定注册的专职执业兽医的动物饲养场(养殖小区)、动物园、实验动物饲育场等销售兽用处方药的。
一、我国兽药安全使用管理规定.

该药仅限量供应乡以上畜牧兽医站(个体兽医医疗站除外)、家 畜饲养场兽医室以及农业科研教学单位所属的兽医院等兽医医疗 单位临床使用。
凭兽用安钠咖注射液经销、使用卡到本省指定的定点经销单位采 购。
兽药管理
兽用复方氯胺酮注射液 全身麻醉药,用于家畜和野生动物的全身麻醉和化学保定。
定点生产 农业部指定的生产企业。 定点经营 省级兽医行政管理部门指定经营单位。 使用单位责任 必须从复方氯胺酮注射液指定经销单位采购产品,产 品仅限自用,不得转手倒买倒卖; 凭兽医处方使用产品。
兽药管理
(3)休药期管理规定 什么是休药期? 是食品动物从停止给药到许可屠宰或其产品(肉、蛋、奶) 许可上市的间隔时间。
奶牛进入休药期, 不能挤奶 停止给药
许可屠宰 产品上市
时间 休药期
依据药物在动物体内的消除规律确定的。 兽药管理
思考
1、不遵守休药期有何危害? 2、如何监督是否执行了休药期的规定? 3、是否所有的兽药都有休药期的规定? 4、不同种类的兽药休药期是否一致? 5、执行休药期的目的是什么?
兽药管理
(5)规定了禁止在饲料和动物饮用水中使用的药物
禁止在饲料和动物饮用水中使用的药物(部分)
序号 1 2 类别 β-兴奋剂类 性激素类 药物名称 盐酸克仑特罗、沙丁胺醇、西马特罗 己烯雌酚、雌二醇
3
抗生素滤渣
抗生素产品生产过程中产生的
工业三废
4
蛋白质同化激素
碘化酪蛋白、苯丙酸诺龙
兽药管理
图片中不规范使用兽药表现为?
目的:强化对兽用处方药的管理,保障 Nhomakorabea药安全。
兽药管理
3、加强对特殊兽药品的管理
农业农村部关于印发《全国兽用抗菌药使用减量化行动方案(2021—2025年)》的通知

农业农村部关于印发《全国兽用抗菌药使用减量化行动方案(2021—2025年)》的通知文章属性•【制定机关】农业农村部•【公布日期】2021.10.21•【文号】农牧发〔2021〕31号•【施行日期】2021.10.21•【效力等级】部门规范性文件•【时效性】现行有效•【主题分类】畜牧业正文农业农村部关于印发《全国兽用抗菌药使用减量化行动方案(2021—2025年)》的通知农牧发〔2021〕31号各省、自治区、直辖市农业农村(农牧)、畜牧兽医厅(局、委),新疆生产建设兵团农业农村局:为切实加强兽用抗菌药综合治理,有效遏制动物源细菌耐药、整治兽药残留超标,全面提升畜禽绿色健康养殖水平,促进畜牧业高质量发展,有力维护畜牧业生产安全、动物源性食品安全、公共卫生安全和生物安全,我部制定了《全国兽用抗菌药使用减量化行动方案(2021—2025年)》,现印发你们,请结合实际认真组织实施,确保如期完成各项工作目标任务。
农业农村部2021年10月21日全国兽用抗菌药使用减量化行动方案(2021—2025年)根据《中华人民共和国生物安全法》《中华人民共和国乡村振兴促进法》《兽药管理条例》规定,以及《国务院办公厅关于促进畜牧业高质量发展的意见》《食用农产品“治违禁控药残促提升”三年行动方案》等文件要求,在全国兽用抗菌药使用减量化行动试点工作基础上,制定本行动方案。
一、行动目标以生猪、蛋鸡、肉鸡、肉鸭、奶牛、肉牛、肉羊等畜禽品种为重点,稳步推进兽用抗菌药使用减量化行动(以下简称“减抗”)行动,切实提高畜禽养殖环节兽用抗菌药安全、规范、科学使用的能力和水平,确保“十四五”时期全国产出每吨动物产品兽用抗菌药的使用量保持下降趋势,肉蛋奶等畜禽产品的兽药残留监督抽检合格率稳定保持在98%以上,动物源细菌耐药趋势得到有效遏制。
到2025年末,50%以上的规模养殖场实施养殖减抗行动,建立完善并严格执行兽药安全使用管理制度,做到规范科学用药,全面落实兽用处方药制度、兽药休药期制度和“兽药规范使用”承诺制度。
我国现行的兽用抗菌药相关现行的有效规章和规范性文件

特别策划我国现行的兽用抗菌药相关现行的有效规章和规范性文件2019年5月,农业农村部汇总了现行的有效规章和规范性文件目录并予以公布。
兽药相关政策有52条,具体如下。
1.兽用麻醉药品的供应、使用、管理办法(1980年11月20日〔80〕农业(牧)字第34号、〔80〕卫药字36号、〔80〕国药供字第545号公布)2.兽用安钠咖管理规定(1999年3月22日农牧发〔1999〕5号公布,2007年11月8日农业部令第6号修订)3.中华人民共和国动物及动物源食品中残留物质监控计划和官方取样程序(1999年5月11日农牧发〔1999〕8号公布)4.兽药质量监督抽样规定(2001年12月10日农业部令第6号公布,2007年11月8日农业部令第6号修订)5.兽药生产质量管理规范(2002年3月19日农业部令第11号公布,2017年11月30日农业部令2017年第8号修订)6.兽药标签和说明书管理办法(2002年10月31日农业部令第22号公布,2004年7月1日农业部令第38号、2007年11月8日农业部令第6号、2017年11月30日农业部令2017年第8号修订)7.兽药注册办法(2004年11月24日农业部令第44号公布)8.新兽药研制管理办法(2005年8月31日农业部令第55号公布,2016年5月30日农业部令2016年第3号、2019年4月25日农业农村部令2019年第2号修订)9.兽用生物制品经营管理办法(2007年3月29日农业部令第3号公布)10.兽药进口管理办法(2007年7月31日农业部、海关总署令第2号公布,2019年4月25日农业农村部令2019年第2号修订)11.动物病原微生物菌(毒)种保藏管理办法(2008年11月26日农业部令第16号公布,2016年5月30日农业部令2016年第3号修订)12.兽药经营质量管理规范(2010年1月15日农业部令2010年第3号公布,2017年11月30日农业部令2017年第8号修订)13.兽用处方药和非处方药管理办法(2013年9月11日农业部令2013年第2号公布)14.兽药产品批准文号管理办法(2015年12月3日农业部令2015年第4号公布,2019年4月25日农业农村部令2019年第2号修订)15.加强氟虫腈管理(2009年2月25日农业部、工业和信息化部、环境保护部公告第1157号)16.氟虫胺管理措施(2019年3月22日农业农村部公告第148号)17.禁止在饲料和动物饮水中使用的药物品种目录(2002年2月9日农业部、卫生部、国家食品药品监督管理局公告第176号)18.食品动物禁用的兽药及其他化合物清单(2002年4月9日农业部公告第193号)19.兽药标签和说明书编写细则(2003年1月22日农业部公告第242号)20.兽药注册资料要求(2004年12月22日农业部公告第442号)21.新兽药监测期期限(2005年1月7日农业部公告第449号)22.农业部关于发布《农业部兽药审评专家管理办法》的通知(2005年3月8日农医发〔2005〕3号)23.兽药品种编号(2005年3月11日农业部公告第472号)24.农业部办公厅关于兽药商品名称有关问题的通知(2006年10月10日农办医〔2006〕48号)25.农业部关于加强兽用生物制品生产检验原料监督管理的通知(2006年11月22日农医发〔2006〕10号)26.农业部关于发布《国家兽药残留基准实验室管理规定》的通知(2008年1月2日农医发〔2008〕1号)27.农业部、国家食品药品监督管理局关于加强麻黄碱监管工作的紧急通知(2008年11月24日农医发〔2008〕24号)28.禁止在饲料中人为添加三聚氰胺和饲料中三聚氰胺限量规定(2009年6月8日农业部公告第1218号)29.进口兽药管理目录(2009年12月31日农业部、海关总署公告第1312号)30.禁止在饲料和动物饮水中使用的物质(2010年12月27日农业部公告第1519号)31.农业部办公厅关于兽药生产企业办理《兽药经营许可证》有关问题的函(2011年2月15日农办医函〔2011〕12号)32.农业部办公厅关于国内兽药生产企业出口兽药使用外文标签和说明书问题的函(2011年10月13日农办医函〔2011〕30号)33.新兽药监测期等有关问题公告(2013年2月16日农业部公告第1899号)(下转第55页)12中国动物保健 | 2019.10Copyright©博看网 . All Rights Reserved.(上接第12页)34.兽用处方药品种目录(第一批)(2013年9月30日农业部公告第1997号)35.食品动物用兽药产品注册要求补充规定(2015年3月2日农业部公告第2223号)36.禁止在食品动物中使用洛美沙星等4种原料药的各种盐、脂及各种制剂的公告(2015年9月1日农业部公告第2292号)37.新兽用生物制品研发临床试验靶动物数量调整(2015年11月24日农业部公告第2326号)38.兽医诊断制品生产质量管理规范(2015年12月9日农业部公告第2334号)39.兽医诊断制品注册规定修订(2015年12月10日农业部公告第2335号)40.兽药非临床研究质量管理规范(2015年12月9日农业部公告第2336号)41.兽药临床试验质量管理规范(2015年12月9日农业部公告第2337号)42.停止硫酸黏菌素作为药物饲料添加剂使用(2016年7月26日农业部公告第2428号)43.《兽药非临床研究质量管理规范监督检查标准》《兽药临床试验质量管理规范监督检查标准》及其监督检查相关要求(2016年10月27日农业部公告第2464号)44.兽药产品说明书范本(2016年10月27日农业部公告第2465号)45.兽用处方药品种目录(第二批)(2016年11月28日农业部公告第2471号)46.兽药产品批准文号批件变更工作要求(2016年12月21日农业部公告第2481号)47.宠物用兽药说明书范本(2017年4月1日农业部公告第2512号)48.停止生产使用狂犬病活疫苗(2017年4月7日农业部公告第2514号)49.农业部兽药评审专家管理办法(2017年6月2日农业部公告第2507号公布)50.兽药注册评审工作程序(2017年10月30日农业部公告第2599号公布)51.兽药生产企业飞行检查管理办法(2017年11月21日农业部公告第2611号)52.兽药严重违法行为从重处罚情形(2018年12月4日农业农村部公告第97号)(文章内容根据公开数据整理或有遗漏)力,一般情况下一两个月便能出栏。
农业部办公厅关于贯彻实施《兽用处方药和非处方药管理办法》的通知
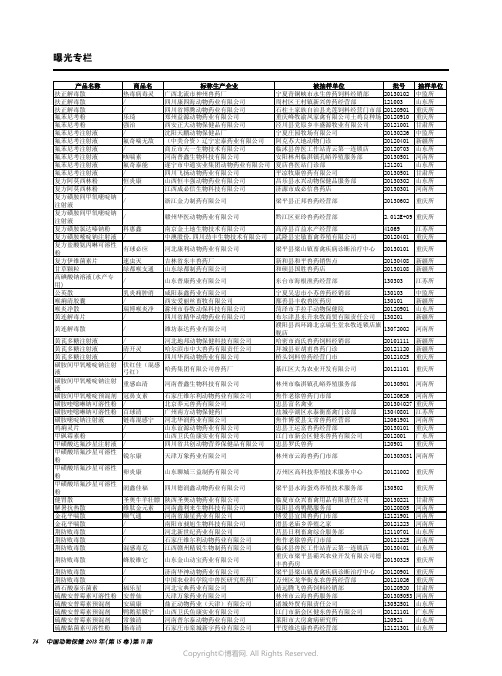
20121120
桥头饲料兽药经营门市
20121025
中监所 新疆所 山东所 新疆所
河南所
新疆所 新疆所 重庆所
綦江区大为农业开发有限公司
20121101 重庆所
Байду номын сангаас
林州市临淇镇孔峪养殖服务部
焦作老徐兽药门市部 忠县富名禽业 盐城亭湖区永泰衡畜禽门诊部 焦作博爱县文常兽药经营部 忠县王运富兽药经营部 江门市新会区健东兽药有限公司 忠县罗氏兽药
130502 重庆所
临夏市众兴畜禽用品有限责任公司 20130221 甘肃所
原阳县鸡鸭鹅服务部
20120805 河南所
博爱县宜国兽药门市部
12121901 河南所
滑县老庙乡养殖之家
20121223 河南所
莒县日利畜禽综合服务部
12110701 山东所
焦作老徐兽药门市部
20121225 河南所
临沭县兽医工作站青云第一连锁店 20130401 山东所
四川省万鑫动物药业有限公司
成都市腾飞动物药业有限公司
潍坊富邦药业有限公司 山东天振药业有限公司
山西美默克生物科技有限公司
郑州爱诺生物科技有限公司 河南三和动物药业有限公司 四川佳泰动物药业有限公司 陕西格林德动物药业有限公司 江苏南农高科动物药业有限公司 湖南丹维生物科技有限公司 河北呈盛堂动物药业有限公司 哈尔滨宏达动物药品厂 济南澳利兽药制品有限公司 河南得康动物药业有限公司 河南普鑫生物科技有限公司 南京惠牧生物科技有限公司
五苓散 五皮散 烟酸诺氟沙星溶液 烟酸诺氟沙星溶液 烟酸诺氟沙星注射液 烟酸诺氟沙星注射液 盐酸林可霉素注射液 盐酸林可霉素注射液 盐酸林可霉素注射液 盐酸林可霉素注射液 盐酸林可霉素注射液 盐酸沙拉沙星可溶性粉
食品动物用兽用抗菌药物临床应用管理办法

食品动物用兽用抗菌药物临床应用管理办法前言近几年,使用抗菌药物的过度使用已导致抗药性菌株的快速增加,这对人类健康和食品安全等方面产生了严重的影响。
因此,严格管理食品动物用兽用抗菌药物的临床应用是防范和控制抗药菌株的重要措施之一。
本文将介绍食品动物用兽用抗菌药物临床应用的管理办法。
一、抗菌药物的分类抗菌药物是指对细菌、病毒、真菌等微生物有杀灭或抑制作用的药物。
根据不同的抗菌谱和药理作用,抗菌药物可分为广谱抗菌药物和狭谱抗菌药物两大类。
广谱抗菌药物适用于多种细菌感染,但易产生耐药性,狭谱抗菌药物适用于特定的细菌感染。
二、抗菌药物的临床应用管理原则1. 临床应用必须遵循临床诊断和抗菌药物应用指南,遵循科学、合理、规范的原则。
2. 抗菌药物的选择应以药敏试验为依据,根据抗菌药物的谱效和安全性、患者的个体差异、感染情况等综合因素,选择合适的抗菌药物。
3. 合理利用狭谱抗菌药物,尽量避免广谱抗菌药物过度使用。
4. 按照医生的处方购买使用抗菌药物,不得随意购买使用,更不得共享、买卖或赠送抗菌药物。
5. 用药过程中应注意药物不良反应和药物的相互作用。
三、抗菌药物的管理1. 应建立健全食品动物用兽用抗菌药物使用管理制度,建立医疗机构和非医疗机构的应用管理机构,并定期进行督导和检查。
2. 明确食品动物用兽用抗菌药物的使用范围和条件,制定科学、合理的使用方案,并记录使用情况。
3. 食品动物用兽用抗菌药物应在药店或有资质的药商处购买,不得在非法渠道购买。
4. 取得食品动物用兽用抗菌药物的单位和个人应当按规定报告使用情况,共同维护食品、环境和生态安全。
四、临床应用记录和追溯管理1. 医疗机构应当建立完整的患者临床应用记录,当患者出现不良反应、治疗失效等事件时应及时记录和报告。
2. 食品生产经营单位应建立完整的抗菌药物使用记录,并追溯抗菌药物使用情况,加强抗菌药物使用情况的信息公示。
五、处罚对违法使用食品动物用兽用抗菌药物的单位和个人,应予以行政处罚,并依法追究刑事责任。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
附件1
食品动物用兽用抗菌药物临床应用管理办法
(征求意见稿)
第一条为加强食品动物用兽用抗菌药物临床应用管理,控制动物源细菌耐药,保障动物疾病防治效果、动物产品质量安全及公共卫生安全,根据《兽药管理条例》《执业兽医管理办法》和《兽用处方药和非处方药管理办法》等规定,制定本办法。
第二条本办法所称兽用抗菌药物是指防治细菌、支原体、衣原体、立克次体、螺旋体、真菌等病原微生物所致感染性疾病的药物,不包括防治各种病毒所致感染性疾病和寄生虫病的药物。
第三条农业部负责全国食品动物用兽用抗菌药物临床应用的监督管理。
县级以上地方人民政府兽医行政管理部门负责本行政区域内食品动物用兽用抗菌药物临床应用的监督管理。
第四条本办法适用于各级各类食品动物养殖场(户)兽用抗菌药物临床应用管理工作。
第五条兽用抗菌药物临床应用应当遵循保障动物健康,维护公共卫生安全和动物产品质量安全的原则。
第六条国家对兽用抗菌药物实行分级管理。
根据安全性、疗效、对动物感染治疗的重要性及细菌耐药性等因素,
将兽用抗菌药物分为非限制使用级、限制使用级、特殊使用级等三级。
具体分级标准如下:
(一)非限制使用级抗菌药物。
经长期兽医临床应用证明安全、有效,对动物严重感染治疗重要,细菌耐药性关注比较小的抗菌药物。
(二)限制使用级抗菌药物。
经长期兽医临床应用证明安全、有效,对动物严重感染治疗高度重要,细菌耐药性关注比较大的抗菌药物。
(三)特殊使用级抗菌药物。
具有以下情形之一的:对动物具有明显或者严重不良反应,不宜随意使用的;对动物严重感染治疗极为重要的;细菌耐药性受到高度关注的;上市不足5 年的抗菌药物新品种。
第七条养殖场(户)应依据有关法律、法规、规章的相关规定制定本机构《兽用抗菌药物临床应用管理办法实施细则》、建立兽用抗菌药物临床应用评估与持续改进制度。
第八条养殖场(户)应当严格执行《兽用处方药和非处方药管理办法》,加强对抗菌药物遴选、采购、处方、调剂、兽医临床应用和药物评价的管理。
第九条养殖场(户)抗菌药物采购目录(包括采购抗菌药物的品种、剂型和规格)应向其所在地县级以上兽医行政管理部门备案。
第十条养殖场(户)应当建立抗菌药物遴选和定期评估制度。
对存在安全隐患、疗效不确定、耐药性严重等情况
的抗菌药物品种,应当予以清退或者更换。
清退或者更换的抗菌药物品种原则上6个月内不得进入本机构药物采购供应目录。
第十一条养殖场(户)应当实施国家兽用抗菌药物临床应用分级管理制度。
第十二条国家将对兽医技术人员兽用抗菌药物临床应用知识和规范化管理进行培训和考核,内容至少应当包括:(一)《兽药管理条例》《执业兽医管理办法》《兽用处方药和非处方药管理办法》等法律、法规、规章和规范性文件;
(二)兽用抗菌药物临床应用及管理制度;
(三)细菌耐药性及抗菌药物相互作用;
(四)抗菌药物不良反应监测与报告。
第十三条农业部开展细菌耐药监测工作,建立全国兽用抗菌药物临床应用监测网,对全国兽用抗菌药物临床应用和细菌耐药情况进行监测,开展临床应用质量管理与控制工作,定期发布细菌耐药信息,建立细菌耐药预警机制,采取相应措施。
第十四条养殖场(户)应当根据细菌培养及药敏试验结果选择使用抗菌药物。
在细菌培养及药敏试验或相关替代试验之前,对于已知的或怀疑为细菌感染的初期治疗,可选用非限制使用级抗菌药物。
经过细菌培养及药敏试验,综合考虑患病动物和感染因素,认为没有合适的非限制使用级抗菌药物可用时,可选用限制使用级抗菌药物。
经过细菌培养及药敏试验,认为感染属于严重威胁动物和种群的生命,并且选用后预期对治疗结果有积极影响时,可选用特殊使用级抗菌药物。
第十五条养殖场(户)应当开展抗菌药物临床应用监测工作,分析本机构抗菌药物使用情况,评估抗菌药物使用适宜性;有条件的应对抗菌药物使用趋势进行分析,对抗菌药物不合理使用情况应当及时采取有效干预措施。
第十六条养殖场(户)应当对接受抗菌药物治疗的患病动物采集微生物样本进行敏感性试验,样本送农业部动物源性耐药性监测机构检验,送检率不得低于10%。
建立细菌耐药预警机制,采取以下相应措施。
(一)对主要目标细菌耐药率超过30%的抗菌药物,应当参照药敏试验结果选用。
(二)对主要目标细菌耐药率超过50%的抗菌药物,应当予以警示,经验使用抗菌药物应当谨慎。
(三)对主要目标细菌耐药率超过75%的抗菌药物,应当暂停临床应用,根据追踪细菌耐药监测结果,再决定是否恢复临床应用。
第十七条养殖场(户)有义务配合农业部动物源性细菌耐药性监测的采样和用药调查,并上报抗菌药物应用情
况。
第十八条县级以上兽医行政管理部门应当加强对本行政区域内养殖场(户)兽用抗菌药物临床应用情况的监督检查。
第十九条兽医行政管理部门工作人员依法对养殖场(户)兽用抗菌药物临床应用情况进行监督检查时,应当出示证件;被检查养殖场(户)应当予以配合,提供必要的资料,不得拒绝、阻碍和隐瞒。
第二十条养殖场(户)有下列情形之一的,由县级以上兽医行政管理部门责令限期改正:
(一)未建立抗菌药物管理相关的规章制度,兽用抗菌药物临床应用管理混乱的;
(二)未按照本办法规定执行抗菌药物分级管理、兽医师抗菌药物处方权限管理,未配备相关专业技术人员的;
(三)未按有关兽药使用规定进行记录的;
(四)违反本办法相关规定造成严重后果的。
第二十一条养殖场(户)应当对以下兽用抗菌药物临床应用的异常情况开展调查,并根据不同情况做出处理:(一)使用量异常增长的抗菌药物;
(二)使用效果不佳的抗菌药物;
(三)耐药性异常增加的抗菌药物;
(四)频繁发生严重不良反应的抗菌药物。
第二十二条执业兽医出现下列情形之一的,养殖场
(户)应当取消其抗菌药物处方权:
(一)抗菌药物使用知识培训考核不合格的;
(二)未按照规定开具抗菌药物处方造成严重后果的;
(三)未按照规定使用抗菌药物造成严重后果的;
(四)开具抗菌药物处方牟取不当利益的。
第二十三条本办法自20xx年x月x日起施行。
