常用缓冲溶液的配制方法-实用篇
常用缓冲溶液配制方法

常用缓冲溶液的配制方法1.甘氨酸–盐酸缓冲液(0.05mol/L)X毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)X毫升0.2 mol/L邻苯二甲酸氢钾 + 0.2 mol/L HCl,再加水稀释到20毫升邻苯二甲酸氢钾分子量 = 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液24Na2HPO4·2H2O分子量 = 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量 = 210.14,0.1 mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液溶液或浓盐酸调节,冰箱保存。
5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L)柠檬酸C6H8O7·H2O:分子量210.14,0.1 mol/L溶液为21.01克/升。
柠檬酸钠Na3 C6H5O7·2H2O:分子量294.12,0.1 mol/L溶液为29.41克/毫升。
7.磷酸盐缓冲液Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液为85.61克/升。
Na 2HPO 4·12H 2O 分子量 = 358.14,0.2 mol/L 溶液为71.628克/升。
NaH 2PO 4·2H 2O 分子量 = 156.01,0.2 mol/L 溶液为31.202克/升。
磷酸盐是生物化学研究中使用最广泛的一种缓冲剂,由于它们是二级解离,有二个pKa 值,所以用它们配制的缓冲液,pH 范围最宽:NaH 2PO 4: pKa1=2.12,pKa2=7.21; Na 2HPO 4:pKa1=7.21,pKa2=12.32配酸性缓冲液:用NaH 2PO 4,pH =1~4,配中性缓冲液:用混合的两种磷酸盐,pH =6~8, 配碱性缓冲液:用Na 2HPO 4,pH =10~12。
常用缓冲溶液配制方法

常用缓冲溶液配制方法一、酸碱配制法:该方法通过酸和碱两种溶液的混合反应来控制溶液的pH值。
常用的酸碱配制法有以下几种:1.酸和碱的摩尔比例法:前提是需要知道所配制溶液的酸碱消耗量。
首先分别测量酸和碱的摩尔消耗量,然后按照摩尔比例混合酸和碱的溶液。
例如,如果酸的摩尔消耗量为1mol,碱的摩尔消耗量为1.5mol,则将1mol酸和1.5mol碱混合配制成缓冲溶液。
2.浓度法:通过将已知浓度的酸和碱溶液混合配制成缓冲溶液。
首先确定所需缓冲溶液的pH值和酸碱消耗量,然后调整酸和碱溶液的浓度,最后按照一定的体积比例混合两种溶液。
二、配制法控制pH值:该方法根据所需缓冲溶液的pH值,通过使用酸和碱的不同混合配比来控制溶液的pH值。
常用的方法有以下几种:1.酸碱体积法:根据Henderson-Hasselbalch方程,通过将酸和碱的体积按照一定比例混合配制成缓冲溶液。
对于酸性缓冲溶液,通常用酸体积除以碱体积;对于碱性缓冲溶液,通常用碱体积除以酸体积。
2.四倍溶液法:如果需要配制缓冲溶液的pH值为pHx,可以制备pH(x-1)和pH(x+1)的四倍浓度溶液,在适当比例下混合这两种溶液,可以得到所需pH值的缓冲溶液。
三、缓冲剂配制法:缓冲剂是一种特殊的溶液,能够在酸和碱之间进行迅速的反应,稳定溶液的pH值。
常见的缓冲剂有磷酸盐缓冲剂、醋酸缓冲剂、碳酸氢盐缓冲剂等。
1.磷酸盐缓冲剂的配制方法:磷酸盐缓冲剂的配制,通常选择以二氢磷酸盐(H2PO4-)和氢磷酸盐(HPO42-)为主要组分。
根据所需pH值和缓冲溶液的酸碱消耗量,可以计算出所需H2PO4-/HPO42-的比例,然后按照一定的体积和浓度配制出满足比例的溶液。
2.醋酸缓冲剂的配制方法:醋酸缓冲剂的配制通常选择乙酸(CH3COOH)和乙酸钠(CH3COONa)为主要组分。
根据所需缓冲溶液的pH值和酸碱消耗量,可以计算出所需CH3COOH/CH3COONa的比例,然后按照一定的体积和浓度配制出满足比例的溶液。
常用缓冲溶液的配制方法
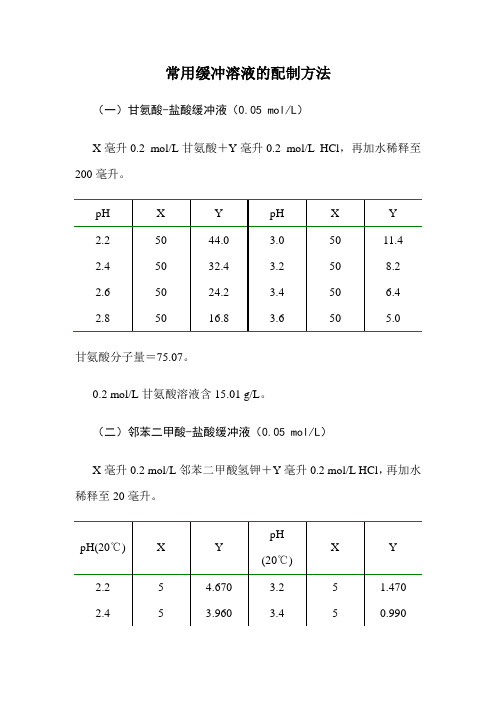
常用缓冲溶液的配制方法(一)甘氨酸-盐酸缓冲液(0.05 mol/L)X毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCl,再加水稀释至200毫升。
甘氨酸分子量=75.07。
0.2 mol/L甘氨酸溶液含15.01 g/L。
(二)邻苯二甲酸-盐酸缓冲液(0.05 mol/L)X毫升0.2 mol/L邻苯二甲酸氢钾+Y毫升0.2 mol/L HCl,再加水稀释至20毫升。
邻苯二甲酸氢钾分子量=204.23。
0.2 mol/L邻苯二甲酸氢钾溶液含40.85 g/L。
(三)磷酸氢二钠-柠檬酸缓冲液Na 2HPO 4分子量=141.98;0.2 mol/L 溶液为28.40 g/L 。
Na 2HPO 4·2H 2O 分子量=178.05;0.2 mol/L 溶液为35.61 g/L 。
Na 2HPO 4·12H 2O 分子量=358.22;0.2 mol/L 溶液为71.64 g/L 。
C 6H 8O 7·H 2O 分子量=210.14;0.1 mol/L 溶液为21.01 g/L 。
(四)柠檬酸-氢氧化钠-盐酸缓冲液①使用时能够每升中加入1克酚,若最后pH值有变化,再用少量50%氢氧化钠溶液或者浓盐酸调节,冰箱储存。
(五)柠檬酸-柠檬酸钠缓冲液(0.1 mol/L)柠檬酸:C6H8O7·H2O分子量=210.14 ;0.1 mol/L溶液为21.01 g/L。
柠檬酸钠:Na3C6H5O7·2H2O分子量=294.12 ;0.1 mol/L溶液为29.41 g/L。
(六)醋酸-醋酸钠缓冲液(0.2 mol/L)NaAc·3H2O分子量=136.09;0.2 mol/L溶液为27.22 g/L。
冰乙酸11.8 mL稀释至1 L(需标定)。
(七)磷酸二氢钾-氢氧化钠缓冲液(0.05 mol/L)X 毫升0.2 mol/L KH2PO4+Y毫升0.2 mol/L NaOH 加水稀释至20毫升。
50种缓冲液的配制

6.2
取2.1%柠檬酸水溶液,用50%氢氧化钠溶液调节pH值至6.2。
枸橼酸-磷酸氢二钠缓冲液
4.0
甲液:取枸橼酸21g或无水枸橼酸19.2g,加水使溶解成1000ml,置冰箱内保存。乙液:取磷酸氢二钠71.63g,加水使溶解成1000ml。取上述甲液61.45ml与乙液38.55ml混合,摇匀。
50
缓冲液
pH
配制
乙醇-醋酸铵缓冲液
3.7
取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml。
三羟甲基氨基甲烷缓冲液
8.0
取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8.0。
甲酸钠缓冲液
3.3
取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3.25~3.30。
邻苯二甲酸盐缓冲液
5.6
取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至5.6,加水稀释至1000ml,混匀。
氨-氯化铵缓冲液
8.0
取氯化铵1.07g,加水使溶解成100ml,再加稀氨溶液调节pH值至8.0。
氨-氯化铵缓冲液
10.0
取氯化铵5.4g,加水20ml溶解后,加浓氯溶液35ml,再加水稀释至100ml。
硼砂-氯化钙缓冲液
8.0
取硼砂0.572g与氯化钙2.94g,加水约800ml溶解后,用1mol/L盐酸溶液约2.5ml调节pH值至8.0,加水稀释至1000ml。
常见缓冲溶液配制方法

常见缓冲溶液配制方法缓冲溶液是一种能够维持溶液酸碱性质相对稳定的溶液。
常见的缓冲溶液配制方法主要包括四种:酸碱对配制、酸碱配制、水解配制和氧化还原配制。
下面将详细介绍这四种配制方法以及常用的缓冲体系。
一、酸碱对配制酸碱对配制是以两种酸碱的共存为基础实现的。
常用的酸碱对包括:醋酸与醋酸钠对、琼脂酸与琼脂酸钠对、乙酸与乙酸-乙酸钠对等。
以醋酸和醋酸钠为例:1.根据所需的pH值,计算所需的酸碱物质的摩尔量比例,使用化学计算方法可以得到这个比例。
2.首先,在一定体积(如100mL)的蒸馏水中加入醋酸的量,根据计算结果。
3.然后,在同样的蒸馏水中加入醋酸钠的量,根据计算结果。
在加入醋酸钠之前,需要校对酸碱物质的总体积是否是所需的目标体积,如果不是,可以再加入适量的蒸馏水进行调整。
4.经过充分搅拌混合后,缓冲溶液就制备好了。
最后,根据需求进行PH值校准。
二、酸碱配制酸碱配制是指利用单一酸或碱的酸碱性质与反应物种数之间的关系,通过精确配比计算得出所需的缓冲体系,使溶液能够保持所需的酸碱性质稳定。
常见的酸碱配制方法有:乙酸钠-盐酸、蒸馏水盐酸-碳酸钠等。
以乙酸钠-盐酸为例:1. 根据所需的pH值,计算所需的酸碱物质的摩尔量比例。
根据缓冲溶液配制公式 pKa=pH-log([A-]/[HA]),可以反推得到[HA]/[A-]的比例,其中[A-]代表酸根离子的浓度,[HA]代表不电离酸的浓度。
2.根据计算结果和所需体积,将乙酸钠溶液添加到蒸馏水中,同时滴加适量的盐酸溶液以调整pH值。
3.增加或减少乙酸钠和盐酸的量,直到所需的pH值达到要求。
三、水解配制水解是指酸碱反应中一种物质在水中发生分解产生酸和碱的反应。
通过精确配比计算得出所需的缓冲体系,既可以保持所需的酸碱性质稳定,又可以实现水解反应的产物稳定。
常见的水解配制方法有:磷酸盐缓冲液、硼酸缓冲液、胸腺嘧啶缓冲液等。
以硼酸缓冲液为例:1.将一定体积(如100mL)的蒸馏水倒入容器中。
(最全)常见缓冲溶液配制方法

常见缓冲溶液配制方法乙醇-醋酸铵缓冲液(pH3.7):取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml。
三羟甲基氨基甲烷缓冲液(pH8.0):取三羟甲基氨基甲烷,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8.0。
三羟甲基氨基甲烷缓冲液(pH8.1):取氯化钙,,用1mol/L盐酸溶液调节pH值至8.1,加水稀释至100ml。
三羟甲基氨基甲烷缓冲液(pH9.0):取三羟甲基氨基甲烷,加盐酸赖氨酸,氯化钠,乙二胺四醋酸二钠,再加水溶解使成1000ml,调节pH值至9.0。
乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液4.2ml,再用水稀释至250ml。
巴比妥缓冲液(pH7.4):取巴比妥钠,加水使溶解并稀释至400ml,,滤过。
巴比妥缓冲液(pH8.6):取巴比妥与巴比妥钠,加水使溶解成2000ml。
巴比妥-氯化钠缓冲液(pH7.8):取巴比妥钠,加氯化钠及水适量使溶解,另取明胶加水适量,加热溶解后并入上述溶液中。
然后用0.2mol/L盐酸溶液调节pH值至7.8,再用水稀释至500ml。
甲酸钠缓冲液(pH3.3):取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再参加2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3.25~3.30。
邻苯二甲酸盐缓冲液(pH5.6):取邻苯二甲酸氢钾10g,加水稀释至1000ml,混匀。
枸橼酸盐缓冲液:取枸橼酸,加1mol/L的20%乙醇制氢氧化钠溶液40ml使溶解,再用20%乙醇稀释至100ml。
枸橼酸盐缓冲液(pH6.2):取2.1%枸橼酸水溶液,用50%氢氧化钠溶液调节pH值至6.2。
枸橼酸-磷酸氢二钠缓冲液(pH4.0):甲液:取枸橼酸21g或无水枸橼酸,加水使溶解成1000ml,置冰箱内保存。
缓冲液配制方法
25.5
5.8
42.3
4.5
8.7
5.2
28.8
5.9
43.7
4.6
11.1
5.3
31.6
4.7
13.6
5.4
34.1
邻苯二甲酸氢钾Mr = 204.23,0.1mol/L溶液为20.42g/L
9.磷酸盐缓冲液
(1)磷酸氢二钠—磷酸二氢钠缓冲液(0.2mol/L)
pH
0.2mol/L
Na2HPO4/ml
pH
Na+浓度
/mol/L
柠檬酸/g
C6H8O7·H2O
氢氧化钠/g
NaOH(97%)
盐酸/ml
HCl(浓)
最终体积/L*
2.2
0.20
210
84
160
10
3.1
0.20
210
83
116
10
3.3
0.20
210
83
106
10
4.3
0.20
210
83
45
10
5.3
0.35
245
144
68
10
5.8
0.45
50
11.0
10.0
50
43.0
9.6
50
23.0
10.1
50
46.0
硼砂Na2B4O7·10H2O,Mr = 381.43,0.05mol/L溶液为19.07g/L
硼砂/ml
0.2mol/L
硼酸/ml
7.4
1.0
9.0
8.2
3.5
6.5
7.6
1.5
常用缓冲溶液的配制方法
常用缓冲溶液的配制方法缓冲溶液是一种能够稳定溶液酸碱度的溶液,是化学和生物学实验中必不可少的试剂。
它们能够在一定范围内抵抗外界酸碱变化,保持溶液的PH值稳定,从而确保实验结果的准确性和可重复性。
本文将介绍一些常用的缓冲溶液的配制方法。
一、醋酸酸钠缓冲溶液醋酸酸钠缓冲溶液适用于酸性条件下的实验。
它的PH值稳定在4.0左右,适用于生物学实验和某些化学分析。
配制方法:1.称取3.9克醋酸酸钠三水合物(CH3COONa·3H2O)并溶解在80毫升蒸馏水中。
2.加入相同质量的冰乙酸,溶解均匀。
3.用蒸馏水稀释至100毫升。
将溶液过滤或使用磁力搅拌器搅拌,使溶液变得均匀。
二、磷酸二氢钠/磷酸氢二钠缓冲溶液磷酸二氢钠/磷酸氢二钠缓冲溶液适用于酸性至中性条件下的实验。
它的PH值稳定在6.8-7.4范围内,适用于细胞培养和某些生物化学实验。
配制方法:1.称取磷酸二氢钠(NaH2PO4)7.5克并溶解在200毫升蒸馏水中。
2.用氢氧化钠(NaOH)溶液调节至PH值7.4。
3.将溶液稀释至250毫升。
使用磁力搅拌器搅拌溶液使其均匀。
三、碳酸氢钠/碳酸钠缓冲溶液碳酸氢钠/碳酸钠缓冲溶液适用于中性至碱性条件下的实验。
它的PH值稳定在9.6-11.0范围内,适用于某些酶反应和某些化学分析。
配制方法:1.称取2.54克碳酸氢钠(NaHCO3)和2.93克碳酸钠(Na2CO3)并溶解在200毫升蒸馏水中。
2.使用酚红指示剂滴定硫酸(H2SO4)溶液,直至PH值为10.0。
3.将溶液稀释至250毫升。
使用磁力搅拌器搅拌溶液使其均匀。
四、Tris缓冲溶液Tris缓冲溶液适用于酸性至中性条件下的实验。
它是一种常用的生物化学缓冲溶液,适用于DNA/RNA电泳和蛋白质电泳等实验。
配制方法:1.称取12.11克Tris氨基甲烷(Tris base)并溶解在800毫升蒸馏水中。
2.使用盐酸(HCl)溶液调节至PH值 7.4。
3.加入1克EDTA四钠盐并溶解。
缓冲溶液【(最全)常见缓冲溶液配制方法】
缓冲溶液【(最全)常见缓冲溶液配制方法】缓冲溶液【(最全)常见缓冲溶液配制方法】常见缓冲溶液配制乙醇-醋酸铵缓冲液(pH3.7):取5mol/L醋酸溶液15.0ml,加乙醇60ml和水20ml,用10mol/L氢氧化铵溶液调节pH值至3.7,用水稀释至1000ml。
三羟甲基氨基甲烷缓冲液(pH8.0):取三羟甲基氨基甲烷12.14g,加水800ml,搅拌溶解,并稀释至1000ml,用6mol/L盐酸溶液调节pH值至8.0。
三羟甲基氨基甲烷缓冲液(pH8.1):取氯化钙0.294g,加0.2mol/L 三羟甲基氨基甲烷溶液40ml使溶解,用1mol/L盐酸溶液调节pH值至8.1,加水稀释至100ml。
三羟甲基氨基甲烷缓冲液(pH9.0):取三羟甲基氨基甲烷6.06g,加盐酸赖氨酸3.65g,氯化钠5.8g,乙二胺四醋酸二钠0.37g,再加水溶解使成1000ml,调节pH值至9.0。
乌洛托品缓冲液:取乌洛托品75g,加水溶解后,加浓氨溶液4.2ml,再用水稀释至250ml。
巴比妥缓冲液(pH7.4):取巴比妥钠4.42g,加水使溶解并稀释至400ml,用2mol/L盐酸溶液调节pH值至7.4,滤过。
巴比妥缓冲液(pH8.6):取巴比妥5.52g与巴比妥钠30.9g,加水使溶解成2000ml。
巴比妥-氯化钠缓冲液(pH7.8):取巴比妥钠5.05g,加氯化钠3.7g 及水适量使溶解,另取明胶0.5g加水适量,加热溶解后并入上述溶液中。
然后用0.2mol/L盐酸溶液调节pH值至7.8,再用水稀释至500ml。
甲酸钠缓冲液(pH3.3):取2mol/L甲酸溶液25ml,加酚酞指示液1滴,用2mol/L氢氧化钠溶液中和,再加入2mol/L甲酸溶液75ml,用水稀释至200ml,调节pH值至3.25~3.30。
邻苯二甲酸盐缓冲液(pH5.6):取邻苯二甲酸氢钾10g,加水900ml,搅拌使溶解,用氢氧化钠试液(必要时用稀盐酸)调节pH值至5.6,加水稀释至1000ml,混匀。
常见缓冲溶液配制方法
常见缓冲溶液配制方法1.醋酸/醋酸钠缓冲溶液:醋酸/醋酸钠缓冲溶液具有较宽的酸碱度范围,在生物化学以及分析化学实验中得到广泛应用。
其配制方法如下:(1)准备一定浓度的醋酸溶液,可以采用浓缩醋酸与适量的水混合而成。
(2)根据所需的缓冲溶液pH值,计算所需浓度的醋酸钠。
(3)将计算所需的醋酸钠溶解在适量的去离子水中,得到所需的缓冲溶液。
2.磷酸盐缓冲溶液:磷酸盐缓冲溶液在生物化学以及分子生物学实验中常用于维持pH值。
以下介绍两种常见的磷酸盐缓冲溶液的配制方法:(1)磷酸盐酸性缓冲液:-准备所需的酸性磷酸盐缓冲液,将一定量的二氢磷酸钠溶解在适量的去离子水中。
-根据所需的pH值,使用盐酸调节溶液的酸度,直至达到所需的pH 值。
(2)磷酸盐碱性缓冲液:-准备所需的碱性磷酸盐缓冲液,将一定量的氢磷酸二钠溶解在适量的去离子水中。
-根据所需的pH值,使用氢氧化钠调节溶液的碱性,直至达到所需的pH值。
3.碳酸盐缓冲溶液:碳酸盐缓冲溶液在一些生物化学实验中用于控制pH值。
以下介绍两种常见的碳酸盐缓冲溶液的配制方法:(1)酸性碳酸盐缓冲液:-准备所需的酸性碳酸盐缓冲液,将一定量的二氧化碳通过气体输注器向含有一定浓度的NaHCO3溶液中通入,直至溶液中的二氧化碳饱和。
(2)碱性碳酸盐缓冲液:-准备所需的碱性碳酸盐缓冲液,将一定量的Na2CO3溶解在适量的去离子水中。
4.三氯乙酸/氯化钾缓冲溶液:三氯乙酸/氯化钾缓冲溶液在DNA和RNA等生物大分子的提取和纯化过程中常用作酶及细胞的裂解缓冲液。
以下是常见的三氯乙酸/氯化钾缓冲溶液的配制方法:(1)将一定量的三氯乙酸和氯化钾溶解在适量的去离子水中,混合均匀。
(2)根据所需的缓冲溶液pH值,使用醋酸或氢氧化钾调节溶液的pH 值,直至达到所需的pH值。
5.甘氨酸缓冲溶液:甘氨酸缓冲溶液在生物化学实验中常用于维持pH值,并在一些药物的制剂和生物制品的稳定性中得到应用。
以下是甘氨酸缓冲溶液的配制方法:(1)准备一定浓度的甘氨酸溶液,将甘氨酸与适量的去离子水溶解。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
磷酸盐缓冲液 (1)磷酸氢二钠-磷酸二氢钠缓冲液(0.2mol ·L -1
)
Na 2HPO 4·2H 2O 分子量=178.05; 0.2mol·L -1
溶液为35.61 g·L -1。
Na 2HPO 4·12H 2O 分子量=358.22; 0.2mol·L
-1
溶液为71.64 g·L -1。
NaH 2PO 4·H 2O 分子量=138.01; 0.2mol·L -1溶液为27.60 g·L -1。
NaH 2PO 4·2H 2O 分
子量=156.03; 0.2mol·L -1
溶液为31.21 g·L -1。
乙酸-乙酸钠溶液(0.2mol ·L -1
)
柠檬酸-柠檬酸钠缓冲液(0.1mol·L-1)
柠檬酸C6H8O7·H2O分子量=210.14;0.1mol·L-1溶液为21.01 g·L-1。
柠檬酸钠Na3C6H5O7·H2O分子量=294. 12;0.1mol·L-1溶液为29.41 g·L-1。
NaH2PO4•2H2O:10.86105g(或NaHPO4•12H2O:21.8502g)+ NaH2PO4•2H2O:6. 08595g(或NaH2PO4•H2O:10.76g),溶解,定容至1L
上述药品都是极易溶的,直接溶解就行了
附磷酸氢二钠-磷酸二氢钠缓冲液(0.2mol/L)
pH值;0.2mol/LNa2HPO4溶液(mL);0.2mol/LNaH2PO4溶液(mL)
5.8 ;8.0;92.0
5.9 ;10.0 ;90.0
6.0;12.3 ;8
7.7
6.1 ;15.0 ;85.0
6.2 ;18.5 ;81.5
6.3 ;22.5;7
7.5
6.4 ;26.5 ;73.5
6.5 ;31.5 ;68.5
6.6 ;3
7.5;62.5
6.7 ;43.5 ;56.5
6.8 ;49.0;51.0
6.9;55.0 ;45.0
7.0 ;61.0 ;39.0
7.1 ;67.0 ;33.0
7.2 ;72.0 ;28.0
7.3 ;77.0 ;23.0
7.4 ;81.0;19.0
7.5 ;84.0 ;16.0
7.6 ;87.0;13.0
7.7 ;89.5;10.5
7.8 ;91.5;8.5
7.9 ;93.5 ;7.5
8.0;94.7 ;5.3
NaH2PO4•2H2O:Mr=178.05,0.2mol/L溶液为35.61g/L; NaHPO4•12H2O:Mr=358.22,0.2mol/L溶液为71.64g/L;
NaH2PO4•2H2O:Mr=156.03,0.2mol/L溶液为31.21g/L;
NaH2PO4•H2O:Mr=138.01,0.2mol/L溶液为27.6g/L。
1.甘氨酸–盐酸缓冲液(0.05mol/L)
X毫升0.2 mol/L甘氨酸+Y毫升0.2 mol/L HCI,再加水稀释至200毫升
甘氨酸分子量 = 75.07,0.2 mol/L甘氨酸溶液含15.01克/升。
2.邻苯二甲酸–盐酸缓冲液(0.05 mol/L)
X毫升0.2 mol/L邻苯二甲酸氢钾 + 0.2 mol/L HCl,再加水稀释到20毫升
邻苯二甲酸氢钾分子量 = 204.23,0.2 mol/L邻苯二甲酸氢溶液含40.85克/升3.磷酸氢二钠–柠檬酸缓冲液
Na2HPO4分子量 = 14.98,0.2 mol/L溶液为28.40克/升。
Na2HPO4-2H2O分子量 = 178.05,0.2 mol/L溶液含35.01克/升。
C4H2O7·H2O分子量 = 210.14,0.1 mol/L溶液为21.01克/升。
4.柠檬酸–氢氧化钠-盐酸缓冲液
①使用时可以每升中加入1克克酚,若最后pH值有变化,再用少量50% 氢氧化钠溶液或浓盐酸调节,冰箱保存。
②
5.柠檬酸–柠檬酸钠缓冲液(0.1 mol/L)
柠檬酸C6H8O7·H2O:分子量210.14,0.1 mol/L溶液为21.01克/升。
柠檬酸钠Na3 C6H5O7·2H2O:分子量294.12,0.1 mol/L溶液为29.41克/毫升。
6.乙酸–乙酸钠缓冲液(0.2 mol/L )
Na 2Ac·3H 2O 分子量 = 136.09,0.2 mol/L 溶液为27.22克/升。
7.磷酸盐缓冲液
(1)磷酸氢二钠–磷酸二氢钠缓冲液(0.2)
Na 2HPO 4·2H 2O 分子量 = 178.05,0.2 mol/L 溶液为85.61克/升。
Na 2HPO 4·2H 2
O 分子量 = 358.22,0.2 mol/L 溶液为71.64克/升。
Na 2HPO 4·2H 2O 分子量 = 156.03,0.2 mol/L 溶液为31.21克/升。
(2)磷酸氢二钠–磷酸二氢钾缓冲液(1/15 mol/L )
Na2HPO4·2H2O分子量 = 178.05,1/15M溶液为11.876克/升。
KH2PO4分子量 = 136.09,1/15M溶液为9.078克/升。
8.磷酸二氢钾–氢氧化钠缓冲液(0.05M)
X毫升0.2M K2PO4 + Y毫升0.2N NaOH加水稀释至29毫升
9.巴比妥钠-盐酸缓冲液(18℃)
巴比妥钠盐分子量=206.18;0.04M溶液为8.25克/升
10.Tris–盐酸缓冲液(0.05M,25℃)
50毫升0.1M三羟甲基氨基甲烷(Tris)溶液与X毫升0.1N盐酸混匀后,加水稀释至100毫升。
三羟甲基氨基甲烷(Tris)HOCH2 CH2OH
C
HOCH2 NH2
分子量=121.14;
0. 1M 溶液为12.114克/升。
Tris 溶液可从空气中吸收二氧化碳,使用时注意将瓶盖严。
11.硼酸–硼砂缓冲液(0.2M 硼酸根)
硼砂Na 2B 4O 7·H 2O,分子量=381.43;0.05M 溶液(=0.2M 硼酸根)含19.07克/升。
硼酸H 2BO 3,分子量=61.84,0.2M 溶液为12.37克/升。
硼砂易失去结晶水,必须在带塞的瓶中保存。
11.硼酸-硼砂缓冲液(0.2M 硼酸根)
硼砂Na 2B 4O 7·10H 2O,分子量=381.43;0.05M 溶液(=0.2M 硼酸根)含19.07克/升。
硼酸H 2BO 3,分子量=61.84, 0.2M 溶液为12.37克/升。
硼砂 易失去结晶水,必须在带塞的瓶中保存。
12.甘氨酸–氢氧化钠缓冲液(0.05M )
X 毫升0.2M 甘氨酸
+Y 毫升0.2NnaOH 加水稀释至200毫升 甘氨酸分子量=75.07;0.2M 溶液含15.01克/升。
13.硼砂-氢氧化钠缓冲液(0.05M 硼酸根)
X 毫升0.05M 硼砂+Y 毫升0.2NNaOH 加水稀释至200毫升 硼砂Na 2B 4O 7·10H 2O,分子量=381.43;0.05M 溶液为19.07克/升。
14.碳酸钠-碳酸氢钠缓冲液(0.1M )
Ca 2+、Mg 2+
存在时不得使用
Na 2CO 2·10H 2O 分子量=286.2;0.1M 溶液为28.62克/升。
N 2HCO 3分子量
=84.0;0.1M 溶液为8.40克/升。
15.“PBS”缓冲液。
