安徽师范大学2015年《913基础有机化学》考研专业课真题试卷
2015年安徽省高考化学试卷
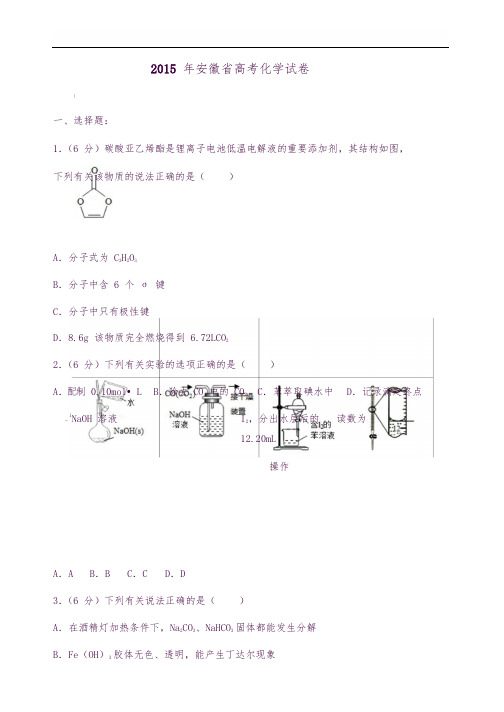
2015 年安徽省高考化学试卷一、选择题:1.(6 分)碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图,下列有关该物质的说法正确的是()A.分子式为 C3H 2 O3B.分子中含 6 个σ键C.分子中只有极性键D.8.6g 该物质完全燃烧得到 6.72LCO22.(6 分)下列有关实验的选项正确的是()A.配制0.10mol•L B.除去 CO 中的 CO2C.苯萃取碘水中D.记录滴定终点﹣1NaOH 溶液I2,分出水层后的读数为12.20mL操作A.A B.B C.C D.D3.(6 分)下列有关说法正确的是()A.在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解B.Fe(OH)3胶体无色、透明,能产生丁达尔现象C.H2、SO2、CO2三种气体都可用浓 H2SO4干燥D.SiO2既能和 NaOH 溶液反应又能和氢氟酸反应,所以是两性氧化物4.(6 分)下列有关 NaClO 和 NaCl 混合溶液的叙述正确的是()A.该溶液中,H+、NH4+、SO42﹣、Br﹣可以大量共存B.该溶液中,Ag+、K+、NO3﹣、CH3CHO 可以大量共存第 1 页(共22 页)C .向该溶液中滴入少量 FeSO 4 溶液,反应的离子方程式为:2Fe 2++ClO ﹣+2H +═Cl﹣+2Fe 3++H 20D .向该溶液中加入浓盐酸,每产生 1molCl 2,转移电子约为 6.02×1023 个 5.(6 分)等物质的量的 N 2(g )和 O 2(g )在恒容密闭容器中反应:N 2(g )+O 2 (g )⇌ 2NO (g ),下图曲线 a 表示该反应在 T ℃时 N 2 的浓度随时间的变化,曲 线 b 表示该反应在某一起始反应条件改变时 N 2 的浓度随时间的变化.下列叙述 正确的是()A .T ℃时,该反应的平衡常数 K=B .T ℃时,随着反应的进行,混合气体的密度减小C .曲线 b 对应的条件改变可能是加入了催化剂D .若曲线 b 对应的条件改变是温度,可判断该反应的△H <06.(6 分)某同学将光亮的镁条放入盛有 NH 4Cl 溶液的试管中,有大量气泡产生, 为探究该反应原理,该同学做了以下实验并观察到相关现象,由此得出的结论不 合理的是()选项 实验及现象结论A将湿润的红色石蕊试纸放在试管口,试 反应中有 NH 3 产生纸变蓝B 收集产生的气体并点燃,火焰呈淡蓝色 反应中有 H 2 产生C 收集气体的同时测得溶液的 pH 为 8.6 弱碱性溶液中 Mg也可被氧化D 将光亮的镁条放入 pH 为 8.6 的 NaHCO3弱碱性溶液中 OH﹣溶液中,有气泡产生氧化了 MgA.A B.B C.C D.D7.(6 分)25℃时,在 10mL 浓度均为 0.1mol•L﹣1 的 NaOH 和 NH3•H2O 混合溶液第 2 页(共22 页)中滴加 0.1mol•L﹣1 盐酸,下列有关溶液中粒子浓度关系正确的是()A.未加盐酸时:c(OH﹣)>c(Na+)=c(NH3•H2O)B.加入 10mL 盐酸时:c(NH4+)+c(H+)=c(OH﹣)C.加入盐酸至溶液 pH=7 时:c(Cl﹣)=c(Na+)D.加入 20mL 盐酸时:c(Cl﹣)=c(NH4+)+c(Na+)二、非选择题8.(14 分)C、N、O、Al、Si、Cu 是常见的六种元素.(1)Si 位于元素周期表第周期第族;(2)N 的基态原子核外电子排布式为;Cu 的基态原子最外层有个电子;(3)用“>”或“<”填空:原子半径电负性熔点沸点Al Si N O 金刚石晶体CH4SiH4硅(4)常温下,将除去表面氧化膜的 Al、Cu 片插入浓 HNO3中组成原电池(图 1),测得原电池的电流强度(I)随时间(t)的变化如图 2 所示,反应过程中有红棕色气体产生.0~t1时,原电池的负极是Al 片,此时,正极的电极反应式是,溶液中的H+向极移动.t1时,原电池中电子流动方向发生改变,其原因是.9.(16 分)四苯基乙烯(TPE)及其衍生物具有聚集诱导发光特性,在光电材料等领域应用前景广泛,以下是 TPE 的两条合成路线(部分试剂和反应条件省略):第 3 页(共22 页)(1)A 的名称是;试剂 Y 为;(2)B→C 的反应类型是;B 中官能团的名称是,D 中官能团的名称是;(3)E→F 的化学方程式是;(4)W 是 D 的同分异构体,具有下列结构特征:①属于萘()的一元取代物;②存在羟甲基(﹣CH2OH),写出W 所有可能的结构简式:;(5)下列说法正确的是.a、B 的酸性比苯酚强b、D 不能发生还原反应c、E 含有 3 种不同化学环境的氢d、TPE 既属于芳香烃也属于烯烃.10.(14 分)硼氢化钠(NaBH4)在化工等领域具有重要的应用价值,某研究小组采用偏硼酸钠(NaBO2)为主要原料制备 NaBH4,其流程如图:已知:NaBH4常温下能与水反应,可溶于异丙胺(沸点:33℃);(1)在第①步反应加料之前,需要将反应器加热至100℃以上并通入氩气,该操作的目的是,原料中的金属钠通常保存在中,实验室取用少量金属钠需要用到的实验用品有、、玻璃片和小刀等;(2)请配平第①步反应的化学方程式:第 4 页(共22 页)NaBO 2+SiO 2+ Na+ H 2 ═ NaBH 4+Na 2SiO 3(3)第②步分离采用的方法是 ;第③步分出 NaBH 4 并回收溶剂,采用的方法是;(4)NaBH 4(s )与 H 2O (l )反应生成 NaBO 2(s )和 H 2(g ).在 25℃、101kPa 下,已知每消耗 3.8gNaBH 4(s )放热 21.6kJ ,该反应的热化学方程式是.11.(14 分)某研究小组将纯净的 SO 2 气体通入 0.1mol •L ﹣1 的 Ba (NO 3)2 溶液中, 得到了 BaSO 4 沉淀.为探究上述溶液中何种微粒能氧化通入的 SO 2,该小组提出 了如下假设:假设一:溶液中的 NO 3﹣假设二:溶液中溶解的 O 2; (1)验证假设一该小组设计实验验证了假设一,请在下表空白处填写相关实验现象.实验步骤实验现象 结论实验 1:在盛有不含 O 2 的 25mL0.1mol •L ﹣1BaCl 2 溶假设一成立液的烧杯中,缓慢通入纯净的 SO 2 气体. 实验 2:在盛有不含 O 2 的 25mL0.1mol •L ﹣1Ba (NO 3)2溶液的烧杯中,缓慢通入纯净的 SO 2 气体(2)为深入研究该反应,该小组还测得上述两个实验中溶液 pH 随通入 SO 2 体积 的变化曲线如图.实验 1 中溶液 pH 变小的原因是 ;V 1 时,实验 2 中溶液 pH 小于实验 1 的原因是(用离子方程式表示).(3)验证假设二请设计实验验证假设二,写出实验步骤、预期现象和结论.实验步骤、预期现象和结论(不要求写具体操作过程):(4)若假设二成立,请预测:在相同条件下,分别用足量的 O 2 和 KNO 3 氧化相 同的 H 2SO 3 溶液(溶液体积变化忽略不计),充分反应后两溶液的 pH 前者 (填“大于”或“小于”)后者,理由是.第 5 页(共 22 页)第 6 页(共22 页)2015 年安徽省高考化学试卷参考答案与试题解析一、选择题:1.(6 分)碳酸亚乙烯酯是锂离子电池低温电解液的重要添加剂,其结构如图,下列有关该物质的说法正确的是()A.分子式为 C3H 2 O3B.分子中含 6 个σ键C.分子中只有极性键D.8.6g 该物质完全燃烧得到 6.72LCO2【分析】A、为有机物的结构简式,其中顶点省略的是 C 原子,每个 C 原子均形成 4 对共价键,每个 O 原子形成 2 对共价键,C 原子价键不饱和的用 H 原子补充,据此判断分子式;B、单键即为σ键,依据此结构简式判断σ键的个数;C、相同原子之间形成非极性共价键,不同原子之间形成极性共价键,据此解答;D、依据 C 的完全燃烧产物为二氧化碳,依据此有机物物质的量判断标准状况下生成二氧化碳的体积.【解答】解:A、,此有机物中含有 3 个 C、3 个 O 和 2 个 H,故分子式为:C3H2O3,故 A 正确;B、此分子中存在 4 个 C﹣O 键、1 个 C=O 双键,还存在 2 个 C﹣H 键,1 个 C=C 双键,总共 8 个σ键,故 B 错误;第7 页(共22 页)C、此有机物中存在 C=C 键,属于非极性共价键,故 C 错误;D、8.6g 该有机物的物质的量为:=0.1mol,由于未指明标准状况,故生成的二氧化碳的体积不一定是 6.72L,故 D 错误,故选:A。
2015年淮北师范大学无机化学2015考研真题/研究生入学考试试题

---------------------------------------------------------------------------------------------------------------------------------------淮北师范大学2015年硕士研究生入学考试试题纸 第 1 页 共 4页 2015 年硕士研究生入学考试试题(A)科目名称: 无机化学 科目代码: 831注:答案必须写在答题纸上,写在本试题纸上的无效!--------------------------------------------------------------------------------------------------------------------一、是非题(对的打√号,错的打×号)(本大题共10小题,每小题2分,共20分)1、H 3BO 3中有三个氢,因此是三元弱酸。
( )2、在周期表中,处于对角线位置的元素性质相似,称为对角线规则。
( )3、CuX 2的稳定性按的 Cl- Br- I- CN-顺序增加。
( )4、σ键总是比π键的键能小。
( )5、XeF 2是直线型分子。
( )6、AgCl 溶解在NH 3水溶液中是盐效应的作用。
( )7、CaH 2便于携带,与水分解放出H 2,故野外常用它来制取氢气。
( )8、向CuSO 4溶液中滴加KI 溶液,生成棕色的CuI 沉淀。
( )9、配位化合物中配位体数和配位数一定相等。
( )10、用AgNO 3溶液这一试剂能将NaCl 、Na 2S 、K 2CrO 4、Na 2S 2O 3、Na 2HPO 4五种物质区分开来。
( )二、填充题(根据题意,在下列各题横线处,填上正确的文字,符号或数值)(本大题共5小题,每空2分,共20分)1、某元素基态原子失去3个电子后,3d 轨道半充满,其原子序数为 , 它在第 周期, 族,属于 区元素。
安徽师范大学高分子化学考研复习题及答案

专业课复习资料(最新版)封面高分子化学-复习题1选择填空,计算,简答,合成及反应式,名词解释,结构式及用途,公式推导选择填空☆表征引发剂活性的参数是()⑴kp(⑵t1/2⑶ki☆下列烯烃中不能进行自由基均聚的是()A)CH2=CCL2B)CH2=CHCN C)CH2=CHCH3☆能自由基聚合的单体是()。
A)CH2=C(CN)2B)CH2=CH-OCOCH3C)CH2=C(CH3)2☆一般不发生诱导分解的引发剂是()A)过氧化苯甲酰B)偶氮二异丁腈C)过氧化氢异丙苯☆易发生热聚合的单体是()A)丙烯酸B)丙烯腈C)苯乙烯☆欲在30度下进行苯乙烯的本体聚合反应,引发剂应选择()A)BPO B)过氧化氢+FeSO4C)BPO+二甲基苯胺☆聚合时主要以链转移方式终止的单体是()A)苯乙烯B)甲基丙烯酸甲酯C)氯乙烯☆苯乙烯进行自由基溶液聚合,在()溶剂中所得聚苯乙烯分子量最大A)四氯化碳B)苯C)乙苯☆单体是聚合物的最好良溶剂是()A)甲基丙烯酸甲酯B)苯乙烯C)丙烯腈☆进行自由基本体聚合时,出现自加速现象最早的是()A)苯乙烯B)甲基丙烯酸甲酯C)氯乙烯☆()可溶于对应的单体中A)聚氯乙烯B)聚丙烯腈C)聚苯乙烯☆偶合终止比歧化终止时聚合度分布()A)宽B)窄C)相同☆下列体系聚合时,发现有一个体系,聚合物的数均聚合度与引发剂用量无关,这是()A)氯乙烯+过氧化苯甲酰B)丙烯腈+偶氮二异丁腈C)甲基丙烯酸甲酯+过氧化苯甲酰+PhN(CH3)2☆工业生产中控制聚氯乙烯分子量的常用方法是()A)改变引发剂量B)改变温度C)添加分子量调节剂☆引发剂引发自由基聚合,提高反应温度,聚合物分子量()A)增大B)降低C)不变☆自动加速效应会使分子量分布()A)变宽B)变窄C)不变☆典型自由基聚合反应速率与引发剂浓度呈1/2级关系,表明聚合反应机理为()A)单基终止B)双基终止C)引发剂分解产生两个自由基☆在乙酸乙烯酯的自由基聚合反应中加入少量苯乙烯,会发生()A)聚合反应加速;B)聚合反应停止;C)聚合反应速度不变☆()共聚时,共聚物组成始终与单体组成一致;()共聚时,共聚物组成与单体组成无关A)交替共聚B)理想共聚C)恒比共聚☆Q值相差不大,e值相差越远的两个单体越易()A)交替共聚B)理想共聚C)恒比共聚☆苯乙烯加醋酸乙烯酯不能很好共聚合是由于()A)Q值相差太大B)Q值相差太小C)e值相差太大☆Q-e概念可以用于()A)预测单体共聚合反应的竞聚率B)计算自由基的平均寿命C)计算共聚物的组成☆当用活性负离子聚合制备甲基丙烯酸甲酯(MMA)苯乙烯(S)和丙烯腈(AN)三嵌段共聚物时,加料顺序为(),按列出顺序加入A)MMA,S,AN B)S,MMA,AN C)AN,S,MMA☆当M1/M2=50/50进行共聚时,所得共聚物中M1和M2具有相同序列长度分布的共聚体系是()A)r1=r2=0。
2015年东北师范大学研究生入学考试有机化学真题

东北师范大学研究生入学考试有机化学真题2015年(总分:150.00,做题时间:120分钟)一、用系统命名法命名下列化合物或写出化合物结构(有立体构型的化合物请标明)(总题数:5,分数:0.00)1.(分数:2.00)___________________________________________________________ _______________________________正确答案:((1R,3R)-1-甲基-1-乙基-3-异丙基环己烷)解析:2.(分数:2.00)___________________________________________________________ _______________________________正确答案:(2,3-二氯丁二酰胺)解析:3.(分数:2.00)___________________________________________________________ _______________________________正确答案:(2-甲基-2,3-环氧丁酸乙酯)解析:4.(分数:2.00)___________________________________________________________ _______________________________正确答案:(6-甲基-4-硝基喹啉)解析:5. NBS(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:二、选择题(总题数:10,分数:0.00)1. 下列反应中间体最稳定的是______A.B.C.D.(分数:2.00)A.AB.BC.CD.D √解析:2. 下列反应获得过Nobel奖的是______(分数:2.00)A.Micheal AdditionB.Grignard Reagent √C.CODe RearrangementD.Aldol Condensation解析:3. 下列化合物最容易与HCN发生反应的是______(分数:2.00)A.PhCH2CHO √B.PhCOCH3C.CF3COCH3D.CH3COCH3解析:4. 下列化合物中碱性最强的是______A.B.C.D.(分数:2.00)A.AB.BC.CD.D √解析:5. 下列化合物中H a和H b磁不等价的是______A.B.C.D.(分数:2.00)A.AB.BC.CD.D √解析:6. 下列化合物酸性最强的是______(分数:2.00)A.NO2CH2COOH √B.CH3SO2CH2COOHC.CH3COOHD.ClCH2COOH解析:7. 下列试剂亲核性最强的是______ (分数:2.00)A.RO-√B.HO-C.ROHD.H2O解析:8. 下列共振极限式中最稳定的是______A.B.C.D.(分数:2.00)A.A √B.BC.CD.D解析:9. 下列化合物具有芳香性的是______ (分数:2.00)A.四氢吡咯B.吡啶-N-氧化物√C.六氢吡啶D.四氢吡咯解析:10. 下列化合物不属于单糖的是______(分数:2.00)A.葡糖糖B.果糖C.麦芽糖√D.阿拉伯糖解析:三、完成下列反应,写主要产物,如涉及立体选择性需标明(总题数:10,分数:0.00)1.(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:2.(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:3.(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:4.(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:5.(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:6.(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:7.(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:8.(分数:2.00)_______________________________正确答案:()解析:9.(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:10.(分数:2.00)___________________________________________________________ _______________________________正确答案:()解析:四、设计一简单化学方法鉴别下列化合物(总题数:1,分数:0.00)1. A.甲酸B.乙酸C.乙醛D.丙酮E.乙醇(分数:10.00)___________________________________________________________ _______________________________正确答案:()解析:五、解释下列概念(总题数:3,分数:0.00)1. 差向异构体(分数:3.00)_______________________________正确答案:(在对映异构体中只有一个*C的构型不同,其他*C的构型均相同的异构体互为差向异构体。
