精选教育人教版九年级化学上册第三章课题2原子的结构(共48张)PPT课件
合集下载
新人教版九年级化学上册各课题PPT课件:第3单元课题2 原子的结构.ppt

解:标准=1.993×10-26kg×1/12=1.66×10-27kg
2.657×10-26kg
氧原子的相对原子质量=
=16
1.66×10-27kg
答:氧原子的相对原子质量是16。
20
3.相对原子质量与原子实际质量的关系 (1)相对原子质量_不__等__于___原子的实际质量,_是__个__比__值_ (2)原子实际质量越大,它的相对原子质量数值__越__大__ (3)相对原子质量的单位:_“__1_”__(_书__写__时__一__般__不__写__出__) 原子实际质量的单位是:____千__克______
B.核电荷数 D.质子数和中子数
4.下列五种微粒中易失去电子的是 A、D ,最易得到电子 的是 E , 具有相对稳定结构是 B、C 。
A +11 2 8 1 B +11 2 8
C +10 2 8
D +12 2 8 2
E +17 2 8 7
28
5.将①分子 ②原子 ③质子 ④中子 ⑤电子等粒子 用序号分别填入下列适当空格中: (1)构成物质的基本粒子是___①__②_______ (2)构成原子的基本粒子是___③__④__⑤_____ (3)显示电中性的粒子是____①__②__④______ (4)带正电的粒子是____③__________ (5)参加化学反应一定发生变化的粒子是___①______ (6)原子中数目一定相等的粒子是_____③__⑤________
失电子
17
三、相对原子质量
1.原子的实际质量
你获得的信息是什么?
几种原子的质量
原子种类 氢 氧 碳 铁
原子质量 1.67×10-27 kg 2.657×10-26 kg 1.993×10-26 kg 9.288×10-26 kg
人教版九年级化学第三单元课题2 原子的结构课件

“阳”)离子。
16 2 3.某粒子的结构示意图如图所示,则m= ,n= ,
8 S x= 。该粒子是
(填粒子的化学符号)
第3题图
第4题图
4.某粒子的结构示意图如图所示,若该粒子带2个
O 单位负电荷,它的化学符号是 2-;若该粒子带
Mg 2个单位正电荷,它的化学符号是 2+;若该
Ne 粒子不显电性,它的化学符号是
把电子在不同的区 域内运动的现象叫做 核外电子的分层排布
二、原子核外电子的排布
1、核外电子是分层排布的 电子层 一 二 三 四 五 六 七
K LMNO P Q
离核远近: 近
远
能量高低: 低
高
2.核外电子分层排布的规律(仅限前3层)
(1)先 “里”后“外” .(能量最低原则) (2)第一层最多排2个,第二层最多排8个;
1.原子是由居于原子中心、带_正__电__的原子核和 核外带_负__电__的电子构成,原子核是由_质__子__和 _中__子__构成。由于它们所带的电荷_相__等__,电性 _相_反__,所以整个原子_不__显__(填显或不显)电性。 2.能保持物质的化学性质的最小粒子是_分__子_; 化学变化中的最小粒子是_原__子__;原子中带正电 荷的粒子是_质子__和__原__子_核__;不显电性的粒子有 、 中子 、 分子 。 原子 3.据报道,1994年12月科学家发现了一种新元 素,它的原子核内有111个质子, 161个中子, 则该元素核外电子数是__1_1_1_ 。
。
四、相对原子质量(Ar)
粒子种类
电性
质量(kg)
质子
1个单位正电荷 1.6726×10-27
中子
不带电
1.6749×10-27
16 2 3.某粒子的结构示意图如图所示,则m= ,n= ,
8 S x= 。该粒子是
(填粒子的化学符号)
第3题图
第4题图
4.某粒子的结构示意图如图所示,若该粒子带2个
O 单位负电荷,它的化学符号是 2-;若该粒子带
Mg 2个单位正电荷,它的化学符号是 2+;若该
Ne 粒子不显电性,它的化学符号是
把电子在不同的区 域内运动的现象叫做 核外电子的分层排布
二、原子核外电子的排布
1、核外电子是分层排布的 电子层 一 二 三 四 五 六 七
K LMNO P Q
离核远近: 近
远
能量高低: 低
高
2.核外电子分层排布的规律(仅限前3层)
(1)先 “里”后“外” .(能量最低原则) (2)第一层最多排2个,第二层最多排8个;
1.原子是由居于原子中心、带_正__电__的原子核和 核外带_负__电__的电子构成,原子核是由_质__子__和 _中__子__构成。由于它们所带的电荷_相__等__,电性 _相_反__,所以整个原子_不__显__(填显或不显)电性。 2.能保持物质的化学性质的最小粒子是_分__子_; 化学变化中的最小粒子是_原__子__;原子中带正电 荷的粒子是_质子__和__原__子_核__;不显电性的粒子有 、 中子 、 分子 。 原子 3.据报道,1994年12月科学家发现了一种新元 素,它的原子核内有111个质子, 161个中子, 则该元素核外电子数是__1_1_1_ 。
。
四、相对原子质量(Ar)
粒子种类
电性
质量(kg)
质子
1个单位正电荷 1.6726×10-27
中子
不带电
1.6749×10-27
人教版初中化学九年级上册《3.2 原子的结构》课件(共37张PPT)
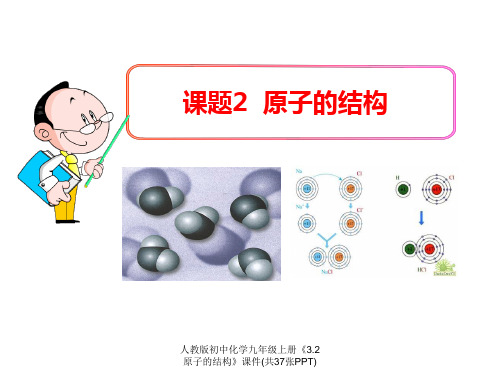
电子层
Si +14 2 8 4
该电子层上 的电子数
核电荷数、核内质子数
人教版初中化学九年级上册《3.2 原子的结构》课件(共37张PPT)
小试牛刀 • 请试试画出1-20号原子的结构示意图
• 请你分别找出稀有气体原子、金属原子、非金属 原子
• 看看它们的最外层电子数有什么特点
人教版初中化学九年级上册《3.2 原子的结构》课件(共37张PPT)
电子不超过2个。
人教版初中化学九年级上册《3.2 原子的结构》课件(共37张PPT)
1.分层排布(高速运动)
电子层 一 二 三 四 五 六 七
近
远
离核远近
能量高低 低
高
思考:如何直观、形象地表示电子的 分层排布呢?
人教版初中化学九年级上册《3.2 原子的结构》课件(共37张PPT)
原子核
原子结构示意图的意义
人教版初中化学九年级上册《3.2 原子的结构》课件(共37张PPT)
二、原子核外电子排布 原子核外电子是分层排布的。
原子的结构可以用原子结构示意图表示。
原子的核外电子排布,特别是最外层的电 子数目,跟原子的化学性质有密切关系。
原子通过得失电子达到8电子的稳定结构——离子
人教版初中化学九年级上册《3.2 原子的结构》课件(共37张PPT)
几种原子的构成
你的结论是什么?
原子种类 氢 碳 氧 钠 氯
质子数 1 6 8 11 17
中子数 0 6 8 12 18
核外电子数 1 6 8 11 17
(1) (2) (3) (4)
人教版初中化学九年级上册《3.2 原子的结构》课件(共37张PPT)
一、原子的构成
质子(带 电) 原子核
原子结构 第三课时 相对原子质量 课件(共34张PPT)-2024-2025学年人教版九年级化学上

2.5×10-6kg
1
玉米
2.5×10-4kg
100
花生
5×10-4kg
200
1. 你能一眼看出上表中四粒种子质量的相对大小吗? 2. 表中的倍数是以哪粒种子的质量做标准得来的?
3.比较原子的质量
一个氧原子的质量 一个氢原子的质量
= =
2.657×10-26kg ≈16
1.67×10-27kg
一个碳原子的质量 = 1.993×10-26kg 一个氢原子的质量 = 1.67×10-27kg ≈12
A.相对原子质量的单位是克 B.相对原子质量是质子质量与中子质量之和 C.相对原子质量就是原子的质量 D.相对原子质量是一个比值,它的国际单位为1
【解析】A、根据相对原子质量是有单位的,其单位为“1”,只不过 常省略而已,可知选项A说法不正确;B、根据相对原子质量=质子数十 中子数,可知选项B说法不正确;C、相对原子质量是一个原子的真实质 量跟一个碳1/12原子质量的1的比值,故选项C不正确; D、根据相对原 子质量是以一个碳-12原子质量的1/12作为标准,任何一个原子的真实 质量跟一个碳-12 原子质量的1/12 的比值,称为该原子的相对原
铝
13
14
13
27
铁
26
30
26
56
找规律:你能得到什么信息?
(1)核电荷数=核内质子数=核外电子 (2)相对原子质量≈质子数+中子数
即时理解
相对原子质量≈质子数+中子数,为什么?
1.决定原子质量大小的主要微粒是什么?
粒子种类
质量
质子
1.6726×10-27 kg
中子
1.6749×10-27 kg
秋人教版九年级化学上册课件:第三单元课题2原子的结构(共18张PPT)

第三单元课题2原子的构成
课题2 原子的结构
缺点:没有发现原子核
1909-1911年卢瑟福:用α粒子轰击金箔
现象:极少数α粒子被反弹
(撞击了带正电、质量大、体积小的 金原子核)
少数α粒子偏转
(途经金原子核附近时受到斥 力而稍微改变了运动方向)
大多数α粒子直线运动
(通过了原子内、原子间的空隙)
原
13、He who seize the right moment, is the right man.谁把握机遇,谁就心想事成。21.9.1121.9.1105:34:5705:34:57September 11, 2021 14、谁要是自己还没有发展培养和教育好,他就不能发展培养和教育别人。2021年9月11日星期六上午5时34分57秒05:34:5721.9.11 15、一年之计,莫如树谷;十年之计,莫如树木;终身之计,莫如树人。2021年9月上午5时34分21.9.1105:34September 11, 2021 16、教学的目的是培养学生自己学习,自己研究,用自己的头脑来想,用自己的眼睛看,用自己的手来做这种精神。2021年9月11日星期六5时34分57秒05:34:5711 September 2021 17、儿童是中心,教育的措施便围绕他们而组织起来。上午5时34分57秒上午5时34分05:34:5721.9.11
You have to believe in yourself. That's the secret of success. 人必须相信自己,这是成功的秘诀。
结论:
1. 原子一般都是由质子、中子、核外 电子构成 ,但有一种氢原子没有中子, 即并不是所有原子里都有中子 。
2. 核电荷数=质子数=核外电子数 (但不一定等于中子数)
课题2 原子的结构
缺点:没有发现原子核
1909-1911年卢瑟福:用α粒子轰击金箔
现象:极少数α粒子被反弹
(撞击了带正电、质量大、体积小的 金原子核)
少数α粒子偏转
(途经金原子核附近时受到斥 力而稍微改变了运动方向)
大多数α粒子直线运动
(通过了原子内、原子间的空隙)
原
13、He who seize the right moment, is the right man.谁把握机遇,谁就心想事成。21.9.1121.9.1105:34:5705:34:57September 11, 2021 14、谁要是自己还没有发展培养和教育好,他就不能发展培养和教育别人。2021年9月11日星期六上午5时34分57秒05:34:5721.9.11 15、一年之计,莫如树谷;十年之计,莫如树木;终身之计,莫如树人。2021年9月上午5时34分21.9.1105:34September 11, 2021 16、教学的目的是培养学生自己学习,自己研究,用自己的头脑来想,用自己的眼睛看,用自己的手来做这种精神。2021年9月11日星期六5时34分57秒05:34:5711 September 2021 17、儿童是中心,教育的措施便围绕他们而组织起来。上午5时34分57秒上午5时34分05:34:5721.9.11
You have to believe in yourself. That's the secret of success. 人必须相信自己,这是成功的秘诀。
结论:
1. 原子一般都是由质子、中子、核外 电子构成 ,但有一种氢原子没有中子, 即并不是所有原子里都有中子 。
2. 核电荷数=质子数=核外电子数 (但不一定等于中子数)
人教版九年级化学上册课件:3.2 原子的结构(共45张PPT)
观察下列原子的质量:
一个氢原子质量= 0.000000000000000000000000000167kg 一个氧原子质量= 0.0000000000000000000000000002657kg 一个碳原子质量= 0.00000000000000000000000000199kg
说一说你对上述数据的感觉。
汤姆逊1906年 获诺贝尔物理学奖
课题2 原子的结构
第三单元 物质构成的奥秘
电子的发现摧毁了“原子不 可再分”的观念,打开了通往原 子世界的大门,科学家们纷纷提 出了自己的原子结构模型......
课题2 原子的结构
第三单元 物质构成的奥秘
汤姆逊原子模型
原子是一个平均分布 着正电荷的粒子,其中镶 嵌着许多电子,中和了电 荷,形成了中性原子。原 子是一个球体,正电荷均 匀分布在整个球体内,电 子像面包里的葡萄干镶嵌 其中。
课题2 原子的结构
第三单元 物质构成的奥秘
【画一画】 请试着画出氧、镁、氩的原子结构示意图。
O
Mg
Ar
课题2 原子的结构
第三单元 物质构成的奥秘
以小组为单位认真研读图3-12部 分原子的结构示意图,回答:
稀有气体的原子结构有什么特点? 原子如何达到相对稳定结构?
课题2 原子的结构
第三单元 物质构稀成的有奥气秘 体原子: 最外层电子数为8(氦为2)
+1 1 相对稳定结构
最外层电子数为8,若只有一个电
氢H
子层则2电子稳定
+2 2
氦He
+3 2 1 +4 2 2 +5 2 3 +6 2 4 +7 2 5 +8 2 6 +9 2 7 +10 2 8
一个氢原子质量= 0.000000000000000000000000000167kg 一个氧原子质量= 0.0000000000000000000000000002657kg 一个碳原子质量= 0.00000000000000000000000000199kg
说一说你对上述数据的感觉。
汤姆逊1906年 获诺贝尔物理学奖
课题2 原子的结构
第三单元 物质构成的奥秘
电子的发现摧毁了“原子不 可再分”的观念,打开了通往原 子世界的大门,科学家们纷纷提 出了自己的原子结构模型......
课题2 原子的结构
第三单元 物质构成的奥秘
汤姆逊原子模型
原子是一个平均分布 着正电荷的粒子,其中镶 嵌着许多电子,中和了电 荷,形成了中性原子。原 子是一个球体,正电荷均 匀分布在整个球体内,电 子像面包里的葡萄干镶嵌 其中。
课题2 原子的结构
第三单元 物质构成的奥秘
【画一画】 请试着画出氧、镁、氩的原子结构示意图。
O
Mg
Ar
课题2 原子的结构
第三单元 物质构成的奥秘
以小组为单位认真研读图3-12部 分原子的结构示意图,回答:
稀有气体的原子结构有什么特点? 原子如何达到相对稳定结构?
课题2 原子的结构
第三单元 物质构稀成的有奥气秘 体原子: 最外层电子数为8(氦为2)
+1 1 相对稳定结构
最外层电子数为8,若只有一个电
氢H
子层则2电子稳定
+2 2
氦He
+3 2 1 +4 2 2 +5 2 3 +6 2 4 +7 2 5 +8 2 6 +9 2 7 +10 2 8
九年级化学第三章_课题2原子的结构_课件最新版

观察表格(表3-1),思考下列问题
原子种类 质子数 中子数 核外电子数 核电荷数 原子序数
1 0 1 1 1 氢 6 6 6 6 6 碳 8 8 8 8 8 氧 11 12 11 11 11 钠 17 18 17 17 17 氯 3. 质子数、中子数在数量上有什么关系?
质子数不一定等于中子数。
4.质子数、电子数、核电荷数、原子序数有什么联系?
8
S
16
2
第3题图 第4题图 4.某粒子的结构示意图如图所示,若该粒子带2个 2-;若该粒子带 单位负电荷,它的化学符号是 2+;若该 2个单位正电荷,它的化学符号是 粒子不显电性,它的化学符号是 。
O Mg Ne
四
相对原子质量(Ar) P56
粒子种 电性 质量(kg) 类 质子 1个单位正电荷 1.6726×10-27 中子 不带电 1.6749×10-27 阅读上表 (表3-2),能得出什么结论? 电子 1个单位负电荷 质子质量的 1/1836 1、质子和中子的质量很小且很接
标准碳原子质量的1/12 m总(质子) m总(中子) m总(电子) Ar= 1.66×10-27 + 1.66×10-27 + 1.66×10-27 x×m(质子) y×m(中子) x×m(电子) Ar= 1.66×10-27 + 1.66×10-27 + 1.66×10-27 x× 1.6726×10-27 y× 1.6749×10-27 Ar≈ 1.66×10-27 + 1.66×10-27
非金属原子
Cl
氯原子
得到电子
阴离子
Cl 8
氯离子 2S 8
得到 1个电子
得到 2个电子 得到 3个电子
人教版化学-九年级上册第三单元 课题2 原子的构成 [配套课件]
![人教版化学-九年级上册第三单元 课题2 原子的构成 [配套课件]](https://img.taocdn.com/s3/m/cd2a78a7a417866fb84a8edc.png)
2.相对原子质量是以一个碳 12 原子质量的___1_/1_2___为标 准,其他原子的质量与它相比较所得的比,作为这种原子的相
对原子质量,符号为____A_r ___ 。如氢原子的相对原子质量为 ____1____。
原子的结构
(1)原子核:体积很小,居于原子中心,但主要的质量集中 在原子核上。原子核由质子和中子构成,一个质子带一个单位 的正电荷,中子不带电。并非所有的原子核都含有质子和中子, 如氢原子(1H)无中子。
第四单元 物质构成的奥秘
课题 1 原子的构成
1.__原__子____是化学变化中的最小粒子,是由居于原子中心 的带____正____电的原子核和核外带___负_____电的___电__子___构成 的。原子核由___质__子___和___中__子___两种粒子构成。原子不显电 性,不同种类的原子,核内的__质__子__数__不同,核外的__电__子__数__ 也不同。
(2)核外电子:一个电子带一个单位的负电荷,质量很小, 在原子核外做高速运动。
原子中各粒子的关系
核电荷数=质子数=核外电子数 在原子核中质子数与中子数无直接关系。
[典例]下列有关原子的叙述,正确的是( ) A.原子是由不带电的粒子构成的 B.原子核都是由质子和中子构成的 C.原子里有相对很大的空间,电子在这个空间里做高速运 动
D.一个质子带一个单位正电荷,原子也带一个单位正电荷 思路点拨:原子核带正电,核外电子带负电,两者所带电
荷数相等,电性相反,对外呈电中性。注意氢原子(1H)无中子。 答案:C
相对原子质量
一个原子的实际质量 1.定义公式:相对原子质量(Ar)=一个碳 12 原子的质量× 1
12
2.近似计算式:相对原子质量=质子数+中子数 原子的质量与相对原子质量的比较
对原子质量,符号为____A_r ___ 。如氢原子的相对原子质量为 ____1____。
原子的结构
(1)原子核:体积很小,居于原子中心,但主要的质量集中 在原子核上。原子核由质子和中子构成,一个质子带一个单位 的正电荷,中子不带电。并非所有的原子核都含有质子和中子, 如氢原子(1H)无中子。
第四单元 物质构成的奥秘
课题 1 原子的构成
1.__原__子____是化学变化中的最小粒子,是由居于原子中心 的带____正____电的原子核和核外带___负_____电的___电__子___构成 的。原子核由___质__子___和___中__子___两种粒子构成。原子不显电 性,不同种类的原子,核内的__质__子__数__不同,核外的__电__子__数__ 也不同。
(2)核外电子:一个电子带一个单位的负电荷,质量很小, 在原子核外做高速运动。
原子中各粒子的关系
核电荷数=质子数=核外电子数 在原子核中质子数与中子数无直接关系。
[典例]下列有关原子的叙述,正确的是( ) A.原子是由不带电的粒子构成的 B.原子核都是由质子和中子构成的 C.原子里有相对很大的空间,电子在这个空间里做高速运 动
D.一个质子带一个单位正电荷,原子也带一个单位正电荷 思路点拨:原子核带正电,核外电子带负电,两者所带电
荷数相等,电性相反,对外呈电中性。注意氢原子(1H)无中子。 答案:C
相对原子质量
一个原子的实际质量 1.定义公式:相对原子质量(Ar)=一个碳 12 原子的质量× 1
12
2.近似计算式:相对原子质量=质子数+中子数 原子的质量与相对原子质量的比较
