5停留时间分布与反应器的流动模型
《反应工程》课程复习大纲

《化学反应工程》课程学习资料继续教育学院《化学反应工程》课程复习大纲一、考试要求本课程是一门专业课,要求学生在学完本课程后,能够牢固掌握本课程的基本知识,并具有应用所学知识说明和处理实际问题的能力。
据此,本课程的考试着重基本知识考查和应用能力考查两个方面,包括识记、理解、应用三个层次。
各层次含义如下:识记:指学习后应当记住的内容,包括概念、原则、方法的含义等。
这是最低层次的要求。
理解:指在识记的基础上,全面把握基本概念、基本原则、基本方法,并能表达其基本内容和基本原理,能够分析和说明相关问题的区别与联系。
这是较高层次的要求。
应用:指能够用学习过的知识分析、计算和处理涉及一两个知识点或多个知识点的会计问题,包括简单应用和综合应用。
二、考试方式闭卷笔试,时间120分钟三、考试题型●判断题:10%●选择题:15%●填空题:25%●简答题:10%●计算题:40%四、考核的内容和要求(基本要求、重点、难点)总要求:掌握反应器设计与分析的最基本原理和处理方法,了解化学反应工程的发展趋势和方向,初步具备对工业反应器进行设计与分析之能力。
第一章绪论基本要求:了解反应工程课程的性质、反应器的操作方式、反应器设计的基本方程和工业反应器的放大方法。
重点:化学反应及反应器的分类、反应器的操作方式。
一些重要的基本术语。
第二章反应动力学基础基本要求:掌握化学反应速率的不同表示方式及其相互关系;理解反应速率的浓度效应和温度效应;掌握复合反应体系中任一组分的消耗速率和生成速率的表达方法;掌握瞬时选择性的概念及其在反应器设计计算中的应用;掌握化学反应速率方程的变换与应用。
掌握定态近似及速率控制步骤的概念,学会推导多相催化反应速率方程的方法。
理解并列反应、平行反应和连串反应的动力学特征。
理解气体在固体催化剂表面上的吸附及吸附等温线,理解用实验确定反应速率方程的方法及由实验数据段动力学参数估值。
重点:化学反应速率的不同表示方式及其相互关系;复合反应体系中任一组分总的消耗速率和生成速率的表达方法;掌握瞬时选择性的概念及其在反应器设计计算中的应用;学会推导多相催化反应速率方程的方法。
化学反应工程(1)

化学反应⼯程(1)1、幂函数型反应动⼒学⽅程和双曲函数型反应动⼒学⽅程⼀般各适⽤什么场合?各有什么特点与区别?答:上述两类动⼒学模型都具有很强的拟合实验数据的能⼒,都既可⽤于均相反应体系,也可⽤于⾮均相反应体系。
以均匀表⾯吸附理论为基础的L -H 型反应动⼒学⽅程称为双曲函数型动⼒学⽅程;以不均匀表⾯吸附理论为基础的反应动⼒学⽅程,且只有单组分吸附态时,可形成幂函数型,称为数型反应动⼒学⽅程。
幂函数反应动⼒学⽅程形式简单,参数数⽬少,通常也能够精确地拟合实验数据,所以在⾮均相反应过程开发和⼯业反应器设计得到⼴泛应⽤。
若反应产物对反应起到抑制作⽤,反应物的浓度将出现在反应动⼒学⽅程中,即)(幂级函数s S C r R C B C A C k A r βα=- )(1双曲函数型s SC r R C k B C A C k A r *+=-βα当反应开始时,反应产物浓度为0,r A 趋于⽆穷⼤,不符合事实。
⽽⽤双曲型函数修正,既可避免上述困难。
2、⽓固催化反应⼀般要经历哪⼏个步骤?其中具有化学变化特征的是哪⼏个步骤?答:⼀般要经历以下⼏个步骤:①反应物从⽓流主体扩散到催化剂颗粒表⾯;②反应物从催化剂颗粒外表⾯向催化剂孔道内部扩散;③在催化剂内部孔道所组成的内表⾯上进⾏催化反应;④产物从外表⾯扩散到内表⾯;⑤产物从外表⾯扩散到⽓流主体。
①⑤称为外扩散过程,②④称为内扩散过程,③为本征动⼒学⽅程,其中步骤三具有化学特征变化。
3、在什么样的情况下,反应原料的预混合相当重要的?答:当反应发⽣在两种或两种以上组分之间时,这些组分必须预先混合,提供不同组分互相接触的机会,反应能进⾏。
当反应速率很快或流体黏度很⾼,达到分⼦尺度的均匀混合时间很长时,预混合将对反应结果产⽣重⼤影响。
如在⽓固催化反应中,反应物⼀经接触就开始反应,必须采⽤有效地预混合措施以保证最佳的浓度和温度分布。
在均相反应的极快反应中,如对⼀些易燃易爆的组分预混合必不可少,否则物料在流动中容易形成爆炸死⾓。
化学反应工程1_7章部分答案

第一章绪论习题1.1 解题思路:(1)可直接由式(1.7)求得其反应的选择性(2)设进入反应器的原料量为100 ,并利用进入原料气比例,求出反应器的进料组成(甲醇、空气、水),如下表:组分摩尔分率摩尔数根据式(1.3)和式(1.5)可得反应器出口甲醇、甲醛和二氧化碳的摩尔数、和。
并根据反应的化学计量式求出水、氧及氮的摩尔数,即可计算出反应器出口气体的组成。
习题答案:(1) 反应选择性(2) 反应器出口气体组成:第二章反应动力学基础习题2.1 解题思路:利用反应时间与组分的浓度变化数据,先作出的关系曲线,用镜面法求得反应时间下的切线,即为水解速率,切线的斜率α。
再由求得水解速率。
习题答案:水解速率习题2.3 解题思路利用式(2.10)及式(2.27)可求得问题的解。
注意题中所给比表面的单位应换算成。
利用下列各式即可求得反应速率常数值。
习题答案:(1)反应体积为基准(2)反应相界面积为基准(3)分压表示物系组成(4)摩尔浓度表示物系组成习题2.9 解题思路:是个平行反应,反应物A的消耗速率为两反应速率之和,即利用式(2.6)积分就可求出反应时间。
习题答案:反应时间习题2.11 解题思路:(1)恒容过程,将反应式简化为:用下式描述其反应速率方程:设为理想气体,首先求出反应物A的初始浓度,然后再计算反应物A的消耗速率亚硝酸乙酯的分解速率即是反应物A的消耗速率,利用化学计量式即可求得乙醇的生成速率。
(2)恒压过程,由于反应前后摩尔数有变化,是个变容过程,由式(2.49)可求得总摩尔数的变化。
这里反应物是纯A,故有:由式(2.52)可求得反应物A的瞬时浓度,进一步可求得反应物的消耗速率由化学计量关系求出乙醇的生成速率。
习题答案:(1)亚硝酸乙酯的分解速率乙醇的生成速率(2)乙醇的生成速率第三章釜式反应器习题3.1 解题思路:(1)首先要确定1级反应的速率方程式,然后利用式(3.8)即可求得反应时间。
(2)理解间歇反应器的反应时间取决于反应状态,即反应物初始浓度、反应温度和转化率,与反应器的体积大小无关习题答案:(1)反应时间t=169.6min.(2)因间歇反应器的反应时间与反应器的体积无关,故反应时间仍为169.6min.习题3.5 解题思路:(1)因为B过量,与速率常数k 合并成,故速率式变为对于恒容过程,反应物A和产物C的速率式可用式(2.6)的形式表示。
实验05 脉冲示踪法测定基本反应器的停留时间分布

σ
2 θ
=
σ
2 t
2
(8)
t
对于两种理想流动,其用无量纲时间标度表示的方差分别为 0 和 1,其它实际流动 反应器的方差皆界于 0 与 1 之间,即:
当σ
2 θ
=0
时,为理想置换流动模型;当σ
2 θ
=1
时,为全混流模型;当
0<σ
2 θ
<1
时,
为非理想流动,因此,根据σ
2 θ
值的大小,可以直观地反映反应器中物料的返混程度,σ
形上可清楚地反映出来),即可关机、关水停止实验; 6.小心将电极从电导池中取出,洗净拭干,妥善收存,同时将搅拌釜内剩余的水虹
吸出来,量取体积,然后将搅拌釜清洗干净,整理仪器,清洁桌面。
六、实验数据处理
1.将各个时刻所记录的电导值,根据不同温度下的κ-c关系,计算出相应的温度下 的c(t)值,并根据公式E(t)=qVc(t)/M0计算出与各个时刻对应的E(t)值;
五、实验操作步骤
(一) 管式反应器 1.整理管式反应器的管路,确保畅通无泄漏; 2.在管式反应器出口支管中小心插入电导率仪光亮铂电极,并将电导率仪与长图平 衡记录仪连接妥当; 3.缓慢打开自来水龙头,向高位槽中注水,待溢流管中有水流出后,打开水槽出口 活塞,调节转子流量计到适宜刻度,使管式反应中充满水流,且电极也应全部侵入水中, 流量稳定; 4.接通长图平衡记录仪电源,并控制其走纸速度为 60×10 mm·h-1; 5.启动已调节好的电导率仪,然后,用注射器瞬时在管式反应器入口橡胶管中快速 注入 1ml 着红色的 KCl 溶液,观察长图平衡记录仪上记录笔绘制的曲线,直至示踪剂全 部流出为止; 6.分别将水量调节为 100 l·h-1,80 l·h-1和 60 l·h-1作三次实验以观察记录电导率 变化与时间的关系; 7.本实验结束后,关闭电导率仪及记录仪电源,关闭水糟出口流活塞,继续进行下 一个实验。
反应工程总结

第一章 绪论 1、化学反应工程是化学工程学科的一个分支,通常简称为反应工程。
其内容可概括为两个方面,即反应动力学和反应器设计与分析。
2、传递现象包括动量、热量和质量传递,再加上化学反应,这就是通常所说的三传一反。
3、反应组分的反应量与其化学计量系数之比的值为定值,ξ叫做反应进度且恒为正值。
、本书规定反应物的化学计量系数一律取负值,而反应产物则取正值。
8、工业反应器有三种操作方式: ① 间歇操作;② 连续操作;③ 半间歇(或半连续)操作 9、反应器设计的基本内容一般包括:1)选择合适的反应型式 ;2)确定最佳操作条件 ;3)根据操作负荷和规定的转化程度,确定反应器的体积和尺寸 。
10.反应器按结构原理的特点可分的类型: 管式,釜式 ,塔式,固定床,流化床,移动床,滴流床反应器。
第二章 3、温度对反应速率的影响 如果反应速率方程可以表示为:r=f1 (T)f2(c ),f1(T)是温度的影响。
当温度一定时,其值一定。
通常用阿累尼乌斯方程(Arrhenius ‘ law )表示反应速度常数与温度的关系, 即, 为指前因子,其因次与k 相同;E 为反应的活化能;R 为气体常数。
两边取对数,则有 : lnk=lnA0-E/RT ,lnk 对 1/T 作图,可得-直线,直线的斜率=-E/RT 。
注意:不是在所有的温度范围内上面均为直线关系,不能外推。
其原因包括:(1)速率方程不合适; (2)反应过程中反应机理发生变化;(3)传质的影响;(4)指前因子A0与温度有关。
速率极大点处有: 对应于极大点的温度叫做最佳温度Top 。
速率为零点处有: rA=0 6、多相催化与吸附 1)、催化剂的用途:①加快反应速度②定向作用(提高选择性)-化学吸附作用结果 2)、催化剂的组成:主催化剂-金属或金属氧化物,用于提供反应所需的活性中心。
助催化剂-提高活性,选择性和稳定性。
助催化剂可以是 ①结构性的;② 调变性的。
载体-用于 ① 增大接触表面积;②改善物理性能。
反应器基础知识—流体流动
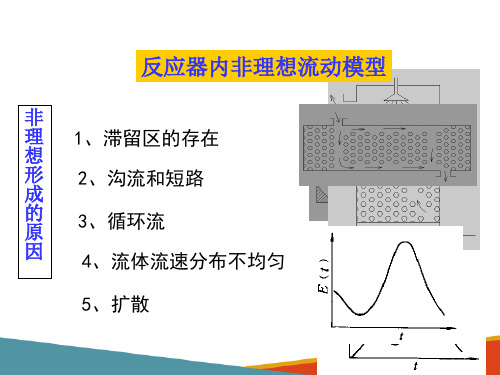
改善措施
1、增大流体在设备内的湍流程度,以消除轴向扩散而造
非 理
成的停留时间分布不均匀的现象。
想 2、在反应器内装设填充物,以改变设备内速度分布和浓
流 动
度分布,从而使停留时间分布趋于均一化。但要注意避免
的 沟流和短路现象的发生。
改
善 3、增加设备级数或在设备内增设挡板。
4、采用适当的气体分布装置,或调节各组反应管的阻力,
停留时间描述
理 想 混 合 流 动 模 型
E(t) 1 et /
F (t) 1 et /
e d 1 0
2
2e d
1 1
0
流体流动
流体的流动特征:
指反应器内流体的流动状态和混合情况,它们随反应器的几何结 构(包括内部构件)和几何尺寸不同发生变化。由于反应流体在反 应器内流动的复杂性导致反应器内不仅存在流体流速的分布,更重 要的是还存在浓度和温度的分布。使得反应器内存在不同停留时间 的流体粒子以及不同停留时间流体粒子之间的混合即返混,从而导 致反应器内反应物料处于不同的温度和浓度下进行反应。影响反应 速率和反应选择性,使反应结果发生变化。
t≤0, F(t)=0 0<t<∞,0<F(t)<1 t=∞, F(t)=1。
E(t) dF(t) dt
1、数学期望
停
留 时 间
1.0
t 0 tdF(t) 0 tE(t)dt
分
布 的 2、方差
特
征 值
2 t
(t t)2 E(t)dt
0
t 2 E(t)dt t 2
0
停
脉冲法:
留
流体流动的描述
1、停留时间分布密度函数
停
停留时间分布

t t
全混流模型
使用阶跃法建立全混流的流动模型,如果所示,将全釜作为 控制体,对示踪剂作物料衡算,有:
流入的摩尔流率=流出的摩尔流率+积累的摩尔流率
q v c0dt q v ct dt VR dc(t)
积分上式,得:
两边同除VRc0dt
qv q v c(t ) dc(t ) vR V R c0 c0 dt C t 由F(t)定义知: F t 所以 C0
t
tm
d. 晚出峰
t
tm
e. 出双峰
t
(有死区)
(示踪剂被吸附) (平行流股)
停留时间分布函数的数字特征
⑴ 数学期望 (平均停留时间)
定义:
0
tE(t)dt tE(t)dt 0 E(t)dt 0 因次:[时间]
E (t )
面积重心
t
其物理意义: 为E(t)曲线的分布中心,即E ~ t曲线所围面积的重 心在t坐标轴上的投影;数学上称: E(t)曲线对于坐标原点的一
示踪剂脉冲注入
示踪剂检测 系统
主流体 V0 c0(t)
δ(t)
c(t)
激励曲线
O
响应曲线
0
t =0
输入
t
输出
t
3. 由响应曲线计算停留时间分布曲线
出口处,停留时间在t ~ t+dt间的量: qvc(t)dt 入口处,t=0时刻 注入的量:m
由E(t)的定义:
q v c(t)dt E t dt m
则:
c(t) F(t) c0
——由阶跃法直接求得的是停留时间分布函数 F(t)
理想连续流动反应器的停留时间分布 活塞流模型
停留时间分布

t 2E(t)dt t 2
0
0
③无因次化
令:
t
t
则
t 1
t
E( )d E(t)dt
d d t
t
E( ) = tE(t)
由于F(t)本身是一累积概率,而θ是t的确定性函 数,根据随机变量的确定性函数的概率应与随机 变量的概率相等的原则,有:
F ( ) F (t)
2
(
1)2 E( )d
即:M
0 Fv0CA (t)dt
或
C0
M Fv0
0 CA (t)dt
C0 等于 CA(t) -t 曲线下面所围的面积,如图所示。
出口物料中在系统内停留了t~t+dt 时间的示踪剂量为
Fv0CA(t)dt,由E(t)的定义可知:
E(t)dt = FV 0C A (t)dt = C A (t) dt
阶跃法测定停留时间分布示意图
在切换成第二流体后的t-dt~t时间间隔,示踪剂流入系统量
为CA0Fv0dt,示踪剂流出系统量为CA(t)Fv0dt,由F(t)定义可
得:
F (t) = Fv0C A (t)dt = C A (t)
Fv0C A0 dt
C A0
即由出口的C(t)~t曲线可获得F(t)曲线.
F (t) t dN
0N
F (t )被称为停留时间分布函数。
从概率论的角度,F(t)表示流体粒子的停留时间小 于t的概率。
1.3. E(t), F (t) 之间的关系
t dN t
F (t) 0 N 0 E(t)dt
E(t) dF (t) dt
1 F (t) t E(t)dt
t 0 F (0) 0;
