高中常见气体的制备
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
常见气体的制备
氯气
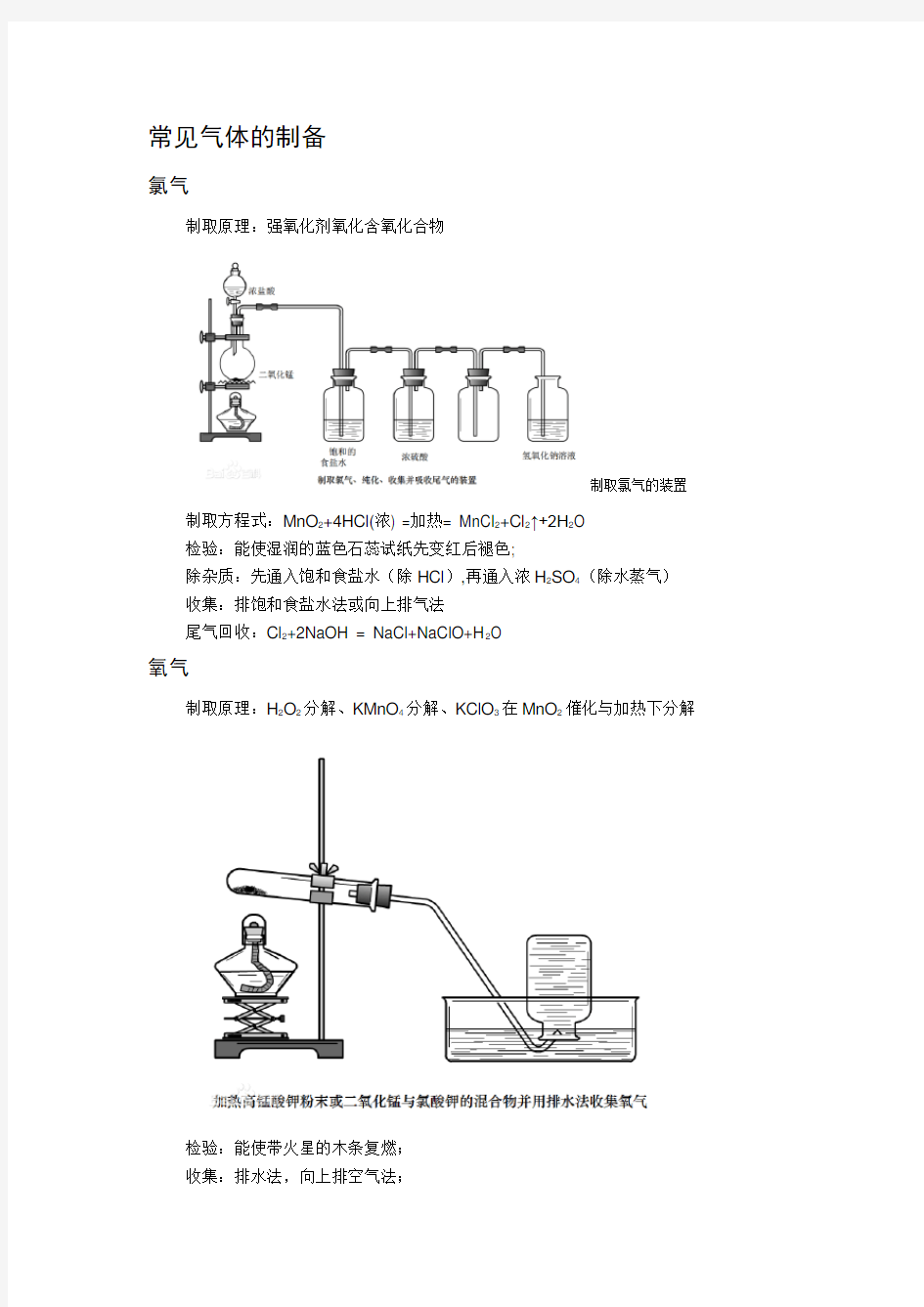
制取原理:强氧化剂氧化含氧化合物
制取氯气的装置制取方程式:MnO2+4HCl(浓) =加热= MnCl2+Cl2↑+2H2O
检验:能使湿润的蓝色石蕊试纸先变红后褪色;
除杂质:先通入饱和食盐水(除HCl),再通入浓H2SO4(除水蒸气)收集:排饱和食盐水法或向上排气法
尾气回收:Cl2+2NaOH = NaCl+NaClO+H2O
氧气
制取原理:H2O2分解、KMnO4分解、KClO3在MnO2催化与加热下分解
检验:能使带火星的木条复燃;
收集:排水法,向上排空气法;
氯化氢
制取原理:高沸点酸与金属氯化物的复分解
制取方程式:NaCl+H2SO4 = Na2SO4+2HCl↑
装置:分液漏斗,圆底烧瓶,加热
检验:通入AgNO3溶液,产生白色沉淀,再加稀HNO3沉淀不溶
除杂质:通入浓硫酸(除水蒸气)
收集:向上排气法
氨气
制取原理:固体铵盐与固体强碱的复分解
加热制取氨气的装置
制取方程式:Ca(OH)2+2NH4Cl = CaCl2+NH3↑+2H2O
装置:略微向下倾斜的大试管,加热
检验:湿润的红色石蕊试纸,变蓝
除杂质:通入碱石灰(除水蒸气)
收集:向下排气法
硫化氢
制取原理:强酸制弱酸的复分解反应
制取方程式:FeS+2HCl = FeCl2+H2S↑
装置:启普发生器
检验:能使湿润的醋酸铅试纸变黑
除杂质:先通入饱和NaHS溶液(除HCl),再通入固体CaCl2(或P2O5)(除水蒸气)收集:向上排气法
二氧化氮、一氧化氮
制取原理:不活泼金属与浓硝酸、稀硝酸的氧化—还原; [8]
制取方程式:Cu+4HNO3 = Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3 (稀) = 3Cu(NO3)2+2NO↑+4H2O
装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)
检验:二氧化氮:红棕色气体,通入AgNO3溶液颜色变浅,但无沉淀生成一氧化氮:通入氧气,很快生成棕红色气体。
收集:二氧化氮:向上排气法一氧化氮:特殊方法
尾气处理:2NO2+2NaOH = NaNO3+ NaNO2+H2O
NO+NO2+2NaOH = 2NaNO2+H2O
二氧化硫
制取原理:稳定性强酸与不稳定性弱酸盐的复分解
制取方程式:Na2SO3+H2SO4 = Na2SO4+SO2↑+H2O
装置:分液漏斗,锥形瓶 [2]
检验:先通入品红试液,褪色。后加热又恢复原红色;
除杂质:通入浓H2SO4(除水蒸气)
收集:向上排气法
一氧化碳
制取原理:浓硫酸对有机物的脱水作用
制取方程式:HCOOH =浓硫酸、加热= CO↑+H2O
装置:分液漏斗,圆底烧瓶
检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊
除杂质:通入浓硫酸(除水蒸气)
收集:排水法
甲烷
制取方程式:CH3COONa+NaOH =加热= CH4↑+Na2CO3
装置:略微向下倾斜的大试管,加热
收集:排水法或向下排空气法
乙烯
制取原理:浓硫酸对有机物的脱水作用
制取方程式:CH3CH2OH =浓硫酸、加热= CH2=CH2↑+H2O
装置:分液漏斗,圆底烧瓶,加热
除杂质:通入NaOH溶液(除SO2、CO2),通入浓硫酸(除水蒸气)
收集:排水法
此实验的注意事项:控制温度。乙醇可以在浓硫酸和高温的催化发生脱水反应,随着温度的不同生成物也不同。如果温度在140℃左右生成物是乙醚。
乙炔
制取原理:电石强烈吸水作用
制取装置
制取方程式:CaC2+2H2O = Ca(OH)2+CH≡CH↑
装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)
检验:无色气体,能燃烧,产生明亮的火焰,并冒出浓的黑烟
除杂质:通入硫酸铜溶液(除H2S、PH3),通入浓硫酸(除水蒸气)
收集:排水法或向下排空气法
此实验的注意事项:不要使用蒸馏水与电石反应,要使用饱和食盐水,避免剧烈反应引发事故。
