Electronic structures of CeRu$_2X_2$ ($X$ = Si, Ge) in the paramagnetic phase studied by so
ceo2化学键

二氧化铈(CeO₂)的化学键研究二氧化铈(CeO₂),作为一种重要的稀土氧化物,在材料科学、催化化学以及固态电解质等多个领域都展现出了独特的应用价值。
而深入理解CeO₂的化学键特性,对于指导其在实际应用中的优化和改性具有至关重要的意义。
一、CeO₂的基本结构CeO₂的晶体结构属于立方萤石型,其中铈离子(Ce⁴⁺)占据阳离子位置,形成面心立方格子,而氧离子(O²⁻)则填充在四面体空隙中。
这种结构赋予了CeO₂高度的稳定性和独特的物理化学性质。
二、CeO₂中的化学键类型在CeO₂中,主要存在两种类型的化学键:离子键和共价键。
这两种键在决定CeO₂的物理和化学性质方面起着不同的作用。
1.离子键:由于铈和氧之间的电负性差异较大,因此它们之间主要形成离子键。
离子键的存在使得CeO₂具有较高的熔点和硬度,同时也赋予了它良好的热稳定性和化学稳定性。
2.共价键:除了离子键外,CeO₂中还存在一定程度的共价键成分。
这是因为铈离子的d轨道和氧离子的p轨道之间可以发生杂化,形成共价键。
共价键的存在增强了CeO₂的结构稳定性,并使其在某些条件下表现出独特的催化活性。
三、CeO₂化学键的表征方法为了深入研究CeO₂中的化学键特性,科学家们发展了一系列先进的表征方法,包括X射线光电子能谱(XPS)、拉曼光谱(Ramanspectroscopy)、傅里叶变换红外光谱(FTIR)以及扩展X射线吸收精细结构谱(EXAFS)等。
这些方法可以从不同的角度揭示CeO₂中化学键的性质和强度。
四、CeO₂化学键与性能的关系CeO₂的化学键特性与其在实际应用中的性能密切相关。
例如,在催化领域,CeO₂的催化活性往往与其表面的氧空位浓度有关,而这些氧空位的形成和稳定性与CeO₂中的化学键类型有着直接的联系。
此外,在固态电解质应用中,CeO₂的离子导电性也与其内部的离子键强度密切相关。
五、CeO₂化学键的调控与改性基于对CeO₂化学键的深入理解,科学家们已经发展出了多种有效的调控和改性方法,以优化其在实际应用中的性能。
无机材料科学基础作业习题

无机材料科学基础作业习题第一章晶体结构基础1-1 定义下述术语,并注意它们之间的联系和区别:晶系;点群;空间群;平移群;空间点阵1-2 简述晶体的均一性、各向异性、对称性三者的相互关系。
1-3 列表说明七个晶系的对称特点及晶体定向规则。
1-4 四方晶系晶体a=b,c=1/2a。
一晶面在X、Y.Z轴上的截距分别为2a, 3b 和6c。
给出该晶面的密勒指数。
1-5 在立方晶系中画出下列晶面:a)(001)b)(110)c)(111)1-6 在上题所画的晶面上分别标明下列晶向:a(210) b(111) c(101)1-7 立方晶系组成{111}单形的各晶面构成一个八面体,请给出所有这些晶面的密勒指数。
1-8 试在完整的六方晶系晶胞上画出(1012)晶面的交线及〔1120〕〔2113〕晶向,并列出{1012}晶面族中所有晶面的密勒指数。
1-9 a≠b≠c α=β=γ=90℃的晶体属什么晶系?a≠b≠c α≠β≠γ≠90℃的晶体属什么晶系?你能否据此确定这二种晶体的布拉维点阵?1-10 下图示正交面心格子中去掉上下底心后的结点排列情况。
以图中的形状在三维空间无限重复,能否形成一空间点阵?为什么?1 –11 图示单斜格子的(010)面上的结点排布。
试从中选出单位平行六面体中的a和c。
1 –12 为什么等轴晶系有原始、面心、体心而无底心格子?1 –13 为什么在单斜晶系的布拉维格子中有底心C格子而无底心B格子?1-14 试从立方面心格子中划分出一三方菱面体格子,并给出其晶格常数。
说明为什么造选取单位平行六面体时不选后者而选前者?1 –15 写出立方面心格子的单位平行六面体上所有结点的座标,注明其中哪些属于基本点。
1 –16 给出(111)面和(111)面交棱的晶棱符号。
1 –17 试证(123)(112)和(110)诸晶面属于同一晶带,并给出其晶带符号。
1-18 证明立方晶系〔111〕晶向垂直于(111)晶面。
二维铁磁体 fe3gete2异质结

二维铁磁体fe3gete2异质结摘要:1.二维铁磁体概述2.Fe3GeTe2异质结的结构特点3.二维铁磁体Fe3GeTe2的磁性能4.二维铁磁体在实际应用中的优势5.前景与挑战正文:一、二维铁磁体概述二维铁磁体是一类具有磁性的二维材料,其磁性来源于原子或分子之间的相互作用。
在过去的几十年里,二维铁磁体因其独特的物理性质和潜在的应用前景而备受关注。
在众多二维铁磁体材料中,Fe3GeTe2异质结备受瞩目。
二、Fe3GeTe2异质结的结构特点Fe3GeTe2是一种具有层状结构的二维材料,属于IV-VI族半导体。
其结构特点是每一层都由铁、锗和碲原子组成,呈蜂窝状排列。
铁原子之间通过共价键相连,形成了一个稳定的晶体结构。
这种结构有利于磁性的产生和发展。
三、二维铁磁体Fe3GeTe2的磁性能由于Fe3GeTe2的层状结构,其在磁性能方面具有独特的优势。
实验研究表明,Fe3GeTe2在低温下表现出铁磁性,而在高温下呈现出顺磁性。
这一特性使得Fe3GeTe2在磁存储、磁传感器等领域具有广泛的应用前景。
四、二维铁磁体在实际应用中的优势1.磁存储:二维铁磁体可以应用于磁存储器件,由于其层状结构,可以实现高密度的信息存储。
2.磁传感器:二维铁磁体的磁性能使其成为磁传感器的理想材料,具有高灵敏度和高分辨率。
3.能量转换:二维铁磁体在磁电转换方面具有优异性能,可应用于磁电发电机、磁电传感器等设备。
4.软磁材料:二维铁磁体具有较低的磁滞损耗,可作为软磁材料应用于各种电磁设备。
五、前景与挑战随着科学技术的不断发展,二维铁磁体材料的研究取得了显著成果。
然而,要充分发挥二维铁磁体的潜力,仍面临诸多挑战,如:1.提高磁性能:通过优化材料结构和组成,进一步提高二维铁磁体的磁性能。
2.降低磁滞损耗:减小磁滞损耗是提高二维铁磁体应用性能的关键,需要寻求新的制备方法和材料设计。
3.规模化制备:实现低成本、高效、可控的规模化制备是二维铁磁体材料应用的基础。
第四版无机化学习题及答案

第一章原子结构和原子周期系1-1根据原子序数给出下列元素的基态原子的核外电子组态:(a)K (b)Al (c)Cl (d)Ti(Z=22)(e)Zn(Z=30)(f)As(Z=33)答:(a)[Ar]4s1(b)[Ne]3s23p1(c)[Ne]3s23p5(d)[Ar]3d54s2(e)[Ar] 3d104s1(f)[Ar]4s24p31-2给出下列原子或离子的价电子层电子组态,并用方框图表示轨道,填入轨道的电子用箭头表示。
(a)Be (b)N (c)F (d)Cl-(e)Ne+(f)Fe3+(g)As3+1-3 Li+、Na+、K+、Rb+、Cs+的基态的最外层电子组态与次外层电子组态分别如何?1-4以下+3价离子那些具有8电子外壳?Al3+、Ga3+、Bi3+、Mn3+、Sc3+答:Al3+和Sc3+具有8电子外壳。
1-5已知电中性的基态原子的价电子层电子组态分别为:(a)3s23p5(b)3d64s2(c)5s2(d)4f96s2(e)5d106s1试根据这个信息确定它们在周期表中属于那个区、哪个族、哪个周期。
答:(a)p区,ⅦA族,第三周期(b)d区,Ⅷ族,第四周期(c)s区,ⅡA族,第五周期(d)f区,ⅢB族,第六周期(e)ds区,ⅠB族,第六周期1-6根据Ti、Ge、Ag、Rb、Ne在周期表中的位置,推出它们的基态原子的电子组态。
答:Ti位于第四周期ⅣB族,它的基态原子的电子组态为[Ar]3d24s2;Ge位于第四周期ⅣA族,它的基态原子的电子组态为[Ar]3d104s24p2;Ag位于第五周期ⅠB族,它的基态原子的电子组态为[Kr] 4d105s1;Rb位于第五周期ⅠA族,它的基态原子的电子组态为[Kr] 5s1;Ne位于第二周期0族,它的基态原子的电子组态为[He] 2s22p6。
1-7某元素的基态价层电子构型为5d36s2,给出比该元素的原子序数小4的元素的基态原子电子组态。
【化学奥赛】晶体结构习题new!
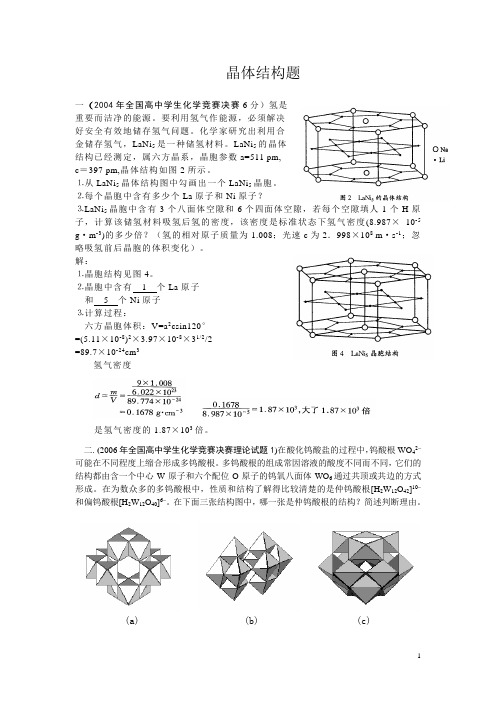
晶体结构题一(2004年全国高中学生化学竞赛决赛6分)氢是重要而洁净的能源。
要利用氢气作能源,必须解决好安全有效地储存氢气问题。
化学家研究出利用合金储存氢气,LaNi5是一种储氢材料。
LaNi5的晶体结构已经测定,属六方晶系,晶胞参数a=511 pm,c=397 pm,晶体结构如图2所示。
⒈从LaNi5晶体结构图中勾画出一个LaNi5晶胞。
⒉每个晶胞中含有多少个La原子和Ni原子?⒊LaNi5晶胞中含有3个八面体空隙和6个四面体空隙,若每个空隙填人1个H原子,计算该储氢材料吸氢后氢的密度,该密度是标准状态下氢气密度(8.987×10-5 g·m-3)的多少倍?(氢的相对原子质量为1.008;光速c为2.998×108 m·s-1;忽略吸氢前后晶胞的体积变化)。
解:⒈晶胞结构见图4。
⒉晶胞中含有1个La原子和5个Ni原子⒊计算过程:六方晶胞体积:V=a2csin120°=(5.11×10-8)2×3.97×10-8×31/2/2=89.7×10-24cm3氢气密度是氢气密度的1.87×103倍。
二. (2006年全国高中学生化学竞赛决赛理论试题1)在酸化钨酸盐的过程中,钨酸根WO42-可能在不同程度上缩合形成多钨酸根。
多钨酸根的组成常因溶液的酸度不同而不同,它们的结构都由含一个中心W原子和六个配位O原子的钨氧八面体WO6通过共顶或共边的方式形成。
在为数众多的多钨酸根中,性质和结构了解得比较清楚的是仲钨酸根[H2W12O42]10-和偏钨酸根[H2W12O40]6-。
在下面三张结构图中,哪一张是仲钨酸根的结构?简述判断理由。
(a) (b) (c)解:提示:考察八面体的投影图,可以得到更清楚地认识。
三.(2006年全国高中学生化学竞赛决赛理论试题4)轻质碳酸镁是广泛应用于橡胶、塑料、食品和医药工业的化工产品,它的生产以白云石(主要成分是碳酸镁钙)为原料。
Ge掺杂二氧化钛复合薄膜制备及光吸收性能研究

水 、 醇 超 声 清 洗 1 mi ) 采 用 经 过 改 造 的 G 乙 0 n, DM一 4 0 N 型真 空 镀 膜 反 应 磁 控 溅 射 设 备 制 得 Ti 薄 5B O
膜 。本底 真空 为 3 0 _ P , 出功率 为 3 W , 材 . X1 ‘a输 0 k 靶
的利用太 阳 能 已 经成 为 人 们 关 注 和 研 究 的热 点E引。
2 2 掺 杂 T O 薄 膜 的制备 . i
与 S相比, i 二氧 化 钛 ( O ) 有 稳 定 性 高 、 学 惰 性 Ti 具 化 和 价格低廉 等显 著 特 点 , 已经 成 为 一 种很 有 前 途 的 光 电转换 材料 。但 Ti 2带 隙较 宽 ( 一 3 O . e , 0 . ~3 2 V) 只能 吸收 波 长< 4 0 m 的紫 外 光 , 可 见光 的吸 收 只 0n 对 有 5 。为 提 高 其 光 吸 收 效 率 , 须 对 其 进 行 改 性 。 必 目前 , 高 T 02 吸收效 率 的研究 主要集 中在 掺杂 改 提 i 光
薄膜 。
关键 词 : 溶胶凝 胶法 ; 离子 注入 ; O Ti 复合薄 膜 ; ; Ge
光 吸 收
中图分类号 : TQ1 4 3 文献标 识码 : A 文章 编号 :0 19 3 (0 0 1— 8 50 10 - 7 1 2 1 )0 1 3 -3
1 引 言
太 阳能是廉 价 的 可循 环 使 用 的 能源 , 何 高效 率 如
注入剂 量为 2 1 0 o / m 离子 注入 后 的薄 膜 在 . ×1 in c ;
性 、 面改性[ 、 表 3 染料 敏化 [ 等 方面 。可 利用 的掺 杂元 ] 4
全国高中学生化学竞赛决赛理论模拟试题十二
●竞赛时间4小时。
迟到超过半小时者不能进考场。
开始考试后1小时内不得离场。
时间到,把试卷(背面朝上)放在桌面上,立即起立撤离考场。
●试卷装订成册,不得拆散。
所有解答必须写在指定的方框内,不得用铅笔填写。
草稿纸在最后一页。
不得持有任何其他纸张。
●姓名、报名号和所属学校必须写在首页左侧指定位置,写在其他地方者按废卷论处。
●允许使用非编程计算器以及直尺等文具。
第1题大自然中的金属A只存在于化合物中,主要是通式为M x(SiO4)y硅酸盐和它的氧化物。
氧化物存在多种形态,并且易形成配位数CN metal = 7的单斜结构。
温度高于1100°C,它的晶格转变为四方结构。
温度超过2000°C它转变成立方结构。
后者的晶格结构是氟化钙型,晶格常数为a0 = 507 pm.。
这个结构在室温下可以被CaO稳定。
纯的氧化物(立方结构)密度为6.27 g·cm-3。
1.画出立方结构的晶胞。
2. 这个氧化物的实验式是什么?3. 这个氧化物中金属的配位数为多少?4. 金属在氧化物中的氧化数和在硅酸盐中的一样。
给出硅酸盐的实验式。
5.这个金属是什么?给出过程。
6.写出这个金属的电子构型。
7. 该氧化物中阳离子和阴离子的配位数为多少?8.运用如下热力学数据,计算氧的电子亲和能∆EA H°(O(g) + 2 e-→ O2-(g)):∆sub H°(M) = 609 kJ·mol-1; ∆IE H°(M/M n+) = 7482 kJ·mol-1; ∆diss H°(O2) = 498 kJ·mol-1;∆lattice H°(M-oxide) = -10945 kJ·mol-1; ∆f H°(M-oxide) = -1100 kJ·mol-1;得到这个金属的过程是一个两步合成。
第一步是硅酸盐的碳氯化,即在高温下与碳和气体氯反应。
化学竞赛晶体结构综合例题
晶体结构综合例题令狐采学一.有一立方晶系的离子晶体,其结构如右图所示,试回答:1.晶体所属的点阵形式及结构基元;2.已知rCs+=169pm,rCl=181pm,试问此两种离于联合组成了何种型式的密聚积;3.Cu2+处在何种空隙里?4.指出各离子的配位情况?解:1. 立方P,CaCsCl3 ;2.A1型(立方面心)聚积, Cs+,Cl-离子半径年夜致相近;3. 八面体空隙中;4. Cu2+周围Cl-配位数6,Cs+配位数8;Cl-周围Cu2+配位数2,Cs+配位数4; Cs+周围Cl-配位数12,Cu2+配位数8。
二.黄铜矿是最重要的铜矿,全世界的2/3的铜是由它提炼的。
1.右图为黄铜矿的晶胞。
计算晶胞中各种原子的数目,写出黄铜矿的化学式;2.在高温下,黄铜矿晶体中的金属离子可以产生迁移。
若铁原子与铜原子产生完全无序的置换,可将它们视作同等的金属离子,请说出它的晶胞。
3.在无序的高温型结构中,硫原子作什么类型的聚积?金属原子占据什么类型的空隙?该空隙被金属原子占据的分数是几多?4.计算黄铜矿晶体的密度; (晶胞参数:a=52.4pm ,c=103.0pm ;相对原子量:Cu63.5 Fe55.84 S32.06)。
解:1. 各种原子的数目Cu, Fe, S: 4, 4, 8; 黄铜矿的化学式CuFeS2 ;2. 它的晶胞与ZnS 晶胞相同;但金属离子随机性为50%;(如图);3. 硫原子作A1型(立方F )聚积;隙;该空隙被金属原子占据的分数1/2;4.容易计算黄铜矿晶体的密度 4.31g/cm3 . 三.冰晶石(Na3AlF6胞是以年夜阴离子(AlF63-)构成的面心立方晶格,Na +可看作是填充在晶格的空隙中,已知冰晶石的密度为 2.95g/cm3,Al —F 键长181 pm ,相对原子质量:Na 23.0;Al 27.0;F 19.0。
1.指出AlF63-配离子中心离子的杂化轨道类型、配离子空间构型和所属分子点群。
材科基网上习题
2.8题(1)一晶面在x、y、z轴上的截距分别为2a、3b、6c,求出该晶面的米勒指数;(2)一晶面在x、y、z轴上的截距分别为a/3、b/2、c,求出该晶面的米勒指数。
2.9题在立方晶系的晶胞中画出下列米勒指数的晶面和晶向:(001)与[210],(111)与[112],(110)与[111],(322)与[236],(257)与[111],(123)与[121],(102),(112),(213),[110],[111],[120],[321]。
2.10题写出面心立方格子的单位平行六面体上所有结点的坐标。
2.16题从理论计算公式计算NaC1与MgO的晶格能。
MgO的熔点为2800℃,NaC1为80l℃, 请说明这种差别的原因。
2.8题参考答案:解:(1)h:k:l=1/2:1/3:1/6=3:2:1,∴该晶面的米勒指数为(321);(2)h:k:l=3:2:1,∴该晶面的米勒指数为(321)。
2.10题参考答案:解:(0,0,0)、(0,1/2,1/2)、(1/2,0,1/2)、(1/2,1/2,0)2.13题参考答案:解:e=1.602×10-19,ε0=8.854×10-12,N0=6.022×1023对于NaCl:z1=1,z2=1,A=1.748,n Na+=7,n Cl-=9,n=8,r0=2.819×10-10m ∴NaCl的晶格能为u NaCl=752KJ/mol;对于MgO:z1=2,z2=2,A=1.748,n O2-=7,n Mg2+=7,n=7,r0=2.12×10-10m ∴MgO的晶格能为u MgO=3920KJ/mol;∵u MgO> u NaCl,∴MgO的熔点高。
2.9题参考答案:2.26下列硅酸盐矿物各属何种结构类型:Mg2[SiO4],K[AISi3O8],CaMg[Si2O6],Mg3[Si4O10](OH)2,Ca2Al[AlSiO7]。
第十三章 p区元素(一)
B2 H 6 (g) + 6Cl 2 (g) 2BCl3 (l) + 6HCl →
△rHm = -1376kJ ⋅ mol-1
2.硼的含氧化合物 ① 三氧化二硼 B2O3 结构:原子晶体:熔点460°C 无定形体:软化
O2
B(无定形)
+H2O
Mg或Al
B2O3
-H2O
H3BO3
∆ 制备: 4B(s) + 3O 2 (g) → 2B 2 O 3 (s) ∆ 2H 3 BO 3 → B 2 O 3 + 3H 2 O
第16章 碳 硅 硼 16章
§ 16.1 碳
§ 16.2 硅 § 16.3 硼
16.1 碳
16.1.1 碳族元素概述 碳族(IVA):C, Si, Ge, Sn, Pb 价电子构型:ns2np2 C Si Ge -4 +2 + 4 (+ 2 ) 氧化值 +4 +4 最大 4 6 6
配位数 单质可形成原子晶体 金属晶体
Sn +2 +4 6
Pb +2 (+ 4 ) 6
存在形式: 碳:金刚石、石墨;煤、石油、天然气; 碳酸盐; CO2 。 硅:SiO2和各种硅酸盐。 锗:硫银锗矿 4Ag2S•GeS2 , 硫铅锗矿2PbS • GeS2 。 锡:锡石 SnO2 。 铅:方铅矿 PbS,白铅矿 PbCO3 。
碳单质的同素异形体: 金刚石:原子晶体,硬度最大,熔点最高。 石墨:层状晶体 ,质软,有金属光泽。 足球烯或富勒烯: C60, C70 等。 C60 是1985年用激光轰击石墨作碳的 气化实验时发现的。 C60 是由12个五边形 和20个六边形组成的 32面体。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
arXiv:0708.1371v2 [cond-mat.str-el] 14 Dec 2007ElectronicstructuresofCeRu2X2(X=Si,Ge)intheparamagneticphasestudiedbysoftX-rayARPESandhardX-rayphotoelectronspectroscopy
M.Yano,1A.Sekiyama,1H.Fujiwara,1Y.Amano,1S.Imada,1T.Muro,2M.Yabashi,2,3K.Tamasaku,3A.Higashiya,3T.Ishikawa,3Y.¯Onuki,4andS.Suga1
1DivisionofMaterialsPhysics,GraduateSchoolofEngineeringScience,
OsakaUniversity,Toyonaka,Osaka560-8531,Japan2JapanSynchrotronRadiationResearchInstitute,Mikazuki,Sayo,Hyogo679-5198,Japan
3RIKEN,Mikazuki,Sayo,Hyogo679-5148,Japan
4DepartmentofPhysics,GraduateSchoolofScience,
OsakaUniversity,Toyonaka,Osaka560-0043,Japan(Dated:February1,2008)
SoftandhardX-rayphotoelectronspectroscopy(PES)hasbeenperformedforoneoftheheavyfermionsystemCeRu2Si2anda4f-localizedferromagnetCeRu2Ge2intheparamagneticphase.Thethree-dimensionalbandstructuresandFermisurface(FS)shapesofCeRu2Si2havebeendeterminedbysoftX-rayhν-dependentangleresolvedphotoelectronspectroscopy(ARPES).ThedifferencesintheFermisurfacetopologyandthenon-4felectronicstructuresbetweenCeRu2Si2andCeRu2Ge2
arequalitativelyexplainedbytheband-structurecalculationforboth4fitinerantandlocalized
models,respectively.TheCevalencesinCeRu2X2(X=Si,Ge)at20KarequantitativelyestimatedbythesingleimpurityAndersonmodelcalculation,wheretheCe3dhardX-raycore-levelPESandCe3dX-rayabsorptionspectrahaveshownstrongerhybridizationandsignatureforthepartial4fcontributiontotheconductionelectronsinCeRu2Si2.
PACSnumbers:
I.INTRODUCTIONStronglycorrelatedelectronsystemsshowmanyin-terestingphysicalpropertiesduetotheircomplicatedelectronicstructures.Particularly,Cebasedcompoundshavebeenextensivelystudiedbybothexperimentalandtheoreticalapproachesbecausetheyshowvarietyof4fstatesduetodifferenthybridizationstrengthbetweentheCe4fandvalenceelectrons.DominanceoftheRKKYinteractionortheKondoeffectisoneoftheattractivesubjectsinthissystem.Especially,CeT2X2(T=Cu,Ag,Au,Ru,etc.;X=SiorGe)withthetetragonalThCr2Si2structure1(a=b∼4˚Aandc∼10˚A)showsvarious4felectronbehaviors.2,3,4,5,6,7Amongthem,the4felectronsinCeRu2Ge2arelocalizedandferromagnet-icallyorderedduetoascendancyoftheRKKYinterac-tionbelowtheCurietemperatureTC∼8Kinambientpressure.8Ontheotherhand,inthecaseofCeRu2Si2,theCe4felectroncoupleswiththevalenceelectronandmakesthesocalledKondosingletstatebelowtheKondotemperatureTK∼20K.9,10CeRu2Si2isknownasatyp-icalheavyfermionsystemwhichhasalargevalueoftheelectronicspecificheatcoefficientγ∼350mJ/molK2(about20timeslargerthanthatofCeRu2Ge2).11,12,13Suchadifferencein4felectronicstatesisthoughttooriginatefromthedifferenthybridizationstrengthbe-tweenthe4fandvalenceelectrons.Forexample,whenhighpressureisappliedtoCeRu2Ge2,thehybridiza-tionstrengthincreasesandtheelectronicstructuresofCeRu2Ge2approachtothoseofCeRu2Si2.6,14Clarifica-tionoftheelectronicstructuresofCeRu2X2isthusthekeytorevealaconnectionbetweenthe4flocalizedanditinerantelectronicstates.Therefore,completestudyoftheelectronicstatesofCeRu2X2isessentialforunder-standingphysicsofthestronglycorrelatedelectronsys-tems.Sofar,CeRu2Si2haseagerlybeenstudiedinordertoelucidatethemechanismofthemetamagnetictransi-tionwhichoccursatHm∼7.7T.15,16AccordingtothedeHaas-vanAlphen(dHvA)studies,17theFermisurface(FS)ofCeRu2Si2approachestothatofLaRu2Si2aboveHmduetothelocalizationofthe4felectrons.However,thedHvAresultsofCeRu2Si2cannotfullybeexplainedbythebandstructurecalculationsunderHexample,theheaviesteffectivemassFSorthesmallestFSsignalshavenotbeenobservedalongthemagneticfielddirectionof<001>.Recently,anotherexperi-mentalmethodnamed“softX-rayhν-dependentangle-resolvedphotoelectronspectroscopy(ARPES)”hasbeenestablishedtodeterminethree-dimensional(3D)FSsbyusingenergytunablesoftXraysfromthird-generationhighbrilliancesynchrotronradiationlightsources.19IntheARPESstudies,wecanobserveelectronicstruc-turesinsolidsatvarioustemperaturesanddeterminetheshapesofFSswhichcanbecomparedwiththeresultsfromdHvAmeasurements.dHvAmeasurementscanbeperformedundermagneticfieldsandhighpressuresbutareconfinedtolowtemperatures.WhiledHvAmea-surementsprobegenuinebulkelectronicstates,conven-tionalphotoelectronspectroscopy(PES)measurementshavebeenbelievedasarathersurfacesensitivetech-niqueasfarasthephotoelectronkineticenergiesareintherangeof20-200eV.However,thebulksensitivityofthesoftX-ray(hν∼800eV)PESwasconfirmedbytheobservationofthe4fPESforCecompounds.20SoftX-rayPESiscurrentlyanessentialapproachtoreveal
