第六章 原生质体培养(4 学时)

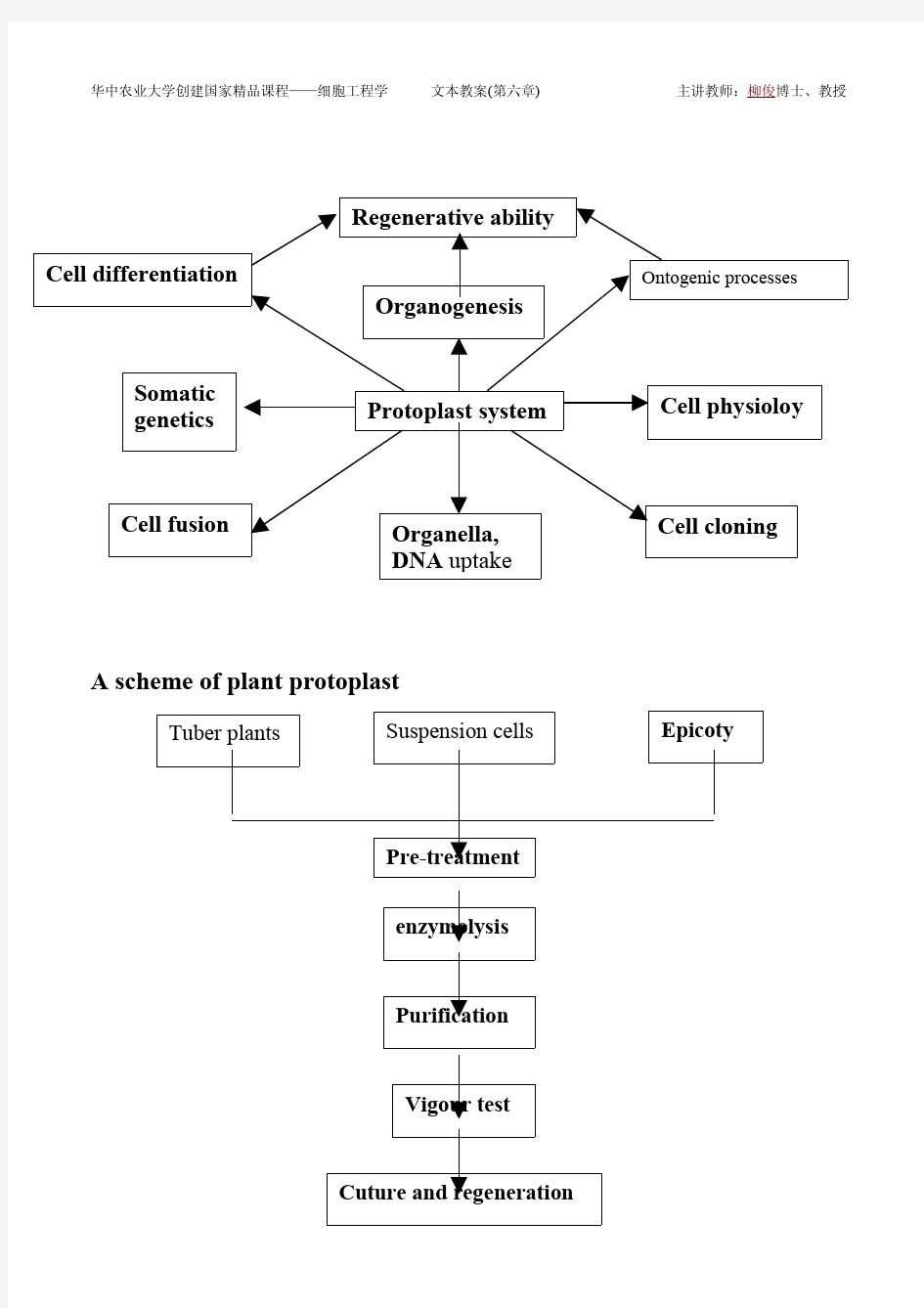
原生质体制备
1.影响原生质体数量和活力的因素 (1)细胞壁降解酶的种类和组合 不同植物种类或同一植物种的不同器官以及它们的培养细胞,由于它们的细胞壁结构组成不同,分解细胞壁所需的酶类也不同。例如,叶片及其培养细胞用纤维素酶和果胶酶,根尖细胞以果胶酶为主附加纤维素酶或粗制纤维素酶(Driselase酶),花粉母细胞和四分体期小孢子用蜗牛酶和胼胝质酶,成熟花粉用果胶酶和纤维素醇。 (2)渗造压稳定剂 用酶法降解细胞壁前,为防止原生质体的破坏,一般需先用高渗液处理细胞,使细胞处于微弱的质壁分离状态,有利于完整原生质体的释放。这种高渗液称为渗透压稳定剂。常用的滲透压稳定剂有甘露醇、山梨醇、蔗糖、葡萄糖、盐类(KCI、MgSO4.7H2O)等。在降解细胞壁时,渗透压稳定剂往往和酶制剂混合使用。滲透压稳定剂中,用得最多的是甘露醇,常用于烟草、胡萝ト、柑橘、蚕豆原生质体制备;蔗糖常用于烟草、月季等;山梨醇常用于油菜原生质体制备。滲透压稳定剂种类及浓度的选择应根据植物种类而异,例如胡萝ト用0.56mol /L甘露醇,月季用14%蔗糖,柑橘用0.8mol/L甘露醇,蚕豆用0.7mol/L甘露醇,烟草的四分体用7%熊糖,烟草的成熟花粉用13%甘露醇。 (3)质膜稳定剂 质膜稳定剂可以增加完整原生质体数量、防止质膜破坏,促进原生质体胞壁再生和细胞分裂形成细胞团。如在分离烟草原生质体时,在酶液中加人入葡聚糖硫酸钾,一旦洗净确液进行培养,原生质体很快长壁并持续细胞分裂形成细胞团。而未加葡聚糖硫酸钾的对照,原生质体经一周培养即解体。常用的原生质膜稳定剂有葡聚糖硫酸钾、MES、氯化钙、磷酸二氢钾等。 (4)pH的影响 分离原生质体时,酶液的pH是值得注意的问题。因为降解酶的活力和细胞活力最适pH是不一致的低pH时(<4.5),酶的活力强,原生质体分离速度快,但细胞活力差,破坏的细胞较多;pH偏高时,酶活力差,原生质体分离速度慢,完整的原生质体数目较多。分离原生质体时,酶液的pH因植物种类不同而有差异,如胡萝ト为5.5、月季为5.5~6.0、烟草为5.4~5.8、柑橘为5.6、蚕豆为5.6~5.7。 (5)温度影响 制备生质体时,一般在26土1℃条件下酶解。 (6)植物材料的生理状态 一般应选择植物体细胞分裂旺盛的部分进行取材。采用那些颗粒细小、疏松易碎的胚性愈伤组织和由其建立的胚性悬浮细胞系,更容易获得高质量的原生质体。要得到良好的供体材料,必要时应对材料进行预处理及预培养。 2.植物原生质体的纯化 材料经过一段时间的酶解后,需要将酶解混合物中破碎的原生质体、未去壁的细胞、细胞器及其他碎片去除出去。纯化原生质体的常用方法有过滤、离心、飘浮法,在实际操作中一般联合运用这三种方法。 1)过滤法用滤网过滤酶解混合物,滤去未被酶解的细胞、细胞团及组织块 2)离心法利用比重原理,在具有一定渗透压的溶液中,先进行过滤然后低速离心,使纯净完整的原生质体沉积于离心管底部。 3)飘浮法采用比原生质体比重大的高渗溶液(如蔗糖、Ficoll溶液),使原生质体漂浮在溶液表面。
植物原生质体的分离及融合
植物原生质体的分离及融合 生93沈睿2009012372同组:古梦婷 实验日期:2011年11月2日 一.实验原理 1.原生质体分离 原生质体指包被在植物细胞壁内的生活物质。细胞壁的主要成分是纤维素和果胶质,它们分别经纤维素酶和果胶酶处理即可分解,从而脱去细胞壁,得到原生质体。 2.原生质体融和 诱导原生质体融合的方法有多种,譬如物理法(电场刺激,激光,显微操作等)、化学法(聚乙二醇结合高钙高pH法)和生物法(仙台病毒法等)。本实验用PEG诱导原生质体融和。 PEG是聚乙二醇的英文缩写,相对分子质量在200-6000之间的均可用作细胞融合剂,20-50%的浓度能对原生质体产生瞬间冲击效应,原生质体很快发生收缩与粘连。PEG诱导融合的机理可能是由于其含有醚键而具负极性,与水、蛋白质、碳水化合物等一些正极化基团能形成氢键。当PEG分子足够长时,可作为相邻原生质体表面之间的分子桥而使之粘连。PEG也能连接Ca2+等阳离子。Ca2+可在一些负极化基团和PEG之间形成桥,因而促进粘连。在洗涤过程中,连接在原生质体膜上的PEG分子可被洗脱,这将引起电荷的紊乱和再分布,从而引起原生质体融合。高钙、高pH洗液清洗则增加了质膜的流动性,因而大大提高了融合频率,洗涤时的渗透冲击对融合也可能起作用。普遍认为PEG分子能改变各类细胞细胞膜的结构,由于两细胞相接处质膜的相互亲和以及彼此的表面张力作用,两细胞接触点处细胞膜的脂类分子发生疏散和重组。 PEG法诱导的优点是取材方便、操作简易、效率高且效果稳定,缺点是对细胞有毒性。二.实验步骤 1.原生质体的制备 (1)将新鲜的剑兰(唐菖蒲)花瓣洗干净,用吸水纸吸干表面水分;将小平皿洗净,用蒸馏水冲洗后晾干或擦干。 (2)向小平皿中加入适量酶液,用尖头镊剥取剑兰花瓣的上、下表皮,27o C恒温振荡1h 左右。 (3)镜检细胞的酶解情况,若酶解效果不佳,可延长酶解时间,并用吸管吹吸。 (4)将酶解好的原生质体混合液经300目尼龙网过滤到10ml离心管,去除未被酶解的大块组织,用洗涤液冲洗平皿若干次,收集冲洗的液体。 (5)配平后,在700rpm下离心5min,弃去上清液;加洗涤液约3ml,吹打均匀,700rpm、5min重复离心一次,彻底去除酶液。 (6)加200μl洗涤液,悬浮原生质体。 (7)镜检原生质形态和浓度,看看是否有碎片;如碎片较多,利用蔗糖溶液漂浮1-2次。(8)蔗糖漂浮方法: 取部分原生质体悬浮液,加入洗涤液定容至1ml。用注射器吸取20%蔗糖溶液,装上长针头后小心插入盛有原生质体悬浊液的离心管底部,缓缓、轻柔地将蔗糖溶液挤出。由于比重不同,蔗糖溶液与原生质体悬液中间有一明显界面。配平后在700rpm下离心5min。用装有长针头的注射器小心吹吸底部沉淀,连同底部碎片一起将底层蔗糖溶液吸出,再小心除去上清液,得到纯净完整的原生质体。 2.PEG融和
原生质体的分离和培养
第十一章原生质体的分离和培养 1 引言 植物原生质体培养和细胞融合是植物细胞工程的核心技术,它是20世纪60年代初,人们为了克服植物远缘杂交的不亲和性,利用远缘遗传基因资源改良品种而开发完善起来的一门技术。植物原生质体是遗传转化的理想受体,能够比较容易地摄取外来遗传物质,如外源DNA、染色体、病毒、细胞器等,为高等植物在细胞水平或分子水平上的遗传操作提供了理想的实验体系。 原生质体是指用特殊方法脱去植物细胞壁的、裸露的、有生活力的原生质团。就单个细胞而言,除了没有细胞壁外,它具有活细胞的一切特征。1960年英国植物生理学家Cocking首次利用纤维素酶等从番茄根细胞分离原生质体获得成功。1971年Takebe等培养烟草叶片原生质体获得再生植株,首次证实了原生质体的全能性。1972年美国科学家Carl.son等利用细胞融合技术,首次获得两种不同烟草原生质体融合的体细胞杂种。1974年高国楠等开发出了PEG(聚乙二醇)融合方法。1978年德国科学家Melchers等把马铃薯和番茄的原生质体进行融合,获得了体细胞杂种——马铃薯番茄。1981年Zimmermann开发出了高压脉冲法,即电融合技术。 植物原生质体培养和细胞融合技术已经成熟,并成为品种改良和创造育种亲本资源的重要途径。迄今已在多种作物上获得了原生质体植株和种、属间杂种植株,也为细胞生物学、植物生理学及体细胞遗传学的研究做出了重要贡献。
第一节植物原生质体分离 一、原生质体分离 (一)植物细胞膜电特性和膜电位 植物细胞膜是一个由脂类和蛋白质等构成的双层分子层膜,其物理性质类似于一个双电层,细胞的内外层带的是同种电荷。不同植物的细胞膜电位不同,同种植物细胞倍性不同以及在不同外界离子环境下,其细胞膜的膜电位也不同(表7-1、表7-2)。了解植物细胞膜的电特性对细胞融合的研究很有-必要。 原核生物遗传饰变过去几十年取得了很大进展,转导和转化现已成为对微生物进行遗传操作的标准方法。利用微生物进行遗传操作研究的优点是:①这些单细胞和单染色体系统既简单又容易控制;②它们的复制周期很短。在真核生物中将遗传物质由一个个体转移给另一个个体的传统方法是有性杂交,它所能进行的范围极为有限,尤其在动物中是这样。就是在植物中,虽然远缘杂交并非不可能,但由于有性不亲合性的障碍,有时在选定的亲本之间也难以获得完全的杂种(见第9章和第10章),这是通过杂交进行作物改良的一个严重障碍。在这点上细胞融合为远缘杂交提供了一个很有潜力的新途径(体细胞杂交)。无论是在植物中还是在动物中,细胞融合必须穿越质膜才能完成。植物与动物不同,在质膜之外还有一层坚硬的纤维素壁,相邻的细胞被一层主要由果胶质构成的基质粘连在一起。主要由于这个原因,体细胞遗传学在动物中的发展远远超过了在植物中的发展。只是自1960年以来,由于Cocking证实了通过酶解细胞壁可以获得大量
植物原生质体相关材料
植物原生质体相关材料 2013-9-2 From HZB 一、植物材料 研究表明,几乎从植物的所有部位都能得到原生质体,其中以叶片为多。根尖组织也是植物原生质体的重要来源,它可由各种植物的种子萌发后取得。花粉经特异酶处理也能得到原生质体,在单倍体遗传育种中有特殊的用途。 但是,要获得高质量的原生质体,则须选用生长旺盛、生命力强的组织作材料。材料的生理状况是原生质体质量的决定性因素之一。 1. 细胞悬浮培养物 在建立细胞悬浮培养物之前,需提前培养愈伤组织: 取用成熟种子胚、未成熟胚、幼穗、花药、胚芽鞘或幼叶,经无菌消毒后,在26℃黑暗条件下,在含2,4-D 2-4mg/L的MS固体培养基上,诱导愈伤组织,每隔2-4d转接一次。从中选出增殖较快而且呈颗粒状的愈伤组织,或经继代培养一次后,转移到液体培养基的100ml三角瓶中进行悬浮培养。具体方法是用旋转式振荡器,速度控制在80-120r/min,在25±1℃下暗培养。通常经悬浮培养3~4月后,悬浮培养细胞的大小变得较为一致,且细胞质变得较浓时,可用作分离原生质体。 2. 叶肉细胞 叶肉细胞是分离原生质体的最好的细胞材料,用叶片的薄壁组织作为材料来源,既要考虑植株的生长环境,又要考虑叶片的年龄及其生理状态对原生质体分离的影响。取生理状态适宜的叶片,有利于原生质体的细胞再生和细胞分裂。要获得良好的培养材料,下列外界因素是需要着重考虑的: (1)光强为3000-6000lx。 (2)温度为20-25℃培养。 (3)相对湿度在60%-80%左右。 植物的其他器官也可用于分离原生质体,如用花粉四分体和花粉壁细胞。 3. 植物材料的预处理 对原生质体材料进行预处理能提高原生质体的分裂频率;也可以逐步提高植物材料的渗透压,以适应培养基中的高渗环境。这些处理包括:暗处理、预培养、低温处理等。 例如,把豌豆的枝条取下后,在分离原生质体前,先让材料在黑暗中的一定湿度条件下放1~2d,这样得到的原生质体存活率高,并能继续分裂。在羽衣甘蓝叶肉组织原生质体分离和培养中,先去掉叶片的下表皮,再在诱导愈伤组织的培养基中预培养7d,然后再去壁;经预培养的叶片分离的原生质体高度液泡化,叶绿体也解体。龙胆试管苗的叶片只有用4CC低温处理后分离得到的原生质体才能分裂。但在很多情况下材料不必经过专门的预处理。 二、酶 1. 酶的种类 构成植物细胞壁的三个主要成分是:①纤维素,占细胞壁干重的25%至50%不等;②半纤维素,平均约占细胞壁干重的53%左右;③果胶质,一般占细胞壁的5%。分离原生质体最常用的酶有纤维素酶、半纤维素酶和果胶酶。 ZA3-867纤维酶是上海植物生理研究所从野生型绿色木霉同各菌种中提取制成的,粗制品是多种酶的复合物,含有纤维素酶(包括C1、CX、B一葡萄糖苷酶等)、果胶质、半纤维素酶等,分离细胞壁的效果较好。这种复合酶使用时不需加半纤维素酶和果胶酶等,就可以分离出植物原生质体。 日本产的Onozuka纤维素酶常和果胶酶结合使用,可先用果胶酶降解果胶,使分开细胞,再用纤维素酶处理降解细胞壁。即二步法降解。 2. 渗透稳定剂
植物原生质体培养方法
植物原生质体培养方法 1 植物原生质体培养的简史 植物细胞原生质体, 在植物学上指植物细胞通过质壁分离后, 可以和细胞壁分开的那部分细胞物质。原生质体分离纯化后, 须在适当的培养基上应用适当的培养方法, 才能再生细胞壁, 并启动细胞持续分裂, 直至形成细胞团、长成愈伤组织或胚状体、分化和发育成苗, 最终再生完整植株。其中, 选择合适的培养方法始终是原生质体培养中最基础也是最关键的一环。 植物原生质体培养方法起源于植物单细胞培养方法。早在1902 年,Haberlant 通过实验就预言: 体外培养单个细胞可通过其分裂得到培养组织。直到1954 年, 植物单细胞培养才获得成功。M uir 将培养的万寿菊及烟草悬浮细胞植入到长有愈伤组织的培养基上而得到了它们的单细胞克隆, 并建立了看护培养的方法。悬滴培养由De Ropp1954 年开创, 1960 年Jones 等完善了这一技术, 并建立了微室培养的方法。同年, Cock ing 应用酶法分离原生质获得了成功, 从而在实验条件下很容易获得大量的原生质体。随着多种适用于原生质体分离的商品酶的出现, 原生质体的培养方法也得到了不断的改进, 现在常用的液体浅层培养、双层培养法、琼脂糖包埋法、琼脂岛培养法以及使用条件培养基或饲喂培养等技术, 使原生质体培养获得了极大的成功。 2 原生质体培养方法 2. 1 液体培养法 2. 1. 1 液体浅层培养(L iquid th in culture) 这是目前较常用的原生质体培养方法, 一般适用于容易分裂的原生质体, 将含有原生质体的培养液在培养皿底部铺一薄层, 封口进行培养。这种方法操作简单, 对原生质体损伤较小, 且易于添加新鲜培养物。用这种方法, J.T rmeouillaax 等成功地培养长春花冠瘿组织的激素自养型的原生质体单细胞克隆; H isato Kunitake 等也在改良的M S 培养基上培育了Eustom a g rend if lorum (龙胆科, 原产美国) 原生质体再生植株。但这种方法也常使原生质体分布不均匀, 发育的原生质体之间产生粘连而影响其进一步的生长和发育, 尤其是难以定点观察单个原生质体的命运。王吉吉之等认为液体浅层培养在培养过程中, 应经常轻轻晃动培养基, 以增强通气, 促进愈伤组织形成。 2. 1. 2 微滴培养(D rop let culture) 微滴培养是由液体浅层培养发展起来的一种方法, 它克服了后者局部密度过高和原生质体粘聚的缺点。此方法是将0. 1m l 或更少的原生质体悬浮液用滴管滴于培养皿底部, 封口后进行培养。为避免微滴蒸发, 可将培养器皿置于湿润的环境中, 或在微滴上覆盖矿物油。此法适用于融合体及单个原生质体培养, 尤其适用于较多组合的实验。为了比较黄瓜两个品系在不同的植板密度以及在不同的激素水平下原生质体生长情况, Z. K. Punja 等选用了此方法获得很好的效果; 同样, S. V essabutr 等培养百脉根时也比较了不同预处理、不同酶液组合对原生质体培养的影响。 2. 2 固体培养—— 琼脂糖平板法(A grose beadmethed) 固体培养作为凝固剂的物质可以是琼脂、琼脂糖或Gellan gum , 近来很多实验证明, 琼脂糖尤其是低熔点的琼脂糖是一种良好的培养基凝固剂, 并且具有促进原生质体细胞分裂的作用。琼脂糖平板法是将原生质体纯化后悬浮在液体培养基中, 然后与热融并冷却到45℃的琼脂糖按一定比例混合, 轻轻摇动使原生质体均匀分布, 凝固后封口培养。由于原生质体彼此分开并固定了位置, 就避免了细胞间有害代谢产物的影响, 既便于定点观察, 又有利于追踪原生质体再生细胞的发育过程。Z. K. Punja 等证明琼脂平板法比微滴培养及液体浅层培养具有更高的植板率; 甘霖等也得出同样结论。但此种方法对操作技术要求比较严格, 尤其是温度一定要适宜; 添加低渗透压的培养基和转移再生愈伤组织也比较繁琐, 而且培养的原生质体极易褐变死亡。 2. 3 液体2固体结合培养 2. 3. 1 双层培养法(A grose2liquid doublelayer) 这种方法即在培养皿的底部先铺一薄层含或不含原生质体或细胞的固体培养基,
植物组织培养 第十章 原生质体培养
第十章原生质体培养 ?教学目的与要求: ?深入了解植物细胞结构功能与细胞全能性表达的关系,掌握原生质体的分离以 及培养过程中渗透压和激素的调控原理与技术。 第一节、原生质体研究概况 一、原生质体的概念 ?原生质体(p r o t o p l a s t):指除去细胞壁的细胞或是说一个被质膜所包围的裸露 细胞。 二、原生质体研究进展 ?据统计,目前已有49个科,146个属的320多种植物经原生质体培养得到了再 生植株(1993)。其趋势仍以农作物和经济作物为主,但从一年生向多年生、草本向木本、高等植物向低等植物扩展。 三、原生质体研究的意义 ?1、除去了细胞壁为植物细胞之间的融合扫平了障碍,同时叶为制造新杂种开辟 了道路。2、原生质体可摄入外源D N A,细胞器、细菌或病毒颗粒,这些特性与植物全能性相结合为高等植物的遗传饰变打下基础。3、获得细胞无性系和选育突变体的优良起始材料。 第二节、原生质体的制备 1、用于分离原生质体的材料准备 ?无菌试管苗叶片 ?上胚轴和子叶 ?培养细胞 2、酶处理 ?原生质体分离常用的商品酶 ?纤维素酶类 ?果胶酶类 ?半纤维素酶 酶溶剂及其渗透压 ?酶溶剂:原生质体培养基或特殊配制。 ?渗透压调节剂:葡萄糖、甘露醇、山梨醇等。 ?酶浓度及酶解时间 ?酶解时间 ?酶浓度酶解温度 3、原生质体的收集和纯化 ?飘浮法:常用的飘浮剂有蔗糖、P e r c o l l、F i c o l l。 ?P e r c o l l是一种包有乙烯吡咯烷酮的硅胶颗粒。渗透压很低(<20m o s m/k g H2O), 粘度也很小,可形成高达1.3g/m l密度,采用预先形成的密度梯度时可在低离心力(200~1000g)于数分至数十分钟内达到满意的细胞分离结果。由于P e r c o l l 扩散常数低,所形成的梯度十分稳定。此外,P e r c o l l不穿透生物膜,对细胞无毒害,因此广泛用于分离细胞、亚细胞成分、细菌及病毒,还可将受损细胞及其碎片与完好的活细胞分离。
原生质体
原生质体(Protoplast):指采用机械或酶解法去掉细胞壁的裸露细胞。 一、原生质体的应用 由于没有细胞壁,原生质体为作物遗传改良和植物学研究提供了极为有利的试验材料。原生质体可以用于下面几种研究。 用作细胞杂交服务于作物改良用作遗传转化的对象 研究细胞壁的发生过程筛选突变体 膜的结构、运输、激素接受位点等的研究用于分离细胞器和大分子 种质资源保存 二、原生质体分离、纯化 原生质体分离的最基本原则是保证原生质体不受伤害及不损害它的再生能力。 (一)分离方法 机械法分离 缺点:产量极低;应用的材料受限制;操作极费力 酶法分离 Cocking最早开展这方面研究 克服了机械法分离的缺陷,可分为直接法和顺序法两种。 酶法可在短时间内获得大量原生质体,缺点是:不纯的酶制剂所含杂质对原生质体可能有不同程度的毒害作用。 (二)影响原生质体分离的因素(酶法) 从理论上讲,只要用适当的酶处理,就能从任何活组织中分离得到原生质体。但是对于原生质体培养来说,要得到活性高、能进行分裂、形成愈伤组织、最后再生完整植株的原生质体则受许多因素的影响。原生质体分离时主要应考虑取材、酶的种类、纯度、酶液的渗透压、酶解时间、温度等。 1. 外植体来源: 生长旺盛、生命力强的组织和细胞是获得高活力原生质体的关键,并影响着原生质体的复壁、分裂、愈伤组织形成乃至植株再生。用于原生质体分离的植物外植体有叶片、叶柄、茎尖、根、子叶、茎段、胚、愈伤组织、悬浮培养物(Suspension cultures)、原球茎、花瓣和叶表皮等。叶肉细胞是常用的材料,因为叶片很易获得而且能充分供应。取材时,一般用刚展开的幼嫩叶片。另一个分离原生质体的常用材料是愈伤组织或悬浮细胞,采用其作材料可以避免植株生长环境的不良影响,可以常年供应,易于控制新生细胞的年龄,处理时操作方便,无需消毒. 选用悬浮细胞作材料时,需每隔3-5天继代一次,培养一段时间使细胞处于旺盛生长状态。一般在继代后的第三天游离原生质体。 2. 酶液组成和浓度: 纤维素,占壁干重的25-50% 植物细胞壁由三个主要成分构成 半纤维素, 平均53% 果胶质, 5%
植物原生质体培养
原生质体的培养 1. 原生质体的分离与纯化 原生质体培养的意义 (1)再生植株由原生质体再生生成植株,不论在进行有关细胞生物学或生物合成和代谢的实验研究上,还是在组织培养实践中,都有一定的优点:①可利用均一的分化细胞群体; ②因无细胞壁,试剂对细胞作用更为直接,其反应能直接测量,以使反应产物能较快的分离出来;③在理论和实践中,可极大节省空间,如在一个三角瓶就能培养210个细胞,但在大田种植需要4亩地;④可缩短实验周期,如悬浮培养时仅需1~2个小时。 原生质体培养可在遗传学方面进行基因互补,不亲和性,连锁群和基因鉴定,分析基因的激活和失活水平的研究。在研究分化问题时,用一个均一的原生质体群体可以筛选数以千计的不同。营养和激素条件,探索诱导单细胞的分化条件等。 (2)用于远缘体细胞融合,进行体细胞杂交。这是一种新的远缘杂交方法,为人们提供新的育种方法。两个亲缘关系较远的植株用一般杂交方法是不容易成功的,而用细胞融合的方法却成为可能。首先,两个原生质体融合形成异核体,异核体再再生细胞壁,进行有丝分裂,发生核融合,产生杂种细胞,由此可培养新的杂种。 一、原生质体(protoplast)的分离 (一)材料来源 原生质体是通过质壁分离与细胞壁分开的部分,是能存活的植物细胞的最小单位。自从1960年用酶法制备大量植物原生质体首次获得成功以来,原生质体培养成为生物技术最重要的进展之一。通过大量的试验表明,没有细胞壁的原生质体仍然具有"全能性",可以经过离体培养得到再生植株。原生质体的分离研究较早,1892年Klereker首先用机械的方法分离得到了原生质体,但数量少且易受损伤。1960年,英国植物生理学家Cocking首先用酶解法从番茄幼苗的根分离原生质体获得成功。他使用一种由疣孢漆斑菌培养物制备的高浓度的纤维素酶溶液降解细胞壁。然而,直至1960年纤维素酶和离析酶成为商品酶投入市场以后,植物原生质体研究才成为一个热门的领域。至今从植物体的几乎每一部分都可分离得到原生质体。并且能从烟草、胡萝、矮牵牛、茄子、番茄等70种植物的原生质体再生成完整的植株。此外,原生质体融合,体细胞杂交的技术也得到广泛的应用。 (二)分离方法 1.机械分离法 1982年,Klercker第一次用机械方法从Stratiots aloides中获得原生质体.他们的做法是首先使细胞发生质壁分离,然后切开细胞壁释放出原生质体. 2.酶法分离 (1)酶的种类及特点 构成植物细胞壁的三个主要成分是: ①纤维素酶类:占细胞壁干重的25%至50%不等。 ②半纤维素酶类:平均约占细胞壁干重的53%左右。 ③果胶酶类:一般占细胞壁的5%。分离原生质体最常用的酶有纤维素酶、半纤维素 酶和果胶酶。
原生质体融合技术
原生质体融合技术的局限性 植物原生质体是指用特殊方法去细胞壁的、裸露的、有生活力的原生团。这种裸露细胞在适当的外界条件下,还可形成细胞壁,进行有丝分裂,形成愈伤组织和诱发再生植株,因而仍然具有细胞的全能性。 植物原生质体融合技术是借鉴于动物细胞融合的研究成果,在原生质体分离培养的基础上建立起来的,以植物的原生质体为材料,通过物理、化学等因素的诱导,使两个原生质体融合在一起以致形成融合细胞的技术。它不是雌雄孢子之间的结合,而是具有完整遗传物质的体细胞之间的融合,是2种原生质体间的杂交。通过原生质体融合可以把带有不同的基因组的两个细胞结合在一起,与有性杂交相比,无疑可以使“杂交”亲本组合的范围扩大,不但可以利用细胞核内基因资源,还可以利用包含在细胞质中的诸如叶绿体和线粒体DNA的遗传资源。 原生质体培养是细胞杂交的基础,但是直到目前为止,也只有360多个种的原生质体培养再生了完整的植株,大多数重要的植物尤其是木本植物如葡萄、棕榈、橡胶、茶、香蕉、椰子和芒果等的原生质体再生仍然很困难,或者还未进行深入研究。在原生质体再生的物种中,茄科占了将近1/4,并且用于育种目的的大多数体细胞杂种和细胞质杂种也比较集中于茄属、烟草属、苜蓿属、柑橘属、芸薹属和番茄属等6个属中。因此,为了有效地进行植物遗传改良,不但要使杂种细胞再生成完整植物,而且还必须提高植株再生的频率,以便有足够的群体进行有效的选择。但目前存在的一个普遍的问题使许多原生质体再生的程序似乎较低,重复性较差,并且还具有基因型的依赖性。为了将体细胞杂交技术应用于更多的植物中,还需要更加深入地研究植物细胞的分化、脱分化和再分化等发育机制。 1.技术局限性 植物细胞杂交的本质是将两种不同来源的原生质体,在人为的条件下进行诱导融合。由于植物细胞的全能性,因此融合之后的杂种细胞,可以再生出具有双亲性状的杂种植株。因此,细胞融合也叫原生质体融合或细胞杂交。其包括三个主要环节:诱导融合;选择融合体或杂种细胞;杂种植株的再生和鉴定。 1.1诱导原生质体融合 诱导原生质体融合是体细胞杂交的最基本的技术环节。融合方法的选择受到很多实验条件的限制。常用的化学方法有化学方法与电融合方法。化学方法中用的最多的是聚已二醇(PEG)融合技术。但是这种方法中PEG与高PH强加于原生质体的非常生理条件,PEG 的相对分子质量、纯度、浓度、处理时间、原生质体的状况和密度等都会影响PEG融合技术,而且其融合过程繁琐,PEG可能对细胞有毒害作用;而影响电融合的因素有电融合技术中交流电的强弱、处理时间的长短、电脉冲的大小电极的材料和间距、直流脉冲的强度、宽幅以及次数等。 而且对于不同的植物材料需要经过多次实验,才能找出这些参数的适当值。这就制约了原生质体融合技术成为常规育种方法。 1.2杂种细胞的选择 为了将杂种细胞与未融合的、同源融合的亲本细胞区分开,一般有以下选择方法: 1.2.1利用或诱导各种缺陷型或抗性细胞系,用选择培养基将互补的杂种细胞选择出来; 互补选择一般要求有相应的突变体。在体细胞杂交的研究中,虽然人们已经建立和利用了各种各样的突变体,但是在植物中要建立突变细胞系比较困难,如果要使突变细胞系保持再生能力就更难了,因此在实际应用中受到很大的限制。 1.2.2机械选择法 利用荧光素标记分离杂种细胞取得了一定的成效,但是显微镜操作费工费时,选择出异
实验一植物原生质体的分离和培养一教学目标 了解植物原生质
实验一植物原生质体的分离和培养 一.教学目标:了解植物原生质体作为细胞工程研究的重要意义,了解原生质体活性鉴定的原理。掌握分离和培养原生质体的技术、方法和原理。掌握细胞活性的检测方法。掌握细胞计数的原理和方法。二.重点:掌握分离和培养原生质体的技术、方法和原理。掌握细胞活性的检测方法。掌握细胞计数的原理和方法。 三.难点:分离和培养原生质体的技术。 四.授课方式与教学方法:讲解原理、实验操作示范或具体指导。 五.教学内容: 实验原理 植物原生质体(protoplast)是除去细胞壁后为原生质所包围的“裸露细胞”,是开展基础研究的理想材料。其中,酶解法分离原生质体是一个常用的技术,其原理是植物细胞壁主要由纤维素、半纤维素和果胶质组成,因而使用纤维素酶、半纤维素酶和果胶酶能降解细胞壁成分,除去细胞壁,即可得到原生质体。由于原生质体内部与外界环境之间仅隔一层薄薄的细胞膜,必须保持在渗透压平衡的溶液中才能保持其完整性, 使原生质体分离后不致膨胀破裂,渗透剂常用甘露醇或蔗糖,酶液还应含一定Ca2+来稳定原生质膜。其次,还应当考虑取材、酶的种类和纯度、酶液的渗透压、酶解时间及温度等因素对分离原生质体的影响。将原生质体接种在培养基上进行培养,细胞壁再生,细胞分裂和再生植株。 测定原生质体的活性有多种方法。荧光素双醋酸酯(FDA)染色是常用的一种方法,FAD 本身无荧光,无极性,可透过完整的原生质膜。一旦进入原生质体后,由于受到酯酶分解而产生具有荧光的极性物质荧光素。它不能自由出入原生质膜,因此有活力的细胞能产生荧光,无活力的原生质体不能分解FAD无荧光产生。 细胞计数一般用血细胞计数极,按白细胞计数法进行计数。 从理论上讲,植物体的任何一部分都可以通过酶解作用去除细胞壁而得到原生质体。但在实际操作中,只有幼嫩的组织才能完成去壁的过程。所以,为了制备健康的原生质体,
园艺植物原生质体融合技术研究报告进展
1引言 原生质体融合
植物原生质体融合方法的研究进展
龙源期刊网 https://www.360docs.net/doc/3f3825812.html, 植物原生质体融合方法的研究进展 作者:李琦 来源:《种子科技》2018年第06期 摘要:原生质体融合(protoplast fusion)是指通过物理或化学方法使两个细胞的原生质体进行融合,经培养获得具有双亲全部或部分遗传物质后代的方法。应用植物原生质体融合技术,可以克服远缘杂交不亲和的障碍,打破物种之间的生殖隔离,扩大杂交亲本范围,实现基因在物种间的转移和遗传重组,培育新品种和创造新物种。主要就植物原生质体融合的方法进行了阐述。 关键词:植物原生质体;融合方法;研究进展 文章编号: 1005-2690(2018)06-0038-02 中图分类号: Q943 文献标志码: A 原生质体是组成细胞的一个形态结构单位,原生质体是指被去掉了细胞壁后的被细胞膜包围的“裸露细胞”,是开展基础研究的主要材料。1960年英国科学家Cocking第一次用酶法大量制备原生质体,Cocking采用的方法是在番茄幼苗的根组织中加入可降解细胞壁的等渗酶液,在一定条件下培养一段时间后,发现大部分细胞的细胞壁被降解,从而制备出大量有活力的原生质体。 1 原生质体融合的目的及意义 原生质体融合技术可克服不同原生质体间的排斥力,使两种不同种属的原生质体间发生膜融合、胞质融合和核融合,进而形成具有含两种遗传物质的杂交细胞,克服远缘杂交的不亲和性和子代不育等障碍。另外,可转移优良的生物性状,实现基因重组,而改良现有品种。目前原生质体融合所改良的目标性状包括抗冻、抗干旱、抗病毒、抗虫、耐高盐等,还可按照人们预先的期望创造出新物种。 2 原生质体的融合方法 2.1 自发融合 在酶解细胞壁形成原生质体的过程中,相邻的原生质体会因细胞间胞间连丝的扩展和粘连而彼此融合形成同核体(homokaryon)。每个同核体内可包含两个或多个核,这种类型原生质体的融合被称作为自发融合。多核融合体常出现在植物幼嫩叶片或分裂旺盛的培养细胞制备的原生质体中。如在玉米胚乳愈伤组织细胞和玉米胚悬浮细胞原生质体中,大约有50%是多核融合体。 2.2 高pH-高Ca2+法
原生质体融合(实验报告)
酵母原生质体融合 ××××××××××酵母有发酵工业的灵魂之称,其发酵性能的好坏直接影响发酵产品的质量,同时也决定着发酵工艺流程和运转周期及运转费用[1]。因此,选育优良的酵母菌种在发酵工业中具有重要的意义[2]。对酿酒酵母的选育始终是酿酒工作者所要从事的重要工作之一。好的酿酒酵母能够提高酒的质量和产量,赋予酒良好的风味;能够简化工艺流程,减少设备投资;能够缩短发酵周期,降低运转费。 原生质体融合育种( protoplast fusion)是20世纪60年代发展起来的基因重组技术。通过两个遗传性状不同的亲株原生质体融合从而达到杂交目的。1960年法国的Barsi研究小组在培养两种不同动物细胞混合时发现了自发融合现象,同时日本的Dkada发现仙台病毒可诱发内艾氏腹水病细胞彼此融合,从而开始了细胞融合的探索。国内外对原生质体融合技术的研究都比较成熟, 一般认为酵母菌原生质体融合技术的关键点有原生质体的制备和再生、原生质体的融合以及融合子的筛选等。传统的对酿酒酵母的选育方法主要有自然分离、连续培养和诱变育种[3]。近年来重组技术,基因工程和原生质体融合技术迅速发展,得到了广泛应用。 两个或两个以上的细胞经过自然的或者人为的作用合并成为一个细胞叫融合细胞,这个过程就称为细胞融合过程。用微生物作材料进行细胞融合,必须消除细胞壁和细胞膜。通常采用酶解作用破除细胞壁,采用聚乙二醇促使细胞膜融合。细胞融合之后,还经过细胞质融合,细胞核重组,细胞壁再生等一系列过程才能形成具有生活能力的新菌株。融合后的细胞有两种可能:一是染色体DNA不发生重组,两种细胞的染色体共存于一个细胞内,形成异核体,这是不稳定的融合。另一类是两亲本细胞核染色体DNA真正发生重组。通过连续传代分离纯化可以区别这两类融合。应该指出,即便是真正的重组融合子,在传代中也有可能发生分离,产生回复或新的遗传重组体。因此,必须经过多次分离纯化才能够获得稳定的融合子。 本实验将通过酿酒酵母2.339与酿酒酵母2.70的融合,以期获得具有更高发酵效率的酿酒酵母新品种并应用于制酒工业,在节省酿酒粮食的投入量前提下提高发酵产量。以期获得更好的经济价值。 1.材料与方法 1.1 材料
植物原生质体的分离与融合
细胞工程 实验六植物原生质体的分离与融合 实验概要 本实验介绍了原生质体分离的方法及利用PEG原生质体融合的原理和方法。 实验原理 植物原生质体是除去细胞壁后为原生质所包围的“裸露细胞”,是开展基础研究的理想材料。其中酶解法分离原生质体是一个常用的技术,其原理是植物细胞壁主要由纤维素、半纤维素和果胶质组成,因而使用纤维素酶、半纤维素酶和果胶酶能降解细胞壁成分,除去细胞壁,即可得到原生质体。由于原生质体内部与外界环境之间仅隔一层薄薄的细胞膜,必须保持在渗透压平衡的溶液中才能保持其完整性。其次,还应当考虑取材、酶的种类和纯度、酶液的渗透压、酶解时间及温度等因素对分离原生质体的影响。测定原生质体的活性有多种方法。荧光素双醋酸酯(FDA)染色是常用的一种方法,FAD本身无荧光,无极性,可透过完整的原生质膜。一旦进入原生质体后,由于受到酯酶分解而产生具有荧光的极性物质荧光素。它不能自由出入原生质膜,因此有活力的细胞能产生荧光,无活力的原生质体不能分解FAD无荧光产生。许多化学、物理学和生物学方法可诱导原生质体融合,现在被广泛采用并证明行之有效的融合方法是聚乙二醇(PEG)法、高钙高pH法和电融合法;聚乙二醇(PEG)作为一种高分子化合物,20~50%的浓度能对原生质体产生瞬间冲击效应,原生质体很快发生收缩与粘连,随后用高钙高pH法进行清洗,使原生质体融合得以完成。聚乙二醇(PEG)诱导如何的机理:聚乙二醇(PEG)由于含有醚键而具有负极性,与水、蛋白质和碳水化合物等一些正极化基团能形成氢键,当聚乙二醇(PEG)分子足够长时,可作为临近原生质表面之间的分子桥而使之粘连、聚乙二醇(PEG)也能连接钙等阳离子,钙可在一些负极化基团和聚乙二醇(PEG)之间形成桥,因而促进粘连。从而引起原生质体融合:高钙高pH由于增加了质膜的流动性,因而也大大提高了融合频率,洗涤时渗透压冲击也可能起作用。原生质体分离纯化后,在适当的培养基上应用合适的培养方法,能够再生细胞壁,并启动细胞持续分裂,直至形成细胞团,长成愈伤组织或胚状体,再分化发育成苗。其中,选择合适的培养基及培养方法时原生质体培养中最基础也是最关键的环节。PEG为一种高分子化合物,能与水、蛋白质、和碳水化合物等一些基团能形成氢键。普遍认为聚乙二醇分子能改变各类细胞的膜结构,使两细胞接触点处质膜的脂类分子发生疏散和重组,由于两细胞接口处双分子层质膜的相互亲和以及彼此的表面张力作用,从而使细胞发生融合。该方法的优点是:用法简单,容易获得融合体,融合效果好。 主要试剂 1. 20%蔗糖; 2. 13%CPW洗液:
原生质体制备方法
原生质体制备方法 培养基: ①PDA:200g土豆、20g葡萄糖、20g琼脂、1L水 ②MYG液体培养基:5g麦芽糖、5g酵母提取物、10g葡萄糖、1L水、 ③MYG液体再生培养基:5g麦芽糖、5g酵母提取物、10g葡萄糖、蔗糖、1L水、 ④MYG软再生培养基:5g麦芽糖、5g酵母提取物、10g葡糖糖、8g琼脂粉、蔗糖、试剂: ①1mol/L MgSO4 ②L MgSO4 ③STC:山梨醇、50mM Tris-Hcl()、50mM CaCl2 ④肝素 ⑤SPTC:山梨醇、40% PEG、50mM Tris-Hcl()、50mM CaCl2 ⑥无菌水 操作步骤: ①倒若干PDA平板,将GF-WT接入PDA平板,23℃,活化5-7days ②用无菌黄枪头在GF-WT平板上打孔,用长牙签挑出4个菌饼接入50ml/瓶的MYG 液体培养基中,120rmp,28℃,12h ③以10%的接种量接5瓶以上50ml/瓶的MYG液体培养基中,60rpm,28℃,16h ④混有大量悬浮菌丝的培养基用无菌的带有三层擦镜纸的漏斗过滤下来,用无菌 水和1mol/L MgSO4各冲洗三次,菌丝发白即可,冰上备用 ⑤酶解体系的配制:取Dryslase 45mg+Yartlase105mg至无菌量管中,用10ml 1mol/L MgSO4溶解彻底,用无菌滤头和针筒过滤除菌,滤液保存于冰上 ⑥1g菌丝加入到10ml酶解体系中,于无菌三角瓶中进行酶解反应,30℃,60rpm, 3h ⑦用带有无菌滤布的漏斗过滤酶解液,滤液用无菌50ml大管收集,用20ml L MgSO4 冲洗三角瓶和漏斗,3500rpm,10min,取上清
第7章 原生质体的培养
第7章原生质体的培养和体细胞杂交(3学时) 目的要求: (1)了解原生质体培养的意义 (2)掌握原生质体分离的大致步骤 (3)掌握原生质体培养的方法 (4)掌握原生质体融合的方凑 第一节原生质体的分离与纯化 原生质体培养的意义 (1)再生植株由原生质体再生生成植株,不论在进行有关细胞生物学或生物合成和代谢的实验研究上,还是在组织培养实践中,都有一定的优点:①可利用均一的分化细胞群体; ②因无细胞壁,试剂对细胞作用更为直接,其反应能直接测量,以使反应产物能较快的分离出来;③在理论和实践中,可极大节省空间,如在一个三角瓶就能培养210个细胞,但在大田种植需要4亩地;④可缩短实验周期,如悬浮培养时仅需1~2个小时。 原生质体培养可在遗传学方面进行基因互补,不亲和性,连锁群和基因鉴定,分析基因的激活和失活水平的研究。在研究分化问题时,用一个均一的原生质体群体可以筛选数以千计的不同。营养和激素条件,探索诱导单细胞的分化条件等。 (2)用于远缘体细胞融合,进行体细胞杂交。这是一种新的远缘杂交方法,为人们提供新的育种方法。两个亲缘关系较远的植株用一般杂交方法是不容易成功的,而用细胞融合的方法却成为可能。首先,两个原生质体融合形成异核体,异核体再再生细胞壁,进行有丝分裂,发生核融合,产生杂种细胞,由此可培养新的杂种。 一、原生质体(protoplast)的分离 (一)材料来源 原生质体是通过质壁分离与细胞壁分开的部分,是能存活的植物细胞的最小单位。自从1960年用酶法制备大量植物原生质体首次获得成功以来,原生质体培养成为生物技术最重要的进展之一。通过大量的试验表明,没有细胞壁的原生质体仍然具有"全能性",可以经过离体培养得到再生植株。原生质体的分离研究较早,1892年Klereker首先用机械的方法分离得到了原生质体,但数量少且易受损伤。1960年,英国植物生理学家Cocking首先用酶解法从番茄幼苗的根分离原生质体获得成功。他使用一种由疣孢漆斑菌培养物制备的高浓度的纤维素酶溶液降解细胞壁。然而,直至1960年纤维素酶和离析酶成为商品酶投入市场以后,植物原生质体研究才成为一个热门的领域。至今从植物体的几乎每一部分都可分离得到
实验一植物原生质体的分离和培养一教学目标 了解植物原生质
实验一植物原生质体的分离和培养一教学目标了解 植物原生质 The following text is amended on 12 November 2020.
实验一植物原生质体的分离和培养 一.教学目标:了解植物原生质体作为细胞工程研究的重要意义,了解原生质体活性鉴定的原理。掌握分离和培养原生质体的技术、方法和原理。掌握细胞活性的检测方法。掌握细胞计数的原理和方法。二.重点:掌握分离和培养原生质体的技术、方法和原理。掌握细胞活性的检测方法。掌握细胞计数的原理和方法。 三.难点:分离和培养原生质体的技术。 四.授课方式与教学方法:讲解原理、实验操作示范或具体指导。 五.教学内容: 实验原理 植物原生质体(protoplast)是除去细胞壁后为原生质所包围的“裸露细胞”,是开展基础研究的理想材料。其中,酶解法分离原生质体是一个常用的技术,其原理是植物细胞壁主要由纤维素、半纤维素和果胶质组成,因而使用纤维素酶、半纤维素酶和果胶酶能降解细胞壁成分,除去细胞壁,即可得到原生质体。由于原生质体内部与外界环境之间仅隔一层薄薄的细胞膜,必须保持在渗透压平衡的溶液中才能保持其完整性, 使原生质体分离后不致膨胀破裂,渗透剂常用甘露醇或蔗糖,酶液还应含一定Ca2+来稳定原生质膜。其次,还应当考虑取材、酶的种类和纯度、酶液的渗透压、酶解时间及温度等因素对分离原生质体的影响。将原生质体接种在培养基上进行培养,细胞壁再生,细胞分裂和再生植株。 测定原生质体的活性有多种方法。荧光素双醋酸酯(FDA)染色是常用的一种方法,FAD 本身无荧光,无极性,可透过完整的原生质膜。一旦进入原生质体后,由于受到酯酶分解而产生具有荧光的极性物质荧光素。它不能自由出入原生质膜,因此有活力的细胞能产生荧光,无活力的原生质体不能分解FAD无荧光产生。 细胞计数一般用血细胞计数极,按白细胞计数法进行计数。 从理论上讲,植物体的任何一部分都可以通过酶解作用去除细胞壁而得到原生质体。但在实际操作中,只有幼嫩的组织才能完成去壁的过程。所以,为了制备健康的原生质体,一般选用根尖、茎尖、嫩叶及对数生长期的愈伤组织为材料,一旦细胞具有木质化或次生加厚的外壁,则不能被酶降解。因此,取材成为实验成功与否的首要问题。花期短的花瓣,由于其组织鲜嫩,又具有色素标记,是该实验中较好的材料。 实验方法 1.把叶片(或花期短的花瓣)洗净,把表面水吸干。(2人一组)
