光谱总结汇编
1、太阳光谱
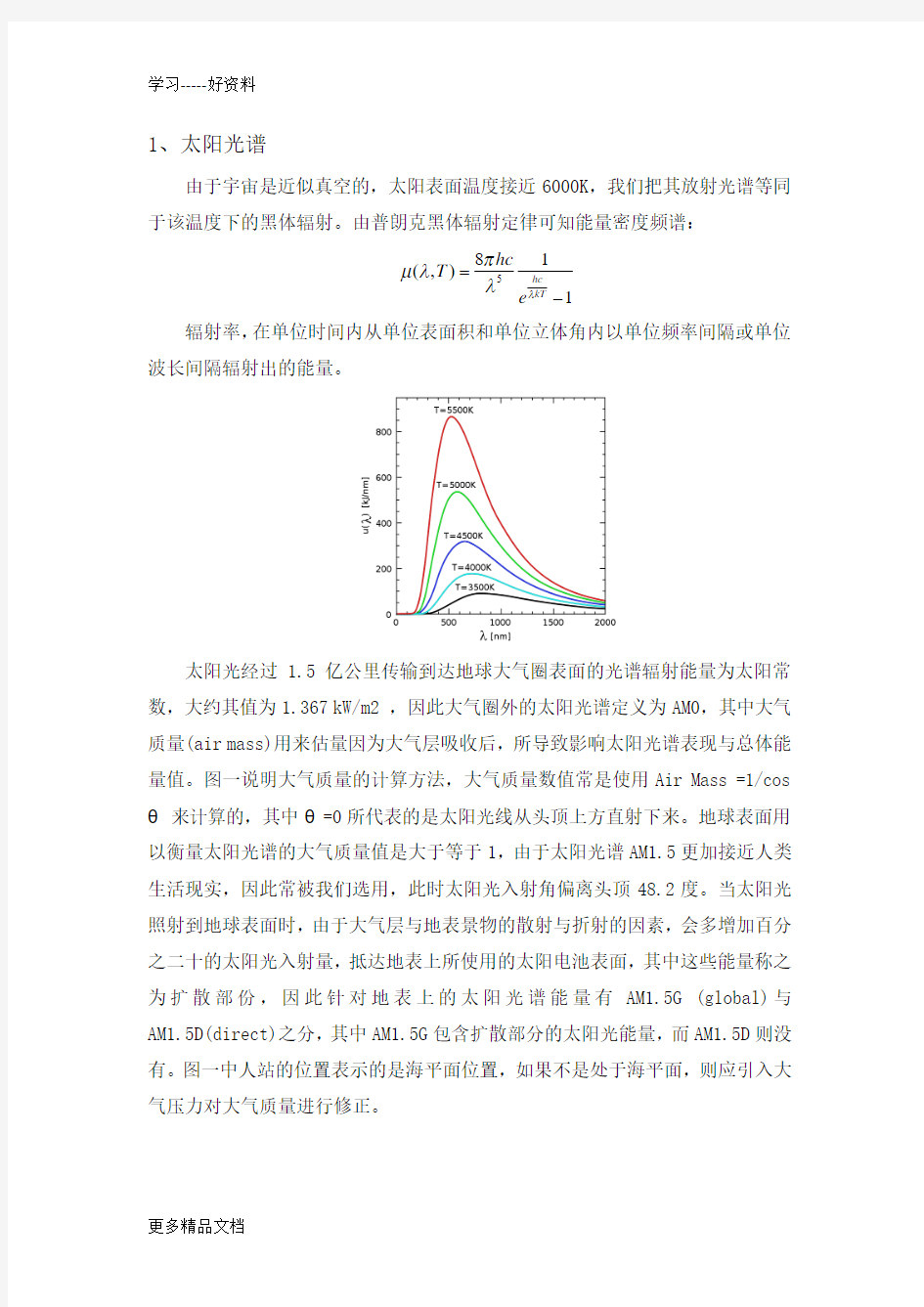
由于宇宙是近似真空的,太阳表面温度接近6000K ,我们把其放射光谱等同于该温度下的黑体辐射。由普朗克黑体辐射定律可知能量密度频谱:
581
(,)1
hc
kT hc T e λπμλλ=- 辐射率,在单位时间内从单位表面积和单位立体角内以单位频率间隔或单位波长间隔辐射出的能量。
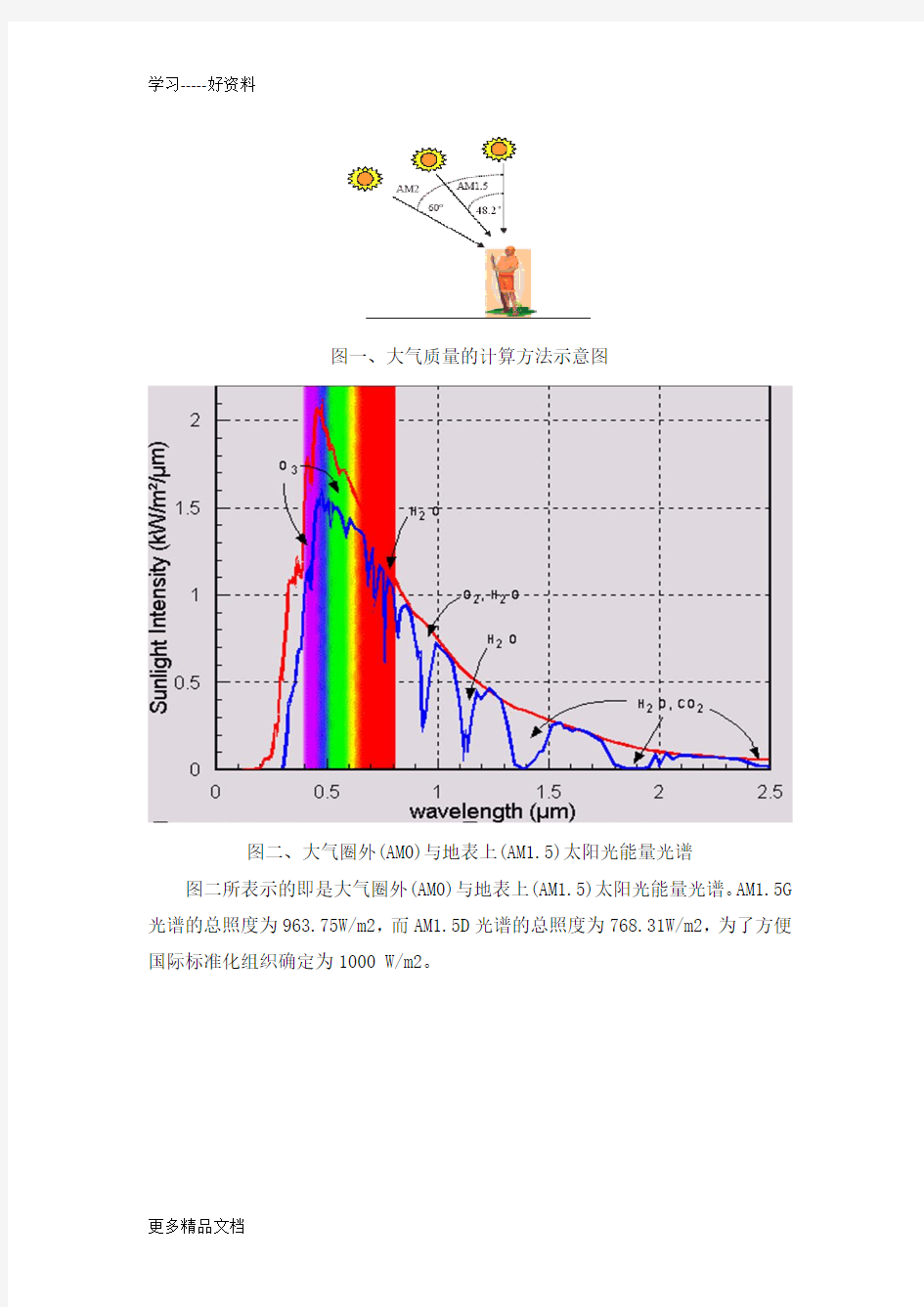
太阳光经过 1.5亿公里传输到达地球大气圈表面的光谱辐射能量为太阳常数,大约其值为1.367 kW/m2 ,因此大气圈外的太阳光谱定义为AM0,其中大气质量(air mass)用来估量因为大气层吸收后,所导致影响太阳光谱表现与总体能量值。图一说明大气质量的计算方法,大气质量数值常是使用Air Mass =1/cos θ来计算的,其中θ=0所代表的是太阳光线从头顶上方直射下来。地球表面用以衡量太阳光谱的大气质量值是大于等于1,由于太阳光谱AM1.5更加接近人类生活现实,因此常被我们选用,此时太阳光入射角偏离头顶48.2度。当太阳光照射到地球表面时,由于大气层与地表景物的散射与折射的因素,会多增加百分之二十的太阳光入射量,抵达地表上所使用的太阳电池表面,其中这些能量称之为扩散部份,因此针对地表上的太阳光谱能量有AM1.5G (global)与AM1.5D(direct)之分,其中AM1.5G 包含扩散部分的太阳光能量,而AM1.5D 则没有。图一中人站的位置表示的是海平面位置,如果不是处于海平面,则应引入大气压力对大气质量进行修正。
图一、大气质量的计算方法示意图
图二、大气圈外(AM0)与地表上(AM1.5)太阳光能量光谱图二所表示的即是大气圈外(AM0)与地表上(AM1.5)太阳光能量光谱。AM1.5G 光谱的总照度为963.75W/m2,而AM1.5D光谱的总照度为768.31W/m2,为了方便国际标准化组织确定为1000 W/m2。
图三、各省太阳能资源分布图
2、大气因素
图四、大气中各成分含量和分布
大气对太能辐射的影响主要有反射、吸收、散射。
大气散射
当太阳光遇到大气中小微粒,且这些分子或者微粒的直径小于或相当于辐射波长时,使传播方向发生改变。大气散射主要形式有:瑞利散射、米氏散射和非选择性散射。
时引起的散射。散射系瑞利散射:散射粒子的直径比光波波长要小很多(d
数于波长的四次方成反比,波长越长,大气散射能力越强。主要由大气分子引起。 米氏散射:当微粒的直径和辐射波长接近时(/3 非选择性散射:质点直径大于电磁波波长时,散射率与波长没关系。 大气反射:太阳辐射穿过大气时,被大气中的云层和较大尘埃将其一部分反射到宇宙空间去,从而削弱到达地面的太阳辐射。大气中的反射对各种波长没有选择性,反射光呈白色。大气反射物质中云最为重要,其反射强度随云状、云厚而不同,高云反射率约为25%,中云为50%,低云为65%,云层愈厚反射愈强,一般情况下云的平均反射率为50—55%。大气反射有助于削弱太阳辐射,尤其能减少紫外线对人体的灼伤。 图五、大气对太阳辐射的吸收、散射、反射 大气吸收 光波在大气中传播时,大气中各气体成分会吸收某些波长的波。吸收作用比较显著的气体成分是水汽、二氧化碳和臭氧等,它将所吸收的光波能量转变成热能和电离能等。臭氧主要吸收紫外光,太阳光辐射中99%的紫外光都被臭氧层吸收了。二氧化碳和水主要吸收的是红外光。 太阳辐射的紫外部分,波长在2000埃以下,主要被大气中原子态或分子态的氧和氮所吸收,完全不能到达地面。波长短于3400埃的太阳紫外辐射,由臭氧的哈特莱吸收带(2000~3000埃)和哈根斯吸收带(3200~3600埃)的共同作 用,在到达地面之前,也绝大部分被吸收(见)。在可见光窗区,大气吸收较少,这里主要有臭氧的夏普伊吸收带(4300~7500埃),氧在5384埃和7621埃附近的吸收,以及水汽在6943.8埃附近的吸收等。 3、太阳能电池及组件系统 太阳能电池基本结构 太阳能电池生产工艺: (1)、表面制绒 单晶硅绒面的制备是利用硅的各向异性腐蚀,在每平方厘米硅表面形成几百万个四面方锥体也即金字塔结构。由于入射光在表面的多次反射和折射,增加了光的吸收,提高了电池的短路电流和转换效率。硅的各向异性腐蚀液通常用热的碱性溶液,可用的碱有氢氧化钠,氢氧化钾、氢氧化锂和乙二胺等。大多使用廉价的浓度约为1%的氢氧化钠稀溶液来制备绒面硅,腐蚀温度为70-85℃。为了获得均匀的绒面,还应在溶液中酌量添加醇类如乙醇和异丙醇等作为络合剂,以加快硅的腐蚀。制备绒面前,硅片须先进行初步表面腐蚀,用碱性或酸性腐蚀液蚀去约20~25μm,在腐蚀绒面后,进行一般的化学清洗。经过表面准备的硅片都不宜在水中久存,以防沾污,应尽快扩散制结。 (2)、扩散制结 太阳能电池需要一个大面积的PN结以实现光能到电能的转换,而扩散炉即为制造太阳能电池PN结的专用设备。管式扩散炉主要由石英舟的上下载部分、废气室、炉体部分和气柜部分等四大部分组成。扩散一般用三氯氧磷液态源作为扩散 源。把P型硅片放在管式扩散炉的石英容器内,在850---900摄氏度高温下使用氮气将三氯氧磷带入石英容器,通过三氯氧磷和硅片进行反应,得到磷原子。经过一定时间,磷原子从四周进入硅片的表面层,并且通过硅原子之间的空隙向硅片内部渗透扩散,形成了N型半导体和P型半导体的交界面,也就是PN结。这种方法制出的PN结均匀性好,方块电阻的不均匀性小于百分之十,少子寿命可大于10ms。制造PN结是太阳电池生产最基本也是最关键的工序。因为正是PN结的形成,才使电子和空穴在流动后不再回到原处,这样就形成了电流,用导线将电流引出,就是直流电。 (3)、去磷硅玻璃 该工艺用于太阳能电池片生产制造过程中,通过化学腐蚀法也即把硅片放在氢氟酸溶液中浸泡,使其产生化学反应生成可溶性的络和物六氟硅酸,以去除扩散制结后在硅片表面形成的一层磷硅玻璃。在扩散过程中,POCL3与O2反应生成P2O5淀积在硅片表面。P2O5与Si反应又生成SiO2和磷原子,这样就在硅片表面形成一层含有磷元素的SiO2,称之为磷硅玻璃。 (4)、等离子刻蚀 由于在扩散过程中,即使采用背靠背扩散,硅片的所有表面包括边缘都将不可避免地扩散上磷。PN结的正面所收集到的光生电子会沿着边缘扩散有磷的区域流到PN结的背面,而造成短路。因此,必须对太阳能电池周边的掺杂硅进行刻蚀,以去除电池边缘的PN结。通常采用等离子刻蚀技术完成这一工艺。 (5)、镀减反射膜 抛光硅表面的反射率为35%,为了减少表面反射,提高电池的转换效率,需要沉积一层氮化硅减反射膜。现在工业生产中常采用PECVD设备制备减反射膜。PECVD 即等离子增强型化学气相沉积。它的技术原理是利用低温等离子体作能量源,样品置于低气压下辉光放电的阴极上,利用辉光放电使样品升温到预定的温度,然后通入适量的反应气体SiH4和NH3,气体经一系列化学反应和等离子体反应,在样品表面形成固态薄膜即氮化硅薄膜。一般情况下,使用这种等离子增强型化学气相沉积的方法沉积的薄膜厚度在70nm左右。这样厚度的薄膜具有光学的功能性。利用薄膜干涉原理,可以使光的反射大为减少,电池的短路电流和输出就有很大增加,效率也有相当的提高。 6、丝网印刷 太阳电池经过制绒、扩散及PECVD 等工序后,已经制成PN 结,可以在光照下产生电流,为了将产生的电流导出,需要在电池表面上制作正、负两个电极。制造电极的方法很多,而丝网印刷是目前制作太阳电池电极最普遍的一种生产工艺。丝网印刷是采用压印的方式将预定的图形印刷在基板上,该设备由电池背面银铝浆印刷、电池背面铝浆印刷和电池正面银浆印刷三部分组成。受丝网技术的限制,前表面的金属电极不能做的很窄,从而遮挡了光在硅片内的有效吸收。取决于硅片的电阻率,由丝网印刷技术生产的晶体硅电池的开路电压在580—620mV 之间,短路电流密度在28—33mA/cm2之间,以及填充因子(填充因子是指太阳电池最大功率与开路电压与短路电流乘积的比值,是评价太阳电池输出特性的一个重要参数。)在70%—75%之间。对于大面积的电池,电池表面10%--15%面积被电池表面电极遮挡了。 7、快速烧结 经过丝网印刷后的硅片,不能直接使用,需经烧结炉快速烧结,将有机树脂粘合剂燃烧掉,剩下几乎纯粹的、由于玻璃质作用而密合在硅片上的银电极。当银电极和晶体硅在温度达到共晶温度时,晶体硅原子以一定的比例融入到熔融的银电极材料中去,从而形成上下电极的欧姆接触,提高电池片的开路电压和填充因子两个关键参数,使其具有电阻特性,以提高电池片的转换效率。烧结炉分为预烧结、烧结、降温冷却三个阶段。预烧结阶段目的是使浆料中的高分子粘合剂分解、燃烧掉,此阶段温度慢慢上升;烧结阶段中烧结体内完成各种物理化学反应,形成电阻膜结构,使其真正具有电阻特性,该阶段温度达到峰值;降温冷却阶段,玻璃冷却硬化并凝固,使电阻膜结构固定地粘附于基片上。 太阳能电池各部分对电池性能影响 (1)、表面金字塔结构 金字塔形角锥体的表面积S 1等于四个边长为a 正三角形S 之和 21142S a a =??= 由此可见有绒面的受光面积比光面提高了倍即1.732倍。 当一束强度为E 0的光投射到图中的A 点,产生反射光1Φ和进入硅中的折射 光2Φ。反射光1Φ可以继续投射到另一方锥的B 点,产生二次反射光3Φ和进入半导体的折射光4Φ;而对光面电池就不产生这第二次的入射。经计算可知还有 11%的二次反射光可能进行第三次反射和折射,由此可算得绒面的反射率为9.04%。 (2)、氮化硅减反射膜 我们所用的PECVD 制备的SiN 薄膜是非晶体膜,其结构与短距离的化学键有关。氮化硅薄膜中除了Si-N 成分以外,还含有相当可观的弱键氢和痕量氧。薄膜的含H 量较高,可达20~30%(原子百分数)。适量的H 会对表面起钝化作用。硅和氮化硅界面处电荷的界面态密度很高,这种界面态对界面附近的载流子会起到陷阱或复合中心的作用。氢钝化能有效降低表面复合速度,增加少子寿命,从而提高太阳电池效率。氮化硅薄膜的折射率比较高,非晶态氮化硅薄膜的折射率随Si/N 比在一定范围内波动,折射率n=1.8~2.4。氮原子含量增加,折射率降低;硅原子含量增加,折射率增大。此外,还和沉积温度有关,沉积温度提高,折射率增大,这是由于温度升高使薄膜致密度提高的缘故。 减反射原理: 照射到硅片上的光因为反射不能全部被硅吸收。反射百分率的大小取决于硅和外界透明介质的折射率。垂直入射时,硅片表面的反射率R 为 2 Si o Si o n n R n n ??-= ?+?? 其中,n Si 为硅的折射率;n o 为外界介质的折射率。在真空或者空气中,我们近似取n o =1。在真空或大气中,如果硅表面没有减反射膜,长波范围(1.1μm )入射光损失总量的34%,短波范围(0.4μm )为54%。即使在硅表面制作了绒面,由于入射光产生多次反射而增加了吸收,但也有约11%的反射损失。 在硅的表面制备一层透明的介质膜,由于介质膜的两个界面上的反射光相互干涉,可以在很宽的波长范围内降低反射率。此时反射率由下式给出 式中,r 1、r 2 分别是外界介质-膜和膜-硅界面上的菲涅尔反射系数;Δ为膜层厚度引起的相位角。它们可分别表示为 010n n r n n -=+ 04nd π λ?= 当薄膜的光学厚度为四分之一个波长,n =时R=0,反射最小。 地面太阳光谱能量的峰值在波长0.5μm ,而硅太阳电池的相对响应峰值在波长0.8~0.9μm 。因此减反射效果最好的波长范围在0.5~0.7μm ,可取λ0=0.6μm 。具有这一厚度减反射膜的硅太阳电池,由肉眼看来呈深蓝色。此时硅的折射率n Si =3.9,所以如果电池直接暴露在真空或大气中使用,最匹配的减反射膜折射率n 约为1.97。 (3)、硅的吸收 半导体与光之间的相互作用,主要是通过光子与半导体中的电子、原子之间的相互作用,表现为对光的吸收,光电导或发光等效应。但在太阳能电池中,主要体现为对光的吸收,导致电子从低能级跃迁到较高能级。我们也仅考虑一个能产生光生载流子的光子只产生一对空穴电子对。尽管半导体对光吸收的过程具有多种2Si Si n n r n n -=+ 机制,如本征吸收、激子吸收、杂质吸收等,但主要表现为本征吸收,这主要通过光学吸收系数来表征。一般来说,吸收系数跟波长和温度相关。温度对吸收系数的影响,主要考虑温度对禁带宽度的影响,在此不加以讨论。 光学吸收系数本征吸收是指在光照下具有足够能量的光子使价带内中的电子越过禁带跃迁到空的导带。这电子吸收光子的过程必须满足选择定则,即能量守恒和动量守恒两个原则,初态能量为E ,波矢为k 的电子吸收能量为ω的光子后,跃迁到能量为f E 、波矢为k '的末态,根据能量守恒和动量守恒,应有如下关系: k k '-=光子动量 f E E ω-= 这使电子跃迁分为直接和间接跃迁。 对于直接跃迁,光子能量与吸收系数的关系为 ()0()g g h E h E ανν=≥=< 上式A 为一个基本常数。 对于间接跃迁,还得考虑电子和晶格之间的相互作用。这是由于要满足动量守恒定则在间接跃迁过程中必须发射或者吸收一个声子,它是一个二级过程。根据相关理论可知,发射声子和吸收声子的过程的光学吸收系数可以写成 ()(exp()1)g p p h E E A E kT να±-±'=±±- 上式中,“+”表示吸收声子的过程,与之相反,“-”表示发射声子的过程,p E 表示声子能量。当g p h E E ν>+时,此时吸收声子和发射声子的跃迁过程均可以发生,此时吸收系数为αα+-+;当g p g p E E h E E ν+≥>-时,此时只能吸收声子跃迁,此时吸收系数为α+;当g p h E E ν≤-时,此时吸收系数为零。 硅晶体的能带结构 硅的晶体结构是金刚石结构,由两个面心立方结构沿对角线平移1/4对角线长度套构而成其能带结构是间接能隙能带。常温下禁带宽度为1.12eV,当入射光子能量大于1.12eV 时.即可发生光跃迁,电子从价带跃迁到导带。 如下图所示光子能量在1-10eV范围内硅的光吸收系数,光子能量小于2.4eV,吸收系数很小发生间接跃迁。光子能量大于2.4eV时,吸收系数开始增大,这时候开始发生垂直跃迁。在3eV-3.5eV吸收系数增加很快,垂直跃迁逐渐成为主要的跃迁形式。 硅晶体的光吸收系数 能量h υ ≥ Eg 的入射光,在太阳能电池中传播时,被价电子吸收而激发光生电子-空穴对,是太阳电池电池中主要的非静电相互作用。它由入射光在太阳电池中传播的衰减规律: I (x ) = I (0)(1? R )exp[?α(λ)x ]决定。 式中α(λ)是太阳电池材料对波长为λ的光的吸收系数。I (0)是太阳电池表面x=0处的入射光强,R 为表面反射率,I(x)是表面至太阳电池内x 处的光强。显然,若研究给定衬底的太阳电池,其截止波长0g hc E λ=,相应地穿透太阳电池中的平均深度x 被看成是能产生光生载流子对的主要工作区,它的值应为: Si 在300K 时Si 的Eg 为1.12 eV ,相应截止波长:0 1.1m λμ=。10()120cm αλ-≈可得83x m μ≈Si 电池的主要工作区不到100μm 。当然,实际的工作区域比这个值要大得多,可由给定的长波限λ0值确定,Si 吸收99%的相应吸收厚度0x =384μm 。 太阳电池对应于不同光的波长的响应特征称为分光感度特征。一般用光的波长与所转换生成的电能的关系,即用分光感度特征来表示。 (4)铝背场 随着生产技术的进步,晶体硅太阳电池的厚度不断减薄,从早期的325μm 到270μm,再到240-220μm,而下一步的发展目标是180-150μm。随着厚度的不断变薄,硅片少子体寿命对电池效率的影响逐步降低,这主要是因为随着硅片厚度减薄,基区少子到达pn结所需距离变短,这就意味着,即便材料的少子寿命较低,仍然有足够的扩散长度保证足够多的少子被pn结收集。与之相对应的,电池片上下表面的复合速率对效率的影响逐步增长。改善表面钝化的质量、降低表面复合速率已经成为提高电池效率的主要手段之一。目前工业上主要采用铝背场进行表面钝化。 (1)表面钝化,降低背表面复合速率,提高少数载流子的收集率,提高开路电压。由于硅太阳电池的吸收峰值在900nm附近,长波穿透深度大,直到靠近背电极一侧都能产生大量的光生载流子,背电极界面处相当于一个无穷大的复合陷阱层,当少数载流子被扩散到背电极界面时,很快被复合。由于背面场的存在,p -p结阻止光生少子向p区扩散,提高了少数载流子的收集效率,降低了暗电流分量。背表面场对开路电压的提高也有很大的作用,随着P层掺杂浓度的提高,层 内电子的扩散系数减小,浓度达到1019cm-3时,电子的扩散系数最小,p-p结 的电场能作用在整个p区内时,背电场对电子的收集和开路电压的提高最为有效。 (2)作为背反射器,增加光程,提高短路电流。 之内的长波,它们在硅片内的穿透深度较长,只有在硅片足够厚的时候对于 才能够被完全吸收。所以,在没有背场的情况下,硅片厚度减薄,减小了光程,降低了硅对长波的吸收,进而减小了短路电流。在有背场的情况下,背场可以把光发射回电池,增加光程,提高了硅对长波段的吸收。 (3) 作为电极输出端,降低接触电阻,提高转换效率。 背电场除了能够提高少子的收集外,还能够很好地作为电极的输出端。因为铝易于与P型硅形成欧姆接触,为此我们一般都采用铝-硅合金来作铝背场p- p结,铝硅合金结构,不仅具有背场的作用,而且还能够很好地构成背面欧姆接触,作为电流的输出电极,降低接触电阻,改善电池的电学性能。 (4) 铝吸杂,提高体寿命。 在700~900 ℃时,许多重金属杂质在铝中的固溶度比在硅中的固溶度高4~10个数量级,并且金属杂质在硅中的扩散速度远大于磷、硼等替位式元素。铝吸杂通常的方法是在硅片表面蒸镀铝并进行一段时间的热处理,金属杂质就被吸附到铝层,以此来改变硅片的性能。 无铝背场时,电池的短路电流随电池厚度的减小而降低。因为太阳电池吸收光子能量产生电子-空穴对, 基体材料对入射光的吸收是按I ( x ) =I0 exp ( - α(λ) x) 规律变化I0是太阳电池表面x = 0 处的入射光强,α(λ)是太阳电池材料对波长为λ的光的吸收系数, I ( x) 是表面至太阳电池内x 处的光强)。单晶硅太阳电池要吸收99 %的光所需要的吸收厚度为384μm。在50~350μm 厚度范围内,随太阳电池厚度的减小,基体不能充分地吸收入射光,从而影响产生电子空穴对数目,导致太阳 电池的短路电流降低。 有铝背场时,只有硅片厚度小于200μm 时,才能很明显地观察到短路电流随着硅 片厚度的减小而减小。I sc的这种变化趋势,我认为是由于铝背场的高反射率所致。一方面,由于铝背场有助于减小金属与半导体间的接触电阻,从而降低R s 值,提高I sc ;另一方面,硅片厚度小于300μm ,基体不能完全地吸收入射光,部分光到达铝背场处,由于发生高内背表面反射,这种作用的最终结果是基体内总的光生载流子数目几乎不变。且由于硅片厚度变薄,电子-空穴对的产生更接近pn结,因而更有利于pn结对载流子的收集。大量的实验证实,铝背场的这种效应能提高短路电流。 上图为丝网印刷工艺技术制备出的铝背场的表面形貌,可见存在大量大小不均的铝颗粒,表面较为粗糙,空隙较多。在制备单晶硅电池的铝背场过程当中,不仅要考虑其接触电阻,吸杂能力,由于铝背场同时还担当起到背反射镜的作用,将到达铝背场的入射光反射回去,从而提高电池对光的利用率。随着硅片进一步减薄,这一作用将越来越明显和重要,所以平整细腻的铝背场表面无疑可大幅度提高其反射率。 (5)栅线 目前常规工业化晶硅太阳电池的正面金属栅线面积约占整个电池面积的8%,其中60%的面积是细栅线(finger,也称为副栅线),40%的面积为主栅线(busbar)。金属栅线由不透光的银颗粒及玻璃体组成。在工艺上要求栅线间距约3mm、宽度约0.10~0.12mm。烧结后高度为12-15μm。 考虑在一般情况下面积为10cm×10cm的正方形单晶硅太阳能电池。细栅线宽度 125μm,厚度12μm,主栅线宽度为0.158cm,厚度35μm。细栅线间距0.274cm。可以计算得到栅线遮盖损失为7.73%。 最近应用材料公司利用两台不同的印刷设备制作了80μm宽30μm高的细栅线。这种方法减少了大约20%的阴影损失,相应的也降低了电阻系数。 因此为了降低栅线遮挡造成的电池效率损失,可以从以下几个方面考虑: 1)缩小细栅的宽度:工业化生产中丝网印刷的细栅线的宽度已经从过去几年的140-150 μm逐步降低到100-120μm左右,并有继续缩小到80 μm左右的潜力。 2)超细主栅或无主栅:主栅的宽度通常为1.5mm(对于125mm边长的电池片,或156 mm边长3根主栅的电池片),将主栅宽度缩小甚至完全移至背面,如metal wrap through技术。 3)背面接触:如果使用emitter wrap through技术则可将正面所有的细栅线和主栅移至背面,大大增加短路电流。 4)栅线内反射:栅线是良好的光线反射体,通过特殊设计,可以将部分反射光线通过玻璃、封装材料等内反射再回到电池片表面。 (6)EV A,钢化玻璃 太阳能电池封装用胶膜是以EV A为基料,辅以数种改性剂,经过膜设备热轧而成薄膜型产品。EV A树脂是乙烯和醋酸乙烯酯的共聚物,结构如下: 醋酸乙烯含量小于40%的产品为EVA树脂。 醋酸乙烯含量40%~70%的产品很柔韧,富有弹性特征,这一含量范围的EVA 树脂有时称为EVA橡胶; 醋酸乙烯含量在70%~95%范围内通常呈乳液状态,称为VAE乳液。VAE乳液外观呈乳白色或微黄色。 太阳能行业一般含量为30%~33%。EVA厚度在0.4mm~0.6mm之间,表面平整,厚度均匀,内含交联剂,能在150℃固化温度下交联,采用挤压成型工艺形成稳定胶层。一般透光率(%):≥91 EV A对玻璃的增透作用:EV A和玻璃的折射率约为1.5,正是EV A的折射率比空气更接近于玻璃,从而降低总反射率。 吸收紫外光的作用:EV A胶膜能够吸收大部分紫外光,从而能够保障太阳电池长年正常工作在日光之下。 封装用的玻璃是采用透光率高的低铁钢化白玻璃,厚度一般为3. 0~ 4.0mm, 在320~ 1100 nm的波长范围内, 其透光率达90% 以上, 对于波长大于1200 nm 的红外线有较高的反射率, 耐紫外光辐射性能好。 TPT一般常用三层结构(PVF/PET/PVF),外层保护层PVF具有良好的抗环境侵蚀能力,中间层为PET聚脂薄膜具有良好的绝缘性能,内层PVF需经表面处理和EV A具有良好的粘接性能。 紫外吸收光谱 UV 分析原理:吸收紫外光能量,引起分子中电子能级的跃迁 谱图的表示方法:相对吸收光能量随吸收光波长的变化 提供的信息:吸收峰的位置、强度和形状,提供分子中不同电子结构的信息 荧光光谱法 FS 分析原理:被电磁辐射激发后,从最低单线激发态回到单线基态,发射荧光 谱图的表示方法:发射的荧光能量随光波长的变化 提供的信息:荧光效率和寿命,提供分子中不同电子结构的信息 红外吸收光谱法 IR 分析原理:吸收红外光能量,引起具有偶极矩变化的分子的振动、转动能级跃迁 谱图的表示方法:相对透射光能量随透射光频率变化 提供的信息:峰的位置、强度和形状,提供功能团或化学键的特征振动频率 拉曼光谱法 Ram 分析原理:吸收光能后,引起具有极化率变化的分子振动,产生拉曼散射 谱图的表示方法:散射光能量随拉曼位移的变化 提供的信息:峰的位置、强度和形状,提供功能团或化学键的特征振动频率 核磁共振波谱法 NMR 分析原理:在外磁场中,具有核磁矩的原子核,吸收射频能量,产生核自旋能级的跃迁 谱图的表示方法:吸收光能量随化学位移的变化 提供的信息:峰的化学位移、强度、裂分数和偶合常数,提供核的数目、所处化学环境和几何构型的信息 电子顺磁共振波谱法 ESR 分析原理:在外磁场中,分子中未成对电子吸收射频能量,产生电子自旋能级跃迁 谱图的表示方法:吸收光能量或微分能量随磁场强度变化 提供的信息:谱线位置、强度、裂分数目和超精细分裂常数,提供未成对电子密度、分子键特性及几何构型信息 质谱分析法 MS 分析原理:分子在真空中被电子轰击,形成离子,通过电磁场按不同m/e分离 谱图的表示方法:以棒图形式表示离子的相对峰度随m/e的变化 提供的信息:分子离子及碎片离子的质量数及其相对峰度,提供分子量,元素组成及结构的信息 气相色谱法 GC 分析原理:样品中各组分在流动相和固定相之间,由于分配系数不同而分离 谱图的表示方法:柱后流出物浓度随保留值的变化 提供的信息:峰的保留值与组分热力学参数有关,是定性依据;峰面积与组分含量有关 反气相色谱法 IGC 【实验数据处理部分】 一.由实验测得的数据可以得到以下几个谱图: 1.苯蒸气的紫外吸收光谱: 左图中,苯的K吸 收带大约在214nm处, B吸收带在256nm左右。 并且,苯蒸气的精细结 构(主要指苯分子的振 动能级)清晰可见。 另外,由于滴加到 比色皿中的苯过多导致 浓度偏大,A值偏大。 (超过了1.0)。 2.不同取代基对苯的紫外吸收带的影响: (1)、苯甲酸与苯乙烯: 左图中,①②标示的 是苯蒸气的K带和B带; ③表示的是苯甲酸的K 吸收带;而④⑤表示的是 苯乙烯的E2带和K带。 (其中为了使谱图便于 比对,将苯蒸气的吸光度 值成比例地缩小了一定 的数值。) 读图可知: 与苯比较,羧基(吸 电子基)取代的苯环,其K 吸收带发生了红移,B吸 收带也有一定程度的红 移,但强度变弱了; 而对于苯乙烯,由于乙烯基双键的存在,增大了苯环的共轭体系,使得价电子跃迁所需要的能量变低,因而发生了很大程度的红移,E2带和K带分别红移至210nm和245nm处。 (2)、苯酚和苯胺: 图中,①②标示的是 苯蒸气的K带和B带; ③④表示的是苯酚的K 吸收带和B吸收带;而 ⑤⑥⑦则表示苯胺的E2 带、K带和B带。 读图可知: 苯酚的E2吸收带与 K吸收带合并了,原因是 酚羟基的助色作用使得 吸收带发生红移,同样 地,与苯相比,苯酚的B 吸收带也发生了红移; 苯胺的氮原子上含 有孤对电子,也和酚羟基一样具有助色效应,因此苯胺的各个吸收带也发生了一定程度的红移(相比较于苯而言)。 二、溶液性质对取代苯紫外吸收的影响: 1.苯酚与其碱性溶液: 图中:①②③分别标 示的是苯酚在碱性溶液 中的E2吸收带、K吸收 带和B吸收带的大致位 置;而④⑤则分别标示苯 酚在中性溶液中的K吸 收带和B吸收带的位置。 读图可知: 由于碱性溶液中的 酚羟基以氧负离子形式 存在,使得酚羟基的助色 作用大大增强,因而苯环 的吸收带均发生较大的 红移。 例如:原本在苯酚的 紫外吸收图谱中未能读出的E1、E2吸收带,此时可以大致从图中读出;另外,碱性溶液中,苯酚的K带红移至245nm左右,B带红移至290nm左右。 苯酚在碱性溶液中的变化见下图: AES 原子发射光谱:原子的外层由高层能及向底层能级,能量以电磁辐射的形式发射出去, 这样就得到了发射光谱。原子发射一般是线状光谱。 原理:原子处于基态,通过电至激发,热至激发或者,光至激发等激发作用下,原子获得能 量,外层电子从基态跃迁到较高能态变成激发态,经过10-8s ,外层电子就从高能级向较低 能级或基态跃迁,多余能量的发射可得到一条光谱线。 光谱选择定律:①主量子数的变化△n 为包括零的整数,②△L=±1,即跃迁只能在S 项与P 项间,P 与S 或者D 间,D 到P 和F 。③△S=0,即不同多重性状间的迁移是不可能的。 ③△J=0,±1。但在J=0时,J=0的跃迁是允许的。 N 2S+1 L J 影响谱线强度的主要因素:1激发电位2跃迁概率3 统计权重4激发温度(激发温度↑离 子↑原子光谱↓离子光谱↑)5原子密度 原子发射光谱仪组成:激发光源,色散系统,检测系统, 激发光源:①火焰:2000到3000K ,只能激发激发电位低的原子:如碱性金属和碱土金属。 ② 直流电弧:4000到7000K ,优点:分析的灵敏度高,背景小,适合定量分析和低含量的 测定。缺点:不宜用于定量分析及低熔点元素的分析。 ③交流电弧:温度比直流高,离子线相对多,稳定性比直流高,操作安全,但灵敏度差 ④火花:一万K ,稳定性好,定量分析以及难测元素。每次放电时间间隔长,电极头温度低。 适合分析熔点低。缺点:灵敏度较差,背景大,不宜做痕量元素分析(金属,合金等组成均 匀的试样)⑤辉光 激发能力强,可以激发很难激发的元素,(非金属,卤素,一些气体)谱 线强度大,背景小,检出限低,稳定性好,准确度高(设备复杂,进样不方便)⑥电感耦合 等离子体10000K 基体效应小,检出限低,限行范围宽⑦激光 一万K ,适合珍贵样品 分光系统:单色器:入射狭缝,准直装置,色散装置,聚焦透镜,出射狭缝。 棱镜:分光原理:光的折射,由于不同的光有不同的折射率,所以分开。 光栅:光的折射与干涉的总效果,不同波长的光通过光栅作用各有不同的衍射角。 分辨率: 原子发射检测法:①目视法,②光电法, ③摄谱法:用感光板来记录光谱,感光板:载片(光学玻璃)和感光乳剂(精致卤化 银精致明胶)。 曝光量H=Et E 感光层接受的照度、 黑度:S=lgT -1=lg io/i io 为没有谱线的光强,i 通过谱线的光强度i ,透过率 T 定性分析:铁光谱比较法,标样光谱比较法,波长测定法。 定量法:①基本原理②内标法 ⑴内标元素和被测元素有相近的物理化学性质,如沸点,熔 点近似,在激发光源中有相近的蒸发性。⑵内标元素和被测元素有相近的激发能,如果选用 离子线组成分析线对时,则不仅要求两线对的激发电位相等,还要求内标元素的电离电位相 近。⑶内标元素是外加的,样品中不应有内标元素,⑷内标元素的含量必须适量且固定,⑸ 汾西线和内标线无自吸或者自吸很小,且不受其他谱线干扰。⑹如采用照相法测量谱线强度, 则要求两条谱线的波长应尽量靠近。 简述内标法基本原理和为什么要使用内标法。 答:内标法是通过测量谱线相对强度进行定量分析的方法。通常在被测定元素的谱线中选一 条灵敏线作为分析线,在基体元素(或定量加入的其它元素)的谱线中选一条谱线为比较线, 又称为内标线。分析线与内标线的绝对强度的比值称为分析线对的相对强度。在工作条件相 对变化时,分析线对两谱线的绝对强度均有变化,但对分析线对的相对强度影响不大,因此 可准确地测定元素的含量。从光谱定量分析公式a c b I lg lg lg +=,可知谱线强度I 与元素 的浓度有关,还受到许多因素的影响,而内标法可消除工作条件变化等大部分因素带来的影 响。 激发电位:原子中某一外层电子由基态激发到高能级所需要的能量。共振线:由激发态像基 态跃迁所发射的谱线。(共振线具有最小电位,最容易被激发,最强谱线) 实验一:紫外—可见吸收光谱 一、实验目的 1.熟悉和掌握紫外—可见吸收光谱的使用方法 2.用紫外—可见吸收光谱测定某一位置样品浓度 3.定性判断和分析溶液中所含物质种类 二、实验原理 紫外吸收光谱的波长范围在200~400,可见光吸收光谱的波长在400~800,两者都属于电子能谱,两者都可以用朗伯比尔(Lamber-Beer’s Law)定律来描述 A=ε bc 其中A为吸光度;ε为光被吸收的比例系数;c为吸光物质的浓度,单位mol/L;b为吸收层厚度,单位cm 有机化合物的紫外-可 见吸收光谱,是其分子中外 层价电子跃迁的结果,其中 包括有形成单键的σ电 子、有形成双键的π电子、 有未成键的孤对n电子。外 层电子吸收紫外或者可见 辐射后,就从基态向激发态 (反键轨道)跃迁。主要有 四种跃迁,所需能量ΔE 大小顺序为σ→σ*> n→σ*>π→π>n→π* 吸收带特征典型基团 σ→σ*主要发生在远紫外区C-C、C-H(在紫外光区观测不到) 跃迁一般发生在150~250nm,因此在紫 n→σ* -OH、-NH 2 、—X、-S 外区不易观察到 跃迁吸收带波长较长,孤立跃迁一般发 π→π* 芳香环 生在200nm左右 跃迁一般发生在近紫外区(200~400n n→π* C=O、C=S、—N=O、-N=N-、C=N ; m) 1、开机 打开紫外-可见分光光度计开关→开电脑→软件→联接→M(光谱方法)进行调节实验需要的参数:波长范围 700-365nm 扫描速度高速;采样间隔: 0.5nm 2、甲基紫的测定 (1)校准基线 将空白样品(水)放到比色槽中,点击“基线”键,进行基线校准(2)标准曲线的测定 分别将5ug/ml、 10ug/ml 、15ug/ml、20ug/ml甲基紫溶液移入比色皿(大约2/3处),放到比色槽中,点击“开始”键,进行扫描,保存 (3)测定试样 将试样甲基紫溶液移入比色皿(大约2/3处),放到比色槽中,点击“开始"键,进行扫描,保存 3、甲基红的测定 (1)校准基线 将空白样品(乙醇)放到比色槽中,点击“基线"键,进行基线校准 (2)测定试样 将试样甲基紫溶液移入比色皿(大约2/3处),放到比色槽中,点击“开始" 键,进行扫描,保存 四、实验结果 1.未知浓度的测定 分别测定了5μg/ml,10μg/ml,15μg/ml,20μg/ml和未知浓度的甲基紫溶液的紫外吸收光谱,紫外吸收谱图如下: 甲基紫在580nm是达到最大吸收见下表: 浓度/μg*ml—1吸光度 50。665 10 1.274 152.048 习题参考答案 第一章紫外光谱 1. (1) 饱和化合物,吸收在远紫外区,故在近紫外区无吸收峰; (2) 结构可看成乙烯中引入了助色基团甲氧基,吸收波长红移,但吸收峰仍在远紫外区,近紫外区无吸收峰; (3) π→π*跃迁。氨基为助色团,其孤对电子与苯环发生p→π共轭,所以E带和B带均发生红移,E1吸收位于远紫外区,E2带(230 nm)和B带(280 nm)处在近紫外区。 (4)取代基与苯环形成大的共轭体系,有π→π*跃迁;结构中含有羰基,有n→π*跃迁。吸收带有K带、B带和R带; (5) 取代基与苯环形成大的共轭体系,π→π*跃迁,主要吸收带为K带和B带; (6) 羰基有n→π*跃迁,为R带吸收。(该结构的烯醇异构体有K带和R带) (7) 该结构为α,β-不饱和羰基化合物,有π→π*跃迁和n→π*跃迁,吸收带为K带和R带。 2. (1) a为饱和烷烃,仅有σ→σ*跃迁,吸收位于远紫外;b有两个双键,但未共轭,吸收位于远紫外;c为共轭二烯,吸收在近紫外;所以最大吸收波长c>b>a;(2) a为同环共轭双烯,波长最大,c和b相比,结构中多了一个甲基,存在超共轭效应,吸收红移。综上所述,a>c>b; (3) a, c为共轭体系,吸收波长均高于b。a和c相比,结构中拥有更多的取代甲基,存在超共轭效应,吸收红移。综上所述,a>c>b; 3. (1) 同环共轭双烯基本值253 4个烷基取代+ 4×5 2个环外双键+ 2×5 计算值283(nm) (3) (4) (5) (6) 骈环异环共轭双烯基本值214 4个烷基取代+ 4×5 2个环外双键+ 2×5 计算值244(nm) 同环共轭双烯基本值253 4个烷基取代+ 4×5 计算值273(nm) 直链α,β-不饱和酮基本值215 1个烷基α取代+ 10 计算值225(nm) 五元环α,β-不饱和酮基本值202 1个烷基α取代+ 10 2个烷基β取代+12×2 2个环外双键+5×2 计算值246(nm) 六元环α,β-不饱和酮基本值215 1个烷基α取代+ 10 2个烷基β取代+12×2 计算值249(nm) 第2章红外光谱 通常红外光谱(infrared spectroscopy, IR)就是指波长2~25 μm的吸收光谱(即中红外区),这段波长范围反映出分子中原子间的振动与变角运动。分子在振动的同时还会发生转动运动,虽然分子的转动所涉及的能量变化较小,处在远红外区域,但转动运动影响振动的偶极矩变化,因而在红外光谱区实际所测的谱图就是分子的振动与转动运动的加与表现,因此红外光谱又称为分子振转光谱。 红外光谱可以应用于化合物分子结构的测定、未知物鉴定以及混合物成分分析。 2、1 红外光谱的基本原理 2、1、1 红外吸收光谱 1、当一束具有连续波长的红外光通过物质,物质分子中某个基团的振动频率或转动频率与红外光的频率一样时,分子就吸收能量由原来的基态振(转)动能级跃迁到能量较高的振(转)动能级,分子吸收红外辐射后发生振动与转动能级的跃迁,该处波长的光就被物质吸收。 波谱区近红外光中红外光远红外光 波长/m 0、75~2、5 2、5~50 50~1000 波数/cm-113333~4000 4000~200 200~10 跃迁类型分子振动分子转动 中红外区:绝大多数有机与无机化合物的基频吸收所在,主要就是振动能级的跃迁; 远红外区:分子纯转动能级跃迁及晶体的晶格振动。 3、波数()单位就是cm-1。波长与波数的关系就是: 4、胡克定律: 其中:——折合质量,,单位为kg; ——化学键力常数,与化学键的键能呈正比,单位为N·m-1; ——波数; ——真空中的光速。 (1)因为,红外频率。 (2)与碳原子城建的其她原子,随着其原子质量的增大,折合质量也增大,则红外波数减小。 (3)与氢原子相连的化学键的折合质量都小,红外吸收在高波数区。 (4)弯曲振动比伸缩振动容易,弯曲振动的K均较小,故弯曲振动吸收在低波数区。 5、光谱选律:原子与分子与电磁波作用发生能级跃迁就是要服从一定的规律的,这些规律由量子化学解释。量子化学解得与体系振动量子数(v)相对应的体系能量(E)为: (v = 0, 1, 2, 3…) 简谐振动光谱选律为:,即跃迁必须在相邻震动能级之间进行。 实验一、有机化合物的紫外吸收光谱及溶剂效应 目的要求: 1、学习用紫外吸收光谱进行化合物的定性分析。 2、学习苯环上取代基的引入对最大吸收波长的影响。 3、了解一元取代苯的紫外光谱的实验规则。 4、熟悉各个吸收带。 基本原理 影响有机化合物紫外吸收光谱的因素,有内因和外因。由于受到溶剂极性的影响,溶质的吸收峰的波长、强度以及形状都会发生不同程度的变化。这是因为溶剂分子和溶质分子间可能形成氢键,或极性溶剂分子的偶极使溶质分子的极性增强,因而在极性溶剂中π→π*跃迁所需能量减消,吸收波 长红移,而在极性溶剂中n→π*跃迁所需能量增大,吸收波长蓝移。 E带和B带是芳香族化合物的特征吸收。它们均由π→π*跃迁产生,当苯环上有取代基时,E带和B带的吸收峰也随之变化。如苯甲酸的E吸收带红移至230nm;ε=11600;B吸收带红移至273nm;ε=970;乙酰苯胺的E吸收带红移至241nm;ε=14000。 本实验通过苯甲酸、乙酰苯胺、苯在乙醇和环己烷的溶剂中紫外吸收光谱的测绘,说明内因和外因对有机化合物紫外吸收光谱的影响;了解一元取代苯的紫外光谱的实验规则,即在苯环上有一元取代基时,复杂的B谱带一般都简单化,并且各谱带的最大吸收波长发生红移,εmax一般增大。 一、仪器 1、紫外-可见分光光度计。型号:760CRT 二、试剂 1、苯甲酸、苯、乙酰苯胺、乙醇和环己烷均为分析纯 2、a 苯甲酸的环己烷溶液0.08g.100ml-1 b 乙酰苯胺的环己烷溶液0.08g.100ml-1 c 苯的环己烷溶液1:250 d 苯甲酸的乙醇溶液0.04g.100ml-1 e 乙酰苯胺的乙醇溶液0.08g.100ml-1 f 苯的乙醇溶液1:250 三、实验条件 1、波长扫描范围:190~300(400) 2、参比: 3、slit: 0.01nm 第一节:紫外光谱(UV) 一、简答 (p36 1-3) 1.丙酮的羰基有几种类型的价电子。并说明能产生何种电子跃迁各种跃迁可在何区域波长处产生吸收 答:有n 电子和π电子。能够发生n →π*跃迁。从n 轨道向π反键轨道跃迁。能产生R 带。跃迁波长在250—500nm 之内。 2.指出下述各对化合物中,哪一个化合物能吸收波长较长的光线(只考虑π→π* 跃迁) (2) (1) 及 NHR 3 CH CH OCH 3 CH 及CH 3 CH CH 2 答:(1)的后者能发生n →π*跃迁,吸收较长。(2)后者的氮原子能与苯环发生P →π共轭,所以或者吸收较长。 3.与化合物(A )的电子光谱相比,解释化合物(B )与(C )的电子光谱发生变化的原因(在乙醇中)。 (C)(B) (A)入max =420 εmax =18600 入max =438 εmax =22000 入max =475 εmax =320003 N N N NO HC 32(CH )2 N N N NO H C 32(CH )2 2 32(CH )(CH )23N N N NO 答:B 、C 发生了明显的蓝移,主要原因是空间位阻效应。 二、分析比较(书里5-6) 1.指出下列两个化合物在近紫外区中的区别: CH CH 3 2 (A)(B) 答:(A)和(B)中各有两个双键。(A)的两个双键中间隔了一个单键,这两个双键就能发生π→π共轭。而(B)这两个双键中隔了两个单键,则不能产生共轭。所以(A)的紫外波长比较长,(B)则比较短。 2.某酮类化合物,当溶于极性溶剂中(如乙醇中)时,溶剂对n→π*跃迁及π→π*跃迁有何影响答:对n→π*跃迁来讲,随着溶剂极性的增大,它的最大吸收波长会发生紫移。而π→π*跃迁中,成键轨道下,π反键轨道跃迁,随着溶剂极性的增大,它会发生红移。 三、试回答下列各问题 *跃迁还是π→π* 1.某酮类化合物λhexane max=305nm,其λEtOH max=307nm,试问,该吸收是由n→π 跃迁引起的(p37-7) 答:乙醇比正己烷的极性要强的多,随着溶剂极性的增大,最大吸收波长从305nm变动到307nm,随着溶剂极性增大,它发生了红移。化合物当中应当是π→π反键轨道的跃迁。 四.计算下述化合物的λ : max 1. 计算下列化合物的λmax:(p37 -11) 五、结构判定 1. 一化合物初步推断其结构不是A就是B,经测定UV λEtOH max=352nm,试问其结构为何 O O (A)(B) 太阳光光谱 紫外线谱带:波长280-400nm之间,其特点是穿透性强,可使人体皮肤黑色素沉积,颜色加深,过度的紫外线曝晒会导致皮肤癌,可导致地毯、窗帘、织物及家具油漆褪色。 可见光谱带:波长380~780nm之间,其特点是肉眼可以看见的唯一光谱,可见光波段进一步可以分为不同的颜色(赤橙黄绿蓝靛紫七色),对人体没有直接伤害。 红外光谱带:波长700~2400nm之间,其特点是我们可以直接感受到阳光“不可见”的热量,所含能量最大,所以热量也高。 各波段的远近红外线构成了太阳能的53%,紫外线占3%,可见光占44%。 元素光谱简介 如果物质是以单原子的形式而存在,关键看该原子的电子激发能了。如果在可见光的某个范围内,并且吸收某一部分光线,那它就显剩下的部分的光线的颜色。如该原子的电子激发能非常低,可以吸收任意的光线,该原子就是黑色的,如果该原子的电子激发能非常高。不能吸收任何光线,它就是白色的。如果它能吸收短波部分的光线,那它就是红色或黄色的。 具体的元素光谱:红色代表硫元素,蓝色代表氧元素,而绿色代表氢元素。 元素燃烧发出的光谱 燃烧所发出的光色根据不同的元素发出不同的光谱,每一种元素燃烧时都发出多条光谱,这种光通过三梭镜或光栅后会在屏障上显现出多条亮线,也就是说只发出有限的几种频率的光,这就是这种元素的光谱。其中会有一条或几条最亮的线,这几条最亮的线决定了在人眼中所看到的颜色。 观察光谱的方法 连续光谱的光线在通过含某种元素的气体时在光谱带上会出现多条暗线,这些暗线刚好与这种元素的光谱线位置相同,强度刚好相反,(光谱线越强的位置暗线越明显)这就是元素的吸收光谱。天文学家就是利用吸收光谱来查明遥远的恒星大气和星云中所含的元素,观察恒星红移或蓝移也要利用吸收光谱。 观察固态或液态物质的原子光谱,可以把它们放到煤气灯的火焰或电弧中去烧,使它们气化后发光,就可以从分光镜中看到它们的明线光谱 原子决定明线光谱 实验证明,原子不同,发射的明线光谱也不同,每种元素的原子都有一定的明线光谱.彩图7就是几种元素的明线光谱.每种原子只能发出具有本身特征的某些波长的光,因此,明线光谱的谱线叫做原子的特征谱线.利用原子的特征谱线可以鉴别物质和研究原子的结构。 吸收光谱 吸收光谱高温物体发出的白光(其中包含连续分布的一切波长的光)通过物质时, 实验一紫外吸收光谱定性分析的应用 一、实验目的 1、掌握紫外吸收光谱的测绘方法。 2、学会利用吸收光谱进行未知物鉴定的方法。 3、学会杂质检出的方法。 二、基本原理 紫外吸收光谱为有机化合物的定性分析提供了有用的信息。其方法是将未知试样和标准品以相同浓度配制在相同的溶剂中,在分别测绘吸收光谱,比较二者是否一致也可将未知试样的吸收光谱与标准图谱,如萨特勒紫外吸收光谱图相比较,如果吸收光谱完全相同,则一般可以认为两者是同一种化合物。但是,有机化合物在紫外区的吸收峰较少,有时会出现不 同的结构,只要具有相同的生色团,它们的最大吸收波长 max λ相同,然而其摩尔吸光系数ε 或比吸光系数E % 1 1cm 值是有差别的。因此需利用 max λ和 max λ处的ε或E%1 1cm 等数据作进一 步比较。 在没有紫外吸收光谱峰的物质中检查含高吸光系数的杂质是紫外吸收光谱的重要用途之一。如乙醇中杂质苯的检查,只需测定256 nm处有无苯的吸收峰即可。因为在这一波段,主成分乙醇无吸收峰。 在测绘比较用的紫外吸收光谱图时,应首先对仪器的波长准确性进行检查和校正。还必须采用相同的溶剂,以排除溶剂的极性对吸收光谱的影响。同时还应注意PH值、温度等因素的影响。在实际应用时,应注意溶剂的纯度。 三、仪器与试剂 1、仪器 T6型(或其他型号)紫外可见分光光度计 1㎝石英比色皿 2、试剂 苯的乙醇溶液 1,4对苯二酚水溶液 苯甲酸的乙醇溶液 四、实验步骤 1、已知芳香族化合物标准光谱的绘制 在一定的实验条件下,以相应的溶剂作参比,用1㎝石英比色皿,在一定的波长范围内扫描(或测绘)各已知标准物质的吸收光谱作为标准光谱。 如苯甲酸的乙醇溶液的和1,4对苯二酚水溶液的标准溶液的标准光谱的绘制。 各已知芳香族化合物的标准光谱也可通过查阅有关手册得到,但应注意实验条件的一致。 2、未知芳香族化合物的鉴定 (1)称取0.100 g未知芳香族化合物,用去离子水溶解后转让100 ml容量瓶中,稀释至刻度,摇匀。实验前,稀释100倍使用。 (2)用1㎝石英比色皿,以去离子水作参比,在200-600波长范围内扫描测定未知芳香族化合物吸收光谱(如使用无扫描功能的紫外可见分光光度计测定时应首先每间隔 20 nm测量一次吸光度,然后每间隔10 nm 、5 nm 、2 nm、1 nm、0.5 nm 测量 一次吸光度。总之,越靠近吸收峰,波长间隔应越小,以得到较准确的吸收曲线)。 3、乙醇中杂质苯的检出 用1㎝石英比色皿,以乙醇作参比,在220-280 nm波长范围内扫描测定乙醇试样的吸收光谱(吸收曲线)。 五、实验结果 1、通过将未知芳香族化合物吸收光谱与已知芳香族化合物标准光谱进行比对,指出未知芳 香族化合物可能为哪种物质。 2、将乙醇试样的吸收光谱与溶解在乙醇中苯的吸收光谱进行比较,指出乙醇试样中是否有 苯存在。 六、思考题 1、配制试样溶液浓度的大小,对吸光度测量值有何影响?在实验中应如何调整? 2、对已经初步确认的化合物纯品,再设计一个实验方案,对未知物作进一步鉴定。 《光谱学与光谱技术》课程总结 第一章 氢原子光谱的基础 1. 氢原子的旧量子理论是由玻尔创立的,玻尔并成功地解释了氢原子光谱。 2. 在光谱学中波数定义为波长的倒数,即 。 3光谱图强度曲线中横坐标可用波长表示,也可用波数表示,还可用频率表示。 4. 当原子被激发到电离限之下时其光谱线为分立谱;当原子被激发到接近或高 于电离限的位置时其光谱线为连续谱。原子光谱是原子的结构的体现。 5. 针对H 原子的Pfund 系光谱, 22115R n ν??=- ??? H , R H =109677.6cm -1 为已知常数。请计算该线系的最长波长和最短波长。 221115R n νλ??==- ???H n =6, 22115R n ??- ??? H 最小,λ最大 n →∞,221115R n νλ??= =- ???H 最大,λ最短 6. 激光作为光谱学研究的光源有优势 (1)单色性好:普通光源发射的光包含各种不相同的频率,含有多种颜色;而激光发射的光频宽极窄, 是最好的单色光源。 (2)相干性好:由于激光是受激辐射的光放大,具有很好的相干性;而普通光 源的光由自发辐射产生是非相干光。 (3)方向性好:激光束的发散角很小,几乎是一平行的光线,便于调整光路;而普 通光源发出的光是发散的,不便于调整光路。 (4)高亮度:激光的亮度可比普通光源高出1012-1019倍,便于做各种实验。 7. 使H 原子解除简并的两种效应及其异同。 部分解除简并是由相对论(速度)效应和LS 耦合(自旋与轨道作用)作用共同 导致的,要想完全解除简并, 则需加磁场(与原子磁矩相互作用产生附加能导致 1λ 江南大学实验报告 实验名称紫外吸收光谱法测定苯的含量 一、实验目的 1、了解紫外光谱法测定苯的原理及方法。 2、了解TU-1901双光束紫外可见分光光度计的使用。 3、学习利用吸收光谱曲线进行化合物鉴定和纯度检查。 二、实验原理 许多有机化合物或其衍生物,在可见光或紫外光区有吸收光谱,各种物质分子有其特征的吸收光谱。吸收光谱的形状和物质的特性有关,可作为定型鉴定的依据,而在某选定的波长下,测量其吸收光度即可对物质进行定量分析。紫外吸收光谱用于定量分析时,符合朗伯比尔定律,即A=κbc,式中A为吸光度,κ为摩尔吸收系数,b为液层厚度。 三、仪器和试剂 1、仪器 TU-1901型紫外-可见分光光度计,1cm石英比色皿,5ml吸量管,10ml容量瓶。 2、试剂 苯(色谱纯),乙醇(AR、95%),0.1g/L苯标准溶液。 四、实验步骤 1、吸收曲线的绘制 将装有参比溶液和标准试样的比色皿放入光路中,在紫外分光光度计上,从波长200-300nm,每隔0.5nm扫描出苯的吸收曲线。指出苯的B吸收带,找出B吸收带的最大吸收波长。2、试样中苯含量的测定 (1)苯标准曲线的绘制分别吸取1.0ml、2.0ml、3.0ml、4.0ml、5.0ml0.1g/l的苯标准溶液于5只10ml容量瓶中,用乙醇稀释至刻度,摇匀。用1ml石英比色皿,以乙醇做参比溶液,在最大吸收波长处分别测定其吸光度。 以吸光度为纵坐标,苯的含量为横坐标绘制标准曲线。 (2)测定乙醇试样中苯的含量准确吸取含苯的试样5ml于10ml容量瓶中,用乙醇稀释至刻度,摇匀,用1cm石英比色皿,以乙醇做参比溶液,在最大吸收波长处测定试样溶液的吸光度,根据苯标准曲线查的相应的样品浓度。 3、结束工作 (1)实验结束,关闭紫外工作软件、电脑电源。 (2)取出吸收池,清洗晾干放入盒内保存。 (3)清理台面,填写仪器使用记录。 五、实验结果 最大吸收波长λmax=254.50nm 实验五色氨酸、苯丙氨酸和酪氨酸的紫外吸收光谱分析 一、实验目的 1. 掌握紫外-可见分光光度计的工作原理和基本操作。 2. 掌握紫外-可见吸收光谱的绘制(包括导数光谱)以及定量测定方法。 3. 掌握。 4. 了解氨基酸类物质的紫外吸收光谱特点。 二、实验原理 1. 紫外-可见吸收光谱法测定蛋白质含量的基本原理 紫外-可见吸收光谱法是根据溶液中物质的分子或离子对紫外和可见光谱区辐射能的吸收来研究物质的组成和结构的方法,也称作紫外和可见吸收广度法,它包括比色分析法和紫外-可见分光光度法。 紫外-可见分光光度法属于吸收光谱法,分子中的电子总是处在某一种运动状态中,每一种状态都具有一定的能量,属于一定的能级。电子由于受到光、热、电等的激发,从一个能级转移到另一个能级,称为跃迁。当这些电子吸收了外来辐射的能量,就从一个能量较低的能级跃迁到另一个能量较高的能级。 图1 电子跃迁示意图 物质对不同波长的光线具有不同的吸收能力,如果改变通过某一吸收物质的入射光的波长,并纪录该物质在每一波长处的吸光度(A),然后以波长为横坐标,以吸光度为纵坐标作图,这样得到的谱图为该物质的吸收光谱或吸收曲线。 当一定波长的光通过某物质的溶液时,入射光强度I。与透过光强度I之比的对数与该物质的浓度c及样品池厚度b成正比。其数学表达式为: 此式为Lambert-Beer定律,是分光光度法定量分析的基础,其中A为吸光度。 由于不同物质具有不同的分子结构,对不同波长的光会产生选择性吸收,具有不同的吸收光谱,因而,我们可以利用紫外-可见吸收光谱法对物质结构进 行鉴定和进行定量分析、根据被测量物质分子对紫外-可见波段范围 原子发射光谱:原子的外层由高层能及向底层能级,能量以电磁辐射的形式发射出去,这样就得到了发射光谱。原子发射一般是线状光谱。 原理:原子处于基态,通过电至激发,热至激发或者,光至激发等激发作用下,原子获得能量,外层电子从基态跃迁到较高能态变成激发态,经过10-8s,外层电子就从高能级向较低能级或基态跃迁,多余能量的发射可得到一条光谱线。 光谱选择定律:①主量子数的变化△n为包括零的整数,②△±1,即跃迁只能在S项与P项间,P与S或者D间,D到P和F。 ③△0,即不同多重性状间的迁移是不可能的。 ③△0,±1。但在0时,0的跃迁是允许的。N21 影响谱线强度的主要因素:1激发电位2跃迁概率3 统计权重4激发温度(激发温度↑离子↑原子光谱↓离子光谱↑)5原子密度 原子发射光谱仪组成:激发光源,色散系统,检测系统, 激发光源:①火焰:2000到3000K,只能激发激发电位低的原子:如碱性金属和碱土金属。 ②直流电弧:4000到7000K,优点:分析的灵敏度高,背景小,适合定量分析和低含量的测定。缺点:不宜用于定量分析及低熔点元素的分析。 ③交流电弧:温度比直流高,离子线相对多,稳定性比直流高,操作安全,但灵敏度差 ④火花:一万K,稳定性好,定量分析以及难测元素。每次放电时间间隔长,电极头温度低。 适合分析熔点低。缺点:灵敏度较差,背景大,不宜做痕量元素分析(金属,合金等组成均匀的试样)⑤辉光激发能力强,可以激发很难激发的元素,(非金属,卤素,一些气体)谱线强度大,背景小,检出限低,稳定性好,准确度高(设备复杂,进样不方便)⑥电感耦合等离子体10000K 基体效应小,检出限低,限行范围宽⑦激光一万K,适合珍贵样品 分光系统:单色器:入射狭缝,准直装置,色散装置,聚焦透镜,出射狭缝。 棱镜:分光原理:光的折射,由于不同的光有不同的折射率,所以分开。 光栅:光的折射与干涉的总效果,不同波长的光通过光栅作用各有不同的衍射角。 分辨率: 原子发射检测法:①目视法,②光电法, ③摄谱法:用感光板来记录光谱,感光板:载片(光学玻璃)和感光乳剂(精致卤化银精致明胶)。曝光量 E感光层接受的照度、 黑度:1为没有谱线的光强,i通过谱线的光强度i ,透过率T 定性分析:铁光谱比较法,标样光谱比较法,波长测定法。 光谱分析技术及应用 一、光谱分析的分类 1、原子吸收光谱法——也叫湿法分析。它是以待测元素的特征光波,通过样品的蒸发,被蒸发中的待测元素的基态原子所吸收,由辐射强度的减弱程度,来测定该元素的存在与否和含量多少;通常是采用火焰或无火焰(也叫等离子)方法,把被测元素转化为基态原子。根据吸收光波能量的多少测定元素的含量。 通常原子吸收光谱法是进行仪器定量分析的湿法分析。 2、原子发射光谱法——利用外部能量激发光子发光产生光谱。 看谱分析法就是原始的、也是最经典的利用原子发射光谱的分析方法。看谱分析法在我国工业生产上的使用是在上世纪50年代,58年北京永定机械厂制造了第一台仿苏联技术的看谱仪,随后天津光学仪器厂成为我国大量生产棱镜分光的看谱镜基地。 上世纪80年代起,德国、英国、美国等国家,开始研制采用CCD (Charge Coupled Device电荷耦合器件)技术作为光谱接收器件的直读式定量光谱仪,德国以实验室用大型直读定量光谱仪为主;英国阿朗公司、美国尼通公司以便携式金属分析仪为主打市场。近年来,德国、芬兰等国家研制生产便携式、直读定量光谱仪,分析精度在一定条件下可以替代实验室直读式定量光谱仪。 二、看谱分析的特点 1、操作简便,分析速度快。 2、适合现场操作。 3、无损检测(现场操作情况下无须破坏样品)。 4、检测成本低。是便携式金属分析仪的1/30左右,是便携式直读定量光谱仪的1/40。 5、有一定的灵敏度和准确度。 三、看谱分析的方法: 定性分析方法,所谓定性就是判定分析的元素是否存在的分析。严格的讲定性分析是根据某元素的特征灵敏线的出现与否,来确定该元素是否存在的分析方法。 那么,什么叫灵敏线呢? 某元素在某几个区域出现的几条与其它元素不同的特征线;或称“在较低含量情况下出现的谱线”,或者说是在某一范围内出现的谱线,叫做灵敏线。 半定量方法就是近似的估计元素含量的方法。 利用谱线进行比较,即通过 亮度比较含量,就是与铁基线进 行比较,含量与亮度的对数成正 比关系。(用来进行比较的铁基线 的亮度应不变。)lgI(谱线强度) 四、看谱分析的一般步骤 1、分析前的准备 利用紫外吸收光谱检查物质纯度 紫外-可见分光光度法测定水中苯酚含量 一、实验目的 1.学会使用Cary50型紫外-可见分光光度计 2.掌握紫外-可见分光光度计的定量分析方法 二、原理简介 紫外-可见吸收光谱是由分子外层电子能级跃迁产生,同时伴随着分子的振动能级和转动能级的跃迁,因此吸收光谱具有带宽。紫外-可见吸收光谱的定量分析采用朗伯-比尔定律,被测物质的紫外吸收的峰强与其浓度成正比,即: 其中A是吸光度,I、分别为透过样品后光的强度和测试光的强度,为摩尔吸光系数,b为样品厚度。 由于苯酚在酸、碱溶液中吸收波长不一致(见下式),实验选择在碱性中测试,选择测试的波长为288nm左右,取紫外-可见光谱仪波长扫描后的最大吸收波长。 Cary50是瓦里安公司的单光束紫外-可见分光光度计。仪器原理是光源发出光谱,经单色器分光,然后单色光通过样品池,达到检测器,把光信号转变成电信号,再经过信号放大、模/数转换,数据传输给计算机,由计算机软件处理。 三、仪器与溶液准备 1、Cary50型紫外-可见分光光度计 2、1cm石英比色皿一套 3、25 ml容量瓶5只,100 ml容量瓶1只,10ml移液管二支 配置250 mg/L苯酚的标准溶液:准确称取0.0250 g苯酚于250 mL烧杯中,加入去离子水20 mL使之溶解,加入0.1M NaOH 2mL,混合均匀,移入100 mL容量瓶,用去离子水稀释至刻度,摇匀。 取5只25 mL容量瓶,分别加入1.00、2.00、3.00、4.00、5.00 mL苯酚标准溶液,用去离子水稀释至刻度摇匀,作为标准溶液系列。 将溶剂,标准溶液,待测水样依此装入石英比色皿。按测试程序的提示,依次放入样品室中进行测试。 四、测试过程 1、确认样品室内无样品 2、开电脑进入Window 系统 3、点击进入Cary50 主菜单 4、双击Cary-WinUV图标 5、在Win-UV 主显示窗口下,双击所选图标“SCAN”以扫描测定吸收曲线:取上述标准系列任一溶液装进1cm石英比色皿至4/5,以装有蒸馏水的1cm石英比色皿作为空白参比,设定在220-350 nm波长范围内扫描,获得波长-吸收曲线,读取最大吸收的波长数据。 6、在Win-UV 主显示窗口下,双击图标“Concentration”进入定量分析主菜单 7、设定测试分析步骤: (l)单击Setup功能键,进入参数设置页面。在Wavelength处填入由步骤5获取的波长数据。 (2)按Cary Control 、Standards、Options、Samples、Reports、Auto store顺序,分别设置好菜单中每页的参数。按OK回到“Concentration”界面主菜单。 (3)单击View莱单,选择需要显示的内容。 例如基本选项Toolbar,buttons,Graphics,Report。 (4)单击Zero,提示“Load blank press OK to read” (放空白按OK读),放入空白蒸馏水到样品室内,按OK测试,测完取出样品。 (5)单击Start, 出现标准/样品选择页。选Selected for Analysis(选择分析的标准和样品)。此框的内容为准备分析的标准和样品。 (6)按OK进行分析测试。 依Presentstdl的提示:放入标准1然后按OK键进行读数。放标准2按OK进行读数。直到全部标准读完。 (7)出现“Present Samplel Press OK to read”提示框,根据提示,放入样品1按OK开始读样品,直到样品测完。 实验三:有机化合物的紫外-可见吸收光谱及溶剂效应 一、实验目的 1、了解紫外-可见分光光度法的原理及应用范围。 2、了解紫外-可见分光光度计的基本构造及设计原理。 3、了解苯及衍生物的紫外吸收光谱及鉴定方法。 4、观察溶剂对吸收光谱的影响。 二、实验原理 紫外-可见分光光度法是光谱分析方法中吸光测定法的一部分。 1、紫外-可见吸收光谱的产生 紫外可见吸收光谱是由于分子中价电子的跃迁而产生的。这种吸收光谱决定于分子中价电子的分布和结合情况。分子内部的运动分为价电子运动、分子内原子在平衡位置附近的振动和分子绕其重心的转动。因此分子具有电子能级、振动能级和转动能级。通常电子能级间隔为1至20eV,这一能量恰落在紫外与可见光区。每一个电子能级之间的跃迁,都伴随着分子的振动能级和转动能级的变化,因此,电子跃迁的吸收线就变成了内含有分子振动和转动精细结构的较宽的谱带。 芳香族化合物的紫外光谱的特点是具有由π→π*跃迁产生的3个特征吸收带。例如,苯在184nm附近有一个强吸收带,ε=68000;在204nm处有一较弱的吸收带,ε=8800;在254nm附近有一个弱吸收带,ε=250。当苯处在气态时,这个吸收带具有很好的精细结构。当苯环上带有取代基时,则强烈地影响苯的3个特征吸收带。 2、紫外-可见光谱分析法的应用 1)化学物质的结构分析; 2)有机化合物分子量的测定; 3)酸碱离解常数的测定; 4)标准曲线法测定有机化合物的含量; 5)络合物中配位体/金属比值的测定; 6)有机化合物异构物的判别等。 3、紫外-可见分光光度计的基本构造 三、实验仪器与试剂 仪器:Cary500紫外-可见-近红外分光光度计 比色管(带塞):5mL10支,10mL3支; 移液管:1mL6支,0.1mL2支 实验一:紫外-可见吸收光谱 一、实验目的 1.熟悉和掌握紫外-可见吸收光谱的使用方法 2.用紫外-可见吸收光谱测定某一位置样品浓度 3.定性判断和分析溶液中所含物质种类 二、实验原理 紫外吸收光谱的波长范围在200~400,可见光吸收光谱的波长在400~800,两者都属于电子能谱,两者都可以用朗伯比尔(Lamber-Beer’s Law)定律来描述 A=ε bc 其中A为吸光度;ε为光被吸收的比例系数;c为吸光物质的浓度,单位mol/L; b为吸收层厚度,单位cm 有机化合物的紫外-可 见吸收光谱,是其分子中 外层价电子跃迁的结果, 其中包括有形成单键的σ 电子、有形成双键的π电 子、有未成键的孤对n电 子。外层电子吸收紫外或 者可见辐射后,就从基态 向激发态(反键轨道)跃 迁。主要有四种跃迁,所 需能量ΔE大小顺序为 σ→σ*>n→σ*>π→π>n→π* 1、开机 打开紫外-可见分光光度计开关→开电脑→软件→联接→M(光谱方法)进行调节实验需要的参数:波长范围700-365nm 扫描速度高速;采样间隔:0.5nm 2、甲基紫的测定 (1)校准基线 将空白样品(水)放到比色槽中,点击“基线”键,进行基线校准 (2)标准曲线的测定 分别将5ug/ml、10ug/ml 、15ug/ml 、20ug/ml甲基紫溶液移入比色皿(大约2/3处),放到比色槽中,点击“开始”键,进行扫描,保存 (3)测定试样 将试样甲基紫溶液移入比色皿(大约2/3处),放到比色槽中,点击“开始” 键,进行扫描,保存 3、甲基红的测定 (1)校准基线 将空白样品(乙醇)放到比色槽中,点击“基线”键,进行基线校准 (2)测定试样 将试样甲基紫溶液移入比色皿(大约2/3处),放到比色槽中,点击“开始” 键,进行扫描,保存 四、实验结果 1.未知浓度的测定 分别测定了5μg/ml,10μg/ml,15μg/ml,20μg/ml和未知浓度的甲基紫溶液的紫外吸收光谱,紫外吸收谱图如下: 甲基紫在580nm是达到最大吸收见下表: AES原子发射光谱:原子的外层由高层能及向底层能级,能量以电磁辐射的形式发射出去,这样就得到了发射光谱。原子发射一般是线状光谱。 原理:原子处于基态,通过电至激发,热至激发或者,光至激发等激发作用下,原子获得能屋,外层电子从基态跃迁到较髙能态变成激发态,经过10%,外层电子就从髙能级向较低能级或基态跃迁,多余能量的发射可得到一条光谱线。 光谱选择定律:①主量子数的变化为包括零的整数,②1,即跃迁只能在S项与P 项间,P与S或者D间,D到P和F。③△$=(),即不同多重性状间的迁移是不可能的。@AJ=0, ±1。但在J=O 时,J=0的跃迁是允许的。N2S+1L J 影响谱线强度的主要因素:1激发电位2跃迁概率3统汁权重4激发温度(激发温度f离子t原子光谱I离子光谱t )5原子密度 原子发射光谱仪组成:激发光源,色散系统,检测系统, 激发光源:①火焰:2000到3000K,只能激发激发电位低的原子:如碱性金属和碱上金属。 ②直流电弧:4000到7000K,优点:分析的灵敏度髙,背景小,适合定量分析和低含量的测定。缺点:不宜用于定量分析及低熔点元素的分析。 ③交流电弧:温度比直流高,离子线相对多,稳左性比直流髙,操作安全,但灵敏度差 ④火花:一万K,稳定性好,泄量分析以及难测元素。每次放电时间间隔长,电极头温度低。适合分析熔点低。缺点:灵敏度较差,背景大,不宜做痕量元素分析(金属,合金等组成均匀的试样)⑤辉光激发能力强,可以激发很难激发的元素,(非金属,卤素,一些气体)谱线强度大,背景小,检岀限低,稳左性好,准确度髙(设备复杂,进样不方便)⑥电感耦合等离子体10000K基体效应小,检岀限低,限行范用宽⑦激光一万K,适合珍贵样品分光系统:单色器:入射狭缝,准直装巻,色散装置,聚焦透镜,出射狭缝。 棱镜:分光原理:光的折射,由于不同的光有不同的折射率,所以分开。 光栅:光的折射与干涉的总效果,不同波长的光通过光栅作用各有不同的衍射角。分辨率: 原子发射检测法:①目视法,②光电法, ③摄谱法:用感光板来记录光谱,感光板:载片(光学玻璃)和感光乳剂(精致卤化银精致明胶)。曝光^H=Et E感光层接受的照度、 黑度:S=lgT-*=lg io/i io为没有谱线的光强,i通过谱线的光强度i,透过率T 定性分析:铁光谱比较法,标样光谱比较法,波长测定法。 龙量法:①基本原理②内标法⑴内标元素和被测元素有相近的物理化学性质,如沸点,熔点近似,在激发光源中有相近的蒸发性。⑵内标元素和被测元素有相近的激发能,如果选用离子线组成分析线对时,则不仅要求两线对的激发电位相等,还要求内标元素的电离电位相近。⑶内标元素是外加的,样品中不应有内标元素,⑷内标元素的含量必须适量且固泄,⑸ 汾西线和内标线无自吸或者自吸很小,且不受其他谱线干扰。⑹如采用照相法测量谱线强度,则要求两条谱线的波长应尽量靠近。 简述内标法基本原理和为什么要使用内标法。 答:内标法是通过测量谱线相对强度进行龙量分析的方法。通常在被测左元素的谱线中选一条灵敏线作为分析线,在基体元素(或定量加入的英它元素)的谱线中选一条谱线为比较线,又称为内标线。分析线与内标线的绝对强度的比值称为分析线对的相对强度。在工作条件相对变化时,分析线对两谱线的绝对强度均有变化,但对分析线对的相对强度影响不大,因此可准确地测泄元素的含量。从光谱泄量分析公式lg/=/?lgc + lgt/,可知谱线强度I与元素的浓度有关,还受到许多因素的影响,而内标法可消除工作条件变化等大部分因素带来的影响。 激发电位:原子中某一外层电子由基态激发到髙能级所需要的能量。共振线:由激发态像基态跃迁所发射的谱线。(共振线具有最小电位,最容易被激发,最强谱线) 火花线:火法激发产生的谱线,激发能量大,产生的谱线主要是离子线。又称共振线。自吸和自各种光谱原理解读
紫外光谱分析实验数据处理部分
仪器分析光谱法总结
实验1紫外可见吸收光谱实验报告
波谱解析 第一章 紫外光谱习题参考答案
红外光谱总结
实验三、有机化合物的紫外吸收光谱及溶剂效应解读
波谱解析习题
光谱基础知识解读
实验一 紫外吸收光谱定性分析的应用
光谱学课程总结
紫外吸收光谱法测定苯的含量
仪器分析实验5-紫外可见光谱分析
仪器分析-光谱法总结
(整理)光谱分析技术及应用
紫外吸收光谱实验报告
高中化学实验三: 有机化合物的紫外-可见吸收光谱及溶剂效应
实验1紫外-可见吸收光谱实验报告
仪器分析光谱法总结
