金刚石的晶体结构分析.doc
金刚石的晶体结构分析
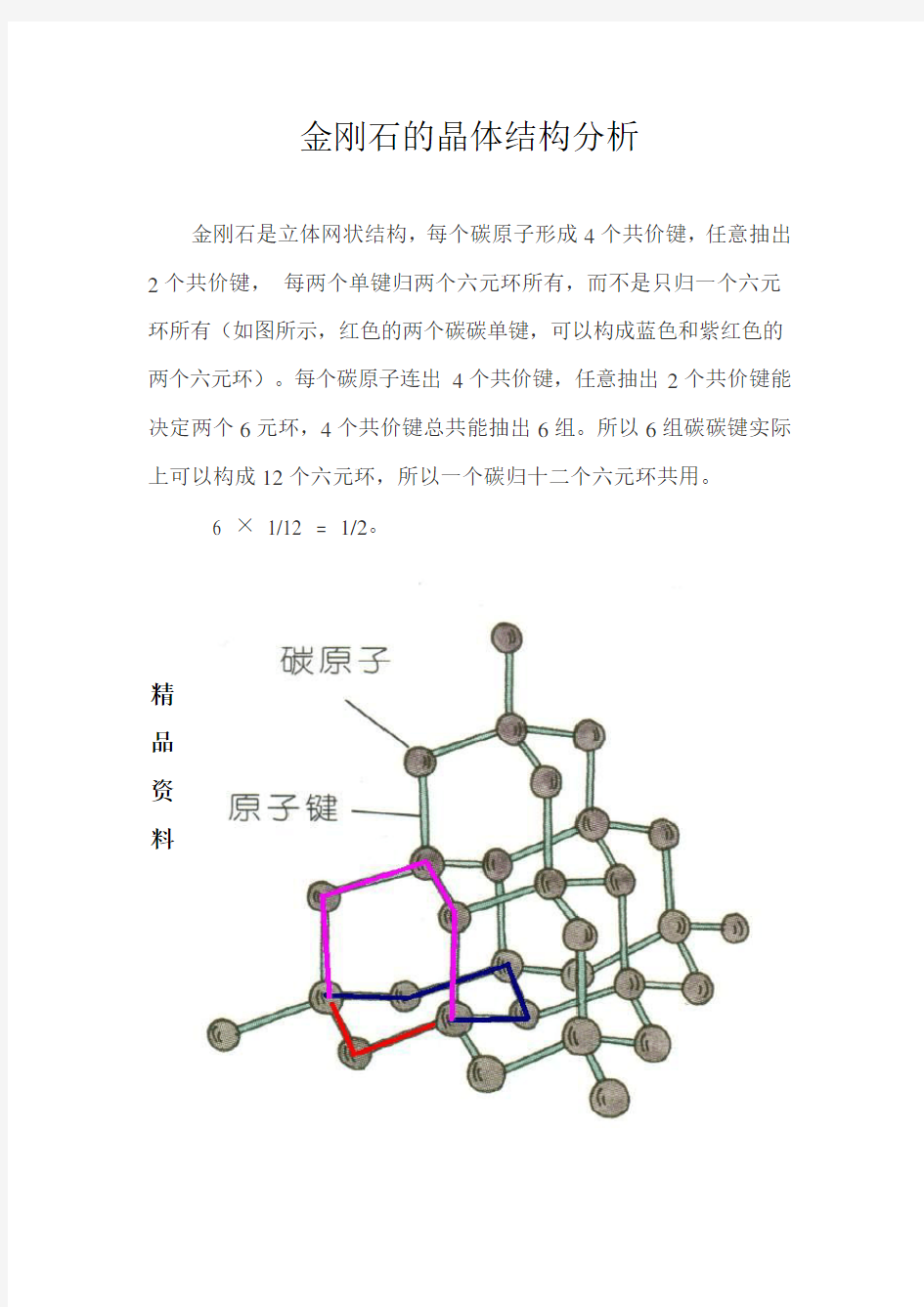
金刚石是立体网状结构,每个碳原子形成4个共价键,任意抽出2个共价键,每两个单键归两个六元环所有,而不是只归一个六元环所有(如图所示,红色的两个碳碳单键,可以构成蓝色和紫红色的两个六元环)。每个碳原子连出4个共价键,任意抽出2个共价键能决定两个6元环,4个共价键总共能抽出6组。所以6组碳碳键实际上可以构成12个六元环,所以一个碳归十二个六元环共用。
6 ×1/12 = 1/2。
精
品
资
料
33 实际金属的晶体结构 一、多晶体结构和亚结构
3.3 实际金属的晶体结构 一、多晶体结构和亚结构 实际使用的工业金属材料,即使体积很小,其内部的晶格位向也不是完全一致的,而是包含着许许多多彼此间位向不同的、称之为晶粒的颗粒状小晶体。而晶粒之间的界面称为晶界。这种实际上由许多晶粒组成的晶体结构称为多晶体结构(polycrystalline structure)。一般金属材料都是多晶体(图3-12)。通常测得的金属性能是各个位向不同的晶粒的平均值,故显示出各向同性。 图3—12 多晶体结构示意图 实践证明,即使在一个晶粒内部,其晶格位向也并不是象理想晶体那样完全一致,而是存在着许多尺寸更小,位向差也很小的小晶块。它们相互嵌镶成一颗晶粒。这些小晶块称为亚结构。可见,只有在亚结构内部,晶格的位向才是一致的。 二、晶体缺陷 实际晶体还因种种原因存在着偏离理想完整点阵的部位或结构,称为晶体缺陷(crystal defect)。晶体缺陷的存在及其多寡,是研究晶体结构、金属塑性变形的关键问题。根据其几何特性,晶体的缺陷可分为三类: 1.点缺陷——空位和间隙原子 实际晶体未被原子占有的晶格结点称为空位;而不占有正常晶格位置而处于晶格空隙之间的原子则称为间隙原子。在空位或间隙原子的附近,由于原子间作用力的平衡被破坏,使其周围的原子离开了原来的平衡位置,即产生所谓的晶格畸变。空位和间隙原子都处于不断的运动和变化之中,这对于热处理和化学处理过程都是极为重要的。 2.线缺陷——位错 晶体中某处有一列或若干列原子发生有规律的错排现象称为位错(dislocation)。有刃型
和螺型两种位错。 刃型位错如图3-13所示。垂直方向的原子面EFGH中断于水平晶面ABCD上的EF处,就像刀刃一样切入晶体,使得晶体中位于ABCD面的上、下两部分出现错排现象。EF线称为刃型位错线。在位错线附近区域,晶格发生畸变,导致ABCD晶面上、下方位错线附近的区域内,晶体分别受到压应力和拉应力。符号“┴”和“┬”分别表示多出的原子面在晶体的上半部和下半部,分别称为正、负刃型位错。 图3—13 刃型位错示意图 螺型位错如图3-14所示。晶体在BC右方的上、下两部分原子排列沿ABCD晶面发生了错动。aa’右边晶体上、下层原子相对移动了一原子间距,而在BC和aa’之间形成了一个上下层原子不相吻合的过渡区域,这里的原子平面被扭成了螺旋面。在原子面上,每绕位错线一周就推进了一个晶面间距。显然,螺型位错附近区域的晶格也发生了严重畸变,形成了一个应力集中区。 3.面缺陷——晶界和亚晶界 晶界实际上是不同位向晶粒之间原子排列无规则的过渡层(图3-15)。晶界处晶格处于畸变状态,导致其能量高于晶粒内部能量,常温下显示较高的强度和硬度,容易被腐蚀,熔点较低,原子扩散较快。
晶体学基础与晶体结构习题与答案
晶体学基础与晶体结构习题与答案 1. 由标准的(001)极射赤面投影图指出在立方晶体中属于[110]晶带轴的晶带,除了已在图2-1中标出晶面外,在下列晶面中哪些属于[110]晶带?(1-12),(0-12),(-113),(1-32),(-221)。 图2-1 2. 试证明四方晶系中只有简单立方和体心立方两种点阵类型。 3. 为什么密排六方结构不能称作为一种空间点阵? 4. 标出面心立方晶胞中(111)面上各点的坐标。 5. 标出具有下列密勒指数的晶面和晶向:a)立方晶系(421),(-123),(130),[2-1-1],[311];b)六方晶系(2-1-11),(1-101),(3-2-12),[2-1-11],[1-213]。 6. 在体心立方晶系中画出{111}晶面族的所有晶面。 7. 在立方晶系中画出以[001]为晶带轴的所有晶面。 8. 已知纯钛有两种同素异构体,密排六方结构的低温稳定的α-Ti和体心立方结构的高温稳定的β-Ti,其同素异构转变温度为882.5℃,使计算纯钛在室温(20℃)和900℃时晶体中(112)和(001)的晶面间距(已知aα20℃=0.29506nm,cα20℃=0.46788nm,aα900℃=0.33065nm)。 9. 试计算面心立方晶体的(100),(110),(111),等晶面的面间距和面致密度,并指出面间距最大的面。 10.平面A在极射赤平面投影图中为通过NS及核电0°N,20°E的大圆,平面B的极点在30°N,50°W处,a)求极射投影图上两极点A、B间的夹角;b)求出A绕B顺时针转过40°的位置。 11. a)说明在fcc的(001)标准极射赤面投影图的外圆上,赤道线上和0°经线上的极点的指数各有何特点,b)在上述极图上标出(-110),(011),(112)极点。 12. 图2-2为α-Fe的x射线衍射谱,所用x光波长λ=0.1542nm,试计算每个峰线所对应晶面间距,并确定其晶格常数。 图2-2 13. 采用Cu kα(λ=0.15418nm)测得Cr的x射线衍射谱为首的三条2θ=44.4°,64.6°和81.8°,若(bcc)Cr的晶格常数a=0.28845nm,试求对应这些谱线的密勒指数。
常见的金属晶体结构
第二章作业 2-1 常见的金属晶体结构有哪几种它们的原子排列和晶格常数有什么特点 V、Mg、Zn 各属何种结构答:常见晶体结构有 3 种:⑴体心立方:-Fe、Cr、V ⑵面心立方:-Fe、Al、Cu、Ni ⑶密排六方:Mg、Zn -Fe、-Fe、Al、Cu、Ni、Cr、 2---7 为何单晶体具有各向异性,而多晶体在一般情况下不显示出各向异性答:因为单晶体内各个方向上原子排列密度不同,造成原子间结合力不同,因而表现出各向异性;而多晶体是由很多个单晶体所组成,它在各个方向上的力相互抵消平衡,因而表现各向同性。第三章作业3-2 如果其它条件相同,试比较在下列铸造条件下,所得铸件晶粒的大小;⑴金属模浇注与砂模浇注;⑵高温浇注与低温浇注;⑶铸成薄壁件与铸成厚壁件;⑷浇注时采用振动与不采用振动;⑸厚大铸件的表面部分与中心部分。答:晶粒大小:⑴金属模浇注的晶粒小⑵低温浇注的晶粒小⑶铸成薄壁件的晶粒小⑷采用振动的晶粒小⑸厚大铸件表面部分的晶粒小第四章作业 4-4 在常温下为什么细晶粒金属强度高,且塑性、韧性也好试用多晶体塑性变形的特点予以解释。答:晶粒细小而均匀,不仅常温下强度较高,而且塑性和韧性也较好,即强韧性好。原因是:(1)强度高:Hall-Petch 公式。晶界越多,越难滑移。(2)塑性好:晶粒越多,变形均匀而分散,减少应力集中。(3)韧性好:晶粒越细,晶界越曲折,裂纹越不易传播。 4-6 生产中加工长的精密细杠(或轴)时,常在半精加工后,将将丝杠吊挂起来并用木锤沿全长轻击几遍在吊挂 7~15 天,然后再精加工。试解释这样做的目的及其原因答:这叫时效处理一般是在工件热处理之后进行原因用木锤轻击是为了尽快消除工件内部应力减少成品形变应力吊起来,是细长工件的一种存放形式吊个7 天,让工件释放应力的时间,轴越粗放的时间越长。 4-8 钨在1000℃变形加工,锡在室温下变形加工,请说明它们是热加工还是冷加工(钨熔点是3410℃,锡熔点是232℃)答:W、Sn 的最低再结晶温度分别为: TR(W) =(~×(3410+273)-273 =(1200~1568)(℃)>1000℃ TR(Sn) =(~×(232+273)-273 =(-71~-20)(℃) <25℃ 所以 W 在1000℃时为冷加工,Sn 在室温下为热加工 4-9 用下列三种方法制造齿轮,哪一种比较理想为什么(1)用厚钢板切出圆饼,再加工成齿轮;(2)由粗钢棒切下圆饼,再加工成齿轮;(3)由圆棒锻成圆饼,再加工成齿轮。答:齿轮的材料、加工与加工工艺有一定的原则,同时也要根据实际情况具体而定,总的原则是满足使用要求;加工便当;性价比最佳。对齿轮而言,要看是干什么用的齿轮,对于精度要求不高的,使用频率不高,强度也没什么要求的,方法 1、2 都可以,用方法 3 反倒是画蛇添足了。对于精密传动齿轮和高速运转齿轮及对强度和可靠性要求高的齿轮,方法 3 就是合理的。经过锻造的齿坯,金属内部晶粒更加细化,内应力均匀,材料的杂质更少,相对材料的强度也有所提高,经过锻造的毛坯加工的齿轮精度稳定,强度更好。 4-10 用一冷拔钢丝绳吊装一大型工件入炉,并随工件一起加热到1000℃,保温后再次吊装工件时钢丝绳发生断裂,试分析原因答:由于冷拔钢丝在生产过程中受到挤压作用产生了加工硬化使钢丝本身具有一定的强度和硬度,那么再吊重物时才有足够的强度,当将钢丝绳和工件放置在1000℃炉内进行加热和保温后,等于对钢丝绳进行了回复和再结晶处理,所以使钢丝绳的性能大大下降,所以再吊重物时发生断裂。 4-11 在室温下对铅板进行弯折,越弯越硬,而稍隔一段时间再行弯折,铅板又像最初一样柔软这是什么原因答:铅板在室温下的加工属于热加工,加工硬化的同时伴随回复和再结晶过程。越弯越硬是由于位错大量增加而引起的加工硬化造成,而过一段时间又会变软是因为室温对于铅已经是再结晶温度以上,所以伴随着回复和再结晶过程,等轴的没有变形晶粒取代了变形晶粒,硬度和塑性又恢复到了未变形之前。第五章作业 5-3 一次渗碳体、二次渗碳体、三次渗碳体、共晶渗碳体、共析渗碳体异同答:一次渗碳体:由液相中直接析出来的渗碳体称为一次渗碳体。二次渗碳体:从 A 中析出的渗碳体称为二次渗碳体。三次渗碳体:从 F 中析出的渗碳体称为三次渗碳体共晶渗碳体:经共晶反应生成的渗碳体即莱氏体中的渗碳体称为共晶渗碳体共析渗碳体:经共析反应生成的渗碳体即珠光体中的渗
几种常见晶体结构分析
几种常见晶体结构分析文档编制序号:[KK8UY-LL9IO69-TTO6M3-MTOL89-FTT688]
几种常见晶体结构分析 河北省宣化县第一中学 栾春武 邮编 075131 栾春武:中学高级教师,张家口市中级职称评委会委员。河北省化学学会会员。市骨干教师、市优秀班主任、模范教师、优秀共产党员、劳动模范、县十佳班主任。 联系电话: E-mail : 一、氯化钠、氯化铯晶体——离子晶体 由于离子键无饱和性与方向性,所以离子晶体中无单个分子存在。阴阳离子在晶体中按一定的规则排列,使整个晶体不显电性且能量最低。离子的配位数分析如下: 离子数目的计算:在每一个结构单元(晶胞)中,处于不同位置的微粒在该单元中所占的份额也有所不同,一般的规律是:顶点上的微粒属于该 单元中所占的份额为18,棱上的微粒属于该单元中所占的份额为1 4,面上 的微粒属于该单元中所占的份额为1 2,中心位置上(嚷里边)的微粒才完 全属于该单元,即所占的份额为1。 1.氯化钠晶体中每个Na +周围有6个Cl -,每个Cl -周围有6个Na +,与一个Na +距离最近且相等的Cl -围成的空间构型为正八面体。每个Na +周围与其最近且距离相等的Na +有12个。见图1。 图1 图2 NaCl
晶胞中平均Cl-个数:8×1 8 + 6× 1 2 = 4;晶胞中平均Na+个数:1 + 12×1 4 = 4 因此NaCl的一个晶胞中含有4个NaCl(4个Na+和4个Cl-)。 2.氯化铯晶体中每个Cs+周围有8个Cl-,每个Cl-周围有8个Cs+,与一个Cs+距离最近且相等的Cs+有6个。 晶胞中平均Cs+个数:1;晶胞中平均Cl-个数:8×1 8 = 1。 因此CsCl的一个晶胞中含有1个CsCl(1个Cs+和1个Cl-)。 二、金刚石、二氧化硅——原子晶体 1.金刚石是一种正四面体的空间网状结构。每个C 原子以共价键与4个C原子紧邻,因而整个晶体中无单 个分子存在。由共价键构成的最小环结构中有6个碳原 子,不在同一个平面上,每个C原子被12个六元环共用,每C—C键共6 个环,因此六元环中的平均C原子数为6× 1 12 = 1 2 ,平均C—C键数为 6×1 6 = 1。 C原子数: C—C键键数= 1:2; C原子数: 六元环数= 1:2。 2.二氧化硅晶体结构与金刚石相似,C被Si代替,C与C之间插 氧,即为SiO 2晶体,则SiO 2 晶体中最小环为12环(6个Si,6个O), 图3 CsCl 晶 图4 金刚石晶
晶体结构的分析与计算训练题
晶体结构的分析与计算训练题 1.(2015·全国卷Ⅰ)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示: (1)在石墨烯晶体中,每个C 原子连接________个六元环,每个六元环占有________个C 原子。 (2)在金刚石晶体中,C 原子所连接的最小环也为六元环,每个C 原子连接______个六元环,六元环中最多有______个C 原子在同一平面。 解析:(1)由石墨烯的结构可知,每个C 原子连接3个六元环,每个六元环占有的C 原子数为1 3 ×6=2。 (2)由金刚石的结构可知,每个C 可参与形成4条C —C 键,其中任意两条边(共价键)可以构成2个六元环。根据组合知识可知四条边(共价键)任选其中两条有6组,6×2=12。因此每个C 原子连接12个六元环。六元环中C 原子采取sp 3 杂化,为空间六边形结构,最多有4个C 原子位于同一平面。 答案:(1)3 2 (2)12 4 2.(2016·全国卷Ⅱ)某镍白铜合金的立方晶胞结构如图所示。 (1)晶胞中铜原子与镍原子的数量比为________。 (2)若合金的密度为d g·cm -3 ,晶胞参数a =________nm 。 解析:(1)由晶胞结构图可知,Ni 原子处于立方晶胞的顶点,Cu 原子处于立方晶胞的面心,根据均摊法,每个晶胞中含有Cu 原子的个数为6×12=3,含有Ni 原子的个数为8×1 8= 1,故晶胞中Cu 原子与Ni 原子的数量比为3∶1。 (2)根据m =ρV 可得, 1 mol 晶胞的质量为(64×3+59)g =a 3 ×d g·cm -3 ×N A ,则a =? ????2516.02×1023×d 1 3 cm =? ?? ??2516.02×1023×d 1 3×107 nm 。 答案:(1)3∶1 (2)? ?? ? ?2516.02×1023×d 1 3×107 3.(2017·全国卷Ⅰ)(1)KIO 3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为a =0.446 nm ,晶胞中K 、I 、O 分别处于顶角、体心、面心位置,如图所示。K 与O 间的最短距离为______
较石墨和金刚石的晶体结构
较石墨和金刚石的晶体结构、结合键和性能。 答:金刚石晶体结构为带四面体间隙的FCC,碳原子位于FCC点阵的结合点和四个不 相邻的四面体间隙位置,碳原子之间都由共价键结合,因此金刚石硬度高,结构致密。石墨晶体结构为简单六方点阵,碳原子位于点阵结点上,同层之间由共价键结合,邻层之间由范德华力结合,因此石墨组织稀松,有一定的导电性,常用作润滑剂。 1. 单晶体:如果一个物体就是一个完整的晶体,这样的晶体~单晶体. 水晶、雪花、食盐小颗粒、单晶硅、晶须 2 多晶体:如果整个物体是由许多杂乱无章地排列着的小晶体组成的,这样的物体~多晶体,其中的小晶体叫做晶粒,其边界称为晶界,多晶体有一定的熔点。各向同性 金属及合金等. 3 非晶体:没有规则的几何形状,原子在三维空间内不规则排列。长程无序,各向同性。常见的非晶体有:玻璃、蜂蜡、松香、沥青、橡胶等. 扩散定理 单位时间内通过垂直于扩散方向的单位截面积的物质量(扩散通量)与该物质在该面积处的浓度梯度成正比。 为扩散通量,表示扩散物质通过单位截面的流量,dC/dx为沿x方向的浓度梯度;D为原子的扩散系数。负号表示扩散由高浓度向低浓度方向进行。 层错能 金属结构在堆垛时,没有严格的按照堆垛顺序,形成堆垛层错。层错是一种晶格缺陷,它破坏了晶体的周期完整性,引起能量升高,通常把单位面积层错所增加的能量称为层错能。 层错能出现时仅表现在改变了原子的次近邻关系,几乎不产生点阵畸变。所以,层错能相对于晶界能而言是比较小的。层错能越小的金属,则层错出现的几率越大。
在层错能较高的金属如铝及铝合金、纯铁、铁素体钢(bcc)等热加工时,易发生动态回复,因为这些金属中易发生位错的交滑移及攀移。而奥氏体钢(fcc)、镁及其合金等由于层错能低,不发生位错的交滑移,所以动态再结晶成为动态软化的主要方式。 面心立方的密排面 晶体中原子的堆垛方面心立方晶格的金属: 铝(Al)、铜(Cu)、镍(Ni)、金(Au)、银(Ag)、γ- 铁( γ-Fe, 912℃~1394℃) 式n面心立方:密排面为{111} A BCABCABC…… 点阵常数与原子半径R的关系 晶胞棱边的长度称为点阵常数或晶格常数。对立方晶系,a=b=c,点阵常数用a表示即可; 对六方晶系,a1=a2=a3?c,需要用a和c两个点阵常数来表示晶胞的大小。 1.面心立方: –最密排方向<110> –即面对角线方向原子半径为
高中化学选修三选修3物质结构与性质第三章第3章常见晶体结构晶胞分析归纳整理总结
1 1. 金刚石晶体结构(硅单质相同) 1mol 金刚石中含有 mol C —C 键, 最小环是 元环,(是、否) 共平面。 每个C-C 键被___个六元环共有,每个C 被_____ 个六元环共有。每个六元环实际拥有的碳原子数为 ______个。C-C 键夹角:_______。C 原子的杂化方式是______ SiO 2晶体中,每个Si 原子与 个O 原子以共价键相结合, 每个O 原子与 个Si 原子以共价键相结合,晶体中Si 原子与 O 原子个数比为 。 晶体中Si 原子与Si —O 键数目之比 为 。最小环由 个原子构成,即有 个O , 个Si ,含有 个Si-O 键,每个Si 原子被 个十二元环,每 个O 被 个十二元环共有,每个Si-O 键被__个十二元环共 有;所以每个十二元环实际拥有的Si 原子数为_____个,O 原子数为____个,Si-O 键为____个。硅原子的杂化方式是______,氧原子的杂化方式是_________. 2 . 在NaCl 晶体中,与每个Na +等距离且最近的Cl -有 个, 这些Cl -围成的几何构型是 ;与每个Na +等距离且最近的 Na +有 个。由均摊法可知该晶胞中实际拥有的Na +数为____个 Cl -数为______个,则次晶胞中含有_______个NaCl 结构单元。 3. CaF 2型晶胞中,含:___个Ca 2+和____个F - Ca 2+的配位数: F -的配位数: Ca 2+周围有______个距离最近且相等的Ca 2+ F - 周围有_______个距离最近且相等的F ——。
2 4.如图为干冰晶胞(面心立方堆积),CO 2分子在晶胞 中的位置为 ;每个晶胞含二氧化碳分子的 个数为 ;与每个二氧化碳分子等距离且最 近的二氧化碳分子有 个。 5.如图为石墨晶体结构示意图, 每层内C 原子以 键与周围的 个C 原子结合,层间作用力为 ; 层内最小环有 _____个C 原子组成;每个C 原子被 个最小环所共用;每个 最小环含有 个C 原子, 个C —C 键;所以C 原子数和C-C 键数之比是_________。C 原子的杂化方式 是__________. 6. 冰晶体结构示意如图 ,冰晶体中位于中心的一个水分子 周围有______个位于四面体顶角方向的水分子,每个水分子通过 ______条氢键与四面体顶点上的水分子相连。每个氢键被_____个 水分子共有,所以平均每个水分子有______条氢键。 7. 金属的简单立方堆积是_________层通过_________对 _________堆积方式形成的,晶胞如图所示:每个金属阳离子的 配位数是_____,代表物质是________________________。 8. 金属的体心立方堆积是__________层通过 ________对________堆积方式形成的,晶胞如图: 每个阳离子的配位数是__________.代表物质是 _____________________ 。
金刚石的消光规律--晶体结构题目例
金刚石的消光规律--晶体结构题目例
(4)金刚石的消光规律计算举例: 金刚石结构中C 的原子坐标: (000)(1/2 1/2 0)(1/2 0 1/2)(0 1/2 1/2) (1/4 1/4 1/4) (3/4 3/4 1/4) (3/4 1/4 3/4) (1/4 3/4 3/4) F hkl =∑f j e 2πi(hxj+kyj+lzj) =fe 2πi(0)+fe 2πi(h/2+k/2)+fe 2πi(h/2+l/2)+fe 2πi(k/2+l/2) +fe 2πi(h/4+k/4+l/4) +fe 2πi(3h/4+3k/4+l/4) +fe 2πi(3h/4+k/4+3l/4) +fe 2π i(h/4+3k/4+3l/4) 前四项为面心格子的结构因子,用F F 表示,后四项可提出公因子e πi/2(h+k+l) 。得: F hkl =F F +fe πi/2(h+k+l) (1+e πi (h+k) +e πi (h+l) +e πi (k+l) ) = F F +F F e πi/2(h+k+l) =F F (1+ e πi/2(h+k+l) ) (1) 由面心格子可知,h 、k 、l 奇偶混杂时,F F =0,F=0; (2) h 、k 、l 全为奇数,且h+k+l=2n+1时, 1+ e πi/2(h+k+l) =1+cosπ/2(h+k+l)+i sinπ/2(h+k+l)
=1+cosπ/2(2n+1)+i sinπ/2(2n+1) =1+(-1)n i F=4f(1±i) F 2 =16f 2 (1+1)=32f (3) h 、k 、l 全为偶数,且h+k+l=4n 时 F=4f(1+e 2niπ) = 4f(1+1) = 8f (4) h 、k 、l 全为偶数,且h+k+l≠4n,即h+k+l=2(2n+1)时 F=4f(1+e (2n+1)iπ )=4f(1-1)=0 对于金刚石 各原子的分数坐标为 )(,0,00,)(,021,21,),(,21,021, ),,(,2 1210 )(41,41,41,)(41,43,43,)(43,43,41, )(4 3 ,41,43 由结构因子得 ) ()()(0[F l k i l h i k h i hkl e e e e f ++++++=πππ
几种常见晶体结构分析.
几种常见晶体结构分析 河北省宣化县第一中学 栾春武 邮编 075131 栾春武:中学高级教师,张家口市中级职称评委会委员。河北省化学学会会员。市骨干教师、市优秀班主任、模范教师、优秀共产党员、劳动模范、县十佳班主任。 联系电话::: 一、氯化钠、氯化铯晶体——离子晶体 由于离子键无饱和性与方向性,所以离子晶体中无单个分子存在。阴阳离子在晶体中按一定的规则排列,使整个晶体不显电性且能量最低。离子的配位数分析如下: 离子数目的计算:在每一个结构单元(晶胞) 中,处于不同位置的微粒在该单元中所占的份额也有 所不同,一般的规律是:顶点上的微粒属于该单元中 所占的份额为18 ,棱上的微粒属于该单元中所占的份额为14,面上的微粒属于该单元中所占的份额为12 ,中心位置上(嚷里边)的微粒才完全属于该单元,即所占的份额为1。 1.氯化钠晶体中每个Na +周围有6个C l -,每个Cl -周围有6个Na +,与一个Na +距离最近且相等的 Cl -围成的空间构型为正八面体。每个N a +周围与其最近且距离相等的Na + 有12个。见图1。 晶胞中平均Cl -个数:8×18 + 6×12 = 4;晶胞中平均Na +个数:1 + 12×14 = 4 因此NaCl 的一个晶胞中含有4个NaCl (4个Na +和4个Cl -)。 2.氯化铯晶体中每个Cs +周围有8个Cl -,每个Cl -周围有8个Cs +,与 一个Cs +距离最近且相等的Cs +有6个。晶胞中平均Cs +个数:1;晶胞中平 均Cl -个数:8×18 = 1。 因此CsCl 的一个晶胞中含有1个CsCl (1个Cs +和1个Cl -)。 二、金刚石、二氧化硅——原子晶体 1.金刚石是一种正四面体的空间网状结构。每个C 原子以共价键与4 个C 原子紧邻,因而整个晶体中无单个分子存在。由共价键构成的最小 环结构中有6个碳原子,不在同一个平面上,每个C 原子被12个六元环 共用,每C —C 键共6个环,因此六元环中的平均C 原子数为6× 112 = 12 ,平均C —C 键数为6×16 = 1。 C 原子数: C —C 键键数 = 1:2; C 原子数: 六元环数 = 1:2。 2.二氧化硅晶体结构与金刚石相似,C 被Si 代替,C 与C 之间插氧,即为SiO 2晶体,则SiO 2晶体中最小环为12环(6个Si ,6个O ), 最小环的平均Si 原子个数:6×112 = 12;平均O 原子个数:6×16 = 1。 即Si : O = 1 : 2,用SiO 2表示。 在SiO 2晶体中每个Si 原子周围有4个氧原子,同时每个氧原子结合2个硅原子。一个Si 原子可形 图 1 图 2 NaCl 晶体 图3 CsCl 晶体 图4 金刚石晶体
较石墨和金刚石的晶体结构
较石墨和金刚石的晶体 结构 Revised as of 23 November 2020
较石墨和金刚石的晶体结构、结合键和性能。 答:金刚石晶体结构为带四面体间隙的FCC,碳原子位于FCC点阵的结合点和四个不 相邻的四面体间隙位置,碳原子之间都由共价键结合,因此金刚石硬度高,结构致密。石墨晶体结构为简单六方点阵,碳原子位于点阵结点上,同层之间由共价键结合,邻层之间由范德华力结合,因此石墨组织稀松,有一定的导电性,常用作润滑剂。 1. 单晶体:如果一个物体就是一个完整的晶体,这样的晶体~单晶体. 水晶、雪花、食盐小颗粒、单晶硅、晶须 2 多晶体:如果整个物体是由许多杂乱无章地排列着的小晶体组成的,这样的物体~多晶体,其中的小晶体叫做晶粒,其边界称为晶界,多晶体有一定的熔点。各向同性 金属及合金等. 3 非晶体:没有规则的几何形状,原子在三维空间内不规则排列。长程无序,各向同性。 常见的非晶体有:玻璃、蜂蜡、松香、沥青、橡胶等. 扩散定理 单位时间内通过垂直于扩散方向的单位截面积的物质量(扩散通量)与该物质在该面积处的浓度梯度成正比。
为扩散通量,表示扩散物质通过单位截面的流量,dC/dx为沿x方向的浓度梯度;D为原子的扩散系数。负号表示扩散由高浓度向低浓度方向进行。 层错能 金属结构在堆垛时,没有严格的按照堆垛顺序,形成堆垛层错。层错是一种晶格缺陷,它破坏了晶体的周期完整性,引起能量升高,通常把单位面积层错所增加的能量称为层错能。 层错能出现时仅表现在改变了原子的次近邻关系,几乎不产生点阵畸变。所以,层错能相对于晶界能而言是比较小的。层错能越小的金属,则层错出现的几率越大。 在层错能较高的金属如铝及铝合金、纯铁、铁素体钢(bcc)等热加工时,易发生动态回复,因为这些金属中易发生位错的交滑移及攀移。而奥氏体钢(fcc)、镁及其合金等由于层错能低,不发生位错的交滑移,所以动态再结晶成为动态软化的主要方式。 面心立方的密排面 晶体中原子的堆垛方面心立方晶格的金属: 铝(Al)、铜(Cu)、镍(Ni)、金(Au)、银(Ag)、γ- 铁( γ-Fe, 912℃~1394℃)
金刚石的消光规律 晶体结构题目例
(4)金刚石的消光规律计算举例: 金刚石结构中C 的原子坐标: (000)(1/2 1/2 0)(1/2 0 1/2)(0 1/2 1/2) (1/4 1/4 1/4) (3/4 3/4 1/4) (3/4 1/4 3/4) (1/4 3/4 3/4) F hkl =∑f j e 2πi(hxj+kyj+lzj) =fe 2πi(0)+fe 2πi(h/2+k/2)+fe 2πi(h/2+l/2)+fe 2πi(k/2+l/2) +fe 2πi(h/4+k/4+l/4)+fe 2πi(3h/4+3k/4+l/4)+fe 2πi(3h/4+k/4+3l/4)+fe 2πi(h/4+3k/4+3l/4) 前四项为面心格子的结构因子,用F F 表示,后四项可提出公因子e πi/2(h+k+l)。得: F hkl =F F +fe πi/2(h+k+l)(1+e πi (h+k) +e πi (h+l)+e πi (k+l)) = F F +F F e πi/2(h+k+l)=F F (1+ e πi/2(h+k+l)) (1) 由面心格子可知,h 、k 、l 奇偶混杂时,F F =0,F=0; (2) h 、k 、l 全为奇数,且h+k+l=2n+1时, 1+ e πi/2(h+k+l)=1+cos π/2(h+k+l)+i sin π/2(h+k+l) =1+cos π/2(2n+1)+i sin π/2(2n+1) =1+(-1)n i F=4f(1±i) F 2=16f 2(1+1)=32f (3) h 、k 、l 全为偶数,且h+k+l=4n 时 F=4f(1+e 2ni π) = 4f(1+1) = 8f (4) h 、k 、l 全为偶数,且h+k+l≠4n,即h+k+l=2(2n+1)时 F=4f(1+e (2n+1)i π)=4f(1-1)=0 对于金刚石 各原子的分数坐标为 )(,0,00, )(,021,21,),(,21,021, ),,(,21210 )(41,41,41,)(41,43,43,)(43,43,41,)(4 3,41,43 由结构因子得 )()()(0[F l k i l h i k h i hkl e e e e f ++++++=πππ ])33(2)33(2)33(2)(2l k h i l k h i l k h i l k h i e e e e ++++++++++++ππ π π =)()()(1[l k i l h i k h i e e e f ++++++πππ
金属的晶体结构
引言 金属学是研究金属及合金的成分、组织、结构与力学性能之间关系的科学。所谓力学性能主要指材料的强度、硬度和塑性。通常用来承受载荷的零件要求材料具有一定的力学性能,我们称这类材料为结构材料。与结构材料对应的另一类材料是功能材料,它一般不要求承受载荷,主要使用它的物理性能,如光、电、磁性能等。功能材料利用它对光、电、磁的敏感特性制作各类传感器。 金属学只讨论金属材料的力学性能,不涉及物理性能。 固态金属通常是晶体,金属学研究的最小结构单元是原子。原子通过不同的排列可构成各种不同的晶体结构,产生不同的性能。原子结构不是金属学研究的范畴。 第1章金属的晶体结构 1-1金属及金属键 金属的定义根据学科的不同有多种划分方法。本人倾向按结合键的性质来划分,即金属是具有金属键的一类物质。这种分类的好处是有利于解释与金属力学性能相关的现象。例如,为什么金属具有较好的塑性? 什么是金属键、离子键、共价键我们早就熟知,金属键的最大特点是无饱和性、无方向性。以后我们将会看到,正是这些特点使金属具有较好的塑性。 研究表明,固态金属通常是晶体,且其结构趋于密堆积结构。这是为什么?下面我们用双原子模型来说明。 当两个原子相距很远时,它们之间不发生作用。当它们逐渐靠近时,一个原子的原子核与另一个原子的核外电子之间将产生引力;而两原子的原子核及电子之间产生斥力。研究表明,引力是长程力,斥力是短程力,即距离较远时,引力大于斥力,表现为相互吸引。随着原子距离的减小,斥力增加的速度逐渐大于引力增加的速度。显然这样作用的结果必然存在一个平衡距离d0,此时,引力等于斥力,偏离这一距离时,都将受到一个恢复力,如P3图2。d c对应最大恢复引力,即最大结合力,它对应着金属的理论抗拉强度。 下面,我们从能量的角度来考虑系统的稳定性。在引力作用下原子移近所做的功使原子的势能降低,所以吸引能是负值。相反,排斥能是正值。吸引能
实际金属的晶体结构
第三讲实际金属的晶体结构 第三节实际金属的晶体结构 一、主要内容: 晶体缺陷的概念,研究晶体缺陷的意义,晶体缺陷的种类 点缺陷的概念、种类,点缺陷产生的原因,晶格畸变的概念,间隙原子,置换原子,晶格空位, 线缺陷的概念,线缺陷的种类,刃型位错、螺型位错的特征,正刃型位错、负刃型位错,左螺型位错、右螺型位错,混合型位错,位错周围的应力场,位错周围的晶格畸变,柏氏矢量的概念,柏氏矢量的确定、表示方法,用柏氏矢量判断位错的类型,位错密度,位错在晶体中的特性。 面缺陷的种类,晶体表面,晶界,小角度晶界,大角度晶界,亚晶界,堆垛层错,相界,晶界的特性。 二、要点: 缺陷的概念及缺陷的种类。 三、方法说明; 晶体内部的缺陷确实存在,晶体内部的缺陷对金属的性能有很大的影响甚至起着决定性的作用。应该了解晶界与相界的区别,晶界的特性。 重点概念:是晶格畸变,间隙原子,置换原子,位错,亚结构。 难点:是螺型位错,用模型讲述会更清楚。 授课内容: 一、点缺陷 点缺陷的类型及特点: 金属晶体中常见的点缺陷有:空位、间隙原子、置换原子等。 晶体中位于晶格结点上的原子并非静止不动的,而是以其平衡位置为中心作热运动。当某一瞬间,某个原子具有足够大的能量,克服周围原子对它的制约,跳出其所在的位置,使晶格中形成空结点,称空位。挤入间隙的原子叫间隙原子; 占据在原来晶格结点的异类原子叫置换原子。 1、空位 空位是一种热平衡缺陷,即在一定温度下,空位有一定的平衡浓度。空位在晶体中的位置不是固定不变的,而是不断运动变化的。空位是由原子脱离其平衡位置而形成的,脱离平衡位置的原子大致有三个去处: (1)迁移到晶体表面上,这样所产生的空位叫肖脱基空位; (2)迁移到晶格的间隙中,这样所形成的空位叫弗兰克尔空位; (3)迁移到其他空位处,这样虽然不产生新的空位,但可以使空位变换位置。 晶格畸变:由于空位的存在。其周围原子失去了一个近邻原子而使相互间的作用失去平衡,因而它们朝空位方向稍有移动,偏离其平衡位置,就会在空位周围出现一个涉及几个原子间距范围的弹性畸变区,叫晶格畸变。 2、间隙原子 处于晶格间隙中的原子即为间隙原子。在形成弗兰克尔空位的同时,也形成一个间隙原子,另外溶质原子挤入溶剂的晶格间隙中后,也称为间隙原子,他们都会造成严重的晶体畸变。间隙原子也是一种热平衡缺陷,在一定温度下有一平衡浓度,对于异类间隙原子来说,常将这一平衡浓度称为固溶度或溶解度。 3、置换原子
金刚石和石墨的晶体结构
书山有路勤为径,学海无涯苦作舟 金刚石和石墨的晶体结构 金刚石和石墨的晶体结构之一1.金刚石的晶体结构金刚石是典型的原子晶体,在这种晶体中的基本结构微粒是碳原子。每个碳原子都以sp3 杂化轨道与四个碳原子形成共价单键,键长为15.5nm,键角为109°28′,构成正四面体。每个碳原子位于正四面体的中心,周围四个碳原子位于四个顶点上,在空间构成连续的、坚固的骨架结构。因此,可以把整个晶体看成为一个巨大的分子。由于C—C 键的键能大(为347kJ/mol),价电子都参与了共价键的形成,使晶体中没有自由电子,所以金刚石是自然界中最坚硬的固体,熔点高达3550 ℃,并且不导电。2.石墨的晶体结构石墨晶体是属于混合键型的晶体。石墨中的碳原子用sp2 杂化轨道与相邻的三个碳原子以σ键结合,形成正六角形蜂巢状的平面层状结构,而每个碳原子还有一个2p 轨道,其中有一个2p 电子。这些p 轨道又都互相平行,并垂直于碳原子sp2 杂化轨道构成的平面,形成了大π键。因而这些π电子可以在整个碳原子平面上活动,类似金属键的性质。而平面结构的层与层之间则依靠分子间力(范德华力)结合起来;形成石墨晶体。石墨有金属光泽,在层平面方向有很好的导电性质。由于层间的分子间作用力弱,因此石墨晶体的层与层间容易滑动,工业上用石墨作固体润滑剂。 金刚石和石墨的晶体结构之二世界上金刚石的主要产地在非洲,近年来我国也发现了有工业开采价值的金刚石矿。金刚石也可以人工合成,它是以石墨为原料,用FeS 作溶剂,在高温高压的条件下制成的。人造金刚石在某些性能方面还胜过天然金刚石(如耐用性),在石油和地质钻探工作中已广泛采用以 金刚石制成的钻具。金刚石是物质中硬度最大的,比重平均为3.5,室温下对所有化学试剂都显惰性,在空气和氧中加热到800℃左右能燃烧生成二氧化碳,它的熔点(3570℃)是所有元素中最高的。金刚石是典型的原子晶体,
常见的金属晶体结构
第二章作业2-1 常见的金属晶体结构有哪几种?它们的原子排列和晶格常数有什么特点?V、Mg、Zn 各属何种结构?答:常见晶体结构有 3 种:⑴体心立方:-Fe、Cr、V ⑵面心立方:-Fe、Al、Cu、Ni ⑶密排六方:Mg、Zn -Fe、-Fe、Al、Cu、Ni、Cr、2---7 为何单晶体具有各向异性,而多晶体在一般情况下不显示出各向异性?答:因为单晶体内各个方向上原子排列密度不同,造成原子间结合力不同,因而表现出各向异性;而多晶体是由很多个单晶体所组成,它在各个方向上的力相互抵消平衡,因而表现各向同性。第三章作业3-2 如果其它条件相同,试比较在下列铸造条件下,所得铸件晶粒的大小;⑴金属模浇注与砂模浇注;⑵高温浇注与低温浇注;⑶铸成薄壁件与铸成厚壁件;⑷浇注时采用振动与不采用振动;⑸厚大铸件的表面部分与中心部分。答:晶粒大小:⑴金属模浇注的晶粒小⑵低温浇注的晶粒小⑶铸成薄壁件的晶粒小⑷采用振动的晶粒小⑸厚大铸件表面部分的晶粒小第四章作业4-4 在常温下为什么细晶粒金属强度高,且塑性、韧性也好?试用多晶体塑性变形的特点予以解释。答:晶粒细小而均匀,不仅常温下强度较高,而且塑性和韧性也较好,即强韧性好。原因是:(1)强度高:Hall-Petch 公式。晶界越多,越难滑移。(2)塑性好:晶粒越多,变形均匀而分散,减少应力集中。(3)韧性好:晶粒越细,晶界越曲折,裂纹越不易传播。4-6 生产中加工长的精密细杠(或轴)时,常在半精加工后,将将丝杠吊挂起来并用木锤沿全长轻击几遍在吊挂7~15 天,然后再精加工。试解释这样做的目的及其原因?答:这叫时效处理一般是在工件热处理之后进行原因用木锤轻击是为了尽快消除工件内部应力减少成品形变应力吊起来,是细长工件的一种存放形式吊个7 天,让工件释放应力的时间,轴越粗放的时间越长。4-8 钨在1000℃变形加工,锡在室温下变形加工,请说明它们是热加工还是冷加工(钨熔点是3410℃,锡熔点是232℃)?答:W、Sn 的最低再结晶温度分别为: TR(W) =(0.4~0.5)×(3410+273)-273 =(1200~1568)(℃)>1000℃ TR(Sn) =(0.4~0.5)×(232+273)-273 =(-71~-20)(℃) <25℃所以W 在1000℃时为冷加工,Sn 在室温下为热加工4-9 用下列三种方法制造齿轮,哪一种比较理想?为什么?(1)用厚钢板切出圆饼,再加工成齿轮;(2)由粗钢棒切下圆饼,再加工成齿轮;(3)由圆棒锻成圆饼,再加工成齿轮。答:齿轮的材料、加工与加工工艺有一定的原则,同时也要根据实际情况具体而定,总的原则是满足使用要求;加工便当;性价比最佳。对齿轮而言,要看是干什么用的齿轮,对于精度要求不高的,使用频率不高,强度也没什么要求的,方法1、2 都可以,用方法3 反倒是画蛇添足了。对于精密传动齿轮和高速运转齿轮及对强度和可靠性要求高的齿轮,方法3 就是合理的。经过锻造的齿坯,金属内部晶粒更加细化,内应力均匀,材料的杂质更少,相对材料的强度也有所提高,经过锻造的毛坯加工的齿轮精度稳定,强度更好。4-10 用一冷拔钢丝绳吊装一大型工件入炉,并随工件一起加热到1000℃,保温后再次吊装工件时钢丝绳发生断裂,试分析原因?答:由于冷拔钢丝在生产过程中受到挤压作用产生了加工硬化使钢丝本身具有一定的强度和硬度,那么再吊重物时才有足够的强度,当将钢丝绳和工件放置在1000℃炉内进行加热和保温后,等于对钢丝绳进行了回复和再结晶处理,所以使钢丝绳的性能大大下降,所以再吊重物时发生断裂。4-11 在室温下对铅板进行弯折,越弯越硬,而稍隔一段时间再行弯折,铅板又像最初一样柔软这是什么原因?答:铅板在室温下的加工属于热加工,加工硬化的同时伴随回复和再结晶过程。越弯越硬是由于位错大量增加而引起的加工硬化造成,而过一段时间又会变软是因为室温对于铅已经是再结晶温度以上,所以伴随着回复和再结晶过程,等轴的没有变形晶粒取代了变形晶粒,硬度和塑性又恢复到了未变形之前。第五章作业5-3 一次渗碳体、二次渗碳体、三次渗碳体、共晶渗碳体、共析渗碳体异同?答:一次渗碳体:由液相中直接析出来的渗碳体称为一次渗碳体。二次渗碳体:从 A 中析出的渗碳体称为二次渗碳体。三次渗碳体:从 F 中析出的渗碳体称为三次渗碳体共晶渗碳体:经共晶反应生成的渗碳体即莱氏体中的渗碳体称为共晶渗碳体共析渗碳体:经共
1.1.1金属的晶体结构试题
1.1.1 金属的晶体结构 (一)填空题 1.同非金属相比,金属的主要特性是导电性、导热性、塑性优良,正的电阻-温度系数2.晶体与非晶体的最根本区别是晶体中原子排列是周期性规则有序的,而非晶体中原子排列是混乱无序的 3.金属晶体中常见的点缺陷是空位和间隙原子,最主要的面缺陷是晶界。 4.位错密度是指单位体积中位错线的总长度,其数学表达式为L / V 。 5.表示晶体中原子排列形式的空间格子叫做晶格,而晶胞是指能表示晶体结构的最小的晶格。 6.在常见金属晶格中,原子排列最密的晶向,体心立方晶格是【111】,而面心立方晶格是【110】。 7 晶体在不同晶向上的性能是不同的,这就是单晶体的各向异性现象。一般结构用金 属为多晶体晶体,在各个方向上性能是相同的,这就是实际金属的伪各向同性现象。 8 实际金属存在有点缺陷、线缺陷和面缺陷三种缺陷。位错是线缺陷。实际晶体 的强度比理想晶体的强度低得多。 9.常温下使用的金属材料以细小晶粒为好。而高温下使用的金属材料在一定范围内以粗大晶粒为好。 10.金属常见的晶格类型是FCC 、BCC 、HCP 。 11.在立方晶格中,各点坐标为:A (1,0,1),B (0,1,1),C (1,1,1/2),D(1/2,1,1/2),那么AB晶向指数为<1-10> 或<-110> ,OC晶向指数为<112> ,OD晶向指数为<212> 。 12.铜是FCC 结构的金属,它的最密排面是(111) ,若铜的晶格常数a=0.36nm,那么最密排面上原子间距为。 13 α-Fe、γ-Fe、Al、Cu、Ni、Pb、Cr、V、Mg、Zn中属于体心立方晶格的有, 属于面心立方晶格的有,属于密排六方晶格的有。 14.已知Cu的原子直径为0.256nm,那么铜的晶格常数为。1mm3Cu中的原子数为。 15.晶面通过(0,0,0)、(1/2、1/4、0)和(1/2,0,1/2)三点,这个晶面的晶面指数为{001} . 16.在立方晶系中,某晶面在x轴上的截距为2,在y轴上的截距为1/2;与z轴平行,则该晶面指数为{120} . 17.金属具有良好的导电性、导热性、塑性和金属光泽主要是因为金属原子具有金属键的结合方式。 18.同素异构转变是指同一成分的金属在固态下具有不同的晶体结构。纯铁在1394C°和912C°温度发生δ-Fe —γ-Fe 和γ-Fe —α-Fe 转变。 19.在常温下铁的原子直径为0.256nm,那么铁的晶格常数为。 20.金属原子结构的特点是原子核外最外层电子数为1-3 。 21.物质的原子间结合键主要包括离子键、共价键和金属键三种。22.大部分陶瓷材料的结合键为离子键和共价键。 23.高分子材料的结合键是共价键。 (二)判断题 1.因为单晶体具有各向异性的特征,所以实际应用的金属晶体在各个方向上的性能也是不相同的。( × ) 2.金属多晶体是由许多结晶位向相同的晶粒所构成。( ×) 3.因为面心立方晶体与密排六方晶体的配位数相同,所以它们的原子排列密集程度也相同 (√) 4.体心立方晶格中最密原子面是{111}。(×) 5.金属理想晶体的强度比实际晶体的强度高得多。(√ )
