5有机溶剂苯胺高分子
苯胺结构简式

苯胺结构简式苯胺是一种有机化合物,化学式为C6H5NH2,也被称为苯基胺或氨基苯。
它是一种无色至黄色的液体,有强烈的氨味,可混溶于水和许多有机溶剂。
苯胺的分子结构可简写为C6H5-NH2。
它属于芳香胺类化合物,是苯环分子中一个氢原子被氨基取代而成的物质。
苯胺的分子结构中,苯环具有6个碳原子,它们处于平面构型,通过共振进行共同稳定。
氨基位于苯环上,和苯环上的一个碳原子相连接,氨基带有一个孤对电子。
这个孤对电子常常与其他电子或化合物发生反应,使得苯胺在化学上具有很大的反应性。
苯胺是一种很重要的化学品,广泛用于染料、药品制造、橡胶和塑料生产等领域。
在染料领域,苯胺是一种重要的中间体,可用于合成各种颜料。
在药品制造领域,苯胺是许多治疗癌症的药物的重要原料。
在橡胶和塑料生产中,苯胺可用来制造聚氨酯、聚酰胺等高分子材料。
另外,苯胺还是化学分析和检测的一种重要试剂。
它可以用于测定元素硒和铁的含量,也可以用于测定氮的量。
虽然苯胺在许多领域有着广泛的应用,但它也有一些危险性。
苯胺容易吸收到人体内,对人体健康造成潜在危害。
长期暴露于苯胺会导致肝脏、肾脏和骨髓等器官受损。
同时苯胺也是致癌物质之一,长期接触苯胺可以引起白血病和其他肿瘤疾病。
因此,在使用苯胺时,需要严格遵守安全操作规程,并采取有效的防护措施。
综合来看,苯胺是一种重要的化学品,在许多领域有广泛的应用。
了解苯胺的分子结构和化学性质有助于人们更好地掌握和应用它。
同时我们也需要注意苯胺带来的潜在危害,保护我们自身和周围环境的安全。
苯胺

1.苯胺aniline苯分子中的一个氢原子为氨基取代而生成的化合物。
分子式C6H5NH2。
是最简单的一级芳香胺。
无色油状液体。
熔点-6.3℃,沸点184℃,相对密度1.02 (20/4℃),相对分子量93.128,加热至370℃分解。
稍溶于水,易溶于乙醇、乙醚等有机溶剂。
暴露于空气中或日光下变为棕色。
可用水蒸气蒸馏,蒸馏时加入少量锌粉以防氧化。
提纯后的苯胺可加入10~15ppm的NaBH4,以防氧化变质。
2.分子结构:苯环上的C原子以sp2杂化轨道成键,N原子以sp3杂化轨道成键。
苯胺苯胺呈碱性,与酸易生成盐。
其氨基上的氢原子可被烃基或酰基取代,生成二级或三级苯胺及酰基苯胺。
当苯胺进行取代反应时,主要生成邻、对位取代产物。
苯胺与亚硝酸反应生成重氮盐,由此盐可制成一系列苯的衍生物和偶氮化合物。
3.工业上主要采用两种方法生产苯胺①由硝基苯经活性铜催化氢化制备,此法可进行连续生产,无污染。
②氯苯和氨在高温和氧化铜催化剂存在下反应得到。
苯胺是重要的化工原料,主要用于医药和橡胶硫化促进剂,也是制造树脂和涂料的原料。
苯胺对血液和神经的毒性非常强烈,可经皮肤吸收或经呼吸道引起中毒。
4.理化特性主要成分:纯品外观与性状:无色或微黄色油状液体,有强烈气味。
pH:熔点(℃):-6.2沸点(℃):184.4相对密度(水=1): 1.02相对蒸气密度(空气=1): 3.22折光率(20℃):1.5863饱和蒸气压(kPa):2.00(77℃)燃烧热(kJ/mol):3389.8临界温度(℃):425.6临界压力(MPa): 5.30辛醇/水分配系数的对数值:0.94闪点(℃):70引燃温度(℃):无资料爆炸上限%(V/V):11.0爆炸下限%(V/V): 1.3溶解性:微溶于水,溶于乙醇、乙醚、苯。
主要用途:用于染料、医药、橡胶、树脂、香料等的合成。
其它理化性质:溶解度:3.6 g/100 mL,20 °C5.稳定性和反应活性稳定性:极易被空气中的氧气氧化。
苯胺

第一章文献综述1.1 引言苯胺是重要的有机化工原料之一[1],广泛的应用于有机化工原料和化工生产工业,制得的化工产品和中间体有三百多种,在燃料、医药、农药、炸药、香料、橡胶硫化促进剂等行业具有广泛的应用,开发利用前景十分广泛,尤其是作为生产聚氨脂产品主要原料MDI(二苯基甲基二异氰酸脂)的重要原料,今年MDI的快速发展,使苯胺需求增长很快。
故苯胺具有很大的市场潜力。
此外,苯胺还可以用作溶剂和其他化工原料,开发利用前景十分广阔。
1.2 苯胺的性质苯胺无色至浅黄色透明液体,在空气中氧的影响下,在光的照射或高温下,苯胺易被氧化:无色-黄色-棕色-黑色。
其相对密度1.02,凝固点-6.2 ℃,沸点184.4 ℃,自燃点:620 ℃(空气中) 530 ℃(氧气中)。
蒸汽压133.3 Pa(34.8 ℃),蒸汽相对密度3.22。
呈弱碱性,常温下微溶于水,与醇,醚,苯等多种有机溶剂混溶。
苯胺俗称阿尼林油,是重要的有机化工原料。
纯苯胺为无色透明油状液体,暴露空气中或见光会逐渐变成棕色。
因此在储存和运输苯胺的时候常常采用氮气作为保护气。
苯胺能随水蒸气挥发,能与醇、醚、苯、硝基苯及其他多种有机溶剂混溶。
苯胺有很强的毒性,能渗透皮肤至血液,口服15滴致死。
生产过程中废水、废气和废渣中苯胺的含量都有相应的标准,应严格控制三废中苯胺含量1.3 苯胺的用途苯胺是一种基本的有机化工原料。
据不完全统计,以苯胺为原料可以制造合成300多种产品和中间体,在许多领域中具有广泛的应用[2]。
1)应用于生产异氰酸脂(MDI),MDI主要用于制人造革、聚氨酯软质或硬质泡沫塑料(主要用于家具、汽车、建筑及冰箱等工业绝缘保温材料)。
2)应用于生产橡胶助剂,在橡胶行业,主要是用于生产防老剂如RD、4010-NA,促进剂如M和DM等,另外可用于橡胶抗氧剂、抗臭氧剂、硫化剂、稳定剂及活性剂等。
3)在染料及医药、农药、等方面的应用,染料行业消耗苯胺量主要有染料和碱性染料。
有机胺
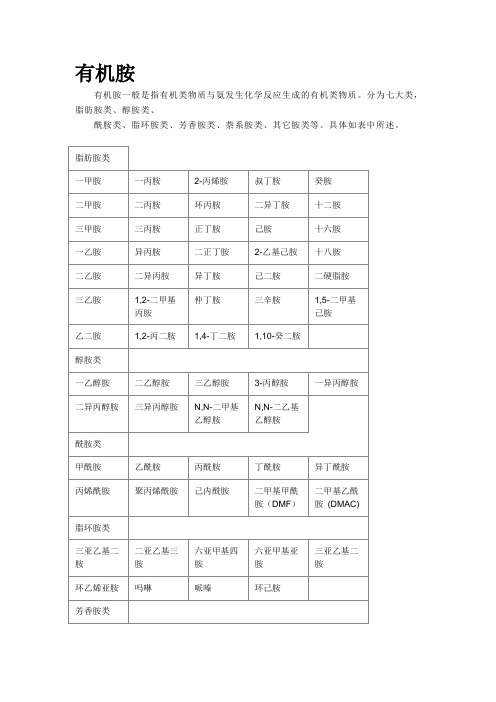
有机胺有机胺一般是指有机类物质与氨发生化学反应生成的有机类物质。
分为七大类,脂肪胺类、醇胺类、酰胺类、脂环胺类、芳香胺类、萘系胺类、其它胺类等。
具体如表中所述。
聚乙烯亚胺羟胺絮凝剂理论基础是;“聚并”理论,絮凝剂主要是带有正电(负)性的基团中和一些水中带有负(正)电性难于分离的一些粒子或者叫颗粒,降低其电势,使其处于不稳定状态,并利用其聚合性质使得这些颗粒,集中,并通过物理或者化学方法分离出来。
一般为达到这种目的而使用的药剂,称之为絮凝剂。
絮凝剂主要应用于给水各污水处理领域。
絮凝剂按照其化学成分总体可分为无机絮凝剂和有机絮凝剂两类。
其中无机絮凝剂又包括无机凝聚剂和无机高分子絮凝剂;有机絮凝剂又包括合成有机高分子絮凝剂、天然有机高分子絮凝剂和微生物絮凝剂。
[编辑本段]无机絮凝剂按其分子量的大小可分为低分子絮凝剂和高分子絮凝剂两大类。
低分子絮凝剂价格低、货源充足、但因其用量大、残渣多、效果差,故无机絮凝剂的发展已经基本上完成了低分子向高分子的转变。
现常用的无机高分子絮凝剂有聚合铝类絮凝剂、聚合铁类絮凝剂和活性硅酸类絮凝剂以及复合絮凝剂四大类。
(1)聚合铝类絮凝剂(如聚合氯化铝,硫酸铝等)聚合铝水解产生高价离子,形成各种类型的羟基多核络合物。
它们通过羰基式桥联作用,处于亚稳定状态。
而OH-与Al3+的比值[2](一般称盐基度或碱基度)对絮凝效果影响很大。
通常盐基度越高,絮凝效果越强,但过高则本身易生成难溶的氢氧化铝沉淀,导致絮凝效果降低。
研究表明,盐基度在75%-85%时最佳,此时絮凝体产生快,颗粒大而重,沉淀性能好。
聚合铝具有投药量少、沉降速度快、颗粒密实、除浊、除色效果明显等特点。
在工业水处理中得到广泛的应用[3]。
值得注意的是铝,尤其是活性铝,毒性较大,同时聚合铝制备方法不完善,致使较多水解铝的微细颗粒存在于溶液中,这在一定程度上限制了聚合铝的使用。
通过改善混凝反应条件,延长慢速混凝时间,能有效降低水中铝的含量。
常用有机溶剂分类

常用有机溶剂分类第一类溶剂是指已知可以致癌并被强烈怀疑对人和环境有害的溶剂。
在可能的情况下,应避免使用这类溶剂。
如果在生产治疗价值较大的药品时不可避免地使用了这类溶剂,除非能证明其合理性,残留量必须控制在规定的范围内,如:苯(2ppm)、四氯化碳(4ppm)、1,2-二氯乙烷(5ppm)、1,1-二氯乙烷(8ppm)、1,1,1-三氯乙烷(1500ppm)。
第二类溶剂是指无基因毒性但有动物致癌性的溶剂。
按每日用药10克计算的每日允许接触量如下:2-甲氧基乙醇(50ppm)、氯仿(60ppm)、1,1,2-三氯乙烯(80ppm)、1,2-二甲氧基乙烷(100ppm)、1,2,3,4-四氢化萘(100ppm)、2-乙氧基乙醇(160ppm)、环丁砜(160ppm)、嘧啶(200ppm)、甲酰胺(220ppm)、正己烷(290ppm)、氯苯(360ppm)、二氧杂环己烷(380ppm)、乙腈(410ppm)、二氯甲烷(600ppm)、乙烯基乙二醇(620ppm)、N,N-二甲基甲酰胺(880ppm)、甲苯(890ppm)、N,N-二甲基乙酰胺(1090ppm)、甲基环己烷(1180ppm)、1,2-二氯乙烯(1870ppm)、二甲苯(2170ppm)、甲醇(3000ppm)、环己烷(3880ppm)、N-甲基吡咯烷酮(4840ppm)、。
第三类溶剂是指对人体低毒的溶剂。
急性或短期研究显示,这些溶剂毒性较低,基因毒性研究结果呈阴性,但尚无这些溶剂的长期毒性或致癌性的数据。
在无需论证的情况下,残留溶剂的量不高于0.5%是可接受的,但高于此值则须证明其合理性。
这类溶剂包括:戊烷、甲酸、乙酸、乙醚、丙酮、苯甲醚、1-丙醇、2-丙醇、1-丁醇、2-丁醇、戊醇、乙酸丁酯、三丁甲基乙醚、乙酸异丙酯、甲乙酮、二甲亚砜、异丙基苯、乙酸乙酯、甲酸乙酯、乙酸异丁酯、乙酸甲酯、3-甲基-1-丁醇、甲基异丁酮、2-甲基-1-丙醇、乙酸丙酯。
常见有机溶剂的性质大全

溶剂的定义溶剂(solvent)这个词广义指在均匀的混合物中含有的一种过量存在的组分。
狭义地说,在化学组成上不发生任何变化并能溶解其他物质(一般指固体)的液体,或者与固体发生化学反应并将固体溶解的液体。
溶解生成的均匀混合物体系称为溶液。
在溶液中过量的成分叫溶剂;量少的成分叫溶质。
溶剂也称为溶媒,即含有溶解溶质的媒质之意。
但是在工业上所说的溶剂一般是指能够溶解油脂、蜡、树脂(这一类物质多数在水中不溶解)而形成均匀溶液的单一化合物或者两种以上组成的混合物。
这类除水之外的溶剂称为非水溶剂或有机溶剂,水、液氨、液态金属、无机气体等则称为无机溶剂。
溶解现象溶解本来表示固体或气体物质与液体物质相混合,同时以分子状态均匀分散的一种过程。
事实上在多数情况下是描述液体状态的一些物质之间的混合,金与铜、铜与镍等许多金属以原子状态相混合的所谓合金也应看成是一种溶解现象。
所以严格地说,只要是两种以上的物质相混合组成一个相的过程就可以称为溶解,生成的相称为溶液。
一般在一个相中应呈均匀状态,其构成成分的物质可以以分子状态或原子状态相互混合。
溶解过程比较复杂,有的物质在溶剂中可以以任何比例进行溶解,有的部分溶解,有的则不溶。
这些现象是怎样发生的,其影响的因素很多,一般认为与溶解过程有关的因素大致有以下几个方面:⑴相同分子或原子间的引力与不同分子或原子间的引力的相互关系(主要是范德华引力);⑵分子的极性引起的分子缔合程度;⑶分子复合物的生成;⑷溶剂化作用;⑸溶剂、溶质的相对分子质量;⑹溶解活性基团的种类和数目。
化学组成类似的物质相互容易溶解,极性溶剂容易溶解极性物质,非极性溶剂容易溶解非极性物质。
例如,水、甲醇和乙醇彼此之间可以互溶;苯、甲苯和乙醚之间也容易互溶,但水与苯,甲醇与苯则不能自由混溶。
而且在水或甲醇中易溶的物质难溶于苯或乙醚;反之在苯或乙醚中易溶的却难溶于水或甲醇。
这些现象可以用分子的极性或者分子缔合程度大小进行判断。
有机溶剂极性大小

首先,在分子结构中原子排列不对称,正负电荷的重心没有重合,这种分子就叫极性分子,由极性分子构成的污染物就叫极性污染物,反之亦然。
常见的极性污染物如:有机酸、无机酸、盐类、碱类、污水、手汗、电镀残液、焊接活化剂等。
常见的非极性污染物如:润滑油、防锈油、机油、淬火油、蜡、脂等。
常见的极性溶剂如:水、甲醇、乙醇、异丙醇、丙酮、环己酮、乙二胺、乙二醇等。
常见的非极性溶剂如:CFC-113、四氯化碳、己烷、庚烷、辛烷、苯、汽油、煤油等。
极性溶剂比较容易溶解极性污染物,反之亦然。
KB值:贝松脂丁醇值,也叫考里丁醇值用来度量有机溶剂溶解非极性污染物的相对能力,值越大,溶解能力越强。
SP值:溶解度参数表示溶剂与溶质(污染物)之间相互作用的一个参数,两者的SP值越接近表示越容易溶解有机试剂极性大小下面这份溶剂极性表列出了常用有机溶剂极性顺序,并有常见溶剂的粘度、沸点、吸收波长等物理参数,在进行薄层色谱柱(TLC)洗脱的时候时很有帮助。
可能有不准确的,希望在留言处给予更正。
化合物名称极性粘度沸点吸收波长i-pentane(异戊烷) 0 - 30 -n-pentane(正戊烷) 0 0.23 36 210 Petroleum ether(石油醚) 0.01 0.3 30~60 210 Hexane(己烷) 0.06 0.33 69 210 Cyclohexane(环己烷) 0.1 1 81 210 Isooctane(异辛烷) 0.1 0.53 99 210 Trifluoroacetic acid(三氟乙酸) 0.1 - 72 - Trimethylpentane(三甲基戊烷) 0.1 0.47 99 215 Cyclopentane(环戊烷) 0.2 0.47 49 210 n-heptane(庚烷) 0.2 0.41 98 200 Butyl chloride(丁基氯; 丁酰氯) 1 0.46 78 220 Trichloroethylene(三氯乙烯; 乙炔化三氯) 1 0.57 87 273 Carbon tetrachloride(四氯化碳) 1.6 0.97 77 265 Trichlorotrifluoroethane(三氯三氟代乙烷) 1.9 0.71 48 231 i-propyl ether(丙基醚; 丙醚) 2.4 0.37 68 220T oluene(甲苯) 2.4 0.59 111 285p-xylene(对二甲苯) 2.5 0.65 138 290 Chlorobenzene(氯苯) 2.7 0.8 132 -o-dichlorobenzene(邻二氯苯) 2.7 1.33 180 295Ethyl ether(二乙醚; 醚) 2.9 0.23 35 220Benzene(苯) 3 0.65 80 280Isobutyl alcohol(异丁醇) 3 4.7 108 220 Methylene chloride(二氯甲烷) 3.4 0.44 240 245Ethylene dichloride(二氯化乙烯) 3.5 0.78 84 228n-butanol(正丁醇) 3.7 2.95 117 210n-butyl acetate(醋酸丁酯;乙酸丁酯) 4 - 126 254n-propanol(丙醇) 4 2.27 98 210Methyl isobutyl ketone(甲基异丁酮) 4.2 - 119 330T etrahydrofuran(四氢呋喃) 4.2 0.55 66 220Ethyl acetate(乙酸乙酯) 4.30 0.45 77 260i-propanol(异丙醇) 4.3 2.37 82 210 Chloroform(氯仿) 4.4 0.57 61 245Methyl ethyl ketone(甲基乙基酮) 4.5 0.43 80 330Dioxane(二恶烷; 二氧六环; 二氧杂环己烷) 4.8 1.54 102 220Pyridine(吡啶) 5.3 0.97 115 305Acetone(丙酮) 5.4 0.32 57 330 Nitromethane(硝基甲烷) 6 0.67 101 330Acetic acid(乙酸) 6.2 1.28 118 230 Acetonitrile(乙腈) 6.2 0.37 82 210Aniline(苯胺) 6.3 4.4 184 -Dimethyl formamide(二甲基甲酰胺) 6.4 0.92 153 270 Methanol(甲醇) 6.6 0.6 65 210Ethylene glycol(乙二醇) 6.9 19.9 197 210Dimethyl sulfoxide(二甲亚砜DMSO) 7.2 2.24 189 268Water(水)10.2 1 100 268下图是混合有机溶剂极性顺序(由小到大,括号内表示的是混合比例)一:溶剂极性参数表,方便以下比较展开剂。
苯胺和铜离子络合-概述说明以及解释

苯胺和铜离子络合-概述说明以及解释1.引言概述部分的内容可以从以下角度进行阐述:1.1 概述苯胺和铜离子络合是一种重要的化学反应,它在有机合成和配位化学中具有广泛的应用。
苯胺是一种重要的有机化学原料,常用于染料、药物和高分子材料的合成等领域。
而铜离子作为过渡金属离子,在生命科学、化学催化和材料科学中也有广泛的应用。
苯胺和铜离子的络合反应是指在适当的条件下,苯胺分子中的氨基(nh2)与铜离子结合形成配位化合物的过程。
这种络合反应具有很高的选择性和反应活性,不仅可以产生新的有机-金属化合物,还可以更好地改变苯胺分子的物化性质。
苯胺和铜离子络合反应的研究已经取得了很多重要的成果。
研究人员通过实验和理论计算等手段,揭示了苯胺和铜离子络合反应的机理、反应条件和产物结构等方面的信息。
这些研究结果为进一步发展苯胺和铜离子络合反应的应用提供了重要的理论基础和实验依据。
据了解,苯胺和铜离子络合反应具有很大的潜力和应用价值。
通过合理设计反应体系,可以进一步优化反应条件和提高反应选择性,从而实现对目标产物的高效合成。
此外,苯胺和铜离子络合反应还可以用于杂化材料、药物合成、金属有机催化等领域,具有广阔的发展空间。
本文旨在对苯胺和铜离子络合反应进行全面深入地探讨,包括其反应机理、影响因素、应用前景等方面的内容。
通过对相关研究的梳理和分析,旨在为进一步开展与苯胺和铜离子络合反应相关的科学研究和应用开发提供一定的借鉴和指导。
1.2 文章结构文章结构是指文章在整体上的组织架构和布局。
一个清晰、合理的文章结构可以帮助读者更好地理解和把握文章的主旨内容。
本文的结构主要分为引言、正文和结论三个部分。
引言部分主要对文章的研究背景和目的进行介绍,引起读者的兴趣。
在引言的基础上,本文选择了以下几个方面来展开论述。
首先,在正文的第一部分(2.1)中,将介绍苯胺的性质和应用。
苯胺是一种重要的有机化合物,具有广泛的应用价值,例如用作染料、药物、塑料等领域。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
②骨髓象 正常骨髓象 局灶增生型骨髓象 再生不良或再生障碍骨髓象 生成↓—各系有核细胞数↓ 形态异常—毒性颗粒/空泡/核质疏松/核浆发育 不平衡/破碎细胞↑/分叶增多 释放障碍—分叶中性粒细胞↑
第五节 有机溶剂中毒 四、二氯乙烷
一.理化特性 1.氯仿样味 加热分解产生光气 2.两种异构体,对称体属高毒类,不对称体属微毒类
二.接触机会 化工合成、溶剂、粘合剂、脱脂剂、萃取剂等
三.毒理 1.吸收 呼吸道、消化道
2.代谢 微粒体氧化产物/原形与GSH结合→环硫化离子 →DNA、RNA等加合物
4.生物转化与排出 生物转化 代谢速率差异(化学结构、个体酶活性) 代谢产物 毒效应
排出 生物半衰期较短 生物蓄积不明显 原形 呼出气排出(多数) 代谢物 尿排出(少数) 胎盘转运、乳汁排出
二.有机溶剂对健康影响 1.皮肤 溶剂皮炎 过敏性接触性皮炎 剥脱性皮炎
2.中枢神经系统 麻醉作用 行为障碍
苯中毒怎样治疗?
1.急性中毒 ①一般措施 转移 去污染 保暖 呼吸道通畅 吸氧 ②静脉注射葡萄糖醛酸、维生素C,促进毒物排出 ③忌用肾上腺素 心肌对内源性肾上腺素敏感性增强,易致室颤猝死
2.慢性中毒 恢复造血功能 —治疗原则与普通内科治疗造血抑制疾病的相同 皮质激素/丙酸睾丸酮/维生素/核苷酸类/升WBC药等 积极对症治疗
酚类化合物与硫酸盐或葡萄糖醛酸结合随尿排出
尿酚含量反映近期苯吸收情况
>10mg/L 班中、班后2h内采样 其它代谢途径(略)
4.排出 50%由呼出气排出 测定呼出气中苯含量可反映接触苯的程度
5.毒作用机制 急性毒作用主要表现为对中枢神经系统的麻醉作用 慢性毒作用主要表现为对造血系统的损害 多认为是酚类代谢产物所致
一.理化特性 易挥发 醚味或烂萝卜味 二.接触机会 粘胶纤维生产 玻璃纸和CCl4制造、橡胶硫化、谷物熏蒸等
三.毒理 1.吸收 呼吸道 2.分布 血液、神经系统、肾脏、脾脏等
3.代谢 70%~90%代谢转化 特异性代谢产物TTCA(与CS2浓度相关性好,生物 学监测指标)
4.排出 呼气排出 代谢产物随尿排出 5.毒作用机制 不十分清楚 ①络合金属离子 ②维生素B6代谢障碍 ③蛋白质共价交联 ④影响儿茶酚胺代谢
七.预防 1.CS2 PC-TWA 5mg/m3;PC-STEL 10mg/m3 2.密闭通风 3.环境监测 4.健康监护等
第六节 苯的氨基和硝基化合物中毒 一、概述
一.化学结构与理化特性 1.化学结构 苯或其同系物(如甲苯、二甲苯、酚)苯环上的氢原 子被一个或几个氨基(-NH2)或硝基(-NO2),或同 时还被卤素或烷基取代而形成的一类芳香族氨基或硝基 化合物
个体遗传易感性如毒物代谢酶基因多态、DNA修复基因 多态等有关
苯中毒有哪些表现?
1.急性中毒 先兴奋(苯醉) 粘膜刺激症状、皮肤潮红、兴奋、欣快感、眩晕等
后抑制 恶心、呕吐、步态不稳、意识障碍等 昏迷、抽搐、谵妄、血压下降 呼吸和循环功能衰竭 死亡
呼气苯、血苯、尿酚↑,SGPT↑、WBC轻↑
2.慢性中毒 #中毒性神经衰弱样症状/植物神经功能紊乱
苯中毒误诊误治实例: 患者,男,21岁,临时工。因意识不清伴恶心、呕吐, 四肢抽搐半小时入院。雇主代述,2小时前患者等3人一 起清理塑料拖鞋仓库,此后进食青菜等,出现头晕、恶 心、呕吐、手足发麻,发音困难,继而意识不清、尿失 禁。体查: T36℃, P102次/min, R24次/min, BP14/8kPa。昏迷状,双侧瞳孔等大等圆,对光反射迟 钝,颜面苍白,口唇发绀。双肺散在细湿罗音,心音有 力,肝、脾不大。双下肢肌张力增高,生理反射减弱。 实验室检测:WBC 3.4×109/L,N:0.63,L:0.37;尿 隐血试验(++);天冬氨酸转氨酶639nmol/L,胆碱酯酶 75U,血电解质正常。考虑有机磷中毒,予以吸氧、阿 托品、解磷定注射液等治疗,病情恶化,于次日死亡。 死亡后对呕吐物及残余毒物定性分析,否定有机磷中毒。 后经检测塑料拖鞋仓库内苯蒸气浓度高达160mg/m3, 认定为急性苯中毒。
8.血液 苯致再障、白血病 乙二醇、醚类致溶贫、再障
9.致癌 苯致急、慢性白血病
肯定的人类致癌物
10.生殖系统 通过胎盘屏障、血睾屏障 CS2对女性生殖功能影响、对胎儿神经系统发育影响
第五节 有机溶剂中毒 二、苯
接触苯的作业有哪些?
1.稀释剂—喷漆 粘合剂—皮革制品 溶 剂—制药、有机合成(树脂)、印刷(油墨) 萃取剂—生药的浸渍、提取、重结晶 苯易挥发,脂溶性,有机互溶
3.代谢 肝微粒体细胞色素P450氧化酶系,生成多种代谢产物 甲苯减慢其代谢,丙酮、甲基乙酮和异丙醇则相反
4.排出 代谢产物随尿排出 5.毒作用机制 未完全阐明 多系统影响
代谢产物2,5-己二酮
四.临床表现 1.急性中毒 眼、上呼吸道刺激及麻醉症状 胃肠道刺激(经口摄入) 中枢性呼吸抑制
2.慢性中毒 神经系统 多发性周围神经病变 视觉和记忆功能缺损 帕金森病(纹状体多巴胺系统和葡萄糖代谢异常)
七.预防 1.完善管理,严禁用正己烷洗手 2. PC-TWA 100mg/m3,PC-STEL 180mg/m3 3.生物监测指标 尿2-己醇(0.2mg/g Cr) 2,5-己二酮(5.3mg/gCr) 血正己烷(150μg/L) 呼出气正己烷(180mg/m3)
第五节 有机溶剂中毒 六、二硫化碳
一经确诊,即应调离苯作业
苯中毒怎样预防?
1.严格管理,控制外流 2.改革工艺、通风排毒 密闭化、自动化和程序化 3.取代苯 汽油、甲苯、二甲苯等作稀释剂或粘胶剂 乙醇等作萃取剂 4.卫生保健措施 环境监测、生物监测、健康监护、个人防护 5. PC-TWA 6mg/m3,PC-STEL 10mg/m3 6.职业禁忌症 血象指标低于或接近正常值下限者,血液病,皮肤病, 月经过多或功能性子宫出血
七.预防 1.毒物替代 205胶代替3435胶,余同前
2. PC-TWA 7mg/m3,PC-STEL 15mg/m3 3.职业禁忌症 神经系统器质性疾病,精神病,肝、肾器质性疾病, 全身性皮肤疾病
第五节 有机溶剂中毒 五、正己烷
一.理化特性 微臭 易挥发 二.接触机会 溶剂 制造胶水、清漆、粘合剂 三.毒理 1.吸收 呼吸道 2.分布 血液、神经系统、肾脏、脾脏等
②心血管系统 高浓度接触冠心病死亡率增高 长期低浓度接触引起心血管系统损害?
③视觉系统 眼底出血、渗出、视神经萎缩、微动脉瘤、血管硬化 及色觉、暗适应等改变 低浓度接触仍有眼部病变(早期检测指标) ④其它 生殖、消化、内分泌等
五.诊断 《GBZ4-2002职业性慢性二硫化碳中毒诊断标准》 六.处理原则 无特效解毒药,对症治疗、支持疗法 观察对象 复查神经-肌电图 中毒确诊者 调离
第五节 有机溶剂中毒 三、甲苯、二甲苯
一.理化特性与接触机会 易挥发
化工中间体 溶剂或稀释剂—苯的替代物 喷漆/皮革/橡胶/汽油掺合剂等 二.体内过程 1.吸收 呼吸道 2.分布 脂肪、肾上腺、骨髓、脑
3.代谢 甲苯→苯甲酸→马尿酸→随尿排出 ↓葡萄糖醛酸↗
二甲苯→甲基苯甲酸等→甲基马尿酸→随尿排出 4.排出 代谢产物随尿排出 呼吸道(少量)
2.慢性中毒 神衰综合征 呼吸道刺激及肝、肾损害
3.致癌、致畸、致突变作用 体外遗传毒性 动物致癌物 人群致癌不肯定 致畸作用不明显
五.诊断
《GBZ39-2002职业性急性1,2-二氯乙烷中毒诊断标准》
六.处理原则 1.急性中毒 转移 去污染 保暖 观察 对症治疗 防治中毒性脑病为重点 2.慢性中毒 无特效解毒剂 对症治疗
3.周围神经 特异毒性 肢端末梢神经炎(CS2、正己烷等) 三叉神经麻痹(三氯乙烯) 非特异毒性 4.呼吸系统 呼吸道刺激作用、急性肺水肿 慢性支气管炎
5.心脏 室颤、猝死(心肌对内源性肾上腺素的敏感性增强)
6.肝脏 肝毒性明显(含卤素或硝基) CCl4 急性肝损害、慢性肝硬化
7.肾脏 急性肾小管坏死性肾衰(CCl4) 慢性肾功能不全(蛋白尿)
5.毒作用机制 CNS麻醉作用 眼睛、呼吸道、皮肤刺激作用(较苯强)
三.临床表现 急性中毒—CNS麻醉作用 + 皮肤粘膜刺激作用 慢性中毒—神经衰弱综合征 + 慢性皮炎/皮肤皲裂 纯甲苯、二甲苯对血液系统无明显影响
四.诊断 《GBZ16-2002职业性急性甲苯中毒诊断标准》
五.处理原则 急性中毒 转移 去污染 对症治疗 慢性中毒 对症治疗 六.预防 PC-TWA 50mg/m3,PC-STEL 100mg/m3,余同苯 职业禁忌症 神经系统器质性疾病,神经衰弱综合征,肝脏疾病
心血管系统 心律不齐,室颤,心肌胞内镁和钾离子水平降低 生殖系统 精子形成障碍,血清卵泡刺激素或睾丸酮水平正常 免疫系统 IgG、IgM、IgA抑制,且与尿2,5-己二酮明显相关
五.诊断 《GBZ84-2002职业性慢性正己烷中毒诊断标准》
六.处理原则 1.急性中毒 转移 去污染 对症处理 2.慢性中毒 调离 对症和支持治疗(多发性周围神经病变)
苯致血液系统毒性机制未完全阐明(简) ①氢醌与纺锤体纤维蛋白结合,抑制造血细胞核分裂 ②干扰细胞因子对造血干细胞生长和分化的调节作用 IL-1↓ IL-2↓ /TNF-α↑ ③代谢物与DNA共价结合/活性氧对DNA氧化损伤→突 变、染色体损伤→再障或急性髓性白血病 ④癌基因(ras、c-fos、c-myc)激活
2.苯原料—生产酚/合成塑料/纤维/洗涤剂/药物/农药/ 炸药
3.苯制造—石油裂解/煤焦油分馏
4.苯燃料
空气苯是怎样引起人体中毒的?
