高中化学常见气体的制取装置图和方程式92124
高中化学常见气体的制取装置图和方程式
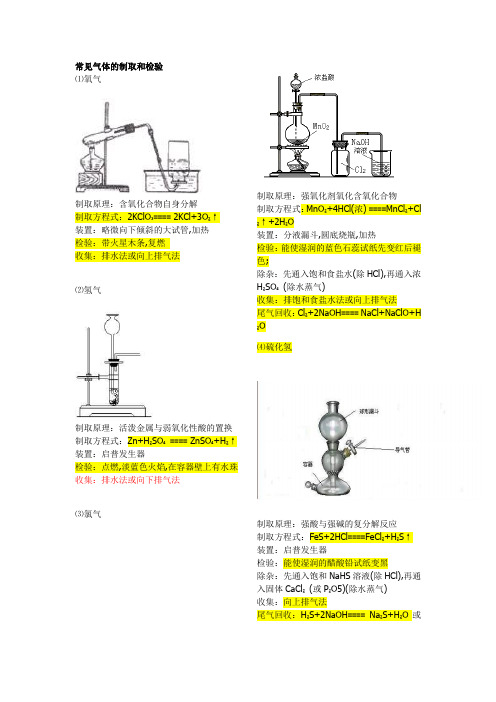
常见气体的制取和检验 ⑴氧气制取原理:含氧化合物自身分解制取方程式:2KClO ₃==== 2KCl+3O ₂↑ 装置:略微向下倾斜的大试管,加热 检验:带火星木条,复燃 收集:排水法或向上排气法⑵氢气制取原理:活泼金属与弱氧化性酸的置换 制取方程式:Zn+H ₂SO ₄ ==== ZnSO ₄+H ₂↑ 装置:启普发生器检验:点燃,淡蓝色火焰,在容器壁上有水珠收集:排水法或向下排气法 ⑶氯气制取原理:强氧化剂氧化含氧化合物 制取方程式:MnO ₂+4HCl(浓) ====MnCl ₂+Cl ₂↑+2H ₂O装置:分液漏斗,圆底烧瓶,加热 检验:能使湿润的蓝色石蕊试纸先变红后褪色;除杂:先通入饱和食盐水(除HCl),再通入浓H ₂SO ₄ (除水蒸气)收集:排饱和食盐水法或向上排气法 尾气回收:Cl ₂+2NaOH ==== NaCl+NaClO+H ₂O ⑷硫化氢制取原理:强酸与强碱的复分解反应 制取方程式:FeS+2HCl ====FeCl ₂+H ₂S ↑ 装置:启普发生器检验:能使湿润的醋酸铅试纸变黑除杂:先通入饱和NaHS 溶液(除HCl),再通入固体CaCl ₂ (或P ₂O5)(除水蒸气) 收集:向上排气法尾气回收:H ₂S+2NaOH ==== Na ₂S+H ₂O 或H₂S+NaOH==== NaHS+H₂O ⑸二氧化硫制取原理:稳定性强酸与不稳定性弱酸盐的复分解制取方程式:Na₂SO₃+H₂SO₄====Na₂SO₄+SO₂↑+H₂O装置:分液漏斗,圆底烧瓶检验:先通入品红试液,褪色,后加热又恢复原红色;除杂:通入浓H₂SO₄(除水蒸气)收集:向上排气法尾气回收:SO₂+2NaOH==== Na₂SO₃+H₂O⑹二氧化碳制取原理;稳定性强酸与不稳定性弱酸盐的复分解制取方程式:CaCO₃+2HCl====CaCl₂+CO₂↑+H₂O装置:启普发生器检验:通入澄清石灰水,变浑浊除杂:通入饱和NaHCO₃溶液(除HCl),再通入浓H₂SO₄(除水蒸气) 收集:排水法或向上排气法⑺氨气制取原理:固体铵盐与固体强碱的复分解制取方程式:Ca(OH)₂+2NH₄Cl====CaCl₂+NH₃↑+2H₂O 装置:略微向下倾斜的大试管,加热检验:湿润的红色石蕊试纸,变蓝除杂:通入碱石灰(除水蒸气)收集:向下排气法⑻氯化氢制取原理:高沸点酸与金属氯化物的复分解制取方程式:NaCl+H₂SO₄====Na₂SO₄+2HCl ↑装置:分液漏斗,圆底烧瓶,加热检验:通入AgNO₃溶液,产生白色沉淀,再加稀HNO₃沉淀不溶除杂:通入浓硫酸(除水蒸气)收集:向上排气法⑼二氧化氮制取原理:不活泼金属与浓硝酸的氧化—还原;制取方程式:Cu+4HNO ₃(浓)====Cu(NO ₃) ₂+2NO ₂↑+2H ₂O 装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:红棕色气体,通入AgNO3溶液颜色变浅,但无沉淀生成 收集:向上排气法尾气处理:3NO ₂+H ₂O ====2HNO ₃+NO NO+NO ₂+2NaOH ====2NaNO ₂+H ₂O⑽一氧化氮制取原理:不活泼金属与稀硝酸的氧化—还原;制取方程式:Cu+8HNO ₃ (稀) ====3Cu(NO ₃) ₂+2NO ↑+4H ₂O 装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:无色气体,暴露于空气中立即变红棕色收集:排水法⑾一氧化碳制取原理:浓硫酸对有机物的脱水作用 在蒸馏烧瓶里加入浓硫酸,在分液漏斗里盛放甲酸制取方程式:HCOOH ====CO ↑+H ₂O 装置:分液漏斗,圆底烧瓶检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊除杂:通入浓硫酸(除水蒸气) 收集:排水法。
常见气体制备装置归纳

图15
图16
图17
Hale Waihona Puke 二、气体净化装置: 气体净化装置: 根据净化剂的状态和条件选择
三、气体的干燥
液态干燥剂
装 置 常见干燥 剂 可干燥 气体 不可干燥 气体 洗气瓶 长进短出) (长进短出)
固态干燥剂
干燥管 大进小出) (大进小出)
浓硫酸
H2,O2,Cl2SO2, CO,N2,CH4 H2S,NH3,HBr ,HI,C2H4
图2
图3
图4
图5
图6
(4)启普发生器及简易装置 )
图7
图8
图9
图10
图11
图12
3、固体+液体或液体 液体加热制气体 、固体 液体或液体 液体或液体+液体加热制气体
①反应容器:试管、烧瓶 反应容器:试管、 ②加液容器:分液漏斗 加液容器: ③注意事项:见图16、17 注意事项:见图 、
图13
图14
• • • 溶液吸收 点燃 充袋法
易溶于水的要 用防倒吸装置
饱 和 食 盐 水
无水CaCl2
O2,Cl2,HCl,SO2, H2, CO,N2,CH4 NH3
碱石灰
H2,O2,N2, CH4,NH3 HX,H2S,SO2, CO2,NO2, Cl2
四、气体收集装置
根据气体的密度和溶解性选择
1. 排空气法
图18
图19
图20
图21 图22
图23
2.排水法 排水法
五、尾气处理装置 根据多余气体的性质选择
中学化学实验中 常见气体制备装置归纳
一、气体发生装置:根据反应物状 气体发生装置: 态及反应条件选择发生装置
1、固体加热制气体 、 反应容器:试管 反应容器: 注意事项:粉末状固 注意事项: 体应在试管口放一团 棉花
常见气体的制备有装置图

Δ
浓H2SO4
CH2=CH2↑+H2O
14. CO
HCOOH
浓H2SO4
CO ↑ +H2O
气体制取装置的设计
1、装置连接顺序
发生 装置 净化 装置 干燥 装置 收集 装置 吸收 装置
及反 反应 应物 条状 件态
的气 性体 质及 杂 质
选气 择体 干的 燥性 剂质
及气 密体 度水 溶 性
选气 择体 吸的 收毒 剂性
(3)燃烧或袋装处理法
如: CH4 、 C2H4 、 C2H2 、 H2、CO等。
防倒吸吸收
标准装置
安全瓶装置
5、气体性质实验装置
• 5.1 装置分类
• (1)常温反应装置
• (2)加热反应装置
• (3)冷却反应装置
6、排水量气装置
标准 装置
注意事项: 左端水位与右 端水位相平
注意事项:
变化 装置
标准装置
1.2.3 固+液
启普发生器变化:
1.2.3 固+液
简易启普发生器:
1.2.3 固+液
其它装置:
2、气体的净化装置
• 2.1 除杂装置
– (1)洗气瓶 – (2)干燥管 – (3)加热管
c d
• 2.2 干燥装置
• 2.2.1 干燥装置
– (1)洗气瓶 – (2)干燥管
干燥剂的选择及使用原则
1、选择原则
①气体在被干燥的过程中要不能被减少 ②不要引入新的杂质。
2、选择方法
酸、碱性 据气体的 氧化、还原性
集装置
• 3.1 判断原则
– (1)易溶或与水反应的气体: 排空气法 – (2)与空气成分反应或与空气密度相近的气体: – 排水(液)法 – (3)可溶性气体考虑用 – 排液法 – (4)两种方法皆可用时,排水法收集的气体较纯。
高中化学常见气体的制取装置图和方程式模板
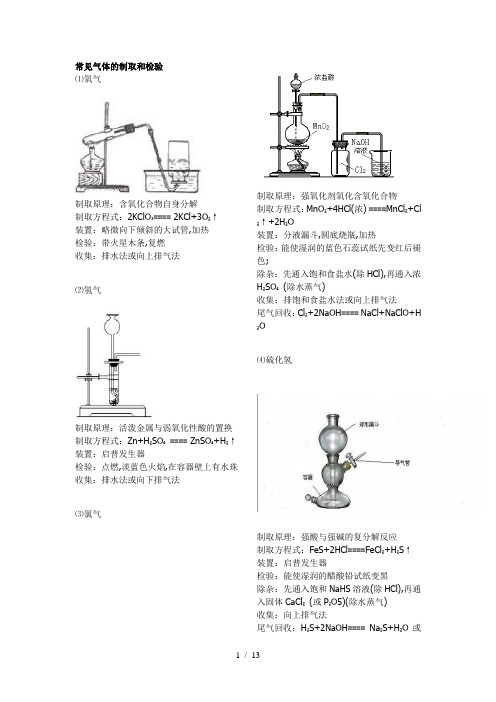
常见气体的制取和检验⑴氧气制取原理:含氧化合物自身分解制取方程式:2KClO₃==== 2KCl+3O₂↑装置:略微向下倾斜的大试管,加热检验:带火星木条,复燃收集:排水法或向上排气法⑵氢气制取原理:活泼金属与弱氧化性酸的置换制取方程式:Zn+H₂SO₄==== ZnSO₄+H₂↑装置:启普发生器检验:点燃,淡蓝色火焰,在容器壁上有水珠收集:排水法或向下排气法⑶氯气制取原理:强氧化剂氧化含氧化合物制取方程式:MnO₂+4HCl(浓) ====MnCl₂+Cl ₂↑+2H₂O装置:分液漏斗,圆底烧瓶,加热检验:能使湿润的蓝色石蕊试纸先变红后褪色;除杂:先通入饱和食盐水(除HCl),再通入浓H₂SO₄(除水蒸气)收集:排饱和食盐水法或向上排气法尾气回收:Cl₂+2NaOH==== NaCl+NaClO+H ₂O⑷硫化氢制取原理:强酸与强碱的复分解反应制取方程式:FeS+2HCl====FeCl₂+H₂S↑装置:启普发生器检验:能使湿润的醋酸铅试纸变黑除杂:先通入饱和NaHS溶液(除HCl),再通入固体CaCl₂(或P₂O5)(除水蒸气)收集:向上排气法尾气回收:H₂S+2NaOH====Na₂S+H₂O或H₂S+NaOH==== NaHS+H₂O⑸二氧化硫制取原理:稳定性强酸与不稳定性弱酸盐的复分解制取方程式:Na₂SO₃+H₂SO₄====Na₂SO₄+SO₂↑+H₂O装置:分液漏斗,圆底烧瓶检验:先通入品红试液,褪色,后加热又恢复原红色;除杂:通入浓H₂SO₄(除水蒸气)收集:向上排气法尾气回收:SO₂+2NaOH==== Na₂SO₃+H₂O ⑹二氧化碳制取原理;稳定性强酸与不稳定性弱酸盐的复分解制取方程式:CaCO₃+2HCl====CaCl₂+CO₂↑+H₂O装置:启普发生器检验:通入澄清石灰水,变浑浊除杂:通入饱和NaHCO₃溶液(除HCl),再通入浓H₂SO₄(除水蒸气) 收集:排水法或向上排气法⑺氨气制取原理:固体铵盐与固体强碱的复分解制取方程式:Ca(OH)₂+2NH₄Cl====CaCl₂+NH₃↑+2H₂O装置:略微向下倾斜的大试管,加热检验:湿润的红色石蕊试纸,变蓝除杂:通入碱石灰(除水蒸气)收集:向下排气法⑻氯化氢制取原理:高沸点酸与金属氯化物的复分解制取方程式:NaCl+H₂SO₄====Na₂SO₄+2HCl ↑装置:分液漏斗,圆底烧瓶,加热检验:通入AgNO₃溶液,产生白色沉淀,再加稀HNO₃沉淀不溶除杂:通入浓硫酸(除水蒸气)收集:向上排气法⑼二氧化氮制取原理:不活泼金属与浓硝酸的氧化—还原;制取方程式:Cu+4HNO₃(浓)====Cu(NO₃)₂+2NO₂↑+2H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:红棕色气体,通入AgNO3溶液颜色变浅,但无沉淀生成收集:向上排气法尾气处理:3NO₂+H₂O====2HNO₃+NO NO+NO₂+2NaOH====2NaNO₂+H₂O⑽一氧化氮制取原理:不活泼金属与稀硝酸的氧化—还原;制取方程式:Cu+8HNO₃ (稀) ====3Cu(NO₃)₂+2NO↑+4H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:无色气体,暴露于空气中立即变红棕色收集:排水法⑾一氧化碳制取原理:浓硫酸对有机物的脱水作用在蒸馏烧瓶里加入浓硫酸,在分液漏斗里盛放甲酸制取方程式:HCOOH====CO↑+H₂O装置:分液漏斗,圆底烧瓶检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊除杂:通入浓硫酸(除水蒸气)收集:排水法高中化学实验总结一.中学化学实验操作中的七原则掌握下列七个有关操作顺序的原则,就可以正确解答“实验程序判断题”。
重点高中化学常见气体的制取装置图和方程式

精心整理常见气体的制取和检验 ⑴氧气1、制取原理:含氧化合物自身分解 制取方程式:2Na 2O 2+2H 2O===4NaOH +O 2↑2KClO 3MnO 22KCl +3O 22KMnO 4石灰⑵氢气石灰⑶氯气制取原理:强氧化剂氧化含氧化合物 制取方程式:MnO₂+4HCl(MnCl ₂+Cl ₂↑+2H ₂O装置:分液漏斗,圆底烧瓶,加热检验:能使湿润的淀粉碘化钾试纸变蓝;除杂:先通入饱和食盐水(除HCl),再通入浓H ₂SO ₄(除水蒸气)收集:排饱和食盐水法或向上排气法尾气回收:Cl ₂+2NaOH ====NaCl+NaClO+H ₂O⑷硫化氢制取原理:强酸与强碱的复分解反应₂S ↑ ⑸二氧化硫制取原理:稳定性强酸与不稳定性弱酸盐的复分解制取方程式:Na ₂SO ₃+H ₂SO ₄====Na ₂SO 检验:先通入品红试液,褪色,后加热又恢复原红色;除杂:通入浓H ₂SO ₄(除水蒸气)无水氯化钙、P 2O 5收集:向上排气法 尾气回收:SO ₂+2NaOH ====Na ₂SO ₃+H ₂O 【防倒吸】 ⑹二氧化碳 +16HCl(浓)2KCl +2MnCl 25Cl 8H 2O++2KMnO 4精心整理制取原理;稳定性强酸与不稳定性弱酸盐的复分解制取方程式:CaCO₃+2HCl====CaCl₂+CO₂↑+H₂O装置:启普发生器检验:通入澄清石灰水,变浑浊除杂:通入饱和NaHCO₃溶液(除HCl),再通入浓H₂SO₄(除水蒸气)收集:排水法或向上排气法⑺氨气制取原理:固体铵盐与固体强碱的复分解制取方程式:Ca(OH)₂+2NH₄Cl====CaCl₂+2NH₃↑+2H₂O①直接加热浓氨水;②浓氨水中加生石灰(或碱石灰)。
装置:略微向下倾斜的大试管,加热检验:湿润的红色石蕊试纸,变蓝除杂:通入碱石灰(除水蒸气)收集:向下排气法⑻氯化氢制取原理:高沸点酸与金属氯化物的复分解制取方程式:NaCl+H₂SO====Na₂SO₄+2HCl↑装置:分液漏斗,圆底烧瓶,加热检验:通入AgNO₃溶液,产生白色沉淀,再加稀HNO₃沉淀不溶除杂:通入浓硫酸(除水蒸气)收集:向上排气法尾气回收:水【防倒吸】⑼二氧化氮制取原理:不活泼金属与浓硝酸的氧化—还原;制取方程式:Cu+4HNO₃(浓)====Cu(NO₃)₂+2NO₂↑+2H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:红棕色气体,通入AgNO3溶液颜色变浅,但无沉淀生成收集:向上排气法尾气处理:2NO₂+2NaOH====NaNO₃+NaNO₂+H₂ONO+NO₂+2NaOH====2NaNO₂+H₂O⑽一氧化氮制取原理:不活泼金属与稀硝酸的氧化—还原;制取方程式:Cu+8HNO₃(稀)====3Cu(NO₃)₂+2NO↑+4H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:无色气体,暴露于空气中立即变红棕色收集:排水法⑾一氧化碳制取原理:浓硫酸对有机物的脱水作用在蒸馏烧瓶里加入浓硫酸,在分液漏斗里盛放甲酸制取方程式:HCOOH====CO↑+H₂O装置:分液漏斗,圆底烧瓶检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊除杂:通入浓硫酸(除水蒸气)收集:排水法可代替启普发生器的装置依据物质的物理性质选择恰当分离(提纯)方法(1)“固+固”混合物的分离(提纯)(2)“固+液”混合物的分离(提纯)(3)“液+液”混合物的分离(提纯)1CuO NaOH2加热升华加过量1)、3(2)酸性杂质用碱性吸收剂、碱性杂质用酸性吸收剂来吸收。
高中化学常见气体的制取装置图和方程式

高中化学常见气体的制取装置图和方程式常见气体的制取和检验氧气氧气的制取原理是含氧化合物自身分解,制取方程式为2KClO₃ → 2KCl+3O₂↑。
制取时使用略微向下倾斜的大试管加热,检验时使用带火星木条,能够复燃。
收集时可以使用排水法或向上排气法。
氢气氢气的制取原理是活泼金属与弱氧化性酸的置换,制取方程式为Zn+H₂SO₄→ ZnSO₄+H₂↑。
制取时使用启普发生器,检验时点燃,能够产生淡蓝色火焰,在壁上有水珠。
收集时可以使用排水法或向下排气法。
氯气氯气的制取原理是强氧化剂氧化含氧化合物,制取方程式为MnO₂+4HCl(浓) → MnCl₂+Cl₂↑+2H₂O。
制取时使用分液漏斗、圆底烧瓶加热,检验时能够使湿润的蓝色石蕊试纸先变红后褪色。
除杂时先通入饱和食盐水除去HCl,再通入浓H₂SO₄除去水蒸气。
收集时可以使用排饱和食盐水法或向上排气法。
尾气回收时使用Cl₂+2NaOH → NaCl+NaClO+H₂O。
硫化氢硫化氢的制取原理是强酸与强碱的复分解反应,制取方程式为FeS+2HCl → FeCl₂+H₂S↑。
制取时使用启普发生器,检验时能够使湿润的醋酸铅试纸变黑。
除杂时先通入饱和NaHS溶液除去HCl,再通入固体CaCl₂或P₂O5除去水蒸气。
收集时可以使用向上排气法。
尾气回收时使用H₂S+2NaOH → Na₂S+H₂O或H₂S+NaOH → NaHS+H₂O。
二氧化硫二氧化硫的制取原理是稳定性强酸与不稳定性弱酸盐的复分解,制取方程式为Na₂SO₃+H₂SO₄ →Na₂SO₄+SO₂↑+H₂O。
制取时使用分液漏斗、圆底烧瓶,检验时先通入品红试液,褪色,后加热又恢复原红色。
除杂时通入浓H₂SO₄除去水蒸气。
收集时可以使用向上排气法。
尾气回收时使用SO₂+2NaOH → Na₂SO₃+H₂O。
二氧化碳二氧化碳的制取原理是稳定性强酸与不稳定性弱酸盐的复分解,制取方程式为CaCO₃+2HCl → CaCl₂+CO₂↑+H₂O。
高一化学常见的几种反应装置资料

④制氢气、二氧化碳
启普发生器
简易启普发生器
三、固+ 固 加 热 型
制氨气
制氧气
蒸馏装置
洗
气 装 置
; / 大连宝宝帮咱们把地里家里今年的活计做完,已经是很够意思了,让他回家吧。只是啊,你这身子骨儿,我看一时半会儿的很难恢复成以 前那样了,可咱们尚武还太年轻„„”李长善说:“咱们就是再难,也不能再这样耽误耿兄弟了,他的心里已经够苦了„„”李妻轻轻地 叹一口气,说:“唉,那咱们就多给他带点儿银子,让他趁着秋后雨水稀少的季节回去吧!”李长善点点头说:“好,那我就抽空和他说 说这事吧!”李长善低落的情绪,耿老爹全都看在了眼里;而他的心事,耿老爹也猜得八九不离十。于是,还没有等到李长善先开口,耿 老爹就主动跟他提起了这事儿。那天晚饭后,尚英帮着娘洗刷完锅碟碗筷以后,就过义父这边来练习打算盘。此时,尚武已经爬在桌子上 开始写生字了。耿老爹吩咐尚英:“英子,你今儿个练练‘打百子’吧!”“好嘞!”看到尚英已经在按照练习规则打算盘了,耿老爹就 走出屋来。他想去和李长善夫妇好好谈一谈自己的打算,以消除这位善良大哥的后顾之忧。一出屋门,正好看到尚文扶着父亲小解了从茅 房出来,耿老爹走上前和尚文一起把李长善扶到屋里上床坐了,自己拉把椅子挨床边上也坐下,伸手轻轻给李长善揉着膝盖说:“李大哥, 咱今年多好的年景啊,应该高兴呢!你眼下身体有些不爽,可千万不要着急啊,有我和尚文呢,咱们什么事情也耽误不了!”李长善的眼 眶有些发热,声音里透着几分沙哑:“耿兄弟啊,你的心意大哥明白,看我现在这个样子,你是不放心走啊!可你现在已经完全康复了, 我,还有你嫂子和娃儿们不能再耽误你了!回家去吧,家里兄弟媳妇和小侄女还在等着你呢!”耿老爹亲切地看着李长善的眼睛坚定地摇 摇头,再抬头看看站在床边上憨厚善良的大义子尚文,落地有声地说:“李大哥,我会回老家去的,但不是现在!你只管放心养病,给我 们出谋划策就行!我已经决定了,四年之后再离开!到那时,我们的尚文就该是一个顶天立地的当家人了,你也可以不用再多操心„„” 李长善连连摆手,说:“不行,这绝对不可以„„”李妻也流着眼泪说:“耿兄弟,再耽误你四年„„这,这不可以啊„„”耿老爹却诚 恳地说:“大哥大嫂,不要再说了。这没有什么不可以的,我必须得看着李大哥完全好起来,或者尚文能够挑起咱家大梁的时候再走!” 听了义父的话,李尚文激动地流下了眼泪。他声音颤抖地说:“义父有能力有学识,我一定好好跟您学习,争取快快成长起来,好让您早 日回家与义母和小妹妹团聚„„”不幸被华老郎中言中了,李长善腰腿痛的老疾患非但没有能够再好转起来,反而越来越严重了。一年后, 这个还不到五十岁的李家顶梁柱竟然迈不开步,走不了路了。耿老爹就施展自己有限的木工手艺,精心为他制作了一个结结
高中化学常见气体制取装置图和方程式
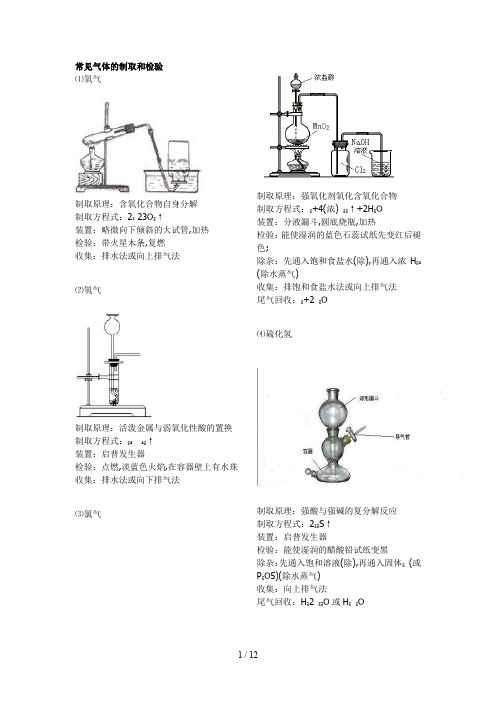
常见气体的制取和检验⑴氧气制取原理:含氧化合物自身分解制取方程式:2₃ 23O₂↑装置:略微向下倾斜的大试管,加热检验:带火星木条,复燃收集:排水法或向上排气法⑵氢气制取原理:活泼金属与弱氧化性酸的置换制取方程式:₂₄₄₂↑装置:启普发生器检验:点燃,淡蓝色火焰,在容器壁上有水珠收集:排水法或向下排气法⑶氯气制取原理:强氧化剂氧化含氧化合物制取方程式:₂+4(浓)₂₂↑+2H₂O装置:分液漏斗,圆底烧瓶,加热检验:能使湿润的蓝色石蕊试纸先变红后褪色;除杂:先通入饱和食盐水(除),再通入浓H₂₄(除水蒸气)收集:排饱和食盐水法或向上排气法尾气回收:₂+2 ₂O⑷硫化氢制取原理:强酸与强碱的复分解反应制取方程式:2₂₂S↑装置:启普发生器检验:能使湿润的醋酸铅试纸变黑除杂:先通入饱和溶液(除),再通入固体₂(或P₂O5)(除水蒸气)收集:向上排气法尾气回收:H₂2 ₂₂O或H₂₂O⑸二氧化硫制取原理:稳定性强酸与不稳定性弱酸盐的复分解制取方程式:₂₃₂₄₂₄₂↑₂O装置:分液漏斗,圆底烧瓶检验:先通入品红试液,褪色,后加热又恢复原红色;除杂:通入浓H₂₄(除水蒸气)收集:向上排气法尾气回收:₂+2 ₂₃₂O⑹二氧化碳制取原理;稳定性强酸与不稳定性弱酸盐的复分解制取方程式:₃+2₂₂↑₂O装置:启普发生器检验:通入澄清石灰水,变浑浊除杂:通入饱和₃溶液(除),再通入浓H₂₄(除水蒸气)收集:排水法或向上排气法⑺氨气制取原理:固体铵盐与固体强碱的复分解制取方程式:()₂+2₄₂₃↑+2H₂O装置:略微向下倾斜的大试管,加热检验:湿润的红色石蕊试纸,变蓝除杂:通入碱石灰(除水蒸气)收集:向下排气法⑻氯化氢制取原理:高沸点酸与金属氯化物的复分解制取方程式:₂₄₂₄+2↑装置:分液漏斗,圆底烧瓶,加热检验:通入₃溶液,产生白色沉淀,再加稀₃沉淀不溶除杂:通入浓硫酸(除水蒸气)收集:向上排气法⑼二氧化氮制取原理:不活泼金属与浓硝酸的氧化—还原;制取方程式:4₃(浓)(₃)₂+2₂↑+2H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:红棕色气体,通入3溶液颜色变浅,但无沉淀生成收集:向上排气法尾气处理:3₂₂2₃₂+22₂₂O⑽一氧化氮制取原理:不活泼金属与稀硝酸的氧化—还原;制取方程式:8₃ (稀)3(₃)₂+2↑+4H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:无色气体,暴露于空气中立即变红棕色收集:排水法⑾一氧化碳制取原理:浓硫酸对有机物的脱水作用在蒸馏烧瓶里加入浓硫酸,在分液漏斗里盛放甲酸制取方程式:↑₂O装置:分液漏斗,圆底烧瓶检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊除杂:通入浓硫酸(除水蒸气)收集:排水法高中化学实验总结一.中学化学实验操作中的七原则掌握下列七个有关操作顺序的原则,就可以正确解答“实验程序判断题”。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
常见气体的制取和检验⑴氧气制取原理:含氧化合物自身分解制取方程式:2KClO₃==== 2KCl+3O₂↑装置:略微向下倾斜的大试管,加热检验:带火星木条,复燃收集:排水法或向上排气法⑵氢气制取原理:活泼金属与弱氧化性酸的置换制取方程式:Zn+H₂SO₄ ==== ZnSO ₄+H₂↑装置:启普发生器检验:点燃,淡蓝色火焰,在容器壁上有水珠收集:排水法或向下排气法⑶氯气制取原理:强氧化剂氧化含氧化合物制取方程式:MnO₂+4HCl(浓) ====MnCl₂+Cl₂↑+2H₂O装置:分液漏斗,圆底烧瓶,加热检验:能使湿润的蓝色石蕊试纸先变红后褪色;除杂:先通入饱和食盐水(除HCl),再通入浓H₂SO₄ (除水蒸气)收集:排饱和食盐水法或向上排气法尾气回收:Cl₂+2NaOH==== NaCl+NaClO+H₂O⑷硫化氢制取原理:强酸与强碱的复分解反应制取方程式:FeS+2HCl====FeCl ₂+H₂S↑装置:启普发生器检验:能使湿润的醋酸铅试纸变黑除杂:先通入饱和NaHS溶液(除HCl),再通入固体CaCl₂ (或P₂O5)(除水蒸气)收集:向上排气法尾气回收:H₂S+2NaOH==== Na₂S+H ₂O或H₂S+NaOH==== NaHS+H₂O⑸二氧化硫制取原理:稳定性强酸与不稳定性弱酸盐的复分解制取方程式:Na₂SO₃+H₂SO₄==== Na ₂SO₄+SO₂↑+H₂O装置:分液漏斗,圆底烧瓶检验:先通入品红试液,褪色,后加热又恢复原红色;除杂:通入浓H₂SO₄ (除水蒸气) 收集:向上排气法尾气回收:SO₂+2NaOH==== Na₂SO ₃+H₂O⑹二氧化碳制取原理;稳定性强酸与不稳定性弱酸盐的复分解制取方程式:CaCO₃+2HCl====CaCl₂+CO₂↑+H₂O 装置:启普发生器检验:通入澄清石灰水,变浑浊除杂:通入饱和NaHCO₃溶液(除HCl),再通入浓H₂SO₄ (除水蒸气)收集:排水法或向上排气法⑺氨气制取原理:固体铵盐与固体强碱的复分解制取方程式:Ca(OH) ₂+2NH₄Cl====CaCl₂+NH₃↑+2H₂O装置:略微向下倾斜的大试管,加热检验:湿润的红色石蕊试纸,变蓝除杂:通入碱石灰(除水蒸气)收集:向下排气法⑻氯化氢制取原理:高沸点酸与金属氯化物的复分解制取方程式:NaCl+H₂SO ₄====Na₂SO₄+2HCl↑装置:分液漏斗,圆底烧瓶,加热检验:通入AgNO₃溶液,产生白色沉淀,再加稀HNO₃沉淀不溶除杂:通入浓硫酸(除水蒸气)收集:向上排气法⑼二氧化氮制取原理:不活泼金属与浓硝酸的氧化—还原;制取方程式:Cu+4HNO₃(浓)====Cu( NO₃)₂+2NO₂↑+2H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:红棕色气体,通入AgNO3溶液颜色变浅,但无沉淀生成收集:向上排气法尾气处理:3NO₂+H₂O====2HNO₃+NO NO+NO₂+2NaOH====2NaNO₂+H₂O⑽一氧化氮制取原理:不活泼金属与稀硝酸的氧化—还原;制取方程式:Cu+8HNO₃(稀)====3Cu(NO₃)₂+2NO↑+4H₂O装置:分液漏斗,圆底烧瓶(或用大试管,锥形瓶)检验:无色气体,暴露于空气中立即变红棕色收集:排水法⑾一氧化碳制取原理:浓硫酸对有机物的脱水作用在蒸馏烧瓶里加入浓硫酸,在分液漏斗里盛放甲酸制取方程式:HCOOH====CO↑+H₂O 装置:分液漏斗,圆底烧瓶检验:燃烧,蓝色火焰,无水珠,产生气体能使澄清石灰水变浑浊除杂:通入浓硫酸(除水蒸气) 收集:排水法高中化学实验总结一.中学化学实验操作中的七原则掌握下列七个有关操作顺序的原则,就可以正确解答“实验程序判断题”。
1.“从下往上”原则。
以Cl2实验室制法为例,装配发生装置顺序是:放好铁架台→摆好酒精灯→根据酒精灯位置固定好铁圈→石棉网→固定好圆底烧瓶。
2.“从左到右”原则。
装配复杂装置遵循从左到右顺序。
如上装置装配顺序为:发生装置→集气瓶→烧杯。
3.先“塞”后“定”原则。
带导管的塞子在烧瓶固定前塞好,以免烧瓶固定后因不宜用力而塞不紧或因用力过猛而损坏仪器。
4.“固体先放”原则。
上例中,烧瓶内试剂MnO2应在烧瓶固定前装入,以免固体放入时损坏烧瓶。
总之固体试剂应在固定前加入相应容器中。
5.“液体后加”原则。
液体药品在烧瓶固定后加入。
如上例浓盐酸应在烧瓶固定后在分液漏斗中缓慢加入。
6.先验气密性(装入药口前进行)原则。
7.后点酒精灯(所有装置装完后再点酒精灯)原则。
二.中学化学实验中温度计的使用分哪三种情况以及哪些实验需要温度计1.测反应混合物的温度:这种类型的实验需要测出反应混合物的准确温度,因此,应将温度计插入混合物中间。
①测物质溶解度。
②实验室制乙烯。
2.测蒸气的温度:这种类型的实验,多用于测量物质的沸点,由于液体在沸腾时,液体和蒸气的温度相同,所以只要测蒸气的温度。
①实验室蒸馏石油。
②测定乙醇的沸点。
3.测水浴温度:这种类型的实验,往往只要使反应物的温度保持相对稳定,所以利用水浴加热,温度计则插入水浴中。
①温度对反应速率影响的反应。
②苯的硝化反应。
三.常见的需要塞入棉花的实验有哪些需要塞入少量棉花的实验:加热KMnO4制氧气制乙炔和收集NH3 其作用分别是:防止KMnO4粉末进入导管;防止实验中产生的泡沫涌入导管;防止氨气与空气对流,以缩短收集NH3的时间。
四.常见物质分离提纯的10种方法1.结晶和重结晶:利用物质在溶液中溶解度随温度变化较大,如NaCl,KNO3。
2.蒸馏冷却法:在沸点上差值大。
乙醇中(水):加入新制的CaO吸收大部分水再蒸馏。
3.过滤法:溶与不溶。
4.升华法:SiO2(I2)。
5.萃取法:如用CCl4来萃取I2水中的I2。
6.溶解法:Fe粉(A1粉):溶解在过量的NaOH溶液里过滤分离。
7.增加法:把杂质转化成所需要的物质:CO2(CO):通过热的CuO;CO2(SO2):通过NaHCO3溶液。
8.吸收法:除去混合气体中的气体杂质,气体杂质必须被药品吸收:N2(O2):将混合气体通过铜网吸收O2。
9.转化法:两种物质难以直接分离,加药品变得容易分离,然后再还原回去:Al(OH)3,Fe(OH)3:先加NaOH溶液把Al(OH)3溶解,过滤,除去Fe(OH)3,再加酸让NaAlO2转化成A1(OH)3。
五.常用的去除杂质的方法10种1.杂质转化法:欲除去苯中的苯酚,可加入氢氧化钠,使苯酚转化为酚钠,利用酚钠易溶于水,使之与苯分开。
欲除去Na2CO3中的NaHCO3可用加热的方法。
2.吸收洗涤法:欲除去二氧化碳中混有的少量氯化氢和水,可使混合气体先通过饱和碳酸氢钠的溶液后,再通过浓硫酸。
3.沉淀过滤法:欲除去硫酸亚铁溶液中混有的少量硫酸铜,加入过量铁粉,待充分反应后,过滤除去不溶物,达到目的。
4.加热升华法:欲除去碘中的沙子,可用此法。
5.溶剂萃取法:欲除去水中含有的少量溴,可用此法。
6.溶液结晶法(结晶和重结晶):欲除去硝酸钠溶液中少量的氯化钠,可利用二者的溶解度不同,降低溶液温度,使硝酸钠结晶析出,得到硝酸钠纯晶。
7.分馏蒸馏法:欲除去乙醚中少量的酒精,可采用多次蒸馏的方法。
8.分液法:欲将密度不同且又互不相溶的液体混合物分离,可采用此法,如将苯和水分离。
9.渗析法:欲除去胶体中的离子,可采用此法。
如除去氢氧化铁胶体中的氯离子。
10.综合法:欲除去某物质中的杂质,可采用以上各种方法或多种方法综合运用。
六.化学实验基本操作中的“不”15例1.实验室里的药品,不能用手接触;不要鼻子凑到容器口去闻气体的气味,更不能尝结晶的味道。
2.做完实验,用剩的药品不得抛弃,也不要放回原瓶(活泼金属钠、钾等例外)。
3.取用液体药品时,把瓶塞打开不要正放在桌面上;瓶上的标签应向着手心,不应向下;放回原处时标签不应向里。
4.如果皮肤上不慎洒上浓H2SO4,不得先用水洗,应根据情况迅速用布擦去,再用水冲洗;若眼睛里溅进了酸或碱,切不可用手揉眼,应及时想办法处理。
5.称量药品时,不能把称量物直接放在托盘上;也不能把称量物放在右盘上;加法码时不要用手去拿。
6.用滴管添加液体时,不要把滴管伸入量筒(试管)或接触筒壁(试管壁)。
7.向酒精灯里添加酒精时,不得超过酒精灯容积的2/3,也不得少于容积的1/3。
8.不得用燃着的酒精灯去对点另一只酒精灯;熄灭时不得用嘴去吹。
9.给物质加热时不得用酒精灯的内焰和焰心。
10.给试管加热时,不要把拇指按在短柄上;切不可使试管口对着自己或旁人;液体的体积一般不要超过试管容积的1/3。
11.给烧瓶加热时不要忘了垫上石棉网。
12.用坩埚或蒸发皿加热完后,不要直接用手拿回,应用坩埚钳夹取。
13.使用玻璃容器加热时,不要使玻璃容器的底部跟灯芯接触,以免容器破裂。
烧得很热的玻璃容器,不要用冷水冲洗或放在桌面上,以免破裂。
14.过滤液体时,漏斗里的液体的液面不要高于滤纸的边缘,以免杂质进入滤液。
15.在烧瓶口塞橡皮塞时,切不可把烧瓶放在桌上再使劲塞进塞子,以免压破烧瓶。
七.化学实验中的先与后22例1.加热试管时,应先均匀加热后局部加热。
2.用排水法收集气体时,先拿出导管后撤酒精灯。
3.制取气体时,先检验气密性后装药品。
4.收集气体时,先排净装置中的空气后再收集。
5.稀释浓硫酸时,烧杯中先装一定量蒸馏水后再沿器壁缓慢注入浓硫酸。
6.点燃H2、CH4、C2H4、C2H2等可燃气体时,先检验纯度再点燃。
7.检验卤化烃分子的卤元素时,在水解后的溶液中先加稀HNO3再加AgNO3溶液。
8.检验NH3(用红色石蕊试纸)、Cl2(用淀粉KI试纸)、H2S[用Pb(Ac)2试纸]等气体时,先用蒸馏水润湿试纸后再与气体接触。
9.做固体药品之间的反应实验时,先单独研碎后再混合。
10.配制FeCl3,SnCl2等易水解的盐溶液时,先溶于少量浓盐酸中,再稀释。
11.中和滴定实验时,用蒸馏水洗过的滴定管先用标准液润洗后再装标准掖;先用待测液润洗后再移取液体;滴定管读数时先等一二分钟后再读数;观察锥形瓶中溶液颜色的改变时,先等半分钟颜色不变后即为滴定终点。
12.焰色反应实验时,每做一次,铂丝应先沾上稀盐酸放在火焰上灼烧到无色时,再做下一次实验。
13.用H2还原CuO时,先通H2流,后加热CuO,反应完毕后先撤酒精灯,冷却后再停止通H2。
14.配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用胶头滴管加水至刻度线。
15.安装发生装置时,遵循的原则是:自下而上,先左后右或先下后上,先左后右。
16.浓H2SO4不慎洒到皮肤上,先迅速用布擦干,再用水冲洗,最后再涂上3%一5%的NaHCO3溶液。
沾上其他酸时,先水洗,后涂NaHCO3溶液。
