江苏省连云港市新海实验中学苏教版高二化学选修五《4.2.3基团间的相互影响》官能团之间的相互影响 教案
高二化学苏教版选修5课件:专题4 第2单元 第2课时 酚的性质和应用 基团间的相互影响用

简单的酚。
2.苯酚的物理性质
无色 晶体,熔点为 40.9 ℃。常温下在水中的溶解度不大, 纯净的苯酚为______ 水层 ,下层是溶有水 当苯酚与水形成的浊液静置后分层,上层是溶有苯酚的______ 易溶于 乙醇等 的________ 苯酚层 ;当温度高于________ 65 ℃ 时,则能与水______ 互溶 。苯酚________
2.苯酚的分离与提纯 (1)有机溶剂中混有苯酚
(2)废水中含有苯酚
(3)乙醇中混有苯酚
冲关] [ 题组· 题组 1 酚的性质与检验 )
1.能证明苯酚具有弱酸性的实验是( A.加入浓溴水生成白色沉淀
B.苯酚钠溶液中通入 CO2 后,溶液由澄清变浑浊 C.浑浊的苯酚加热后变澄清 D.苯酚的水溶液中加 NaOH 溶液,生成苯酚钠
4.含酚废水的处理 (1)酚类化合物的毒性:在石油、煤、化工、制药、油漆工业产生的废水中
苯酚 、______ 甲酚 污染为主,影响水生动物的生长,含 含有较多的酚类物质,以______ 回收利用 和____________ 降解处理 。 酚废水可____________
(2)回收处理方法:
苯 ,萃取分液。 ①废水中加____
A.可以和溴水反应 B.可用有机溶剂萃取 C.分子中有三个苯环 D.1 mol 维生素 P 可以和 4 mol NaOH 反应
【解析】 该物质有酚羟基,苯环的邻对位有氢原子,可以和溴水反应,A 项正确;B 项说法正确,因为该物质也是有机物,根据相似相溶原理;C 项中说 法错误,中间的环不是苯环;D 项正确,因为有 4 个酚羟基。 【答案】 C
__________________________________________。
(2)苯酚的取代反应 苯酚与浓溴水反应的化学方程式为
江苏省连云港市新海实验中学苏教版高二化学选修五 专题二 有机物的结构和分类 复习课件

(4)3苯基1丙烯的结构简式为________。
解析
(1)烯烃的命名是从离碳碳双键较近的一端给主链上的
碳原子编号,则该有机物的系统命名是3,4二甲基2戊烯,其 完全氢化后所得烷烃的系统名称为2,3二甲基戊烷。 (2)炔烃的命名也是从离叁键较近的一端给主链上的碳原子编 号,则该有机物的系统名称为3,5,6三甲基1庚炔,其完全氢 化后所得烷烃的系统名称为2,3,5三甲基庚烷。 (3)该有机物三个甲基相互间处于间位,可命名为间三甲苯; 若用系统命名法,也可命名为1,3,5三甲(基)苯。 (4)依有机物的系统名称,可写出该有机物的结构简式为
(2)乙烯的平面构型:乙烯分子中的所有原子都 在同一平面内,键角为120° 。当乙烯分子中的 某氢原子被其他原子或原子团取代时,则替代 该氢原子的原子一定在原乙烯分子的平面内。 (3)苯的平面构型:苯分子中所有原子都在同一平 面内,键角为120° 。当苯分子中的一个氢原子被其 他原子或原子团取代时,则替代该氢原子的原子一定在原苯 分子的平面内。
方向二
有机物分子中原子共线、共面问题
分子里原子共线、共面的问题,其实就是分子的构型问题。 大多数有机物分子的构型很复杂,但总是与下列简单分子的 几何构型相联系。
(1)甲烷的正四面体构型:在甲烷分子中,碳原子居于正四面 体的中心,分子中的5个原子没有任何4个处于同一平面内, 碳原子和任意两个氢原子确定一个平面,其余两个氢原子分 别位于该平面的两侧,即甲烷分子中有且只有三个原子共平 面。
(4)乙炔的直线构型:乙炔中的碳原子和氢原子 一定在一条直线上,键角为180° 。当乙炔分子 中的一个氢原子被其他原子或原子团取代时,替代该氢原子 的原子一定和乙炔分子的其他原子共线。 在共价型分子里,形成共价单键的原子可以绕键轴旋转,形 成双键、叁键及其他复杂键的原子不能绕键轴旋转。 应用上述基础知识对组成与结构较复杂的有机物分子进行分 析、综合、比较容易应对有机物分子里原子共线、共面的难 题。
最新高中-化学专题4烃的衍生物4-2-3基团间的相互影响课堂反馈苏教版选修5

最新高中-化学专题4烃的衍生物4-2-3基团间的相互影响课堂反馈苏教版选修51.在下列反应中,既不能说明苯酚分子中羟基受苯环影响而使它比乙醇分子中羟基更活泼,也不能说明由于羟基对苯环的影响而使苯酚中苯环比苯更活泼的是( ) 解析要明确以下题意:前一分句是要判断酚羟基比醇羟基活泼,即酚羟基能发生的反应醇羟基不能发生;后一分句说明苯酚中苯环上的H原子比苯上的H原子活泼。
所以从选项中可以看出B符合前一分句的内容,C、D符合后一分句的内容,而A反应不仅酚能发生,醇也能发生。
答案 A2.在实验室中分离苯和苯酚的混合物,可选用下列装置中的( ) 解析方法一:先将苯酚转化为苯酚钠,进入水溶液,分液后得到苯酚钠和苯;然后向苯酚钠中通入足量CO2气体,将其转化为苯酚,因苯酚在水中的溶解度极小,从而游离出来,再采用分液的方法与水分离开,可选用分液漏斗。
方法二:利用二者的沸点不同采用蒸馏法,可选A。
答案 A3.己烯雌酚是人工合成的非甾体雌激素物质,主要用于治疗雌激素低下症及激素平衡失调所引起的功能性出血等,如图所示分别取1 mol己烯雌酚进行4个实验。
下列对实验数据的预测与实际情况吻合的是( ) A.①中生成7 mol H2O B.②中无CO2生成C.③中最多消耗3 mol Br2D.④中发生消去反应解析己烯雌酚的分子式为C18H22O2,反应①中应生成11 mol H2O,A项错;酚的酸性比H2CO3的弱,不能与NaHCO3溶液反应生成CO2,B项对;两个酚羟基的邻位上共有4个氢原子,它们均可被卤素原子取代,故反应③中最多可以消耗4 mol Br2,C项错;苯环上的酚羟基不能发生消去反应,D项错。
答案 B4.Ⅰ.在某有机物的分子中,若含有一个“—C6H5”、一个“—C6H4—”、一个“—CH2—”、一个“—OH”,则属于酚类的同分异构体有________种,它们的结构简式是___________________________。
高中化学苏教版选修5课件:4.2.2 酚的性质和应用 基团间的相互影响

溴水和苯酚 常温,不需催化剂 取代苯环上的三个氢原子
苯酚与溴的取代反应比苯与溴的取代反应易进行 酚羟基对苯环的影响,使苯环上的氢原子变得更活泼
重点难点探究
重要考向探究
随堂检测
2.脂肪醇、芳香醇、酚的比较
类别 实例 结构 特点 主要 化学 性质 特性 脂肪醇 CH3CH2OH 醇羟基—OH —OH 与苯环侧 链碳原子相连 酚羟基—OH —OH 与苯环直接相连 (1)弱酸性;(2)取代反 应;(3)显色反应;(4)加成 反应;(5)与钠反应;(6)氧 化反应;(7)缩聚反应 与 FeCl3 溶液反应显紫 色 —OH 与链 烃基相连 芳香醇 苯酚
阅读思考
自主检测
1.下列有机物,属于酚类的是(
)
A.
B.
C. D. 答案:A 2.苯酚和苯甲醇共同的化学性质是( ) A.具有酸性 B.与钠反应放出氢气 C.遇FeCl3溶液显紫色 D.与NaOH溶液反应 答案:B
重点难点探究
重要考向探究
随堂检测
探究问题 1.从结构上看,苯酚分子是由一个苯环和一个羟基组成的。那么, 苯酚是否具有与苯或醇相同的化学性质呢? 提示:苯酚分子中羟基和苯环直接相连,由于官能团之间的相互 影响使得苯酚的化学性质与醇或苯的化学性质有明显的不同。
自主检测
3.苯酚与氢氧化钠溶液怎么反应?该反应表现出苯酚的什么性质? 试写出二氧化碳通入苯酚钠溶液发生反应的化学方程式,该反应说 明了苯酚的酸性比碳酸强还是弱?为什么?
提示: 苯酚跟氢氧化钠溶液的反应:
+NaOH
+H2O。该反应表现出苯酚的酸性。二氧化碳通入苯酚 钠溶液发生反应的化学方程式: +CO2+H2O
最新江苏版化学选修五课件:专题4 第2单元 第2课时 酚的性质和应用、基团间的相互影响

物称为醇。酚遇氯化铁显特征颜色,并不是生成沉淀。
答案:C
3.由 C6H5—、—C6H4—、—CH2—、—OH 四种原子团一起组成
属于酚类物质的种类有
()
A.1 种
B.2 种
C.3 种
D.4 种
解 析 : 酚 类 物 质 必 须 是 —OH 与 苯 环 直 接 相 连 , 其 组 成 为
C6H5CH2C6H4OH,移动—OH 的位置,有三种同分异构体:
1.羟基影响苯环使苯酚分子中苯环比苯活泼的是( )
A.①③ B.只有② C.②和③ D.全部 解析:羟基对苯环影响的结果是使苯环上的氢活泼性增强,
更易发生取代反应。
答案:B
2.能说明苯环对羟基有影响,使羟基变得活泼的事实是( ) A.苯酚能和溴水迅速反应 B.苯酚具有酸性 C.室温时苯酚不易溶解于水 D.液态苯酚能与钠反应放出氢气 解析:A 项,是羟基使苯环上羟基邻对位的氢原子变得活泼。C 项是苯酚的物理性质。D 项,只要是羟基均可以与钠反应,不 具有可比性。B 项,醇羟基为中性,但苯酚却呈弱酸性,显然 是受苯环的影响,正确。 答案:B
如 1 mol
最多可以消耗 2 mol Br2。
1 mol
最多可以消耗 3 mol Br2。
(6)从工业废水中分离回收苯酚的工艺流程
1.能证明苯酚的酸性很弱的实验有
()
A.常温下苯酚在水中的溶解度不大
B.能跟 NaOH 溶液反应
C.遇 FeCl3 溶液变紫色
D.将 CO2 通入苯酚钠溶液中,出现浑浊 解析:判断苯酚酸性很弱的依据是利用“强酸”制“弱酸”的原
NaHCO3 而不是 Na2CO3?
提ห้องสมุดไป่ตู้
示
苏教版高中化学选修五课件第二单元醇酚-基团间的相互影响原创.pptx

•
9
基团间的相互影响
官能团对烃基的影响
〔解释二〕虽然苯和苯酚都能发生溴代反应,
但苯酚能与溴水发生取代反应,而苯不能与溴水 反应,为什么?
原因:羟基使苯环变得活泼,易在相对于羟 基的邻、对位发生取代反应)
不和溴水反应
—OH 和浓溴水作用产生白色沉淀 (-OH对苯环的影响)
•
10
基团间的相互影响
×
无现象
通过苯与甲苯、甲苯与甲烷的性质差异, 可知有机分子中基团之间存在着相互的影响
•
3
基团间的相互影响
完成下列反应的化学方程式
+ HNO3
浓硫酸 60℃
— NO2 + H2O
/NO2
浓硫酸
+ 2HNO3 100~110℃
C| H3
+ 3HNO3
浓硫酸 100℃
O2N
+ 2H2O
\NO2 C| H3 NO2
举例
O ||
O ||
CH3—C —OH中的—OH受 —C— 影响
使得-COOH的氢较易电离,显酸性。
从而是乙酸的酸性比苯酚还强。
CH3—CH3难以去氢。 CH3CH2OH较易发生烃基上的氢和羟基之间的 脱水(-OH对乙基的影响)。 CH3CH2Br较易发生烃基上的氢和Br之间的脱水 (-Br对乙基的影响)。
反应物 反应条件
苯 苯、液溴 催化剂
苯酚 苯酚、浓溴水 通常条件
观察被氢与取原代子思的数考(P76)1或2
3
反应速率
较慢很快
•
7
基团间的相互影响
交流讨论
以上事实说明:尽管在苯酚和乙醇分子中 都存在羟基,但是这两种物质与钠反应的剧烈 程度存在较大的差异;苯酚和苯都含有分换, 但苯环上的氢原子被取代的难易程度存在明显 差异。你能对上述事实做出解释吗?请阐述你 的观点,并通过适当方式与同学交流。
江苏省连云港市新海实验中学苏教版高二化学五《专题四 烃的衍生物》小结 导学案
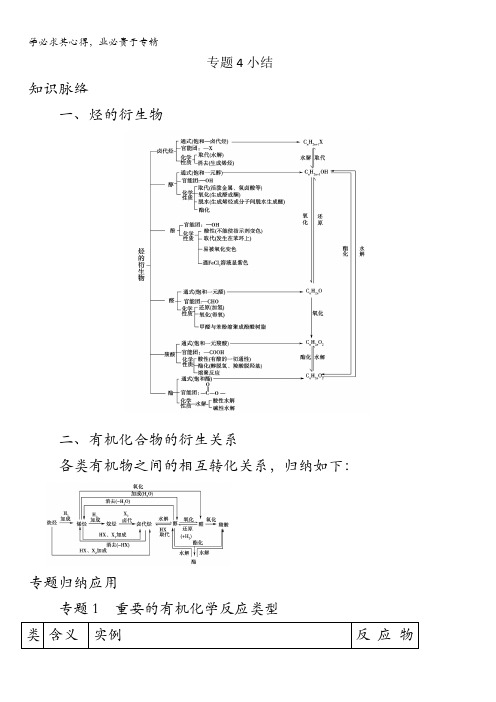
专题4小结知识脉络一、烃的衍生物二、有机化合物的衍生关系各类有机物之间的相互转化关系,归纳如下:专题归纳应用专题1 重要的有机化学反应类型类含义实例反应物别类属取代反应有机物分子里某些原子或原子团被其他原子或原子团所代替的反应卤代:CH4+Cl2−→−光CH3Cl+HCl烷、环烷、芳香烃、苯酚硝化:+HO—NO2芳香烃,芳香化合物酯化:CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O水解:CH3CH2Br+NaOH CH3CH2OH+NaBrCH3COOCH2CH3+H2O CH3COOH+CH3CH2OH羧酸,醇、卤代烃,酯分子间脱水:2C2H5OH C2H5—O—C2H5+H2O醇加成反应有机物分子里的不饱和加氢:CH2==CH2+H2−−→−催化剂CH3CH3烯,炔,芳香烃,醛,酮加卤素:CH2==CH2+Cl2−→−CH2ClCH2Cl烯、炔加水:CH2==CH2+H2O CH-烯、炔碳原子跟其他原子或原子团直接结合生成比较饱和的碳原子的反应3CH2OH加卤化氢:CH≡CH+HCl CH2==CHCl加HCN:CH3CHO+HCN−→−醛消去反应有机物从分子里脱去一个小分子而成分子内脱水:C2H5OH CH2==CH2↑+H2O醇分子内脱卤化氢:CH3CH2Cl CH2==CH2↑+HCl卤代烃为不饱和分子的反应氧化反应有机物得氧或失氢的反应催化氧化:2CH3CH2OH+O22CH3CHO+2H2O醇银镜反应:CH3CHO+2Ag(NH3)2OH CH3COONH4+2Ag+3NH3+H2O醛被酸性KMnO4溶液氧化:醇、酚、醛、烯、炔、苯的同系物燃烧:CH4+2O2−−→−点燃CO2+2H2O烃、烃的含氧衍生物等还原反应有机物得氢或失氧的反应有机物加氢:CH2==CH2+H2CH3—CH3CH3CHO+H2CH3CH2OH烯、烃、醛、酮、苯环、(注:羧酸、酯不与H2反应)羧酸与强还原剂反应:CH3COOH−−→−4LiAlH CH3CH2OH羧酸聚合反应由相对分子质量小的化合物分子相互结合成相对分子质量大的高分子合物的反应.聚合反应包烯烃、含碳碳双键的化合物可发生加聚反应。
新苏教版选修5化学同步课件:酚的性质和应用、基团间的相互影响PPT共39页

15、机会是不守纪律的。——雨果的相
互影响
11、战争满足了,或曾经满足过人的 好斗的 本能, 但它同 时还满 足了人 对掠夺 ,破坏 以及残 酷的纪 律和专 制力的 欲望。 ——查·埃利奥 特 12、不应把纪律仅仅看成教育的手段 。纪律 是教育 过程的 结果, 首先是 学生集 体表现 在一切 生活领 域—— 生产、 日常生 活、学 校、文 化等领 域中努 力的结 果。— —马卡 连柯(名 言网)
51、 天 下 之 事 常成 于困约 ,而败 于奢靡 。——陆 游 52、 生 命 不 等 于是呼 吸,生 命是活 动。——卢 梭
53、 伟 大 的 事 业,需 要决心 ,能力 ,组织 和责任 感。 ——易 卜 生 54、 唯 书 籍 不 朽。——乔 特
55、 为 中 华 之 崛起而 读书。 ——周 恩来
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
官能团之间的相互影响
在有机化学的学习中,掌握官能团的性质和它们之间的关系是学好有机化学的基本要求。
高中阶段必须掌握的官能团有:碳碳双键、碳碳叁键、卤素原子、羟基、醛基、羰基、羧基、氨基、硝基、磺酸基等。
有机物分子的官能团不同,则性质不同。
本文主要就官能团之间的影响,做一简要介绍:
一、官能团的定位作用
苯环上有连接有不同的基团或官能团,当进一步引入基团时,其引入的位置与原有官能团(基团)有关,而且不同的基团,还会使苯环的反应活性发生较大的变化。
1.邻对位定位基团,苯环的活性增强
当苯环上连接烃基(甲基、乙基、苯基等)、氨基(-NH
2、-NHR、-NR
2
,R为
烷基)、羟基(-OH)、烷氧基(-OCH
3、-OC
2
H
5
)等基团,使苯的反应活性增
强,新引入的基团进入原基团的邻对位位置。
教材上制备硝基苯需要在浓硫酸、浓硝酸混酸与苯在55℃条件下制得,而通常只能得到,很难得到二硝基化合物。
甲苯中新引入的-NO
2均处于甲基(-CH
3
)的邻位或对位。
在过量硝酸存在下,
很容易得到三硝基化合物(TNT),这也看出甲基提高了苯环的活性。
2.邻对位定位基团——苯的活性减弱
当苯环上连接有卤素原子(-F、-Cl、-Br、-I)-CH
2
Cl、-CH=CH-等基团时,苯环的反应活性降低,这类反应比较特殊,往往需要在特殊溶剂、催化剂条件下才可能发生反应。
3.间位定位基
当苯环上的取代基为-NO
2、-SO
3
H、-SO
2
R、-COOH、-COOR、-CHO、-COR、
-CN等时,使苯环钝化,但邻位和对位钝化程度较间位大,在取代反应中,新取代基大多进入间位,形成间位异构体。
这类取代基称为有钝化作用的间位取代基。
如硝基苯在发烟硝酸、发烟硫酸存在下,长时间加热,可以制得少量的间硝基苯(),同时比较硝基苯的制法可以看出,硝基的引入使苯的活性降低,反应的条件明显提高。
二、官能团(基团)之间相互影响
1.官能团(基团)之间的相互活化
(1)苯环与烷烃基的相互活化
当苯环上连接饱和链烃基时,苯环的活动性增强,使苯的取代变的比较容易,如苯硝化一般得到一硝基化合物,而甲苯硝化则可以得到三硝基化合物。
同时苯环对直接相连的烃基碳上的氢原子也有活化作用,我们知道,饱和烃是不容易被氧化剂氧化的,由于苯环能活化烃基与苯环相连碳原子的氢,使这样的氢原子活性增强,变的容易被氧化,如甲苯、乙苯等均能被酸化的高锰酸钾溶液氧化,产物得到苯甲酸等化合物。
乙苯、丙苯氧化的方程式如下:
C 6H
5
-CH
2
CH
3
C
6
H
5
-COOH+CO
2
+H
2
O
C 6H
5
-CH
2
CH
2
CH
3
C
6
H
5
-COOH+CH
3
COOH
C 6H
5
-CH(CH
3
)
2
C
6
H
5
-COOH+CO
2
+H
2
O
由于苯环活化的是直接相连的烃基碳原子上的氢原子,因此当该碳原子没有氢原
子时,该氧化反应就不能发生了,如叔丁基苯[C
6H
5
-C(CH
3
)
2
]不能使酸化高锰酸
钾溶液褪色。
(2)某些官能团(基团)与羟基的相互影响
醇、苯酚和羧酸的分子里都含有羟基,故皆可与钠作用放出氢气,但由于所连的基团不同,在酸性上存在差异。
醇(R-OH)显中性,不能与NaOH、Na
2CO
3
反应;与苯环直接相连的羟基成为酚
羟基,不与苯环直接相连的羟基成为醇羟基。
①苯酚(C
6H
5
-OH)具有极弱酸性,比碳酸弱,但比HCO
3
-(碳酸氢根)要强。
不
能使指示剂变色,能与NaOH反应。
苯酚还可以和碳酸钠反应,生成苯酚钠与碳酸氢钠;由此可以看出苯环能使羟基的活性增强,而烃基(非苯基)则往往是使羟基的活性减弱,如乙醇的电离程度较水(可以看成是氢原子连接羟基)小的多。
②R-COOH 弱酸性,具有酸的通性,能与NaOH、Na
2CO
3
反应。
显然,羧酸中,羧
基中的羰基的影响使得羟基中的氢易于电离。
苯环可以进一步加强羰基对羟基的活化作用,如苯甲酸的酸性比乙酸强。
③羟基对苯环的影响也是非常大的(较-CH
3大的多),如苯与Br
2
的取代反应,
需要Fe(实际上为FeBr
3
)催化下才能发生反应,苯酚则可以和溴水直接发生取代反应,而且反应能定量的完成,得到三溴苯酚(),这说明在羟基的影响下,苯环的活性有了很大的提高。
苯环也变的容易被氧化,如苯酚在空气中被氧气逐渐氧化而显示粉红色。
苯环上的羟基越多,苯环越容易被氧化,其还原性越强。
④羟基对其他烃基也有活化作用,如:乙醇烃基上的碳氢键较容易断裂,可发生氧化反应和消去反应。
若羟基与碳碳双键相连,由于其对碳碳双键官能团的活化作用,立即发生反应,使碳氢键断裂。
所以羟基不能与碳碳双键官能团直接连接。
⑤羟基还可以活化-X原子,卤代烃需要在强碱条件下才能发生水解反应,当羟基与卤素原子连接在同一个碳原子上时,由于羟基的活化作用,C-X极易断裂,生成羰基(=CO)结构,同时生成HX。
这说明羟基不能与卤素原子共存与同一个碳原子上。
⑥羟基与羟基之间也有很强的相互影响。
当多个羟基连接在同一个碳原子上,会立即失去水分子而转化为羰基(-CO-)。
即碳原子上不可能同时存在两个羟基。
⑦多羟基之间的也存在相互影响。
当相邻碳原子上均连接有羟基时,这些羟基之间也有相互作用。
例如在新制氢氧化铜中滴加乙醇,无变化,滴加甘油或葡萄糖溶液,氢氧化铜悬浊液消失,转化为绛蓝色溶液,这就是由于这些羟基中的氧氢键断裂与Cu2+离子结合的结果。
另外多羟基还对羰基也有一定的影响,如果糖中的官能团为多羟基和羰基,结构中并不含有醛基,但是果糖却能发生银镜反应,也能与新制氢氧化铜反应。
这说明多羟基与羰基直接存在着相互作用。
2.官能团(基团)之间的相互钝化
在前面已经说过,某些基团可以使苯环的活性降低,这就是官能团之间的钝化问题。
官能团的钝化也是一个非常普遍的问题。
在教材中我们知道,乙炔在一定条件下,可以与HCl加成,生成氯乙烯,氯乙烯是可以通过加聚反应得到聚氯乙烯,这个反应在工业生产上是十分有意义的。
为什么氯乙烯不会进一步加成为二氯乙烷呢?这就是由于碳碳双键原子团连接Cl原子后使碳碳双键官能团的活性降低,与HCl的加成难度增加,所以人们控制反应条件很容易的得到纯度较高的氯乙烯。
综上所述,我们学习有机物的性质,不但要学习根据官能团判断有机物的性质,以及根据性质判断官能团的存在。
但是,还要注意官能团(基团)间接的相互作用,从原理上掌握有机官能团的特点,以及有机物的结构特点等。
只有这样才能在学习上做到融会贯通,才能在探究中,升华自己的能力。
