2007年全国高中学生化学竞赛(安徽赛区)初赛试题
安徽化学竞赛试题
一、制备PbS 纳米粒子的方法如下:EDTA 为乙二胺四乙酸,它是一种弱酸,简写成H 4Y ,EDTA 二钠简写成Na 2H 2Y ,它们可以与Pb 2+及其它许多金属离子形成稳定的配离子。
⑴ 从平衡的观点解释增大酸度对PbY 2-的影响。
⑵ 为什么不用硫化氢气体直接通入硝酸铅溶液来制备PbS 纳米粒子?⑶ 为什么用Na 2H 2Y 而不用H 4Y 来制备PbY 2-?⑷ 在医学上可以用形成PbY 2-来治疗人体的铅中毒,临床上是在葡萄糖输液中加入适量CaH 2Y 代替Na 2H 2Y 给病人输液治疗。
请说明这种取代的理由。
(2001安徽29)二、CH2N2有七种同分异构体,其中有一种命名为重氮甲烷。
试画出重氮甲烷的两种路易斯结构式(即成键电子对用短线“-”表示,孤电子用黑点表示“· ”)___;在有机反应中重氮甲烷是重要的试剂之一,这是利用它的___性质(用化学反应方程式表示)。
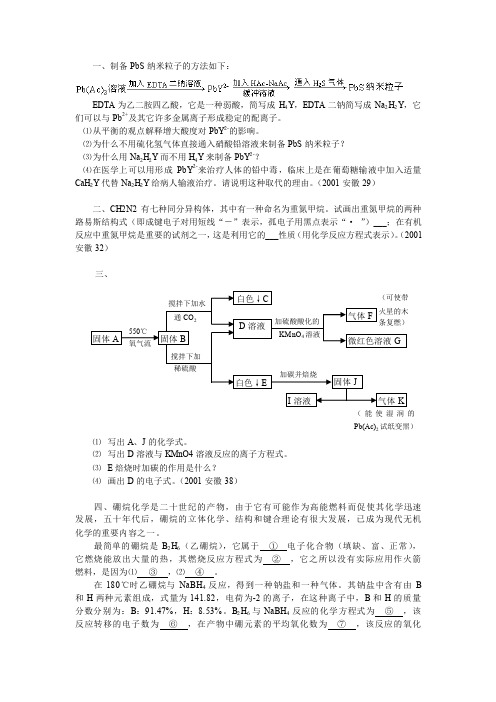
(2001安徽32)三、⑴ 写出A 、J 的化学式。
⑵ 写出D 溶液与KMnO4溶液反应的离子方程式。
⑶ E 焙烧时加碳的作用是什么? ⑷ 画出D 的电子式。
(2001安徽38)四、硼烷化学是二十世纪的产物,由于它有可能作为高能燃料而促使其化学迅速发展,五十年代后,硼烷的立体化学、结构和键合理论有很大发展,已成为现代无机化学的重要内容之一。
最简单的硼烷是B 2H 6(乙硼烷),它属于 ① 电子化合物(填缺、富、正常),它燃烧能放出大量的热,其燃烧反应方程式为 ② ,它之所以没有实际应用作火箭燃料,是因为⑴ ③ ,⑵ ④ 。
在180℃时乙硼烷与NaBH 4反应,得到一种钠盐和一种气体。
其钠盐中含有由B 和H 两种元素组成,式量为141.82,电荷为-2的离子,在这种离子中,B 和H 的质量分数分别为:B :91.47%,H :8.53%。
B 2H 6与NaBH 4反应的化学方程式为 ⑤ ,该反应转移的电子数为 ⑥ ,在产物中硼元素的平均氧化数为 ⑦ ,该反应的氧化白色↓ C D 溶液固体JI 溶液气体K(能使湿润的Pb(Ac)2试纸变黑)白色↓E加碳并焙烧固体A固体B550℃ 氧气流搅拌下加水通CO 2搅拌下加 稀硫酸气体F微红色溶液G火星的木条复燃)KMnO 4溶液加硫酸酸化的剂是 ⑧ ,还原剂是 ⑨ 。
年全国高中化学竞赛(安徽赛区)初赛试题

年全国高中化学竞赛(安徽赛区)初赛试题H 1.008 元素周期表He4.003Li 6.941Be9.012B10.81C12.01N14.01O16.00F19.00Ne20.18Na 22.99Mg24.31Al26.98Si28.09P30.97S32.07Cl35.45Ar39.95K 39.10Ca40.08Sc44.96Ti47.88V50.94Cr52.00Mn54.94Fe55.85Co58.93Ni58.69Cu63.55Zn65.39Ga69.72Ge72.61As74.92Se78.96Br79.90Kr83.80Rb 85.47Sr87.62Y88.91Zr91.22Nb92.91Mo95.94Tc[98]Ru101.1Rh102.9Pd106.4Ag107.9Cd112.4In114.8Sn118.7Sb121.8Te127.6I126.9Xe131.3Cs 132.9Ba137.3La-LuHf178.5Ta180.9W183.8Re186.2Os190.2Ir192.2Pt195.1Au197.0Hg200.6Tl204.4Pb207.2Bi209.0Po[210]At[210]Rn[222]Fr [223]Ra[226]Ac-La......................一、本题包括25小题,每小题2分,共50分。
每小题有1个或2个选项符合题意。
若该题只有1个选项合题意,多选或错选均不得分。
若该题有2个选项合题意,选对1个得1分,选对2个得2分;选错1个,该题不得分。
⒈我国有些煤矿的坑道中具有丰富的可燃性气体。
目前已建成利用坑道气的发电厂,这样既充分利用了能源,又保证了煤矿的安全生产,坑道中的可燃性气体是A.H2B.COC.CH4D. CH4和CO的混合气体⒉A是烷烃,B是单烯烃,B分子中的碳原子数比A分子中多。
常温下1L该混合气体充分燃烧可得到同温同压下的二氧化碳气体2.5L,则原混合气体中A和B的组合方式可能有A.2和B.3和C.4和D.5和⒊某种混合气体,可能含有N2、HCl、CO。
全国高中学生化学竞赛(安徽赛区)初赛试题及参考答案
2012年全国高中学生化学竞赛(安徽赛区)初赛试题注意:考试时间3小时,满分150分。
直接在试卷上答题,允许使用非编程计算器。
第一大题(选择题)答案写在下表..中,其余题答案写在试卷上1.为了缓解石油危机,科学家正在进行“生物质油”代替柴油的试验。
所谓“生物质油”是指以光合作用产生的植物、农作物等富含纤维素、半纤维素和木质素的物质为原料,采用生物热解液化技术而产生的新能源。
下列有关说法错误..的是 A 、生物质油是一种有机化合物 B 、这一类能源属于可再生能源 C 、利用生物质能就是间接利用太阳能D 、生物质油提炼技术中只要利用的是化学变化2.一块铜板被等分成两块,Cu(a)和Cu(b);锤打Cu(a),Cu(b)不动。
再由Cu(a)、Cu(b)及CuSO 4溶液组成电池:一、本题包括25小题,每小题2分,共50分。
每小题有1个或2个选项符合题意,若该题只有1个选项符合题意,多选或错选均不得分。
若该题有2个选项符合题意,选对1个得1分,选对2个得2分;错选1个该题不得分。
Cu(a)|CuSO 4(c mol/L)|Cu(b),测得电动势E >0,因为Cu(a)的A .ΔS >0,ΔH =0B .ΔS >0,ΔH <=0C .ΔS ><0,ΔH =0D .ΔS <0,ΔH <0 3.空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC ),RFC 是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。
下图为RFC 工作原理示意图,有关说法正确的是A 、当有0.1mol 电子转移时,a 电极产生1.12L H 2(标准状况下)B 、b 电极上发生的电极反应是: 4H 2O+4e -=2H 2↑+4OH -C 、c 电极上进行还原反应,B 电池中的H +可以通过 隔膜进入A 池D 、d 电极上发生的电极反应是:O 2+4H ++4e -=2H 2O 4.室温下,下列各组离子在指定溶液中一定能大量共存的是A .pH=12的溶液中:AlO 2-、Na +、SO 42-、SO 32-B .水电离出的c (H +)=10﹣12mol/L 的溶液中:K +、Na +、SO 42-、AlO 2-C .能与铝反应生成氢气的溶液中:Mg 2+、Na +、Cl -、NO 3-D .c (H +)=0.10mol/L 的溶液中:CH3COO -、NH 4+、Cl -、Na +5.已知化学反应A 2(g)+B 2(g)=2AB(g)的能量变化如右图所示,下列叙述中正确的是A .每生成2分子AB 吸收bkJ 热量 B .该反应焓变为ΔH=+(a -b)kJ/molC .该反应中反应物的总能量高于生成物的总能量D .断裂1molA -A 键和1molB -B 键,放出a kJ 能量6.中学化学教材中有大量的数据教材,下面是某学生对数据的利用情况,其中错误..的是 A .利用K sp 数据可判断BaCO 3与NaCO 3溶液能否反应 B .利用沸点数据可推测将一些液体混合物分离出来的可能性 C .利用第一电离能数据可判断同周期元素的金属性强弱 D .利用液体密度可以判断液体物质挥发的难易7.As 2S 3和HNO 3有如下反应:As 2S 3+10H -++10NO 3-→2H 3AsO 4+3S+10NO 2↑+2H 2O ,下列说法正确的是能量(kJ ·mol -1)1molA 2 1molB 22molABabA .生成1molH 3AsO 4时,转移电子个数为10N AB .将该反应设计成一原电池,则NO 2应该在正极附近逸出C .该反应的氧化产物之一为SD .反应产物NO 2与11.2LO 2(标准状况)混合后用水吸收全部转化为浓HNO 3,然后与过量的碳反应,所产生的CO 2的量为0.5mol 8.关于下列各装置的叙述中,错误..的是 A .装置①中,d 为阳极、c 为阴极 B .装置②可用于收集H 2、CO 2 C .装置③中X 若为CCl 4,可用于吸收 氨气或氯化氢,并能防倒吸D .装置④可用于干燥、收集NH3,并吸收多余的氨气9.可逆反应2A(g)+B(g) 2C(g),根据下表中的数据判断下列图像错误..的是A .B .C .D .10.能正确表示下列反应的离子方程式的是A .足量的硫酸铝溶液与纯碱溶液反应:2Al 3++3CO 32-+3H 2O =2Al(OH)3+3CO 2↑ B .NaHS 溶液的水解方程式:HS ﹣+H 2O H 3O ++S 2﹣C .Fe(OH)3与足量的HI 溶液反应:Fe(OH)3+3H +=Fe 3++3H 2OD .向饱和亚硫酸氢钠溶液中加入足量的NaOH 溶液:Ba 2++2HSO 3-+2OH -=BaSO 3+2H 2O+SO 32-11.在室温下,向氢硫酸中通入二氧化硫气体,溶液的pH 发生变化。
安徽省高中化学竞赛初赛试题及答案

2004年全国中学生化学竞赛(安徽赛区)初赛试题一、本题包括25小题,每小题2分,共50分。
每小题有1个或2个选项符合题意。
若该题只有1个选项符合题意,多选或错选均不得分。
若该题有2个选项符合题意,选对1个得1分,选对2个得2分;选错1个,该题不得分。
1.下列卤素互化物中,最不稳定的是(A)ClI3(B)ClF3(C)BrF3(D)ICl32.下列各结构式中,最有可能的N2OLewis结构式为(A)N=N=O —O (C)N—(D)N=O=N3.下列各金属碳化物中,与水反应能生成C3H4的是(A)Be2C (B)Na2C3(C)Mg2C3(D)A14C34.在一定温度下,某浓度的硝酸与金属锌反应,生成NO2和NO的物质的量之比为1:3 则要使1摩金属锌完全反应,需要HNO3的物质的量为(A)0.8 (B)2.4 (C)2.6 (D)2.85.在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g) A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡。
下列说法中正确的是(A)平均反应速度:乙>甲(B)平衡时nc(甲)>nc(乙)(C)平衡时C的转化率:乙>甲(D)平衡时A的物质的量甲>乙6.对手由CrO42—转化为Cr2O72—的下列各叙述中,正确的是(A)这是Lewis酸碱反应(B)这是氧化还原反应(C)加酸,该反应向右移动(D)加酸,该反应向左移动7.在水溶液中,KHSO3(aq)的电荷平衡式为(A)[H3O+]十[K+]=[OH—]+[HSO3—]+[SO32—](B) [H3O+]十[K+]=[OH—]+[HSO3—]+2[SO32—](C) [H3O+]十[K+]=[OH—]+[HSO3—]+1/2[SO32—](D) [H3O+]十2[K+]=[OH—]+[HSO3—]+2[SO32—]8.下列各组离子中,能在强碱性溶液中共存,且在滴加盐酸过程中会生成气体和沉淀的是(A)Na+、CrO2—、SO42—、CO32—(B)NH4+、A1O2—、SO42—、CO32—(C)K+、A1O2—、SO42—、HCO3—(D)K+、ZnO2—·、SO42—、CO32—9.已知Al和Ga是同族元素,且都是两性元素,并知A1(OH)3的碱性比Ga(OH)3大。
2007年安徽省怀宁中学高二化学竞赛试卷

1.008Zr Nb Mo Tc Ru Rh P d Ag CdIn Sn Sb Te I Hf Ta W Re Os Ir P t Au Hg Tl P b Bi P o At Ac-Lr HLi BeB C N O F Na MgAl Si P Cl S K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Rb Cs Fr Sr BaRaY La Lu -6.9419.01222.9924.3139.1040.0885.4787.62132.9137.3[223][226]44.9647.8850.9452.0054.9455.8558.9363.5558.6965.3910.8126.9869.7212.0128.0972.61114.8204.4118.7207.2112.4200.6107.9197.0106.4195.1102.9192.2101.1190.298.91186.295.94183.992.91180.991.22178.588.9114.0116.0019.0030.9774.92121.8209.032.0778.96127.6[210][210][210]126.979.9035.454.00320.1839.9583.80131.3[222]He Ne Ar Kr Xe Rn 相对原子质量Rf Db Sg Bh Hs Mt第Ⅰ卷 选择题(共80分 请将答案填在答题卡上)一、选择题(本题包括20小题,每小题3分,共60分,每小题只有一个选项符合题意)1.以下说法正确的是 ( )A 纳米材料是一种称为“纳米”的新物质制成的材料B 绿色食品是指不含任何化学物质的食品C 生物固氮是指植物通过叶面直接吸收空气中的氮气D 光导纤维是以二氧化硅为主要原料制成的2、某同学在实验报告中记录下列数据,其中正确的 ( ) A 、用25mL 量筒量取12.36mL 盐酸B 、用托盘天平称取8.75克食盐C 、用标准的NaOH 溶液滴定未知浓度的盐酸,用去NaOH 溶液23.10mLD 、用广泛pH 试纸测得某溶液pH 为3.5 3.用石灰水保存鲜蛋是一种化学保鲜法。
近几年全国高中学生化学竞赛(安徽赛区)初赛试题【精美Word版含答案】

乱shi 佳人编辑整理学校 班级 考号 姓名_________________试场号______________装订线内不要答题 ◆◆◆◆◆◆◆◆◆◆◆◆◆装◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆订◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆线◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆◆2010年全国高中学生化学竞赛(安徽赛区)初赛试题注意:考试时间3小时,满分150分。
直接在试卷上答题,允许使用非编程计算器。
1. 化学作为一门实用性很强的学科与社会、环境等密切相关。
下列有关说法中正确的是( ) A 、“低碳经济”主要是指减少对化石能源的依赖B 、光导纤维主要成分是晶体硅C 、制作航天服的聚酯纤维属于有机高分子化合物D 、甲型H1N1流感病毒的蛋白质由C 、H 、O 元素组成 2.下列溶液中,一定能大量共存的离子组是( ) A 、pH=1的溶液中:Na +、Mg 2+、SO 42- 、HCO 3-B 、含有大量Fe 3+的溶液中:Al 3+、Cu 2+、Cl - 、SO 42- C 、加入铝能放出H 2的溶液中:K + 、NH 4+ 、NO 3- 、Cl -D 、水电离产生的c (H +)=10-12mol ²L -1的溶液中:K + 、Ba 2+ 、NO 3- 、OH - 3.用N A 表示阿伏伽德罗常数,一下叙述正确的是( )A 、1mol 甲烷中的氢原子被氯原子完全取代,需要氯气分子数为2N AB 、1.7g H 2O 2中含有的电子数为0.9N AC 、2mol 的NO 2与水完全反应转移电子数为N AD 、在pH=13的NaOH 溶液中,OH -数目为0.1 N A一、本题包括25小题,每小题2分,共50分。
每小题有1个或2个选项符合题意,若该题只有1个选项符合题意,多选或错选均不得分。
若该题有2个选项符合题意,选对1个得1分,选对2个得2分;错选1个该题不得分。
4.科学解释能力是科学素养的重要组成部分。
年全国中学生化学竞赛初赛试题

年全国中学生化学竞赛(安徽赛区)初赛试卷一、本题包括小题,每小题分,共分。
每小题有个或个选项符合题意。
若该题只有个选项符合题意,多选或错选均不得分。
若该题有个选项符合题意,选对个得分,选对个得分;选错个,该题不得分。
.下列卤素互化物中,最不稳定的是() () () ().下列各结构式中,最有可能的结构式为() ()().下列各金属碳化物中,与水反应能生成的是() () () ().在一定温度下,某浓度的硝酸与金属锌反应,生成和的物质的量之比为则要使摩金属锌完全反应,需要的物质的量为() () () ().在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充有气体,若发生可逆反应() ()(),经一段时间后,甲、乙两容器反应都达到平衡。
下列说法中正确的是()平均反应速度:乙>甲()平衡时(甲)>(乙)()平衡时的转化率:乙>甲()平衡时的物质的量甲>乙.对手由—转化为—的下列各叙述中,正确的是()这是酸碱反应()这是氧化还原反应()加酸,该反应向右移动()加酸,该反应向左移动.在水溶液中,()的电荷平衡式为()[]十[][—][—][—]() []十[][—][—][—]() []十[][—][—][—]() []十[][—][—][—].下列各组离子中,能在强碱性溶液中共存,且在滴加盐酸过程中会生成气体和沉淀的是()、—、—、—()、—、—、—()、—、—、—()、—·、—、—.已知和是同族元素,且都是两性元素,并知()的碱性比()大。
若将等物质的量的的和溶于溶液中,然后再通入,则()()先沉淀()()和()同时沉淀出来()()先沉淀()无法判断两种沉淀的先后次序.在抢救大出血的病危病人时,常需静脉点滴.%氯化钠溶液(从俗称“生理盐水’’),是由于人体血液的“矿化度”(即无机盐的含量)为.%。
全国高中化学竞赛(安徽赛区)初赛试题及参考标准答案

年全国高中化学竞赛(安徽赛区)初赛试题及参考答案————————————————————————————————作者:————————————————————————————————日期:22001年全国高中化学竞赛(安徽赛区)初赛试题(考试时间3小时,满分150分)注意:⒈本试卷分试题卷和答题卷两部分,所有的答案必须写在答题卷上,写在试题卷上无效......................。
⒉考生开始答题前,请先将答题卷上密封线内的项目填写完整。
⒊有关计算中,请遵循近似数计算法则。
H1.008 元素周期表He 4.003Li 6.941Be9.012B10.81C12.01N14.01O16.00F19.00Ne20.18Na 22.99Mg24.31Al26.98Si28.09P30.97S32.07Cl35.45Ar39.95K 39.10Ca40.08Sc44.96Ti47.88V50.94Cr52.00Mn54.94Fe55.85Co58.93Ni58.69Cu63.55Zn65.39Ga69.72Ge72.61As74.92Se78.96Br79.90Kr83.80Rb 85.47Sr87.62Y88.91Zr91.22Nb92.91Mo95.94Tc[98]Ru101.1Rh102.9Pd106.4Ag107.9Cd112.4In114.8Sn118.7Sb121.8Te127.6I126.9Xe131.3Cs 132.9Ba137.3La-LuHf178.5Ta180.9W183.8Re186.2Os190.2Ir192.2Pt195.1Au197.0Hg200.6Tl204.4Pb207.2Bi209.0Po[210]At[210]Rn[222]Fr [223]Ra [226]Ac-La一、本题包括5小题,每小题1分,共5分。
每小题只有一个选项符合题意。
⒈下列各组离子中,能大量共存的是A.H+、Cl-、HPO42-、K+B.OH-、Zn2+、Al3+、Mn2+C.OH-、HPO42-、Na+、SO42-D.OH-、CO32-、AlO2-、Na+⒉现有X、Y、Z、W四种主族元素。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2007年全国高中学生化学竞赛(安徽赛区)初赛试题(考试时间3小时,满分150分)注意:答案必须写在答题卷上,写在试卷上无效。
......................一、本题包括25小题,每小題2分,共50分。
每小题有1个或2个选项符合题意。
若该题只有1个选项符合题意,多选或错选均不得分。
若该题有2个选项符合题意,选对1个得1分,选对2个得2分;选错1个,该题不得分。
1.空气中含有NO x 、CO 2、CH 4、O 3、含氟化合物等等会引起光化学污染、空洞效应、温室效应等破坏环境的作用。
下列气体中产生温室效应最大的气体是 A .CO 2 B .CH 4 C . NO x D. CCl 2F 2 2.物质的量浓度相同时,下列溶液既能与NaOH(aq)反应,又能与盐酸反应且pH 值最大的是A .Na 2CO 3(aq) B. NH 4HCO 3(aq) C. NaHCO 3(aq) D .NaHSO 4(aq) 3.下列叙述中,不正确的是A.目前加碘食盐中,主要添加的是KIO 3 B .绿色食品是不含任何化学物质的食品 C .硅材料广泛用于光纤通讯 D .增加植被,保护环境是人类生存的需要 4.三聚氰酸[C 3N 3(OH)3]可用于消除汽车尾气中的NO 2。
其反应原理为:C 3N 3(OH)3−→−∆HNCO HNCO +NO 2−→−∆N 2+CO 2+H 2O 下列说法中正确的是A. C 3N 3(OH)3与HNCO 为同一种物质B. HNCO 是一种很强的氧化剂C. 反应中NO 2是还原剂 D .1mol NO 2在反应中转移4mol 电子 5.X 、Y 为短周期元素,X 位于IA 族,X 与Y 可形成化合物X 2Y ,下列说法中正确的是 A. X 2Y 可能是离子化合物,也可能是共价化合物B .两元素形成的化合物中,原子个数比不可能为1:1C . X 的原子半径一定大于Y 的原子半径D . X 与Y 的简单离子不可能具有相同的电子层结构 6.氯气溶于水达到平衡后,若其它条件不变,只改变某一条件,下列叙述正确的是A. 再通入少量氯气,[H +]/[ClO -]减少B. 加入少量水,水的电离平衡向正反应方向移动C. 通入少量SO 2,溶液漂白性增强D. 加入少量固体NaOH ,一定有[Na +]=[Cl -]+[ClO -]7.下列实验操作中,符合“绿色化”的有:①在萃取操作的演示实验中,将CCl 4萃取溴水,改为CCl 4萃取碘水; ②在铜与浓硝酸反应的实验中,将铜片改为可调节高度的铜丝; ③将实验室的废酸液和废碱液中和后再排放;A.①和②B.①和③ C .②和③ D.①、②和③ 8.在[(OC)3Ni -Co(CO)3]x 中,x 应为A .+ B. - C.3- D. 3+9.下列离子方程式中,正确的是A. NaHCO 3(aq)中加入过量的Ba(OH)2(aq): 2HCO 3-+Ba 2++2OH -=BaCO 3↓B .氢氧化钡溶液与稀硫酸反应: Ba 2++SO 42-+H ++OH -=BaSO 4↓+H 2OC.NaNO 2(aq)中加入酸性KMnO 4(aq) 2MnO 4-+5NO 2-+6H +=2Mn 2++5NO 3-+3H 2OD .Fe(NO 3)3(aq)加入过量的KI(aq) 2Fe 3++2I -=2Fe 2++I 210.核磁共振(NMR )技术已广泛应用于复杂分子结构的测定和医学论断等高科技领域。
已知:只有质子数或中子数为奇数的原子核有核磁共振(NMR )现象。
则下列哪组原子均可产生NMR 现象A .18O 、31P 、119Sn C .元素周期表中第1周期所有元素的原子B .27Al 、19F 、12CD .元素周期表中V A 族所有元素的原子 11.某无色溶液能与铝反应放出氢气,该溶液中肯定不能大量共存的离子组是A. Na +、Fe 2+、NO 3-、K +B. HCO 3-、K +、NO 3-、SO 42-C. SO 42-、Cl -、CO 32-、Na +D. NH 4+、Cl -、Na +、Ba 2+12. 2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200o C 左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全。
电池总反应为:C 2H 5OH +3O 22CO 2 +3H 2O , 电池示意如右图,下列说法不正确...的是 A.a 极为电池的负极B.电池工作时电流由b 极沿导线经灯泡再到a 极C.电池正极的电极反应为:4H + + O 2 + 4e -== 2H 2OD.电池工作时,1mol 乙醇被氧化时就有6mol 电子转移13.下列溶液中,微粒的物质的量浓度关系正确的是A. 1.0 mol·L -1的Na 2CO 3(aq):[OH -]=[HCO 3-]+[H +]+2[H 2CO 3]B .1.0 mol·L -1的NH 4Cl(aq):[NH 4+]=[Cl -]C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:[Na +]>[CH 3COO -]> [H +]>[OH -]D .向硝酸钠溶液中滴加稀盐酸,得到pH =5的混合溶液:[Na +]=[NO 3-] 14.反应X (g )+3Y (g )2Z (g );ΔH <0,在不同温度、不同压强(P 1>P 2)φ(Z)(Z)(Z)下,达到平衡时,混合气体中Z 的体积分数φ(Z )随温度变化的曲线应为A B C D15.下列物种中,不属于C 3O 2的等电子体的是A .N 5+ B. C 2NO 2+ C .NCN 2O D .NC 3O -16.(H 3C)NCO 分子可能的共振结构式的数目有A . 1B . 2C . 3D . 417.下列溶液中,能使H 2S 生成S 的溶液是A.FeCl 3B.Fe 2(SO 4)3C.K 3[Fe(CN)6]和NaHCO 3D. K 3[Fe(CN)6]和Na 2CO 318.关于下列各装置图的叙述中,不正确的是A .装置①中,d 为阳极、c 为阴极B .装置②可用于收集H 2、NH 3、CO 2、Cl 2、HCl 、NO 2等气体C .装置③中X 若为四氯化碳,可用于吸收氨气或氯化氢,并防止倒吸D .装置④可用于干燥、收集氨气,并吸收多余的氨气19.三种二氯代苯中,I :ClCl II:ClClIII:ClCl偶极距由大至小为:A. II>III>I B .III > II >I C .II >I>III D. I > II > III20.我国支持“人文奥运”的一个重要的体现是坚决反对运动员服用兴奋剂,某种兴奋剂的结构简式如右图,有关该物质的说法不正确的是 A .滴入酸性KMnO 4溶液,紫色褪去,可证明结 构中存在碳碳双键B .1mol 该物质与H 2(一定条件下)反应时,最 多消耗H 2的物质的量为7molC .该分子中所有的碳原子不可能在同一平面上D .该物质的化学式为C 20H 24O 321.下列化合物中,能与FeCl 3溶液发生颜色反应的是A . CH 3OCH 3B .NO 2C. CH 323 O OD.CH 322.反应 BrNaOH产物为A .B . C.BrOHD .BrOH23.下面反应可得到的产物是24.下列有机物中,可发生碘仿反应的化合物是A. CHOHCH 3 B.CH 3OHC.CH 3D .CH 3OH25.下列各对物质中,互为同分异构体的是 A.CH 3CH 2CH 2CH 3和CH 3CH =CHCH 3 B .CH 3CH =CHCH 3和 CH 3C≡CCH 3CH 3CH CHCH 3C.和 CH 3CH CCH 33CH 3CH 2CH 2OH 和CH 3CHCH 3D.二、本题包括6小题,共30分。
26. (5分)将KOH 和Ca(OH)2混合物1.86g 全部溶于一定量水中形成稀溶液,再缓缓通入足量的CO 2气体。
当生成沉淀的质量刚好最大时,消耗CO 2的体积为224mL (标准状况,忽略CO 2溶于水情况,以下情况相同。
) (1)原混合物中Ca(OH)2的质量为 g ;(2)沉淀恰好溶解时,消耗CO 2的体积为 mL ;(3)写出溶液中生成沉淀的质量m (g)与通入CO 2的体积V (mL)之间的函数表达式 ; (4)在图示坐标系上,画出生成沉淀的质量m (g)与通入CO 2的体积V (mL)的关系曲线。
CH 3CH CHCH 2Br H 2ONaOHCH 2CH CHCH 2Br A.CH 3CH CCH 3B.CH 3CH CHCH 3C.CH 3CH CHCH 2OH +D. CH 3CHCH CH 227.(8分)科学家发现C 60分子由60个碳原子构成,它的形状像足球(图C ),含有C=C 键,因此又叫足球烯。
1991年科学家又发现一种碳的单质——碳纳米管,是由六边环形的碳原子构成的具有很大表面积管状大分子(图D ),图A 、图B 分别是金刚石和石墨的结构示意图。
图中小黑点或小黑圈均代表碳原子。
(1)金刚石、石墨、足球烯和碳纳米管四种物质互称为同素异形体,它们在物理性质上存在较大的差异,其原因是 ;(2)相同条件下,足球烯、石墨分别和气体单质F 2反应时,化学活泼性的比较为足球烯比石墨 (填“活泼”、“一样活泼”、“更不活泼”)理由是: ; (3)由右边石墨的晶体结构俯视图可推算在石墨晶体中,每个正六边 形平均所占有的C 原子数与C —C 键数之比为 ;(4)在金刚石的网状结构中,含有共价键形成的碳原子环、其中最小的环上有___个碳原子(填数字),每个碳原子上的任两 个C —C 键的夹角都是_____(填角度)。
(5)燃氢汽车之所以尚未大面积推广,除较经济的制氢方法尚未完全解决外,还需解决H 2的贮存问题,上述四种碳单质中有可能成为贮氢材料的是:_____。
(6)下列图象是从NaCl 或CsCl 晶体结构图中分割出来的部分结构图,试判断NaCl 晶体结构的图象是 。
A B C D28. (6分)在SeOF 6化合物中,Se 和O 的实际氧化数分别为 ① 、 ② ;Se 原子采用 ③ 杂化方式,其几何构型名称是 ④ 。
该化合物与苛性碱反应,其离子方程式为 ⑤ ,它 ⑥ (填是或不是)氧化还原反应。
29.(5分)在液态SO 2中,以物质的量比为1:1混合SbCl 3和GaCl 3得到一个化学式为GaSbCl 6的固态离子化合物。
其离子式为[SbCl 2+][GaCl 4-]或者[GaCl 2+][SbCl 4-],这两种阳离子的几何构型名称分别为 ① 和 ② ;这两种阴离子的几何构型名称分别为 ③ 和 ④ 。
