初中化学方程式总汇修订版学生
九年级化学反应方程式汇总

九年级化学反应方程式汇总1. 红磷燃烧:4P + 5O_2→(点燃)2P_2O_52. 硫燃烧:S + O_2→(点燃)SO_23. 铁燃烧:3Fe + 2O_2→(点燃)Fe_3O_44. 镁燃烧:2Mg + O_2→(点燃)2MgO5. 碳完全燃烧:C + O_2→(点燃)CO_26. 碳不完全燃烧:2C + O_2→(点燃)2CO7. 氢气燃烧:2H_2 + O_2→(点燃)2H_2O8. 实验室用过氧化氢制氧气:2H_2O_2stackrel{MnO_2}{===}2H_2O + O_2↑9. 实验室用氯酸钾制氧气:2KClO_3stackrel{△、MnO_2}{===}2KCl + 3O_2↑10. 实验室用高锰酸钾制氧气:2KMnO_4→(△)K_2MnO_4 + MnO_2 + O_2↑11. 水通电分解:2H_2O→(通电)2H_2↑ + O_2↑12. 氢气还原氧化铜:H_2 + CuO→(△)Cu + H_2O13. 碳还原氧化铜:C + 2CuO→(高温)2Cu + CO_2↑14. 一氧化碳还原氧化铜:CO + CuO→(△)Cu + CO_215. 二氧化碳与水反应:CO_2 + H_2O = H_2CO_316. 碳酸分解:H_2CO_3 = H_2O + CO_2↑17. 二氧化碳通入澄清石灰水:CO_2 + Ca(OH)_2 = CaCO_3↓ + H_2O18. 实验室制取二氧化碳:CaCO_3 + 2HCl = CaCl_2 + H_2O + CO_2↑19. 高温煅烧石灰石:CaCO_3→(高温)CaO + CO_2↑20. 一氧化碳燃烧:2CO + O_2→(点燃)2CO_221. 氢氧化钠与二氧化碳反应:2NaOH + CO_2 = Na_2CO_3 + H_2O22. 一氧化碳还原氧化铁:3CO + Fe_2O_3→(高温)2Fe + 3CO_223. 锌与稀硫酸反应:Zn + H_2SO_4 = ZnSO_4 + H_2↑24. 铁与稀硫酸反应:Fe + H_2SO_4 = FeSO_4 + H_2↑25. 镁与稀硫酸反应:Mg + H_2SO_4 = MgSO_4 + H_2↑26. 铝与稀硫酸反应:2Al + 3H_2SO_4 = Al_2(SO_4)_3 + 3H_2↑27. 锌与稀盐酸反应:Zn + 2H Cl = ZnCl_2 + H_2↑28. 铁与稀盐酸反应:Fe + 2HCl = FeCl_2 + H_2↑29. 镁与稀盐酸反应:Mg + 2HCl = MgCl_2 + H_2↑30. 铝与稀盐酸反应:2Al + 6HCl = 2AlCl_3 + 3H_2↑31. 铁与硫酸铜溶液反应:Fe + CuSO_4 = FeSO_4 + Cu32. 铜与硝酸银溶液反应:Cu + 2AgNO_3 = Cu(NO_3)_2 + 2Ag。
初中常见化学方程式大全-完美版

初中常见化学方程式初中化学方程式全(已配平)。
一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃 2MgO2、铁在氧气中燃烧:3Fe +2O2点燃 Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃 2Al2O34、氢气在空气中燃烧:2H2 +O2点燃 2H2O5、红磷在空气中燃烧:4P +5O2点燃 2P2O56、硫粉在空气中燃烧: S+ O2点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2C +O2点燃 2CO9、二氧化碳通过灼热碳层: C +CO2高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O = H2CO312、生石灰溶于水:CaO+ H2O = Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 +5H2O = CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 +O2↑17、水在直流电的作用下分解:2H2O 通电 2H2↑+O2↑18、碳酸不稳定而分解:H2CO3 = H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温 CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 = FeSO4 +Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4 = ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl = MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4 +2O2 点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2 +CO27、焦炭还原氧化铁:3C +2Fe2O3高温 4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4 = Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O30、酒精在空气中燃烧:C2H5OH+ 3O2点燃 2CO2 +3H2O31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe+ 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+ CO2 = CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 = Na2CO3 +H2O35、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl = CaCl2 +H2O +CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理):Na2CO3+ 2HCl = 2NaCl +H2O +CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1。
初中化学方程式大全(免费修订版)

化学方程式大全一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg + O2点燃2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃Fe3O43. 铜在空气中受热:2Cu + O2 △2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 + O2点燃2H2O6. 红磷在空气中燃烧:4P + 5O2点燃2P2O57. 硫粉在空气中燃烧:S + O2点燃SO28. 碳在氧气中充分燃烧:C + O2点燃CO29. 碳在氧气中不充分燃烧:2C + O2点燃2CO (2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2点燃2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验2HgO △2Hg+ O2 ↑14.加热高锰酸钾:2KMnO4△K2MnO4 + MnO2 + O2↑15.过氧化氢在二氧化锰作催化剂条件下分解反应:H2O2 MnO2 2H2O+ O2 ↑二、自然界中的水:16.电解水:2H2O 通电2H2↑+ O2 ↑17.生石灰溶于水:CaO + H2O = Ca(OH)218.二氧化碳可溶于水:H2O + CO2=H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg + O2 点燃2MgO20.铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu21.氢气还原氧化铜:H2 + CuO △Cu + H2O22. 镁还原氧化铜:Mg + CuO △Cu + MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃CO224.木炭还原氧化铜:C+ 2CuO 高温2Cu + CO2↑25.焦炭还原氧化铁:3C+ 2Fe2O3高温4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C + O2点燃CO227.煤炉的中层:CO2 + C 高温2CO28.煤炉的上部蓝色火焰的产生:2CO + O2点燃2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑30.碳酸不稳定而分解:H2CO3 = H2O + CO2↑31.二氧化碳可溶于水:H2O + CO2=H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温CaO + CO2↑33.石灰水与二氧化碳反应:Ca(OH)2 + CO2 = CaCO3↓+ H2O (4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO △Cu + CO235.一氧化碳的可燃性:2CO + O2点燃2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理): Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 + 2O2点燃CO2 + 2H2O38.酒精在空气中燃烧:C2H5OH + 3O2点燃2CO2 + 3H2O39.氢气中空气中燃烧:2H2 + O2点燃2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg + O2点燃2MgO41.铁在氧气中燃烧:3Fe + 2O2点燃Fe3O442. 铜在空气中受热:2Cu + O2 △2CuO43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3(2)金属单质+ 酸-------- 盐+ 氢气(置换反应)44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑48. 锌和稀盐酸Zn + 2HCl = ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl =FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl = MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl =2AlCl3 + 3 H2↑(3)金属单质+ 盐(溶液)------- 新金属+ 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 =ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2= Cu(NO3)2 + Hg (3)金属铁的治炼原理:55.3CO+ 2Fe2O3高温4Fe + 3CO2↑七、酸、碱、盐56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl =2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl =CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 =CuSO4 + H2O(3)酸+ 碱-------- 盐+ 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH = NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 = CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 = AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH =Na2SO4 + 2H2O(4)酸+ 盐-------- 另一种酸+ 另一种盐64.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 2、碱的化学性质(1)碱+ 非金属氧化物-------- 盐+ 水68.苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 =Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 = CaCO3↓+ H2O 72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3↓+ H2O (2)碱+ 酸-------- 盐+ 水(中和反应,方程式见上)(3)碱+ 盐-------- 另一种碱+ 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液)+ 金属单质------- 另一种金属+ 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu(2)盐+ 酸-------- 另一种酸+ 另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl =2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑(3)盐+ 碱-------- 另一种碱+ 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH (4)盐+ 盐----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 =AgCl↓+ NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓+ 2NaCl。
初中化学方程式大全(免费修订版)[1]1
![初中化学方程式大全(免费修订版)[1]1](https://img.taocdn.com/s3/m/32d6141d6bd97f192279e9e3.png)
化学方程式大全一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg + O2点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43. 铜在空气中受热:2Cu + O2 △ 2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2点燃 2H2O6. 红磷在空气中燃烧:4P + 5O2点燃 2P2O57. 硫粉在空气中燃烧: S + O2点燃 SO28. 碳在氧气中充分燃烧:C + O2点燃 CO29. 碳在氧气中不充分燃烧:2C + O2点燃 2CO (2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2点燃 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO △ 2Hg+ O2 ↑14.加热高锰酸钾:2KMnO4△ K2MnO4 + MnO2 + O2↑15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2 MnO2 2H2O+ O2 ↑二、自然界中的水:16.电解水:2H2O 通电 2H2↑+ O2 ↑17.生石灰溶于水:CaO + H2O = Ca(OH)218.二氧化碳可溶于水: H2O + CO2=H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg + O2 点燃 2MgO20.铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu21.氢气还原氧化铜:H2 + CuO △ Cu + H2O22. 镁还原氧化铜:Mg + CuO △ Cu + MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃 CO224.木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO2↑25.焦炭还原氧化铁:3C+ 2Fe2O3高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C + O2点燃 CO227.煤炉的中层:CO2 + C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO + O2点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑30.碳酸不稳定而分解:H2CO3 = H2O + CO2↑31.二氧化碳可溶于水: H2O + CO2=H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温 CaO + CO2↑33.石灰水与二氧化碳反应:Ca(OH)2 + CO2 = CaCO3↓+ H2O (4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO △ Cu + CO235.一氧化碳的可燃性:2CO + O2点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理): Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 + 2O2点燃 CO2 + 2H2O38.酒精在空气中燃烧:C2H5OH + 3O2点燃 2CO2 + 3H2O39.氢气中空气中燃烧:2H2 + O2点燃 2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg + O2点燃 2MgO41.铁在氧气中燃烧:3Fe + 2O2点燃 Fe3O442. 铜在空气中受热:2Cu + O2 △ 2CuO43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3(2)金属单质 + 酸 -------- 盐 + 氢气(置换反应)44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑48. 锌和稀盐酸Zn + 2HCl = ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl =FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl = MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl =2AlCl3 + 3 H2↑(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 =ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2= Cu(NO3)2 + Hg (3)金属铁的治炼原理:55.3CO+ 2Fe2O3高温 4Fe + 3CO2↑七、酸、碱、盐56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl =2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl =CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 =CuSO4 + H2O(3)酸 + 碱 -------- 盐 + 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH = NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 = CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 = AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH =Na2SO4 + 2H2O(4)酸 + 盐 -------- 另一种酸 + 另一种盐64.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 2、碱的化学性质(1)碱 + 非金属氧化物 -------- 盐 + 水68.苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 =Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 = CaCO3↓+ H2O72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3↓+ H2O (2)碱 + 酸-------- 盐 + 水(中和反应,方程式见上)(3)碱 + 盐 -------- 另一种碱 + 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液) + 金属单质------- 另一种金属 + 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu(2)盐 + 酸-------- 另一种酸 + 另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl =2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑(3)盐 + 碱 -------- 另一种碱 + 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH (4)盐 + 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 =AgCl↓ + NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl。
初中化学方程式大全(修订版)

48. 锌和稀盐酸Zn + 2HCl = ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl =FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl = MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl =2AlCl3 + 3 H2↑(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 =ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2= Cu(NO3)2 + Hg (3)金属铁的治炼原理:55.3CO+ 2Fe2O3高温 4Fe + 3CO2↑七、酸、碱、盐56. 氧化铁和稀盐酸反应:Fe2O3 + 6HCl =2FeCl3 + 3H2O57. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反应:CuO + 2HCl =CuCl2 + H2O59. 氧化铜和稀硫酸反应:CuO + H2SO4 =CuSO4 + H2O(3)酸 + 碱 -------- 盐 + 水(中和反应)60.盐酸和烧碱起反应:HCl + NaOH = NaCl +H2O61. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 = CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 = AlCl3 + 3H2O63. 硫酸和烧碱反应:H2SO4 + 2NaOH =Na2SO4 + 2H2O(4)酸 + 盐 -------- 另一种酸 + 另一种盐64.大理石与稀盐酸反应:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 2、碱的化学性质(1)碱 + 非金属氧化物 -------- 盐 + 水68.苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 =Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 = CaCO3↓+ H2O72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3↓+ H2O(2)碱 + 酸-------- 盐 + 水(中和反应,方程式见上)(3)碱 + 盐 -------- 另一种碱 + 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液) + 金属单质------- 另一种金属 + 另一种盐74. 铁和硫酸铜溶液反应:Fe + CuSO4 = FeSO4 + Cu(2)盐 + 酸-------- 另一种酸 + 另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 + 2HCl =2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反应:NaHCO3 + HCl= NaCl + H2O + CO2↑(3)盐 + 碱 -------- 另一种碱 + 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH (4)盐 + 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 =AgCl↓ + NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl。
初中化学方程式大全(免费修订版)

2
)HO(uC 铜化氧氢�淀沉色蓝源自;粉铁、锰化氧二、铁三化氧四、铜化氧、炭木�体固色黑 色无液溶、体液、体气分部大�色白体固分部大
色颜的质物见常
3 2
OCaC
钙酸碳 钙化氧氢 钙化氧 钠氢酸碳 汞 碳化氧二态固 硫 名学
石灰石 、灰石熟 灰石生 打苏小 银水 冰干 磺硫 名俗
4
HC
烷甲 钠化氯 酸乙 钠酸碳 钠化氧氢 醇乙 碳 名学
3
ONaN + ↓lCgA= 3ONgA + lCaN�液溶银酸硝和液溶钠化氯�77
盐新种两 ----- 盐 + 盐�4�
HOaN2 +↓3OCaC= 3OC2aN + 2)HO(aC�钠酸碳与钙化氧氢 .67
盐种一另 + 碱种一另 -------- 碱 + 盐�3�
↑2OC + O2H + lCaN =lCH + 3OCHaN�应反酸盐稀与钠氢酸碳 ↑2OC + O2H + lCaN2= lCH2 + 3OC2aN :应反酸盐稀与钠酸碳�57
3 2
O lA2 = 2O3 + lA4�膜化氧成形中气空在铝 .34 OuC2 △ 2O + uC2�热受中气空在铜 .24
4 3
O eF 燃点 2O2 + eF3�烧燃中气氧在铁 �14 OgM2 燃点 2O + gM2�烧燃中气空在镁 �04 �应反气氧与属金�一�
属金、六
O2H2 燃点 2O + 2H2�烧燃中气空中气氢 �93 O2H3 + 2OC2 燃点 2O3 + HO5H2C�烧燃中气空在精酒�83 O2H2 + 2OC 燃点 2O2 + 4HC�烧燃中气空在烷甲�73
初中化学方程式大全
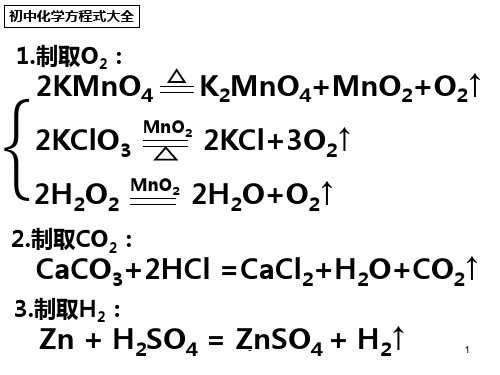
等等。。。
-
13
15、碱与铵盐反应: Ca(OH)2+2NH4Cl =CaCl2+2NH3↑+2H2O
Ca(OH)2+2NH4NO3=Ca(NO3)2+2NH3↑+2H2O
Ca(OH)2+(NH4)2SO4 =CaSO4+2NH3↑+2H2O Ca(OH)2+(NH4)2CO3 =CaCO3+2NH3↑+2H2O
7、还原反应:(C、CO、H2具有还原性)
Fe2O3+3CO 高温 2Fe +3CO2 (炼铁原理)
2Fe2O3+3C 高温 4Fe +3CO2 Fe2O3+3H2 高温 2Fe +3H2O
CuO+CO △ Cu +CO2 CuO+H2 △ Cu +H2O
2CuO+C 高温 2Cu +CO2 (两种黑色固体反
-
7
活泼金属与稀盐酸或稀硫酸的反应:
Mg+2HCl =MgCl2+H2↑
Zn+2HCl =ZnCl2+H2↑ Fe+2HCl =FeCl2+H2↑ 2Al+6HCl =2AlCl3+3H2↑ Mg+H2SO4 =MgSO4 +H2↑ Zn+H2SO4 =ZnSO4 +H2↑ Fe+H2SO4 =FeSO4 +H2↑ 2Al+3H2SO4 =Al-2(SO4)3+3H2↑ 8
-பைடு நூலகம்
10
初中化学方程式大全修订版

44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3H2↑48. 锌和稀盐酸Zn + 2HCl = ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl =FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl = MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl =2AlCl3 + 3 H2↑〔3〕金属单质+ 盐〔溶液〕------- 新金属+ 新盐52. 铁和硫酸铜溶液反响:Fe + CuSO4 = FeSO4 + Cu53. 锌和硫酸铜溶液反响:Zn + CuSO4=ZnSO4 + Cu54. 铜和硝酸汞溶液反响:Cu + Hg(NO3)2= Cu(NO3)2 + Hg 〔3〕金属铁的治炼原理:55.3CO+ 2Fe2O3高温4Fe + 3CO2↑七、酸、碱、盐56. 氧化铁和稀盐酸反响:Fe2O3 + 6HCl =2FeCl3 + 3H2O57. 氧化铁和稀硫酸反响:Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O58. 氧化铜和稀盐酸反响:CuO + 2HCl =CuCl2 + H2O59. 氧化铜和稀硫酸反响:CuO + H2SO4 =CuSO4 + H2O〔3〕酸+ 碱-------- 盐+ 水〔中和反响〕60.盐酸和烧碱起反响:HCl + NaOH = NaCl +H2O61. 盐酸和氢氧化钙反响:2HCl + Ca(OH)2 = CaCl2 + 2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3= AlCl3 + 3H2O63. 硫酸和烧碱反响:H2SO4 + 2NaOH =Na2SO4 + 2H2O〔4〕酸+ 盐-------- 另一种酸+ 另一种盐64.大理石与稀盐酸反响:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑65.碳酸钠与稀盐酸反响: Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑66.碳酸氢钠与稀盐酸反响:NaHCO3 + HCl= NaCl + H2O + CO2↑67. 硫酸和氯化钡溶液反响:H2SO4 + BaCl2 == BaSO4 ↓+ 2HCl 2、碱的化学性质〔1〕碱+ 非金属氧化物-------- 盐+ 水68.苛性钠暴露在空气中变质:2NaOH + CO2 = Na2CO3 + H2O 69.苛性钠吸收二氧化硫气体:2NaOH + SO2 =Na2SO3 + H2O 70.苛性钠吸收三氧化硫气体:2NaOH + SO3 = Na2SO4 + H2O 71.消石灰放在空气中变质:Ca(OH)2 + CO2 = CaCO3↓+ H2O 72. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 = CaSO3↓+ H2O 〔2〕碱+ 酸-------- 盐+ 水〔中和反响,方程式见上〕〔3〕碱+ 盐-------- 另一种碱+ 另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH 3、盐的化学性质〔1〕盐〔溶液〕+ 金属单质------- 另一种金属+ 另一种盐74. 铁和硫酸铜溶液反响:Fe + CuSO4 = FeSO4 + Cu〔2〕盐+ 酸-------- 另一种酸+ 另一种盐75.碳酸钠与稀盐酸反响: Na2CO3 + 2HCl =2NaCl + H2O + CO2↑碳酸氢钠与稀盐酸反响:NaHCO3 + HCl= NaCl + H2O + CO2↑〔3〕盐+ 碱-------- 另一种碱+ 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 =CaCO3↓+ 2NaOH 〔4〕盐+ 盐----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl + AgNO3 =AgCl↓+ NaNO3 78.硫酸钠和氯化钡:Na2SO4 + BaCl2 == BaSO4↓+ 2NaCl。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学方程式小测
姓名:分数一.物质与氧气的反应:
(1)单质与氧气的反应:
1. 镁在空气中燃烧:
2. 铁在氧气中燃烧:
3. 铜在空气中受热:
4. 铝在空气中燃烧:
5. 氢气中空气中燃烧:
6. 红磷在空气中燃烧:
7. 硫粉在空气中燃烧:
8. 碳在氧气中充分燃烧:
9. 碳在氧气中不充分燃烧:
(2)化合物与氧气的反应:
10. 一氧化碳在氧气中燃烧:
11. 甲烷在空气中燃烧:
12. 酒精在空气中燃烧:
二.几个分解反应:
13. 水在直流电的作用下分解:
14 加热氯酸钾(有少量的二氧化锰):
15 加热高锰酸钾:
16 碳酸不稳定而分解:
17 高温煅烧石灰石:
三.几个氧化还原反应:
18 氢气还原氧化铜:
19 木炭还原氧化铜:
20 焦炭还原氧化铁:
21 焦炭还原四氧化三铁:
22 一氧化碳还原氧化铜:
23 一氧化碳还原氧化铁:
24 一氧化碳还原四氧化三铁:
四.单质、氧化物、酸、碱、盐的相互关系
(1)金属单质 + 酸 -------- 盐 + 氢气(置换反应)
25 锌和稀硫酸
26 铁和稀硫酸
27 镁和稀硫酸
28 铝和稀硫酸
29 锌和稀盐酸
30 铁和稀盐酸
31 镁和稀盐酸
32 铝和稀盐酸
(2)金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐
33 铁和硫酸铜溶液反应:
34 锌和硫酸铜溶液反应:
35 铜和硝酸汞溶液反应:
(3)碱性氧化物 +酸 -------- 盐 + 水
36 氧化铁和稀盐酸反应:
37 氧化铁和稀硫酸反应:
38 氧化钙和稀盐酸反应:
(4)酸性氧化物 +碱 -------- 盐 + 水
39性钠暴露在空气中变质:
40苛性钠吸收二氧化硫气体:
41苛性钠吸收三氧化硫气体:
42消石灰放在空气中变质:
(5)酸 + 碱 -------- 盐 + 水
43盐酸和烧碱起反应:
44盐酸和氢氧化铜反应:
45盐酸和氢氧化钙反应:
46盐酸和氢氧化铁反应:
47氧化铝药物治疗胃酸过多:
48酸和烧碱反应:
(6)酸 + 盐 -------- 另一种酸 + 另一种盐
49大理石与稀盐酸反应:
50碳酸钠与稀盐酸反应:
51酸和硝酸银溶液反应:
52酸和碳酸钠反应:
(7)碱 + 盐 -------- 另一种碱 + 另一种盐
53氧化钠与硫酸铜:
54氧化钠与氯化铁:
55氢氧化钙与碳酸钠:
(8)盐 + 盐 ----- 两种新盐
56化钠溶液和硝酸银溶液:
57硫酸钠和氯化钡:
五.其它反应:
58二氧化碳溶解于水:
59.石灰溶于水:
其他
60、氢氧化钠溶液与硫酸铜溶液反应:
61、甲烷在空气中燃烧:
62、酒精在空气中燃烧:
63、一氧化碳还原氧化铜:
64、一氧化碳还原氧化铁:
65、二氧化碳通过澄清石灰水(检验二氧化碳):
66、氢氧化钠和二氧化碳反应(除去二氧化碳):
67、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):
68、碳酸钠与浓盐酸反应(泡沫灭火器的原理):
Na2CO3 + 2HCl ===
69. 加热碱式碳酸铜:
70. 加热氯酸钾(有少量的二氧化锰):
71. 加热高锰酸钾:
72. 碳酸不稳定而分解:
73. 高温煅烧石灰石:
74. 氢气还原氧化铜:
75. 木炭还原氧化铜:
76. 焦炭还原氧化铁:
77. 焦炭还原四氧化三铁:
78. 一氧化碳还原氧化铜:
79. 一氧化碳还原氧化铁:
80. 一氧化碳还原四氧化三铁:81.苛性钠暴露在空气中变质:82.苛性钠吸收二氧化硫气体:83.苛性钠吸收三氧化硫气体:84.消石灰放在空气中变质:
85. 消石灰吸收二氧化硫:
86、氧化钙与水反应:
87、氢氧化钠与二氧化碳反应:
88、氧化钠与水反应:
89、铁与氧气反应:
90、铝与硫酸溶液反应:
91、氧化钙与水反应:
92、氧化铁与盐酸反应:
93、氧化铝与盐酸反应:
94、硫化氢与氢氧化钠溶液反应:
95、氯化铁与氢氧化钠溶液反应:
96、硫酸亚铁与氢氧化钠溶液反应:
97、氢氧化亚铁跟硫酸:
98、氢氧化铁加热分解:
99、实验室制取二氧化碳:
100、氢氧化铝与盐酸反应:。
