食品中叶酸的测定原始记录表格
叶酸测定

1.原理叶酸是酪乳酸杆菌(Lactobacillus casei, L. C,ATCC7469)生长所必需的营养素。
在一定条件下,L.C的生长繁殖与培养基中叶酸含量呈正比关系,细菌增殖的量以光密度值计,通过与标准曲线相比较,计算出样品中叶酸的含量。
2.适用范围参考《Methods of Vitamin Assay》,第4版。
本方法适用于各类食物中叶酸的测定。
检测限为0.1ng。
3.仪器与设备(1)恒温培养箱(2)离心机(3)高压消毒锅(4)震荡器(5)接种针和接种环(6)分光光度计4.试剂除特殊说明外,本实验中所有试剂均为分析纯,水为蒸馏水。
(1)菌种:酪乳酸杆菌(Lactobacillus casei, L.C, ATCC 7469)(2)磷酸缓冲液(0.05mol/L, pH6.8):称取4.35gNa3PO4·12H2O,10.39gNa2HPO4·7H2O溶解于800ml水中。
临用前用约5g抗坏血酸调节pH至6.8。
(注:叶酸对光、热敏感,易被氧化破坏,抗坏血酸有助于保护叶酸被氧化。
)(3)鸡胰酶溶液:称取100mg干燥的鸡胰酶(Difco公司)(注:含有叶酸轭合酶,用于水解叶酸多谷氨酸盐),加入20ml磷酸缓冲液制成匀浆,3000rpm离心10min,取上清液备用。
临用前现配。
(4)蛋白酶-淀粉酶溶液:分别称取200mg蛋白酶(Sigma公司)和淀粉酶(Sigma公司),加入20ml磷酸缓冲液制成匀浆,离心3000rpm10min,取上清液备用。
临用前配制。
(5) 2+8乙醇溶液:量取20ml无水乙醇溶液,加入80ml水混匀。
(6) 0.1mol/L NaOH: 称取0.4g氢氧化钠,加2+8乙醇溶液溶解并稀释至1L。
(7) 10mol/L NaOH。
称取400g氢氧化钠,加水溶解并稀释至1L。
(8)叶酸标准储备液(200mg/ml):准确称取200mg叶酸标准品(Sigma公司,纯度大于98%),用0.01mol/LNaOH溶解并定容至1L。
食品中亚硝酸盐含量测定原始记录表
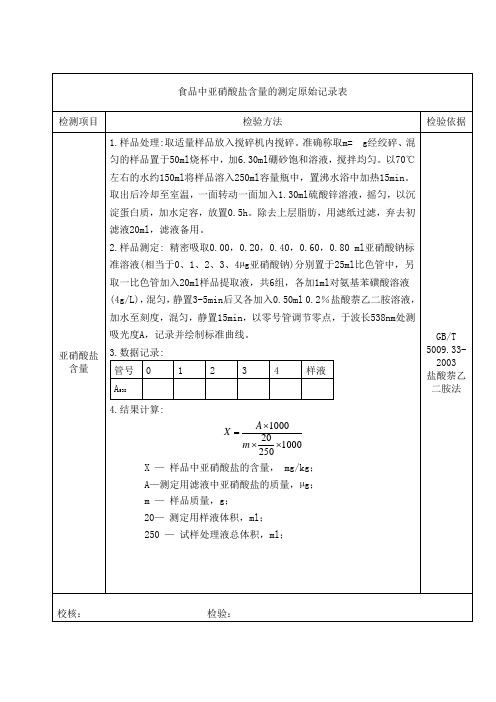
食品中亚硝酸盐含量的测定原始记录表
检测项目检验方法检验依据
亚硝酸盐含量1.样品处理:取适量样品放入搅碎机内搅碎。
准确称取m= g经绞碎、混
匀的样品置于50ml烧杯中,加6.30ml硼砂饱和溶液,搅拌均匀。
以70℃
左右的水约150ml将样品溶入250ml容量瓶中,置沸水浴中加热15min。
取出后冷却至室温,一面转动一面加入1.30ml硫酸锌溶液,摇匀,以沉
淀蛋白质,加水定容,放置0.5h。
除去上层脂肪,用滤纸过滤,弃去初
滤液20ml,滤液备用。
2.样品测定: 精密吸取0.00,0.20,0.40,0.60,0.80 ml亚硝酸钠标
准溶液(相当于0、1、2、3、4µg亚硝酸钠)分别置于25ml比色管中,另
取一比色管加入20ml样品提取液,共6组,各加1ml对氨基苯磺酸溶液
(4g/L),混匀,静置3-5min后又各加入0.50ml 0.2%盐酸萘乙二胺溶液,
加水至刻度,混匀,静置15min,以零号管调节零点,于波长538nm处测
吸光度A,记录并绘制标准曲线。
3.数据记录:
管号0 1 2 3 4 样液
A538
4.结果计算:
1000
250
20
1000
⨯
⨯
⨯
=
m
A
X
X —样品中亚硝酸盐的含量, mg/kg;
A—测定用滤液中亚硝酸盐的质量,µg;
m —样品质量,g;
20—测定用样液体积,ml;
250 —试样处理液总体积,ml;
GB/T
5009.33-
2003
盐酸萘乙
二胺法
校核:检验:。
高效液相色谱法测定叶酸片中叶酸含量

( h r c u ia o l g , i i g M e ia Un v r i Rih o 2 6 2 Ch n ) P a ma e t lC l e J n n d c l c e ie st y, z a 7 8 6。 i a
Abta tOb e t e Toe tbiha L to o h ee miaino li A i n F l cd T bes sr c : j ei v sa l n HP C me h dfrte d tr n t fF 1 cdi oi A i a lt . s o 0c c
( O: 0 6 4 )wi h lw aea . / n. s l Th ie a g f oi i s2 . 81 / -8 . 2 ̄ / t tef h o rt t1 0mlmi Reu t s el rr n eo l Acdwa O O g ml 1 0 7 g ml n F c a
叶酸 是治 疗 贫 血 的 特 效药 物 。近 年来 叶酸 成 为 了营养 医学 界 的新 宠 , 目前 市 场上销 售 的营养 保
限公 司) KQ 5 , 0型 超 声 波 清 洗 器 ( 山 市 超 声 波 昆
仪 器有 限公 司 ) S 一5 , YZ 5 0型石 英 亚 沸 高 纯 水 蒸 馏 器 ( 苏金坛 市金 城 国胜 实验 仪 器 厂) B 2 4S型 江 , S 2
M eho FolcAcd wa e e m i d o t ds i i s d t r ne n HPLC nsr i tumen i d a D im o i t fxe a nsl c18 ol c umn (2 0 5 m m × 4 m m . .6 5
( = 0 99 r .9 9), nd t e a r ge r o er s 1 0. a h ve a ec v y wa 0 5% wih RS 1 2% . t D . Con l s o Th e ho Ssm pl s ns. cu in e m t d i i e, e i
叶酸代谢能力测定

MTHFR基因及相关SNP位点
• MTHFR全称5,10-亚甲基四氢叶酸还原酶,位于第一号
染色体1p36.3位置,全长19.3kb,共有外显子12个,mRNA 全长7,105 nt,编码657个氨基酸残基组成的蛋白。 SNP: (1)MTHFR C677T rs1801133;
(2)MTHFR A1298C rs1801131;
缺血性心脏病前瞻性研究和MTHFR突变文献数据汇总
研究类型 研究数
缺血性心脏病
MTHFR
46
Prospective
16
静脉血栓
MTHFR
26
脑卒中
MTHFR
7
Prospective
8
样本量
12193 3144 3439 1217 676
血清同型半胱氨酸浓度上升 5μmol/l
Summary odds ratio (95% CI)
随机、对照研究。在对2万余例中国高血压患者平均4.5年的随访中显示, 在降压治疗同时补充叶酸,可以显著降低首次卒中的风险。
补充叶酸
中美脑卒中一级预防研究
MTHFR基因型的影响
叶酸水平在基 准1/4以下
叶酸水平在基 准1/4以上
CT基因型
TT基因型
脑卒中发病率
注:TT基因型脑卒中风险最高
为什么需要MTHFR基因检测?
合
肝脏吸收合成叶酸的量有限,未被吸收的过量合成叶酸会进入 血液,有可能引起白血病、关节炎等疾病
常见血清学叶酸水平低的原因
➢ 巨幼细胞性贫血,溶血性贫血 ➢ 甲亢 ➢ 营养不良,慢性腹泻,吸收不良 ➢ 酒精中毒 ➢ 重症皮肤病 ➢ 恶性肿瘤 ➢ 骨髓增生性疾病 ➢ 肝脏疾病 ➢ 正常妊娠
食品检验原始记录表

食品检验原始记录表一、引言食品安全是人们关注的重要问题之一,食品检验是保障食品安全的重要手段之一。
食品检验原始记录表是食品检验过程中的重要文件,记录了食品样品的检验过程和结果,对于保障食品质量和消费者健康具有重要意义。
二、食品检验原始记录表的作用食品检验原始记录表是食品检验工作的重要组成部分,其作用主要体现在以下几个方面:1. 提供检验依据食品检验原始记录表记录了食品样品的检验项目、方法、仪器设备等信息,为后续的食品检验提供了重要依据。
在进行食品检验时,可以根据原始记录表中的信息选择合适的检验项目和方法,确保食品检验的准确性和可靠性。
2. 保障食品质量食品检验原始记录表记录了食品样品的检验结果,可以及时了解食品的质量状况。
通过食品检验原始记录表的结果,可以判断食品是否符合相关标准和法规的要求,及时采取相应的措施,保障食品质量。
3. 追溯食品安全问题在食品安全问题发生时,食品检验原始记录表可以作为证据,帮助追溯食品安全问题的起因和责任。
通过对原始记录表的分析和比对,可以找出食品安全问题的源头,采取相应的措施加以解决。
三、食品检验原始记录表的内容食品检验原始记录表的内容应当包括以下几个方面:1. 样品信息食品检验原始记录表应当记录样品的基本信息,包括样品的名称、产地、生产日期、保质期等。
这些信息对于后续的食品检验和食品追溯具有重要意义。
2. 检验项目和方法食品检验原始记录表应当记录检验项目和方法,包括检验项目的名称、检验方法的编号和描述等。
这些信息可以帮助食品检验人员选择合适的检验项目和方法,确保食品检验的准确性和可靠性。
3. 仪器设备和试剂食品检验原始记录表应当记录使用的仪器设备和试剂,包括仪器设备的名称、型号、生产厂家等信息,试剂的名称、批号、有效期等信息。
这些信息对于食品检验的可追溯性和结果的可靠性具有重要意义。
4. 检验结果和评定标准食品检验原始记录表应当记录检验结果和评定标准,包括检验结果的数值、单位、评定标准的编号和描述等信息。
叶酸的测定方法

叶酸的测定方法微生物法1.原理叶酸是酪乳酸杆菌(Lactobacillus casei, L. C, ATCC 7469)生长所必需的营养素。
在一定条件下,L.C的生长繁殖与培养基中叶酸含量呈正比关系,细菌增殖的量以光密度值计,通过与标准曲线相比较,计算出样品中叶酸的含量。
2.适用范围参考《Methods of Vitamin Assay》,第4版。
本方法适用于各类食物中叶酸的测定。
检测限为0.1ng。
3.仪器与设备(1)恒温培养箱(2)离心机(3)高压消毒锅(4)震荡器(5)接种针和接种环(6)分光光度计4.试剂除特殊说明外,本实验中所有试剂均为分析纯,水为蒸馏水。
(1)菌种:酪乳酸杆菌(Lactobacillus casei, L.C, ATCC 7469)(2)磷酸缓冲液(0.05mol/L, pH6.8):称取4.35g Na3PO4·12H2O,10.39g Na2HPO4·7H2O溶解于800ml水中。
临用前用约5g抗坏血酸调节pH至6.8。
(注:叶酸对光、热敏感,易被氧化破坏,抗坏血酸有助于保护叶酸被氧化。
)(3)鸡胰酶溶液:称取100mg干燥的鸡胰酶(Difco公司)(注:含有叶酸轭合酶,用于水解叶酸多谷氨酸盐),加入20ml磷酸缓冲液制成匀浆,3000rpm离心10min,取上清液备用。
临用前现配。
(4)蛋白酶-淀粉酶溶液:分别称取200mg蛋白酶(Sigma公司)和淀粉酶(Sigma公司),加入20ml磷酸缓冲液制成匀浆,离心3000rpm 10min,取上清液备用。
临用前配制。
(5) 2+8乙醇溶液:量取20ml无水乙醇溶液,加入80ml水混匀。
(6) 01mol/L NaOH: 称取0.4g氢氧化钠,加2+8乙醇溶液溶解并稀释至1L。
(7) 10mol/L NaOH。
称取400g氢氧化钠,加水溶解并稀释至1L。
(8)叶酸标准储备液(200mg/ml):准确称取200mg叶酸标准品(Sigma公司,纯度大于98%),用0.01mol/L NaOH溶解并定容至1L。
食品卫生微生物检验原始记录表
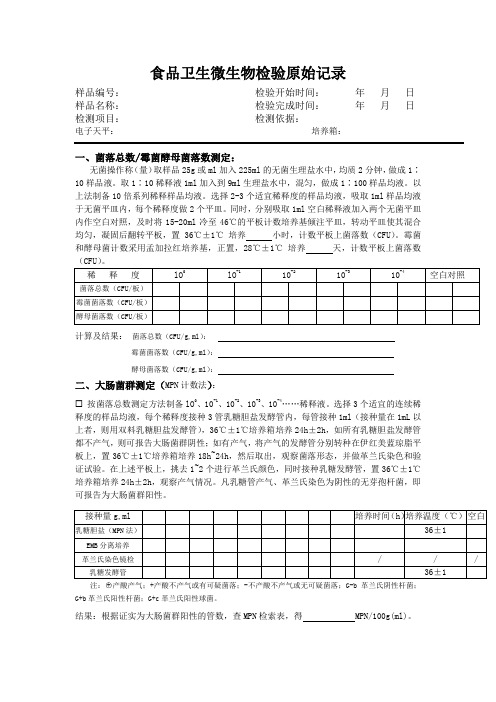
食品卫生微生物检验原始记录样品编号:检验开始时间:年月日样品名称:检验完成时间:年月日检测项目:检测依据:电子天平:培养箱:一、菌落总数/霉菌酵母菌落数测定:无菌操作称(量)取样品25g或ml加入225ml的无菌生理盐水中,均质2分钟,做成1∶10样品液。
取1∶10稀释液1ml加入到9ml生理盐水中,混匀,做成1∶100样品均液。
以上法制备10倍系列稀释样品均液。
选择2-3个适宜稀释度的样品均液,吸取1ml样品均液于无菌平皿内,每个稀释度做2个平皿。
同时,分别吸取1ml空白稀释液加入两个无菌平皿内作空白对照,及时将15-20ml冷至46℃的平板计数培养基倾注平皿,转动平皿使其混合均匀,凝固后翻转平板,置 36℃±1℃培养小时,计数平板上菌落数(CFU)。
霉菌和酵母菌计数采用孟加拉红培养基,正置,28℃±1℃培养天,计数平板上菌落数(CFU)。
计算及结果:菌落总数(CFU/g,ml):霉菌菌落数(CFU/g,ml):酵母菌落数(CFU/g,ml):二、大肠菌群测定(MPN计数法):按菌落总数测定方法制备lO0、10-1、10-2、10-3、10-4……稀释液。
选择3个适宜的连续稀释度的样品均液,每个稀释度接种3管乳糖胆盐发酵管内,每管接种1ml(接种量在1mL以上者,则用双料乳糖胆盐发酵管),36℃±1℃培养箱培养24h±2h,如所有乳糖胆盐发酵管都不产气,则可报告大肠菌群阴性;如有产气,将产气的发酵管分别转种在伊红美蓝琼脂平板上,置36℃±1℃培养箱培养18h~24h,然后取出,观察菌落形态,并做革兰氏染色和验证试验。
在上述平板上,挑去1~2个进行革兰氏颜色,同时接种乳糖发酵管,置36℃±1℃培养箱培养24h±2h,观察产气情况。
凡乳糖管产气、革兰氏染色为阴性的无芽孢杆菌,即可报告为大肠菌群阳性。
注:○+产酸产气;+产酸不产气或有可疑菌落;-不产酸不产气或无可疑菌落;G-b革兰氏阴性杆菌;G+b革兰氏阳性杆菌;G+c革兰氏阳性球菌。
食品中酸价测定的原始记录
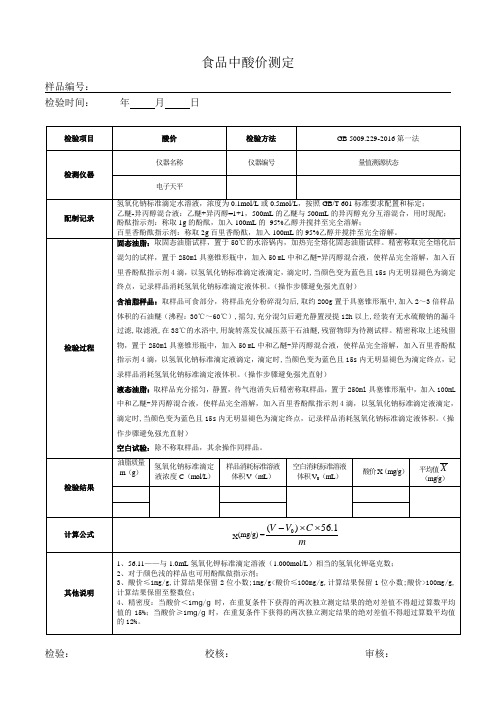
百里香酚酞指示剂:称取2g百里香酚酞,加入100mL的95%乙醇并搅拌至完全溶解。
检验过程
固态油脂:取固态油脂试样,置于50℃的水浴锅内,加热完全熔化固态油脂试样。精密称取完全熔化后混匀的试样,置于250ml具塞锥形瓶中,加入50 mL中和乙醚-异丙醇混合液,使样品完全溶解,加入百里香酚酞指示剂4滴,以氢氧化钠标准滴定液滴定,滴定时,当颜色变为蓝色且15s内无明显褪色为滴定终点,记录样品消耗氢氧化钠标准滴定液体积。(操作步骤避免强光直射)
检验时间:_____年月日
含油脂样品:取样品可食部分,将样品充分粉碎混匀后,取约200g置于具塞锥形瓶中,加入2~3倍样品体积的石油醚(沸程:30℃~60℃),摇匀,充分混匀后避光静置浸提12h以上,经装有无水硫酸钠的漏斗过滤,取滤液,在38℃的水浴中,用旋转蒸发仪减压蒸干石油醚,残留物即为待测试样。精密称取上述残留物,置于250ml具塞锥形瓶中,加入50 mL中和乙醚-异丙醇混合液,使样品完全溶解,加入百里香酚酞指示剂4滴,以氢氧化钠标准滴定液滴定,滴定时,当颜色变为蓝色且15s内无明显褪色为滴定终点,记录样品消耗氢氧化钠标准滴定液体积。(操作步骤避免强光直射)
液态油脂:取样品充分摇匀,静置,待气泡消失后精密称取样品,置于250ml具塞锥形瓶中,加入100mL中和乙醚-异丙醇混合液,使样品完全溶解,加入百里香酚酞指示剂4滴,以氢氧化钠标准滴定液滴定,滴定时,当颜色变为蓝色且15s内无明显褪色为滴定终点,记录样品消耗氢氧化钠标准滴定液体积。(操作步骤避免强光直射)
空白试验:除不称取样品,其余操作同样品。
检验结果
油脂质量m(g)
氢氧化钠标准滴定液浓度C(mol/L)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
GB/T 5009.211-2008食品中叶酸的测定
检出限
仪器名称
紫外可见分光光度计
仪器型号
754PC
仪器编号
N-12-06-009
仪器条件
波长540 nm 比色皿1 cm
环境条件
温度(℃):湿度(%RH):
分析步骤:
按照GB/T 5009.211-2008中6.1制备接种液,按7.1进行试样的处理提取,按需按7.2稀释,按照7.3制备测定管,按照7.4进行培养,按7.5步骤进行分析测定。操作需避光进行
标准曲线的绘制
标准溶液名称:叶酸标准工作液标准曲线工作液:0.200ng/ml
试管号
S1
S2
S3
S4
S5
S6
S7
S8
S9
S10
0.200ng/ml标准曲线工作液
0.00
0.25
0.50
1.00
1.50
2.00
2.50
3.00
4.00
5.00
叶酸含量ng
0.00
0.05
0.10
0.20
0.30
0.40
试样中叶酸含量ug/100g
a2
b2
c2
a3
b3
c3
计算公式:
————————————(1)
————————(2)
备注:
检验日期:
0.50
0.60
0.80
1.00
透光率两次测定均值%
回归方程
样品测定
提取液定容体积V2ml;
空白
吸取酶空白液液体积V1
透光率%
从曲线查得叶酸含量m3(ng)
酶液中叶酸含量m1(ng)
/
/
试样中叶酸含量X
ug/100g
相对偏差%
a1
b1
c1
序号
试样质量m(g)
稀释倍数f
吸取试样液体积V1
透光率%
从曲线查得叶酸含量m2(ng)
